泪点闭锁症
定义:上下泪点狭窄或闭合的状态。
主要原因:烧伤或化学腐蚀后的瘢痕、Stevens-Johnson综合征、眼类天疱疮。
药物性:噻吗洛尔、多佐胺、毛果芸香碱等青光眼滴眼液,IDU(抗病毒药),S-1(替吉奥®)。

泪道(泪点→泪小管→泪囊→鼻泪管→下鼻道开口)的通过障碍(狭窄或阻塞)导致溢泪的疾病称为泪道阻塞。其中,鼻泪管入口及以后的阻塞称为鼻泪管阻塞(NLDO)。
裂隙灯检查可见泪液半月面增高,荧光素染色清除延迟提示泪道阻塞可能。通过泪道冲洗试验确诊。
根据阻塞部位,大致分为以下四种类型。
泪点闭锁症
定义:上下泪点狭窄或闭合的状态。
主要原因:烧伤或化学腐蚀后的瘢痕、Stevens-Johnson综合征、眼类天疱疮。
药物性:噻吗洛尔、多佐胺、毛果芸香碱等青光眼滴眼液,IDU(抗病毒药),S-1(替吉奥®)。
泪小管阻塞症
定义:泪小管(上/下)阻塞的状态。
矢部·铃木分类:1级(总泪小管阻塞,有交通)/2级(上下无交通,可插入7~8mm以上)/3级(比2级更近端的阻塞)。
特征:抗癌药物相关者多为双侧性、上下同时受累。
总泪小管阻塞症
鼻泪管阻塞症
自2018年泪道内镜纳入医保以来1),可以观察阻塞部位的纤维化程度和黏膜炎症表现,提高了对总泪小管或鼻泪管阻塞的鉴别准确性。冲洗试验估计的阻塞部位与泪道内镜所见的一致率约为70%1),内镜直接观察具有重要意义。
溢泪不仅包括泪道阻塞,也包括泪液分泌过多(如干眼引起的反射性溢泪)。泪道冲洗有反流则可判断为阻塞。通过BUT测量或Schirmer试验评估泪液分泌量进行鉴别。
使用S-1(替加氟/吉美嘧啶/奥替拉西钾复方制剂,TS-1®)抗癌治疗期间发生的泪点和泪小管阻塞常较严重。建议早期置管。抗癌药相关泪道阻塞中,泪点和泪小管病变约占60%1)。抗癌药使用期间拔管易再阻塞,因此建议在用药期间持续留置泪道管1)。
矢部·铃木分类用于泪小管阻塞的严重程度分级1)。
| 分级 | 定义 | 治疗方法 |
|---|---|---|
| 1级 | 可插入探针≥11 mm;上下泪点间交通存在(总泪小管阻塞) | DEP/SEP,置管时间2~10个月 |
| 2级 | 上下泪点间无交通;可插入探针≥7~8 mm | DEP/SEP(难度高),也可考虑CDCR |
| 3级 | 阻塞位置比2级更近端 | DEP/SEP困难,尝试金属探针,考虑CDCR |
鼻泪管阻塞是成人溢泪的最常见原因。多见于女性和老年人,鼻泪管的解剖性狭窄被认为是原因之一。锥形束CT泪道造影分析显示,眶上缘-内总泪点-鼻泪管开口的角度在92%的病例中呈前屈曲3),这种形态特征被认为有助于阻塞的风险。
鼻泪管阻塞的原因包括慢性炎症、年龄相关变化,以及Stevens-Johnson综合征、眼类天疱疮、药物性(青光眼滴眼液、抗病毒药、抗癌药)等。
| 检查 | 可检测的信息 | 侵袭性 | 医保覆盖 |
|---|---|---|---|
| 泪道冲洗(通水检查) | 有无阻塞及反流方向 | 低 | 有 |
| 染料消失试验 | 泪液清除率降低 | 低 | 有 |
| 泪囊造影 | 阻塞部位、泪囊扩大、造影剂中断 | 中 | 有 |
| 泪道内镜 | 直接观察阻塞部位、纤维化、黏膜炎症 | 中 | 自2018年起 |
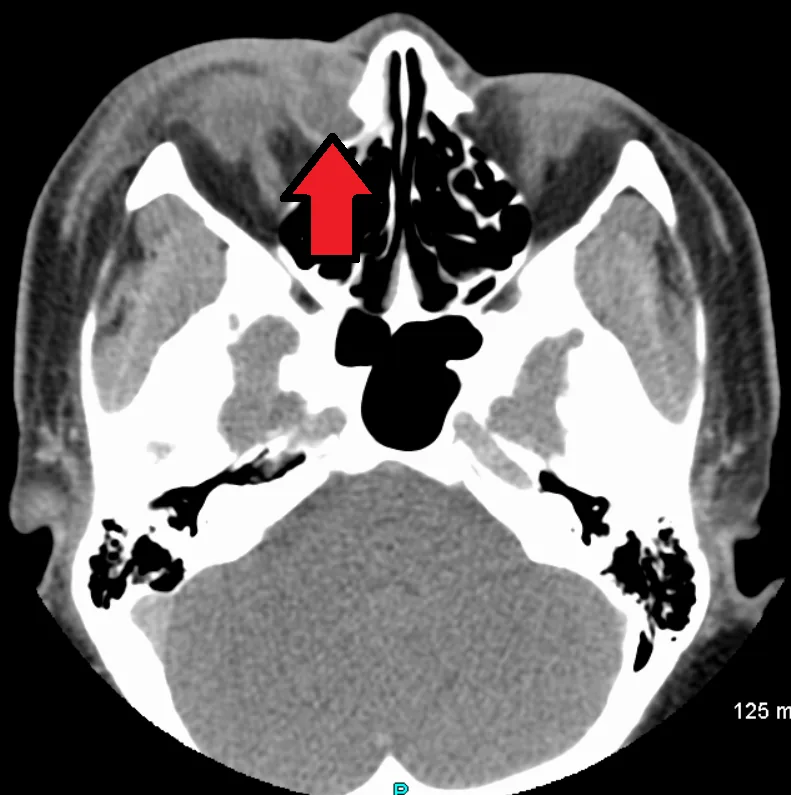
| 眼眶及鼻窦CT | 泪囊窝、鼻腔形态、鼻窦炎、肿物 | 中等 | 有(术前) |
泪道内镜检查于2018年被纳入医保1),对诊断阻塞部位的纤维化程度、黏膜炎症及泪道内肿物有用。若怀疑泪道外病变,则联合使用CT或MRI。
泪囊造影有时难以判断造影剂是否到达阻塞部位1),其作用主要是对泪道内镜直接观察的补充。
流泪的原因大致分为“泪道通过障碍(分泌量正常但无法排出)”和“泪液分泌过多(刺激导致泪液增加)”。泪道阻塞是最常见的原因,但干眼引起的反射性流泪、结膜炎、角膜炎等也会导致流泪。通过BUT测量和Schirmer试验评估泪液分泌量,并通过泪道冲洗确认有无通过障碍来进行鉴别。
自2018年起已纳入医保。泪道内镜可直接观察阻塞部位,有助于诊断纤维化程度、黏膜炎症及泪道内肿瘤。对于通水试验难以判断的阻塞部位详细分类(如总泪小管阻塞与鼻泪管阻塞的鉴别、泪囊-鼻泪管移行部阻塞与下部膜性鼻泪管阻塞的区别等)尤其有用。
根据阻塞部位、严重程度及患者意愿选择治疗方法。
急性期/初期处理如下:
在滴眼麻醉下,用泪点扩张针或尖刀切开并扩张泪点。留置泪点塞24周后取出,若再次闭塞,则留置泪小管硅胶管12个月后取出。
逐步扩张泪点(由细到粗)后留置泪管可预防再次闭塞。留置时间为17个月,拔管后312个月的成功率据报道为81.8~100%1)。
用4%盐酸利多卡因溶液进行泪道内麻醉后,用泪点扩张针充分扩张泪小管。从泪点小心插入双头或导管型硅胶管,同时确认阻塞部位的触感,留置1~2个月后取出。
使用DEP(泪道内镜直接穿破法)或SEP(鞘引导内镜下穿破法)穿破阻塞部位1)。
置管时间为2~10个月。据报道,术后878天Kaplan-Meier法的通畅率为94%1)。
难度显著增加,若DEP/SEP穿通困难,则尝试用细金属探针穿通1)。若上下泪小管均无法开放,则考虑CDCR(结膜泪囊鼻腔吻合术)。
用DEP或SEP穿通阻塞部位,通过SGI(鞘引导插管)或G-SGI置入导管1)。
直接置管有22%的黏膜下误置报道1),推荐使用SGI/G-SGI方法。置管时间为2~12个月。拔管后1年手术成功率为70~87%1)。DSI(直接硅胶插管)的成功率较低,约52.5%(拔管后8~30个月)1),拔管后3000天的通畅率为64%,有长期复发风险的报道1)。复发危险因素包括泪囊炎病史、病程长、阻塞距离长、男性1)。
适用于长期溢泪、眼部分泌物症状且患者希望手术的情况。急性泪囊炎时,在切开引流、抗生素消炎后制定手术计划。对于不希望根治手术的患者,可通过探通或置管推迟手术时间,但需事先充分说明鼻泪管阻塞的置管术效果不佳。
外路DCR手术步骤:
外路DCR的成功率为90~99%1),多数报告显示再闭塞率低于10%。有报告指出,由于骨窗较小,内路(内镜下)DCR的效果略差。
| 术式 | 成功率 | 留置/通畅时间 | 主要适应症 |
|---|---|---|---|
| 直接硅胶管插入(DSI) | 约52.5%(8~30个月后) | 留置2~12个月 | 鼻泪管阻塞(轻度) |
| 泪道内镜下置管(DEP/SEP+SGI) | 70~87%(1年后) | 留置2~12个月 | 鼻泪管阻塞/泪小管阻塞 |
| DCR鼻外法 | 90~99%1) | — | 鼻泪管阻塞(根治) |
| DEP/SEP(1级泪小管阻塞) | 通畅率94%(878天后) | 留置2~10个月 | 总泪小管阻塞 |
泪道内镜手术及泪管置管相关的主要并发症如下所示1)。
S-1(TS-1®)引起的泪道阻塞常发生在泪点和泪小管,且易加重,因此建议早期行硅胶管置入术。化疗期间拔管易再阻塞,故治疗期间最好维持置管。如出现症状,请及时咨询眼科医生。
因阻塞部位和术式而异。泪点置管:17个月;泪小管泪道内镜下治疗(DEP/SEP):210个月;鼻泪管置管术:2~12个月。未来有望根据泪道内镜所见确定最佳拔管时机。
鼻泪管入口处阻塞最常见。慢性炎症、年龄相关变化和解剖狭窄共同参与。
阻塞发生后,泪液和分泌物在阻塞近端(泪囊侧)积聚。积聚的黏液成为细菌培养基,导致Moraxella lacunata、S. mitis、铜绿假单胞菌、α溶血性链球菌等过度生长,进展为慢性泪囊炎1)。泪液清除减少也会导致角膜和结膜的慢性改变。
一项使用锥形束CT泪道造影分析泪道形态的报告显示,眶上缘-内总泪点-鼻泪管开口的角度在92%的病例中向前弯曲3),这种形态特征被认为影响器械插入鼻泪管的难度以及阻塞的形成。
泪道内窥镜有两种规格:外径0.9毫米、观察像素10,000(2012年改进型)和外径0.7毫米、3,000像素的操作优先型1)。2020年,景深得到改善,可适应1.5至7毫米的观察距离。主要使用尖端10毫米处向上弯曲27°的弯曲型,根据病例选择使用直型和双弯曲型1)。
泪囊结石由慢性炎症和分泌物潴留形成4)。泪道内肿瘤有时通过泪道内窥镜发现,有恶性黑色素瘤、乳头状瘤和肉芽肿的报道1)。由于在DCR手术时的病理检查中约1.0%(占所有肿瘤的69%)发现恶性肿瘤,因此建议对手术标本进行组织病理学检查5)。