放线菌性(最常见)
致病菌:Actinomyces israelii
厌氧、革兰阳性丝状菌。最适应泪小管内的厌氧环境,形成硫磺颗粒。菌石由放线菌菌落沉积钙质生长而成。

泪小管炎(canaliculitis)是构成泪道系统的泪小管(上泪小管和下泪小管)发生的慢性感染性炎症。最常见的致病菌是放线菌(Actinomyces israelii),它在泪小管内形成菌石(concretion/dacryolith)。少数情况下也可由丙酸杆菌、链球菌等细菌或真菌(曲霉菌、念珠菌)引起。
泪道是从泪点→泪小管(上下)→总泪小管→泪囊→鼻泪管连续的结构,泪小管炎是局限于泪小管的感染。好发于下泪小管,多见于中老年女性。
患者常因单眼难治性结膜炎就诊于眼科门诊,可能需要较长时间才能得到正确诊断和治疗。注意泪点的特征性变化(扩张、发红、可挤出分泌物)是早期诊断的关键。
放线菌性(最常见)
致病菌:Actinomyces israelii
厌氧、革兰阳性丝状菌。最适应泪小管内的厌氧环境,形成硫磺颗粒。菌石由放线菌菌落沉积钙质生长而成。
细菌性
致病菌:丙酸杆菌、诺卡菌、链球菌、金黄色葡萄球菌、铜绿假单胞菌
诺卡菌属于需氧放线菌。梭杆菌是厌氧菌,这些也能形成菌石。
真菌性
致病菌:曲霉菌、念珠菌
虽然罕见,但容易变得难治。可能需要加用抗真菌药物(如匹马霉素滴眼液等)。
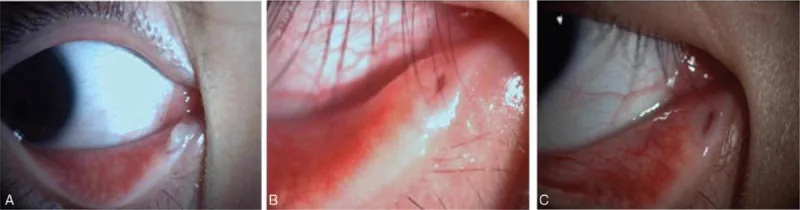
主诉为充血、眼部分泌物和流泪,症状类似于单眼慢性结膜炎。多数情况下病变发生在下泪小管。初期作为慢性结膜炎使用抗菌滴眼液治疗,但无改善,常呈难治性经过。
| 所见 | 内容 | 临床意义 |
|---|---|---|
| 泪点扩张(打孔样外观) | 泪点扩大并呈红色 | 最具特征性所见;提示泪小管炎 |
| 泪点周围肿胀 | 沿泪小管走行的索状肿胀 | 提示泪小管内炎症或菌块存在 |
| 压迫后分泌物排出 | 压迫泪点后排出脓性或硫磺颗粒样分泌物 | 具有病理特异性(pathognomonic)的所见 |
| 睑结膜炎症 | 充血、肥厚、乳头增生 | 难治性结膜炎表现 |
压迫泪点排出硫磺颗粒样分泌物是泪小管炎高度特异性的表现,若确认此表现,临床诊断基本可以确定。
肉眼观察为黄白色颗粒状物质的菌块,由放线菌菌落沉积钙盐形成。“硫磺”一词源于其外观颜色和形状,并非真正的硫磺。显微镜下可见密集的放线菌丝状结构。
硫磺颗粒在泪小管内滞留并生长形成的结石样物质。菌石存在于泪小管内会导致慢性炎症持续,是单用抗菌药物无法治愈的原因。
多见于中老年女性,常以单眼难治性结膜炎就诊于眼科门诊。已知好发于下泪小管。虽然明确的人口统计数据有限,但在以溢泪和眼部分泌物为主诉的患者中,与慢性结膜炎的鉴别很重要。
在泪道阻塞病例中,泪道内结石(dacryolith)的合并率很高。根据泪道内镜诊疗指南,泪囊结石合并于鼻泪管阻塞病例的7.5% 1),表明整个泪道系统可能存在结石形成的倾向。
用于干眼治疗的泪点塞可能移位进入泪小管,作为异物反应和炎症的核心引发泪小管炎 1)。有泪点塞留置史的患者出现难治性结膜炎时,需考虑泪点塞移位导致的泪小管炎。
当单眼难治性结膜炎持续存在时,应积极怀疑泪小管炎。门诊诊断步骤如下所示。
步骤1:泪点视诊 检查泪点有无发红、扩张(punch-out appearance)。
步骤2:泪点压迫试验 沿泪小管走行压迫泪点,检查分泌物排出。若排出脓性或硫磺颗粒样分泌物,则可临床诊断为泪小管炎。
步骤3:泪道冲洗 进行泪道冲洗。泪小管炎常无泪道阻塞,而泪囊炎常伴有泪道阻塞,因此通畅性检查有助于鉴别。
步骤4:微生物学检查 采集从泪小管排出的脓性分泌物,进行革兰染色、涂片镜检和厌氧培养,以鉴定致病菌。
| 检查 | 方法/判定 | 意义 |
|---|---|---|
| 革兰染色 | 革兰阳性、分支状丝状菌体(放线菌特征) | 可快速推定放线菌感染 |
| 厌氧培养 | 厌氧条件下培养 | 放线菌为厌氧菌,需厌氧培养 |
| 需氧培养 | 常规培养 | 检测诺卡菌、念珠菌、曲霉菌等 |
放线菌的涂片镜检所见具有特征性,通过确认革兰阳性分支丝状菌体,可以推定诊断放线菌性泪小管炎。
泪道内镜可以直接观察泪小管内的菌石和炎症表现。它有助于确认菌石的确切位置和大小,并验证完全摘除1)。在泪道内镜引导下摘除菌石可实现直视操作,有助于预防术后复发2)。
| 鉴别疾病 | 特征性表现 | 泪道冲洗 | 鉴别要点 |
|---|---|---|---|
| 泪小管炎 | 泪点扩张、硫磺颗粒排出、索状肿胀 | 通畅 | 单眼难治性结膜炎 + 泪点表现 |
| 泪囊炎 | 泪囊部肿胀、压迫泪囊有大量脓液反流 | 阻塞 | 以泪道阻塞和泪囊部肿胀为主 |
| 慢性结膜炎 | 睑结膜充血、肥厚 | 正常 | 多为双眼性,无泪点所见 |
| 霰粒肿 | 眼睑皮下无痛性肿块 | 正常 | 以眼睑肿块为中心,无泪点所见 |
泪小管炎的特征是泪点周围肿胀和泪点扩张,泪道冲洗通常无阻塞。而泪囊炎主要表现为泪囊区(内眼角下方)肿胀,压迫泪囊时大量脓液从泪点反流,泪道冲洗可确认阻塞。有无局部泪点所见(扩张、压迫时分泌物排出)是最大的鉴别点。
完全物理清除泪小管内的菌块(菌石)是治疗的根本。菌石是致密的菌块结构,抗菌药物难以渗透,单独使用抗菌药物滴眼液无法清除菌块,无法治愈。必须进行外科切开和刮除。
步骤1:泪小管切开及菌块清除
在局部麻醉下进行泪小管切开术。
用锐匙(刮匙)彻底刮除泪小管内容物,完全清除菌块和菌石。菌块残留是复发的主要原因,因此完全清除最为重要。
使用泪道内镜时,可以在直视下摘除菌石并确认完全清除1)。
步骤2:术后抗菌药物滴眼液和泪小管冲洗
术后继续使用新喹诺酮类滴眼液。
左氧氟沙星滴眼液0.5%(可乐必妥®)每日4~6次。使用新喹诺酮类滴眼液进行泪小管冲洗也有助于术后管理。
真菌性泪小管炎时,考虑加用抗真菌药物(如匹马霉素滴眼液等)。
步骤3:全身抗菌药物和随访
放线菌感染时,全身使用青霉素类药物数周。
阿莫西林250~500mg(如沙威西林®)每日3次,持续数周。术后反复进行泪道冲洗,预防复发。根据培养结果适当调整抗菌药物。
泪小管切开术
完全清除菌块最为重要,因切除不彻底导致菌块残留是复发的主要原因。
泪道内镜下取菌石
使用泪道内镜,可在直接观察菌石准确位置的同时将其取出。可确认完全取出,有助于防止复发2)。
处理移位的泪点塞
如果原因是泪点塞移位,可通过泪点切开取出,或在泪道内镜下尝试将其排入鼻腔1)。
| 药物 | 剂量和用法 | 适应症 |
|---|---|---|
| 左氧氟沙星滴眼液0.5%(可乐必妥®) | 每日4~6次 | 术后持续使用、泪小管冲洗 |
| 阿莫西林胶囊250mg(沙威西林®等) | 每日3次,持续数周 | 放线菌性(全身给药) |
| 匹马利星滴眼液(那他霉素滴眼液) | 每日4~6次 | 真菌性(必要时) |
因菌块未完全摘除导致的复发需再次手术(再切开及刮除)。若泪道闭塞进展,可能需要留置泪管或行DCR(泪囊鼻腔吻合术)。
通常单用滴眼液无法治愈。泪小管内形成的菌块(菌石)结构致密,抗菌药物难以到达菌块内部的菌体。治疗核心是在局部麻醉下切开泪小管,用锐匙物理性完全去除菌块。术后联合使用抗菌滴眼液(新喹诺酮类)和全身给药(放线菌性用青霉素类)可提高治愈率。
若能完全去除菌块,预后良好,复发较少。反之,若菌块摘除不完全,泪小管内残留菌石,则易复发。使用泪道内镜确认菌石完全摘除有助于预防复发。复发时再次行切开刮除术。
泪小管始于泪点,沿眼睑缘水平走行。上、下泪小管各长约8~10mm,汇合形成总泪小管后开口于泪囊。泪小管管腔扁平,正常直径约0.5~1mm。
泪小管管腔与外界空气交通有限,易形成厌氧环境。衣氏放线菌是专性或兼性厌氧菌,适应并易于在此环境中增殖。一般开放部位(皮肤、结膜)不易增殖的放线菌能在泪小管内优势定植,正是由于这一解剖特性。
结石的结构类似于钙沉积在密集菌落上的固体,抗菌药物分子难以到达菌块内部的细菌。此外,菌块表面的生物膜样结构阻碍药物渗透。因此,单用抗菌眼药水只能部分清除表面细菌,无法去除整个菌块,停药后容易再生长和复发。这就是手术物理去除菌块是唯一根治方法的原因。
泪道内镜是一种将细径纤维镜插入泪道内直视观察泪道内腔的技术1)。在泪小管炎中,可以直接确认结石的存在、位置和大小,并验证是否完全摘除2)。与传统的盲目泪小管切开和刮除相比,有望更可靠地去除结石。泪道内镜诊疗指南也指出,伴有泪小管结石的泪小管炎中,完全摘除结石直接关系到治愈1),内镜技术的普及有助于改善治疗效果。
有报道称,广泛用于干眼治疗的泪点栓子移位可导致泪小管炎1)。栓子脱落到泪小管后,作为异物成为炎症和感染的核心。对于留置泪点栓子后出现难治性结膜炎的患者,应考虑本病。处理方法包括通过泪点切开摘除或泪道内镜下经鼻排出。
日本涙道・涙液学会涙道内視鏡診療の手引き作成委員会. 涙道内視鏡診療の手引き. 日本眼科学会雑誌. 2023;127(10):896-917.
Ali MJ, Alam MS, Naik MN. Dacryoendoscopic features in a case of canaliculitis with concretions. Ophthalmic Plast Reconstr Surg. 2017;33:228-229.