術式別リスク比較

屈折矯正手術後のドライアイ(Post-Refractive Surgery Dry Eye)
1. 屈折矯正手術後のドライアイとは
Section titled “1. 屈折矯正手術後のドライアイとは”屈折矯正手術後のドライアイ(post-refractive surgery dry eye)は、LASIK(laser in situ keratomileusis)・PRK(photorefractive keratectomy)・SMILE(small incision lenticule extraction)など、角膜形状を変化させる屈折矯正手術の後に生じるドライアイである。
ドライアイとは「さまざまな要因により涙液層の安定性が低下する疾患であり、眼不快感や視機能異常を生じ、眼表面の障害を伴うことがある」と定義される。屈折矯正手術後のドライアイはこの定義の「さまざまな要因」のうち、角膜手術による角膜神経切断・涙腺反射弧の遮断が主因となったものである。
角膜上皮障害と涙液層破壊時間(BUT)の低下は、LASIK・PRKをはじめとする前眼部手術全般によって誘発される可能性が高いことが示唆されている。涙液分泌量(Schirmer値)は角膜切開または切除を行う手術で低下することが示唆されている2)。
屈折矯正手術のガイドライン(第8版)では、ドライアイはLASIK術後合併症の一つとして明記されており1)、術前からの評価と積極的な管理が求められる。
術後ドライアイの時系列
Section titled “術後ドライアイの時系列”術後早期のドライアイ症状は一般的に6〜12か月で改善するが、少数の症例では従来の治療に反応しない難治性ドライアイへと移行する3)。
LASIKではマイクロケラトームまたはフェムト秒レーザーで角膜フラップを作成する際、前実質の角膜神経叢が広範囲に切断されます。これにより三叉神経を介した涙腺への反射性信号が大幅に遮断され、基礎分泌・反射性分泌の両方が低下します。また、術後の瞬目減少・マイボーム腺機能不全の悪化も加わり、多くの患者が術後1〜3か月間、ドライアイ症状を経験します。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”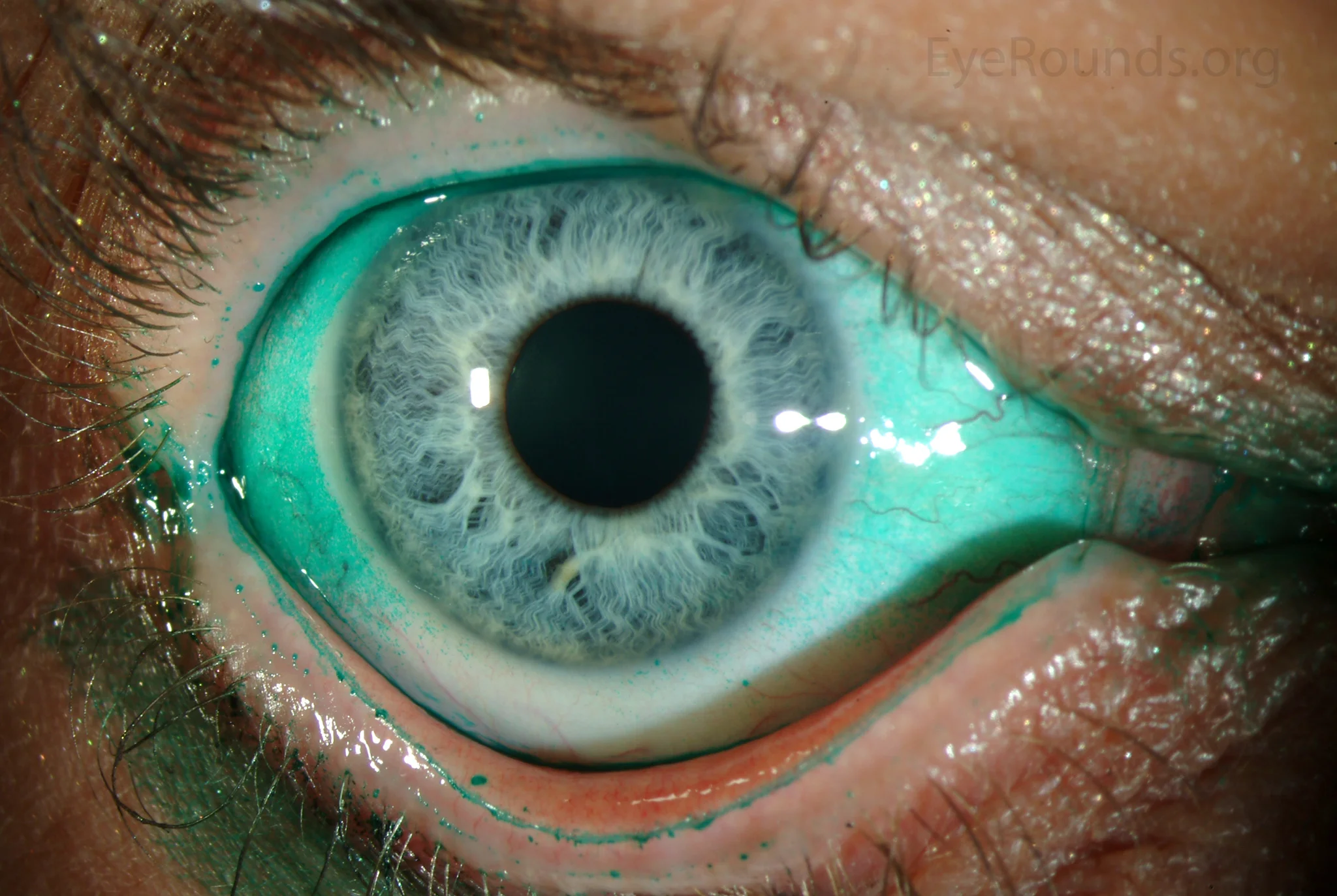
屈折矯正手術後のドライアイの症状は通常のドライアイと共通しているが、視機能に関連した症状が前景に出やすい。
- 乾燥感・異物感・灼熱感・眼痛
- 霧視・見えにくさの変動(瞬目後一時的に改善する)
- 光過敏・羞明
- コンタクトレンズ装用不快感(手術前に装用していた場合)
涙液層の変化:
- BUT(涙液破壊時間)の短縮(5秒以下が異常基準)
- Schirmer値の低下(5mm/5分以下)
- 涙液メニスカス高さの低下(0.25mm未満)
- 蒸発亢進による油層不均一
角膜知覚の変化:
TFOD(涙液層破綻パターン):
- Spot break(水濡れ低下型):点状の早期破綻。角膜神経切断後のムチン層異常が主因
- Line break(涙液減少型):線状の破綻。反射性分泌低下の影響
- Area break:広範囲な早期破綻
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”角膜神経切断による病態
Section titled “角膜神経切断による病態”LASIK術後のドライアイの主要機序は以下のとおりである。
- フラップ作成時に前実質の角膜神経叢(三叉神経眼枝由来)が広範囲に切断される
- 三叉神経を介した涙腺への反射性信号が遮断される → 基礎分泌・反射性分泌の低下
- 角膜知覚低下により瞬目反射が減弱 → 不完全瞬目増加 → 蒸発亢進
- 涙液量減少・安定性低下 → 角結膜上皮障害の悪循環
- 術後炎症によるマイボーム腺機能の一時的な悪化 → 蒸発亢進型の要素が加わる
術前リスク因子
術前ドライアイ:術前にドライアイの患者はLASIK後も非ドライアイ患者に比較してドライアイの程度が強いことが示唆されている2)
女性・高齢:ドライアイの一般的リスク因子が術後にも影響する
高度近視矯正(高い切除量):より深い切除により角膜神経の温存率が低下する
術前のマイボーム腺機能不全(MGD):術後の蒸発亢進型ドライアイのリスクが高い
コンタクトレンズ長期装用歴:術前からの角膜神経密度低下・涙液層異常が術後に悪化しやすい
ドライアイのサブタイプ(TFOD)
Section titled “ドライアイのサブタイプ(TFOD)”術後ドライアイは以下のパターンが混在することが多い。
4. 診断と検査方法
Section titled “4. 診断と検査方法”日本のドライアイ診断基準(2016年改訂)
Section titled “日本のドライアイ診断基準(2016年改訂)”以下の2項目をともに満たせばドライアイと確定診断される2)。
- 自覚症状(眼不快感・視機能異常)がある
- 涙液層破壊時間(BUT)が5秒以下
屈折矯正手術後は術前から定期的にBUT・自覚症状を評価することで、術後変化を客観的に評価できる。
検査の順序と推奨項目
Section titled “検査の順序と推奨項目”術後ドライアイの診断には以下の検査が推奨される(涙液に影響を与えにくい順)。
| 検査項目 | 評価内容 | 異常基準 |
|---|---|---|
| 自覚症状評価(OSDI/SPEED) | 症状の頻度・重症度 | OSDI≥13が軽症 |
| 涙液メニスカス観察 | 涙液量の多寡(細隙灯) | 0.25mm未満で低下 |
| NIBUT(非侵襲的BUT) | 涙液安定性(非侵襲) | 短縮(機器依存) |
| フルオレセインBUT | 涙液安定性(標準法) | 5秒以下で異常 |
| フルオレセイン染色 | 角結膜上皮障害 | SPK所見 |
| Schirmer I試験 | 涙液分泌量 | 5mm/5分以下で異常 |
| 角膜知覚検査(Cochet-Bonnet) | 角膜神経機能 | 45mm以下で低下 |
| マイボグラフィ | マイボーム腺構造 | 腺消失・閉塞 |
角膜知覚検査は屈折矯正手術後のドライアイ特有の検査であり、術後の角膜神経切断の程度を評価するために有用である。
TFOD(Tear Film Oriented Diagnosis)によるサブタイプ診断
Section titled “TFOD(Tear Film Oriented Diagnosis)によるサブタイプ診断”開瞼直後の涙液層破綻パターンを観察し、ドライアイのサブタイプを特定する。術後ドライアイではSpot/Dimple break(水濡れ低下型)とLine break(涙液減少型)の混合が多く、TFOTに直結した診断が可能となる。
術前スクリーニング
Section titled “術前スクリーニング”屈折矯正手術前に以下を評価し、術前からドライアイ治療を開始することが推奨される3)。
- OSDI等の自覚症状スコアリング(OSDI≥13が軽症の目安)
- BUT・Schirmer値(BUT5秒以下・Schirmer5mm/5分以下は術前治療の適応)
- マイボグラフィ・眼瞼縁評価(MGDの有無と重症度の確認)
- 角膜・結膜染色(リサミングリーン・フルオレセイン)
- 角膜知覚検査(Cochet-Bonnet)
- 非侵襲的涙液破綻時間(NIBUT)
術前にドライアイを検出し積極的に治療することで、術後の視覚的転帰と患者満足度が改善する3)。特にMGDを合併する場合、術前のIPL治療・LipiFlow・温罨法を行うことで術後3か月のOSDI・BUTが有意に改善することが報告されており3)、術前の眼表面最適化は術後ドライアイ予防の最も効果的な戦略の一つである。屈折矯正手術のガイドライン(第8版)1)では、ドライアイは実施に慎重を要する因子として位置づけられており、眼球乾燥症候群はSMILEの絶対禁忌とされている。
術前にドライアイがあっても、LASIK施行後の有用性と安全性は非ドライアイ患者と同等と考えられています2)。ただし、術前にドライアイの患者はLASIK後もドライアイの程度が強い状態が続きやすいため、術前から積極的にドライアイ治療を行い、眼表面の状態を最適化してから手術を行うことが重要です。MGD(マイボーム腺機能不全)がある場合は、LipiFlowや温罨法で術前治療を行うことで術後3か月のOSDI・BUTが有意に改善したとの報告があります3)。
5. 標準的な治療法
Section titled “5. 標準的な治療法”TFOT(Tear Film Oriented Therapy)— 層別治療
Section titled “TFOT(Tear Film Oriented Therapy)— 層別治療”TFODで特定した涙液層安定性低下の原因に基づき、原因層に応じた治療を選択する(TFOT)。
TFOT 層別治療対応表:
| 治療対象層 | 治療法 |
|---|---|
| 液層(涙液減少型) | ジクアホソルナトリウム点眼、ヒアルロン酸点眼、涙点プラグ |
| 油層(蒸発亢進型・MGD) | 温罨法、眼瞼清拭、ジクアホソルナトリウム(油層伸展促進)、IPL、LipiFlow |
| 分泌型・膜型ムチン | ジクアホソルナトリウム、レバミピド |
| 上皮・杯細胞 | レバミピド、自己血清点眼 |
| 炎症(難治性) | ステロイド短期使用、シクロスポリン点眼 |
術後ドライアイの特異性として、角膜知覚低下(神経切断)による「知覚型ドライアイ(neurotrophic component)」が合併することに注意する。知覚低下がある場合はTFOT標準治療に加えて、神経回復を促進する治療(オメガ3脂肪酸・PRGF・自己血清点眼等)を補助的に追加することが有効である3)。
点眼薬治療(第一選択)
Section titled “点眼薬治療(第一選択)”術後ドライアイの第一選択治療は防腐剤フリーの人工涙液・ムチン産生促進薬である。
3% ジクアホソルナトリウム点眼液(ジクアス®): P2Y2受容体作動薬。水分・ムチン分泌促進と油層伸展促進の複合作用を持つ。術後ドライアイへの有効性が示されており、ドライアイ診療ガイドラインは「実施する」推奨(強い推奨)としている2)。フェムト秒LASIKの61眼を対象としたRCTで、3%ジクアホソル+0.15% HA点眼が0.15% HA単独よりOSDI・TBUT・脂質層を有意に改善したことが報告されている3)。
2% レバミピド点眼液UD(ムコスタ®点眼液UD): ムチン産生促進・抗炎症作用を持つ。角膜屈折矯正手術後のドライアイ60眼を対象としたRCTで、レバミピド4回/日が人工涙液に比べSchirmer値・BUT・角膜染色・乱反射指数を有意に改善したことが報告されている3)。
0.1% / 0.3% ヒアルロン酸ナトリウム点眼液(ヒアレイン®): 角膜上皮保護・水分保持。防腐剤フリー製剤(ヒアレインミニ®)が望ましい。TFOS DEWS IIIでは、HAを含む多くの涙液補充剤が術後ドライアイの症状・所見を改善することが確認されている5)。
処方例(術後軽〜中等症)
Section titled “処方例(術後軽〜中等症)”- ジクアス点眼液(3%)1日6回
- ヒアレインミニ点眼液(0.1%)乾燥時・頓用
- ムコスタ点眼液UD(2%)1日4回 + ヒアレインミニ(0.1%)乾燥時
処方例(術後重症・難治性)
Section titled “処方例(術後重症・難治性)”反射性分泌低下が著明な場合は防腐剤フリー点眼薬を選択する。炎症が疑われる場合は短期ステロイドを追加する。
- ヒアレインミニ点眼液(0.3%)1日6回
- フルメトロン点眼液(0.1%)1日4回(ステロイドの使用期間は必要最小限にとどめる)
- ジクアス点眼液(3%)1日6回
涙点閉鎖(涙点プラグ)
Section titled “涙点閉鎖(涙点プラグ)”点眼治療で効果不十分な涙液減少型ドライアイに適応がある。ドライアイ診療ガイドラインは涙点プラグを「実施する」推奨としており、LASIK後ドライアイへの涙点プラグ治療前後で症状の改善が報告されている2)。
シリコンプラグ: スーパーイーグル™プラグ、パンクタルプラグ®F等。永続的な閉鎖を提供する。
液体コラーゲンプラグ(キープティア®): アテロコラーゲン製液体プラグ。体温(36℃)でゲル化し涙小管を閉塞する。一時的なドライアイ増悪期に適する。保管は2〜10℃冷蔵。
マイボーム腺機能不全(MGD)の治療
Section titled “マイボーム腺機能不全(MGD)の治療”術後ドライアイにMGDが合併する場合は積極的に治療する3)。
温罨法・眼瞼清拭:ホットタオル(40〜42℃、5〜10分)後の眼瞼マッサージ。MGDの基本的ケア。
IPL(強度変調パルス光):2件の前向き研究でLASIK誘発難治性ドライアイ(1年以上の通常治療に反応しない中等度〜重症例)を対象に有効性が検討された。1件(42眼)では2回のIPL後にNIBUT・OSDI・涙液脂質層・マイボーム腺機能が有意に改善した。もう1件(50例のRCT)では、IPL単独よりもIPL+温熱アイマスク併用で主観的・客観的パラメータの改善が顕著であった3)。
術前MGD治療の効果: LASIK術前に既存MGDを有する患者(32例)でLASIK 1週前にベクトル化熱パルス療法を施行したところ、術後3か月のOSDI・BUTが有意に改善した3)。
IPLの周術期管理
Section titled “IPLの周術期管理”術前IPL3回(術前・術後1週・術後3週)を受けた61例のRCT(masked)では、IPL群が術後3か月のOSDI・NIBUT・TMH・マイボグラフィで有意に改善し、対照群は術後にTMHが低下した。術後6か月ではOSDIの差は縮小したが、客観的涙液パラメータの差は持続した3)。
IPLは532〜1200nmの光パルスを眼周囲に照射し、毛細血管を閉塞させることで慢性的なマイボーム腺周囲炎症を軽減し、腺分泌を改善する。通常4〜5回のセッション(3〜4週間隔)が1クールの治療として実施される。治療後に担当医がマイボーム腺を圧出することで効果が最大化される。色素性皮膚疾患・フィッツパトリック皮膚タイプVI・術後間もない(4週以内)の屈折矯正手術眼はIPLの適応外または慎重な適応となる。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”角膜神経と涙液分泌の関係
Section titled “角膜神経と涙液分泌の関係”角膜の感覚神経は主に三叉神経眼枝(V1)の鼻毛様体神経由来の角膜神経叢によって構成される。これらの神経は前実質に密な神経叢を形成し、角膜の主要な感覚入力を担う。
LASIK術中のフラップ作成(マイクロケラトームまたはフェムト秒レーザー)は、前実質神経叢を周方向に広範囲に切断する。この神経切断が以下の連鎖を引き起こす。
反射弓の遮断:
- 角膜表面刺激(求心性経路)→ 三叉神経核 → 涙腺への副交感神経(遠心性経路)が切断される
- 反射性涙液分泌(基礎分泌・反射分泌の両方)が著明に低下する
- 涙液量の減少 → 角結膜上皮の乾燥 → BUT短縮
膜型ムチンへの影響: 角膜神経は角膜上皮への神経栄養因子供給源でもある。神経切断後は神経栄養因子(EGF・NGF等)の供給が減少し、膜型ムチン(MUC16)の発現が低下する。ムチン発現低下 → 水濡れ性低下 → Spot/Dimple break(水濡れ低下型ドライアイ)が生じる。
神経再生の経過:
- 角膜神経は術後6〜12か月にかけて徐々に再生する
- LASIK後は360°神経切断のため再生に時間を要する。多くの症例で1年以内に8割程度が回復するが、一部では数年を要することがある
- SMILE後は2〜3mmの小切開のみのため神経密度の回復が速い4)
- in vivo共焦点顕微鏡(IVCM)により角膜神経密度を経時的に評価することで、神経回復を客観的にモニタリングすることが可能である
- 角膜知覚低下が6か月以上持続する場合は神経栄養性角膜症への移行リスクがあり、神経成長因子(NGF)点眼の適応を検討する
SMILE vs LASIKの神経保護
Section titled “SMILE vs LASIKの神経保護”SMILEは2〜3mmの小切開のみで角膜実質内レンチクルを摘出するため、周方向の神経切断が最小限となる。FS-LASIKとSMILEの比較研究で、SMILEがFS-LASIKより術後の角膜神経密度の回復が速く、涙液パラメータへの影響が小さいことが報告された4)。
手術に伴う炎症がMGD機能を一時的に悪化させ、蒸発亢進型ドライアイを促進する。LASIK術後の結膜・角膜実質への炎症性サイトカイン(MMP-9・IL-1β等)浸潤が涙液層の不安定化に関与する。シクロスポリン点眼は、LASIKを含む各種屈折矯正手術後のOSDI・BUT・角膜感度を有意に改善するとの報告がある3)。
術後炎症は多くの場合1〜3か月で自然軽快するが、術前のアレルギー性結膜疾患・MGD合併例・ステロイドレスポンダー等では炎症の遷延・悪化が生じやすい。術後に長期のステロイド点眼が必要な場合は、眼圧モニタリングを定期的に行い、IFS(インターフェース液症候群)との関連にも注意が必要である。
角膜形状変化と眼表面の関係
Section titled “角膜形状変化と眼表面の関係”屈折矯正手術による角膜形状の変化が上まぶたと角膜の接触様式(lid-globe apposition)に影響を与え、涙液の分布・拡散に変化をきたすことがある。特に強度近視矯正後の角膜偏平化が涙液拡散を阻害する可能性が示唆されている。
また、術後の角膜知覚低下は瞬目反射を減弱させ、完全瞬目の回数を減少させる。これにより涙液の機械的拡散と油層の再分布が阻害され、蒸発亢進型ドライアイが助長される。完全瞬目トレーニング(意識的な完全瞬目の練習)は術後のドライアイ管理において推奨されるセルフケアの一つとされている3)。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”TFOS DEWS III(2025)の推奨
Section titled “TFOS DEWS III(2025)の推奨”TFOS DEWS III(2025)は、角膜屈折矯正手術の前後における眼表面の最適化を標準治療として推奨することを提言している5)。特に、蒸発亢進型ドライアイ(MGD)を有する患者に対して術前介入を行うことで、術後の眼表面状態・視覚パラメータが改善することが複数の前向き研究で示されている3)。
TFOS DEWS IIIではまた、次世代の涙液補充剤(たとえばperfluorohexyloctane・シルク由来タンパク・rhPRG4等)について最新のエビデンスが整理されており、これらが標準HA点眼に加わる治療選択肢として期待されている5)。
ボツリヌス毒素(ボトックス)の試験的使用
Section titled “ボツリヌス毒素(ボトックス)の試験的使用”下眼瞼内側へのボツリヌス毒素注射がDEDの症状・所見を改善するとの報告がある。さらに、ボツリヌス毒素がLASIK後ドライアイ症状を涙点プラグや点眼薬より少ない合併症で有意に改善したという研究もあり、今後の選択肢として注目されている3)。ボツリヌス毒素は涙小管の収縮を抑制することで涙液の排出を遅らせ、眼表面に滞留する涙液量を増加させる機序が考えられている。ただし眼瞼下垂・複視等の副作用のリスクがあり、専門施設での施行が必要である。
PRGF(Plasma Rich in Growth Factors)点眼
Section titled “PRGF(Plasma Rich in Growth Factors)点眼”LASIK術後のドライアイ患者を対象とした後ろ向き比較研究(77眼)で、PRGF点眼が通常の人工涙液と比較して、視力・TBUT・OSDI・症状スコア・Schirmer値を有意に改善した3)。PRGFは成長因子(EGF・NGF等)を含み角膜神経回復を促進する可能性がある。自己血清点眼は患者自身の血清から作製する類似の生物学的点眼薬であり、角膜神経障害に伴う難治性ドライアイに対して有効性が示されている。ただし自己血清・PRGF点眼の作製・使用には専門施設でのプロトコル管理が必要である3)。
神経栄養因子の応用
Section titled “神経栄養因子の応用”オメガ3脂肪酸摂取と角膜神経パラメータ改善の関連が示唆されており、屈折矯正手術後の角膜神経回復補助として注目されている5)。神経栄養性角膜症や術後の角膜神経障害に対する神経栄養因子(NGF)点眼の研究も進行中である。
低レベル光療法(LLLT)
Section titled “低レベル光療法(LLLT)”TFOS DEWS IIIでは低レベル光療法(LLLT)がMGD合併のドライアイに対してIPLと同様の効果をもつ可能性が示されており、非接触・無痛での新しい治療選択肢として研究が進んでいる5)。LLLTは633〜850nmの近赤外光を眼周囲に照射し、マイボーム腺の機能を改善するとともに抗炎症・組織再生促進効果をもつとされる。術後ドライアイへの応用はまだ臨床エビデンスが限られているが、IPLが適応外の患者(色素性病変合併例等)や、より低侵襲な治療を希望する患者の選択肢として期待されている5)。
KLExガイドラインにおける術後ドライアイ管理
Section titled “KLExガイドラインにおける術後ドライアイ管理”Wang et al.6)のKLEx(小切開角膜片抽出術)国際ガイドラインでは、SMILE術後の眼表面管理についてもエビデンスに基づく推奨が示されており、術前からのドライアイ評価と術後の積極的な点眼治療が推奨されている。SMILEはLASIKよりも術後ドライアイリスクが低いが、術前のドライアイ状態を改善してから手術を行うことが最善とされている6)。
角膜拡張症PPPとドライアイの関連
Section titled “角膜拡張症PPPとドライアイの関連”AAO角膜拡張症PPP7)では、術後エクタジアの管理において角膜神経障害に伴うドライアイの合併が認識されており、不正乱視補正(RGP・強膜レンズ等)とドライアイ治療の並行管理が必要とされる。強膜レンズは不正乱視矯正とドライアイ症状改善の双方に有効な選択肢として位置づけられている7)。
角膜tensile strengthとドライアイ
Section titled “角膜tensile strengthとドライアイ”Reinstein et al.8)の数学モデルは、SMILEが前部角膜実質を相対的に温存しうることを示した。術後ドライアイとの関連は、この力学モデルだけでなく、角膜神経と涙液指標を扱う臨床研究と組み合わせて解釈する必要がある4, 8)。
エクタジア発生率の比較とドライアイ
Section titled “エクタジア発生率の比較とドライアイ”Moshirfar et al.9)の系統的レビューは、術後エクタジアのリスク評価を整理したものである。術式選択では、エクタジアリスク評価と術前ドライアイ評価を別々に行い、角膜形状・切除量・涙液状態を総合して判断する。
進行性角膜拡張症とドライアイの合併管理
Section titled “進行性角膜拡張症とドライアイの合併管理”Gomes et al.10)の国際コンセンサスでは、角膜拡張症患者はドライアイを高率に合併することが示されており、CXL(角膜クロスリンキング)前後の眼表面管理において涙液補充と抗炎症治療を積極的に行うことが推奨されている10)。
レバミピドの有効性に関するRCT
Section titled “レバミピドの有効性に関するRCT”Igarashi et al.11)は角膜屈折矯正手術後ドライアイを対象としたRCTで、2%レバミピド点眼液が人工涙液と比較してSchirmer値・BUT・角膜染色スコア・乱反射指数を有意に改善したことを報告した。レバミピドはムチン産生促進と抗炎症の複合作用を有し、術後ドライアイにおける水濡れ低下型とムチン減少型の両者に有効であることが示されている11)。
KERALINK試験における眼表面管理の示唆
Section titled “KERALINK試験における眼表面管理の示唆”Larkin et al.12)のKERALINK試験では若年の円錐角膜患者に対するCXLの有効性が示されたが、試験中の点眼管理において涙液補充剤の継続使用が推奨されており、角膜拡張症とドライアイの合併管理の重要性が改めて示された12)。
PTA(percent tissue altered)とドライアイリスク
Section titled “PTA(percent tissue altered)とドライアイリスク”Santhiago et al.13)はPTA≥40%が術後エクタジアのリスク因子であることを示した。深い切除は角膜神経にも影響しうるため、術式設計ではエクタジアリスクとドライアイリスクを並行して評価することが合理的である4, 13)。
Randlemanリスクスコアとドライアイ術前評価の統合
Section titled “Randlemanリスクスコアとドライアイ術前評価の統合”Randleman et al.14)のエクタジアリスクスコアリングシステムは、角膜形状・残存実質厚・近視量などを評価する枠組みである。術前にはこれと別にBUT・Schirmer・OSDIなどでドライアイを評価し、術後合併症のリスクを総合的に見積もる。
forme fruste角膜拡張症とドライアイの関連
Section titled “forme fruste角膜拡張症とドライアイの関連”Seiler et al.15)が報告したforme fruste keratoconusへのLASIK後エクタジアは、潜伏型角膜拡張症の術前評価が重要であることを示す初期報告である。ドライアイ重症化リスクは、角膜形状リスクとは別に術前から評価する。
8. 参考文献
Section titled “8. 参考文献”-
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第8版). 日眼会誌. 2024;128(2):135-138.
-
ドライアイ研究会診療ガイドライン作成委員会(島﨑潤ほか). ドライアイ診療ガイドライン. 日本眼科学会雑誌. 2019;123(5):489-592.
-
Jones L, Downie LE, Korb D, et al. TFOS DEWS III: Management and Therapy. Am J Ophthalmol. 2025;279:289-386.
-
Recchioni A, Sisó-Fuertes I, Hartwig A, et al. Short-term impact of FS-LASIK and SMILE on dry eye metrics and corneal nerve morphology. Cornea. 2020;39(7):851-857.
-
Jones L, Craig JP, Markoulli M, et al. TFOS DEWS III: Management and Therapy report. Am J Ophthalmol. 2025;279:289-386.
-
Wang Y, Xie L, Yao K, et al. Evidence-Based Guidelines for Keratorefractive Lenticule Extraction Surgery. Ophthalmology. 2025;132:397-419.
-
American Academy of Ophthalmology Corneal/External Disease Preferred Practice Pattern Panel. Corneal Ectasia Preferred Practice Pattern. San Francisco, CA: AAO; 2024.
-
Reinstein DZ, Archer TJ, Randleman JB. Mathematical model to compare the relative tensile strength of the cornea after PRK, LASIK, and SMILE. J Refract Surg. 2013;29:454-460.
-
Moshirfar M, Tukan AN, Bundogji N, et al. Ectasia after corneal refractive surgery: a systematic review. Ophthalmol Ther. 2021;10:753-776.
-
Gomes JA, Tan D, Rapuano CJ, et al. Global consensus on keratoconus and ectatic diseases. Cornea. 2015;34:359-369.
-
Igarashi T, Ogawa K, Utsugi C, et al. Rebamipide ophthalmic suspension for dry eye after refractive surgery: a randomized controlled trial. Jpn J Ophthalmol. 2015;59(5):349-355.
-
Larkin DFP, Chowdhury K, Burr JM, et al. Effect of corneal cross-linking versus standard care on keratoconus progression in young patients: The Keralink randomized controlled trial. Ophthalmology. 2021;128:1516-1526.
-
Santhiago MR, Smadja D, Gomes BF, et al. Association between the percent tissue altered and post-LASIK ectasia in eyes with normal preoperative topography. Am J Ophthalmol. 2014;158:87-95.e1.
-
Randleman JB, Woodward M, Lynn MJ, Stulting RD. Risk assessment for ectasia after corneal refractive surgery. Ophthalmology. 2008;115:37-50.
-
Seiler T, Quurke AW. Iatrogenic keratectasia after LASIK in a case of forme fruste keratoconus. J Cataract Refract Surg. 1998;24:1007-1009.
