不同術式的風險比較

屈光矯正手術後乾眼症
1. 什麼是屈光矯正手術後的乾眼
Section titled “1. 什麼是屈光矯正手術後的乾眼”屈光矯正手術後乾眼(post-refractive surgery dry eye)是指進行LASIK(雷射原位角膜磨鑲術)、PRK(光屈光性角膜切除術)、SMILE(小切口角膜基質透鏡取出術)等改變角膜形狀的屈光矯正手術後發生的乾眼。
乾眼定義為「因各種因素導致淚膜穩定性下降,引起眼部不適和視功能異常,並可能伴隨眼表損傷的疾病」。屈光矯正手術後乾眼是此定義中「各種因素」裡,以角膜手術導致的角膜神經切斷、淚腺反射弧阻斷為主要原因的類型。
有研究指出,角膜上皮損傷和淚膜破裂時間(BUT)縮短很可能由包括LASIK、PRK在內的眼前段手術普遍誘發。淚液分泌量(Schirmer值)在進行角膜切開或切除的手術中可能下降2)。
屈光矯正手術指南(第8版)中,乾眼被明確列為LASIK術後併發症之一1),要求術前評估和積極管理。
術後乾眼的時間進程
Section titled “術後乾眼的時間進程”術後早期的乾眼症狀通常在6~12個月內改善,但少數病例會轉變為對常規治療無效的難治性乾眼3)。
2. 主要症狀和臨床所見
Section titled “2. 主要症狀和臨床所見”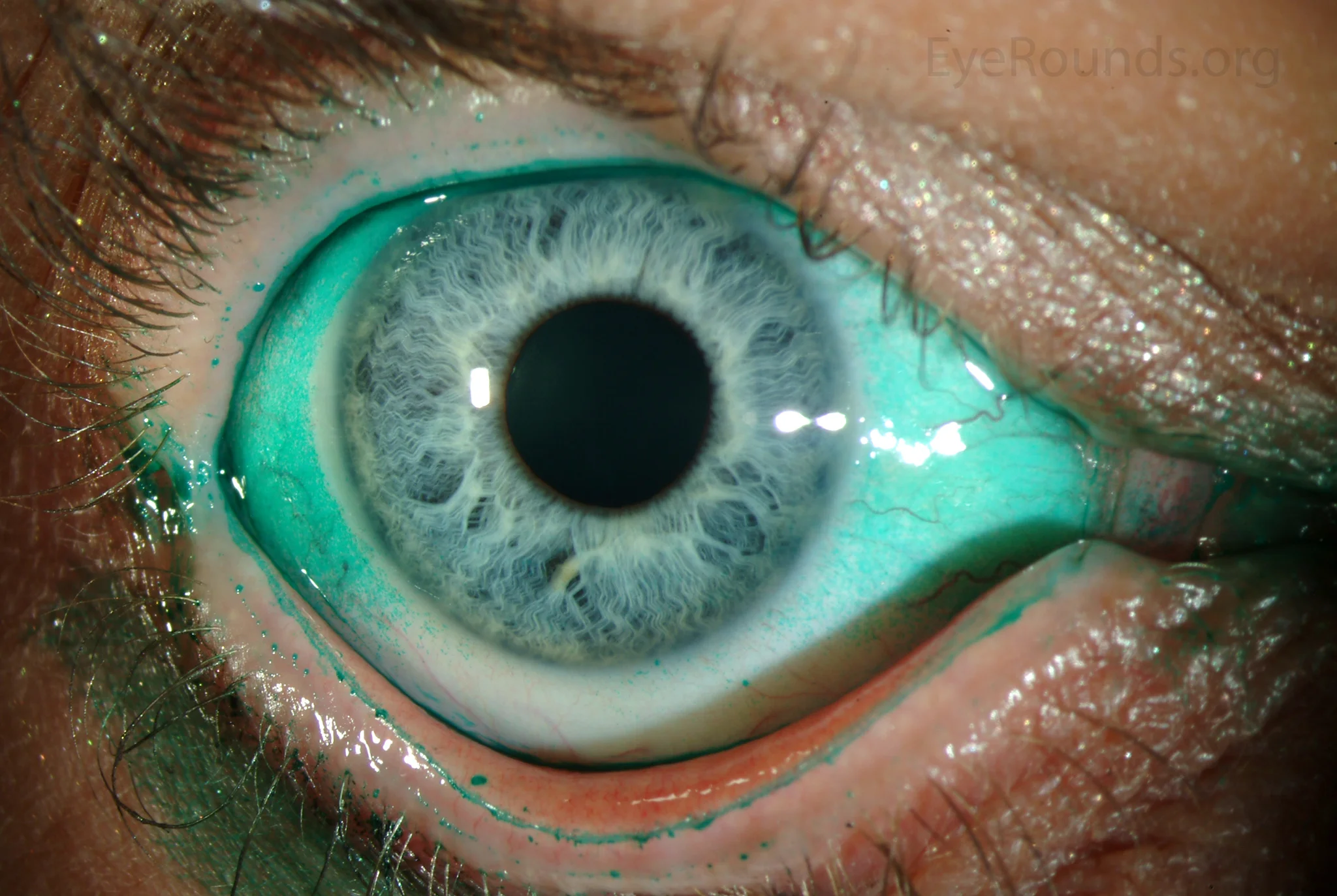
屈光矯正手術後乾眼的症狀與普通乾眼相同,但與視功能相關的症狀更突出。
- 乾燥感、異物感、灼熱感、眼痛
- 霧視、視力波動(瞬目後暫時改善)
- 畏光、眩光
- 隱形眼鏡配戴不適(術前有配戴者)
淚膜變化:
- 淚膜破裂時間(BUT)縮短(≤5秒為異常)
- Schirmer試驗值降低(≤5 mm/5 min)
- 淚河高度降低(<0.25 mm)
- 蒸發亢進導致脂質層不均勻
角膜知覺變化:
淚膜破裂模式(TFOD):
- 點狀破裂(濕潤性下降型):點狀早期破裂,主要因角膜神經切斷後黏蛋白層異常
- 線狀破裂(淚液減少型):線狀破裂,因反射性分泌減少
- Area break:廣泛早期破裂
3. 原因與風險因素
Section titled “3. 原因與風險因素”角膜神經切斷的病理生理
Section titled “角膜神經切斷的病理生理”LASIK術後乾眼的主要機制如下:
- 製作角膜瓣時,前基質中的角膜神經叢(源自三叉神經眼支)被廣泛切斷
- 經由三叉神經傳遞至淚腺的反射訊號被阻斷 → 基礎分泌與反射性分泌減少
- 角膜知覺下降導致眨眼反射減弱 → 不完全眨眼增加 → 蒸發增強
- 淚液量減少與穩定性下降 → 角結膜上皮損傷的惡性循環
- 術後發炎導致瞼板腺功能暫時惡化 → 增加蒸發過強型因素
術前風險因素
乾眼的亞型(TFOD)
Section titled “乾眼的亞型(TFOD)”術後乾眼常混合以下模式。
- 水液缺乏型(ATD):Schirmer試驗值低。主要由反射性分泌減少引起。
- 蒸發過強型(EDE):合併MGD。脂質層不均勻,BUT縮短。
- 濕潤性降低型(LWE):角膜神經切斷後黏蛋白分泌和膜結合黏蛋白減少。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”日本乾眼診斷標準(2016年修訂版)
Section titled “日本乾眼診斷標準(2016年修訂版)”滿足以下兩項即可確診為乾眼2)。
- 有自覺症狀(眼部不適、視功能異常)
- 淚膜破裂時間(BUT)≤5秒
屈光矯正手術後,透過術前和術後定期評估BUT和自覺症狀,可以客觀評價術後變化。
檢查順序與建議項目
Section titled “檢查順序與建議項目”術後乾眼的診斷建議進行以下檢查(依對淚液影響最小的順序)。
| 檢查項目 | 評估內容 | 異常標準 |
|---|---|---|
| 主觀症狀評估(OSDI/SPEED) | 症狀頻率和嚴重程度 | OSDI≥13為輕度 |
| 淚液半月板觀察 | 淚液量(裂隙燈) | <0.25 mm表示減少 |
| NIBUT(非侵入性淚膜破裂時間) | 淚膜穩定性(非侵入性) | 縮短(取決於設備) |
| 螢光素淚膜破裂時間 | 淚膜穩定性(標準方法) | ≤5秒為異常 |
| 螢光素染色 | 角結膜上皮損傷 | SPK所見 |
| Schirmer I試驗 | 淚液分泌量 | ≤5mm/5分鐘為異常 |
| 角膜知覺檢查(Cochet-Bonnet) | 角膜神經功能 | ≤45mm為降低 |
| 瞼板腺攝影 | 瞼板腺結構 | 腺體消失與阻塞 |
角膜知覺檢查是屈光矯正手術後乾眼的特有檢查,有助於評估術後角膜神經切斷的程度。
基於TFOD(淚膜導向診斷)的亞型診斷
Section titled “基於TFOD(淚膜導向診斷)的亞型診斷”觀察睜眼後即刻的淚膜破裂模式,以確定乾眼亞型。術後乾眼常表現為斑點/凹點破裂(濕潤不良型)和線狀破裂(淚液減少型)的混合,可直接進行TFOT導向的診斷。
屈光矯正手術前應評估以下項目,並建議術前開始乾眼治療3)。
- 主觀症狀評分如OSDI(OSDI≥13為輕度乾眼的參考值)
- BUT和Schirmer值(BUT≤5秒、Schirmer≤5mm/5分鐘為術前治療的適應症)
- 瞼板腺成像和眼瞼邊緣評估(確認MGD的有無及嚴重程度)
- 角膜和結膜染色(麗莎明綠、螢光素)
- 角膜知覺檢查(Cochet-Bonnet)
- 非侵入性淚膜破裂時間(NIBUT)
術前檢測並積極治療乾眼可改善術後視覺結果和患者滿意度3)。特別是合併MGD時,術前進行IPL治療、LipiFlow或熱敷可顯著改善術後3個月的OSDI和BUT3)。術前眼表優化是預防術後乾眼最有效的策略之一。屈光矯正手術指南(第8版)1)將乾眼列為需謹慎實施的因素,眼球乾燥症候群是SMILE的絕對禁忌症。
5. 標準治療方法
Section titled “5. 標準治療方法”TFOT(淚膜導向治療)——分層治療
Section titled “TFOT(淚膜導向治療)——分層治療”根據TFOD確定的淚膜層穩定性下降的原因,選擇針對相應層的治療(TFOT)。
TFOT分層治療對應表:
| 治療目標層 | 治療方法 |
|---|---|
| 水液層(淚液分泌不足型) | 地夸磷索鈉眼藥水、玻尿酸眼藥水、淚點栓塞 |
| 脂質層(蒸發過強型/MGD) | 熱敷、眼瞼清潔、地夸磷索鈉(促進脂質層擴展)、IPL、LipiFlow |
| 分泌型及膜型黏蛋白 | 地夸磷索鈉、瑞巴派特 |
| 上皮細胞/杯狀細胞 | 瑞巴派特、自體血清眼藥水 |
| 發炎(難治性) | 短期使用類固醇、環孢素眼藥水 |
注意術後乾眼的特異性:可能合併因角膜知覺減退(神經切斷)導致的「神經營養性乾眼」。知覺減退時,在TFOT標準治療基礎上,輔助添加促進神經恢復的治療(如Omega-3脂肪酸、PRGF、自體血清眼藥水等)是有效的3)。
眼藥水治療(第一線治療)
Section titled “眼藥水治療(第一線治療)”術後乾眼的第一線治療是無防腐劑的人工淚液和黏蛋白促泌劑。
3%地夸磷索鈉點眼液(Diquas®): P2Y2受體促效劑。具有促進水分與黏液素分泌及促進油層擴散的複合作用。已證實對術後乾眼有效,乾眼診療指引建議「實施」(強烈建議)2)。一項針對61眼飛秒LASIK的RCT報告,3%地夸磷索+0.15% HA點眼液比0.15% HA單用顯著改善OSDI、TBUT及脂質層3)。
2%瑞巴派特點眼液UD(Mucosta®點眼液UD): 促進黏液素產生並具抗發炎作用。一項針對60眼角膜屈光手術後乾眼的RCT報告,瑞巴派特每日4次比人工淚液顯著改善Schirmer值、BUT、角膜染色及不規則指數3)。
0.1%/0.3%玻尿酸鈉點眼液(Hyalein®): 角膜上皮保護與保濕。建議使用不含防腐劑的製劑(Hyalein Mini®)。TFOS DEWS III確認,包括HA在內的許多淚液補充劑可改善術後乾眼的症狀與徵象5)。
處方範例(術後輕至中度)
Section titled “處方範例(術後輕至中度)”- Diquas點眼液(3%)每日6次
- Hyalein Mini點眼液(0.1%)乾燥時按需使用
- Mucosta點眼液UD(2%)每日4次 + Hyalein Mini(0.1%)乾燥時按需使用
處方範例(術後重度或難治性)
Section titled “處方範例(術後重度或難治性)”如果反射性分泌減少明顯,選擇不含防腐劑的點眼液。如果懷疑有發炎,短期加用類固醇。
- Hyalein Mini點眼液(0.3%)每日6次
- 氟美瞳點眼液(0.1%)每日4次(類固醇使用時間限制在必要最短期間)
- Diquas點眼液(3%)每日6次
淚點栓塞(淚點塞)
Section titled “淚點栓塞(淚點塞)”適用於點眼液治療無效的水液缺乏型乾眼。乾眼診療指引建議「實施」淚點塞,有報告指出LASIK術後乾眼在淚點塞治療前後症狀改善2)。
矽膠塞:Super Eagle™塞、Punctal Plug® F等。提供永久性封閉。
液體膠原蛋白塞(Keeptear®):由去端肽膠原蛋白製成的液體塞。在體溫(36°C)下凝膠化並阻塞淚小管。適用於乾眼症的暫時性惡化期。需在2–10°C冷藏保存。
瞼板腺功能障礙(MGD)的治療
Section titled “瞼板腺功能障礙(MGD)的治療”如果術後乾眼合併MGD,應積極治療3)。
熱敷和眼瞼清潔:熱毛巾(40–42°C,5–10分鐘)後進行眼瞼按摩。MGD的基礎護理。
IPL(強脈衝光):兩項前瞻性研究評估了其對LASIK誘發的難治性乾眼(常規治療1年以上無效的中重度病例)的療效。一項研究(42眼)顯示,兩次IPL後NIBUT、OSDI、淚液脂質層和瞼板腺功能顯著改善。另一項RCT(50例)發現,IPL聯合熱敷眼罩比單獨IPL更能改善主觀和客觀參數3)。
術前MGD治療的效果:在LASIK術前已有MGD的患者(32例)中,術前1週進行向量熱脈衝治療,術後3個月的OSDI和BUT顯著改善3)。
IPL的圍手術期管理
Section titled “IPL的圍手術期管理”在一項包含61例患者的設盲RCT中,術前接受3次IPL(術前、術後1週、術後3週)的IPL組在術後3個月的OSDI、NIBUT、TMH和瞼板腺成像方面顯著改善,而對照組術後TMH下降。術後6個月時,OSDI的差異縮小,但客觀淚液參數的差異持續存在3)。
IPL將532–1200 nm的光脈衝照射到眼周區域,通過閉塞毛細血管減少瞼板腺周圍的慢性炎症,改善腺體分泌。通常4–5次治療(間隔3–4週)為一個療程。治療後由醫生擠壓瞼板腺可最大化效果。色素性皮膚病變、Fitzpatrick皮膚類型VI以及術後4週內的屈光手術眼是IPL的禁忌或需謹慎使用。
對於常規眼藥水治療無效的LASIK術後難治性乾眼,IPL(強脈衝光)、熱敷和向量熱脈衝治療(LipiFlow)被認為是有效的3)。IPL可改善瞼板腺功能、NIBUT、OSDI和脂質層。IPL聯合熱敷眼罩比單獨IPL更有效。難治病例也可選擇自體血清眼藥水(PRGF)。
6. 病理生理學與詳細發病機制
Section titled “6. 病理生理學與詳細發病機制”角膜神經與淚液分泌的關係
Section titled “角膜神經與淚液分泌的關係”角膜的感覺神經主要由三叉神經眼支(V1)的鼻睫神經來源的角膜神經叢構成。這些神經在前基質形成密集的神經叢,負責角膜的主要感覺輸入。
LASIK術中製作角膜瓣(使用微型角膜刀或飛秒雷射)會沿周向廣泛切斷前基質神經叢。這種神經切斷會引發以下連鎖反應。
反射弧阻斷:
- 角膜表面刺激(傳入路徑)→ 三叉神經核 → 淚腺的副交感神經(傳出路徑)被切斷
- 反射性淚液分泌(基礎分泌和反射分泌)顯著減少
- 淚液量減少 → 角結膜上皮乾燥 → 淚膜破裂時間(BUT)縮短
對膜結合型黏蛋白的影響: 角膜神經也是角膜上皮神經營養因子的來源。神經切斷後,神經營養因子(如EGF、NGF)的供應減少,導致膜結合型黏蛋白(MUC16)表現下降。黏蛋白表現下降 → 濕潤性降低 → 出現點狀/凹痕狀破裂(濕潤性降低型乾眼)。
神經再生的過程:
- 角膜神經在術後6至12個月逐漸再生
- LASIK術後因360°神經切斷,再生需要時間。多數病例在1年內恢復約80%,但部分病例可能需要數年
- SMILE術後僅需2-3mm小切口,因此神經密度恢復較快4)
- 透過活體共聚焦顯微鏡(IVCM)隨時間評估角膜神經密度,可以客觀監測神經恢復情況
- 如果角膜感覺減退持續超過6個月,存在進展為神經營養性角膜病的風險,應考慮使用神經生長因子(NGF)眼藥水
SMILE vs LASIK的神經保護
Section titled “SMILE vs LASIK的神經保護”SMILE僅透過2-3mm的小切口取出角膜基質內透鏡,因此對周邊神經的損傷最小。FS-LASIK與SMILE的比較研究報告,SMILE術後角膜神經密度恢復更快,對淚液參數的影響小於FS-LASIK4)。
手術相關的發炎會暫時惡化MGD功能,促進蒸發過強型乾眼。LASIK術後結膜和角膜基質中發炎細胞因子(MMP-9、IL-1β等)的浸潤與淚膜不穩定有關。有報告指出,環孢素眼藥水可顯著改善包括LASIK在內的各種屈光手術後的OSDI、BUT和角膜敏感性3)。
術後發炎通常在1-3個月內自然消退,但在術前有過敏性結膜炎、MGD或類固醇反應者中,發炎容易持續或加重。如果術後需要長期使用類固醇眼藥水,應定期監測眼壓,並注意與IFS(介面液症候群)的可能關聯。
角膜形狀變化與眼表的關係
Section titled “角膜形狀變化與眼表的關係”屈光手術引起的角膜形狀變化會影響上眼瞼與角膜的接觸方式(眼瞼-眼球貼合),從而改變淚液的分佈和擴散。特別是高度近視矯正後的角膜變平可能阻礙淚液擴散。
此外,術後角膜知覺減退會減弱眨眼反射,減少完全眨眼的次數。這會阻礙淚液的機械擴散和油脂層的重新分佈,促進蒸發過強型乾眼。完全眨眼訓練(有意識地練習完全眨眼)被認為是術後乾眼管理的推薦自我照護方法之一3)。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”TFOS DEWS III(2025)的建議
Section titled “TFOS DEWS III(2025)的建議”TFOS DEWS III(2025)建議將角膜屈光手術前後的眼表優化作為標準治療5)。多項前瞻性研究表明,對蒸發過強型乾眼(MGD)患者進行術前介入可改善術後眼表狀態和視覺參數3)。
TFOS DEWS III還總結了下一代淚液補充劑(如全氟己基辛烷、絲蛋白、rhPRG4等)的最新證據,這些有望成為標準HA眼藥水之外的額外治療選擇5)。
肉毒桿菌毒素(保妥適)的試驗性使用
Section titled “肉毒桿菌毒素(保妥適)的試驗性使用”有報告指出,下眼瞼內側注射肉毒桿菌毒素可改善DED的症狀與徵象。此外,一項研究顯示,與淚點塞或眼藥水相比,肉毒桿菌毒素能顯著改善LASIK術後乾眼症狀,且併發症較少,作為未來選擇備受關注3)。其機制被認為是肉毒桿菌毒素抑制淚小管收縮,延緩淚液排出,增加眼表淚液滯留量。但存在眼瞼下垂、複視等副作用風險,需在專業機構實施。
PRGF(富含生長因子血漿)眼藥水
Section titled “PRGF(富含生長因子血漿)眼藥水”一項針對LASIK術後乾眼患者的回顧性比較研究(77眼)顯示,與常規人工淚液相比,PRGF眼藥水顯著改善了視力、TBUT、OSDI、症狀評分和Schirmer值3)。PRGF含有生長因子(EGF、NGF等),可能促進角膜神經恢復。自體血清眼藥水是一種類似的生物眼藥水,由患者自身血清製備,已顯示對角膜神經病變引起的難治性乾眼有效。但自體血清和PRGF眼藥水的製備與使用需在專業機構進行方案管理3)。
神經營養因子的應用
Section titled “神經營養因子的應用”有研究顯示,攝取omega-3脂肪酸與角膜神經參數改善相關,作為屈光手術後角膜神經恢復的輔助手段備受關注5)。針對神經營養性角膜病變和術後角膜神經病變的神經營養因子(NGF)眼藥水研究也在進行中。
低階光療法(LLLT)
Section titled “低階光療法(LLLT)”TFOS DEWS III指出,低階光療法(LLLT)對合併MGD的乾眼可能具有與IPL相似的效果,作為一種非接觸、無痛的新治療選擇正在研究中5)。LLLT使用633-850nm的近紅外光照射眼周,改善瞼板腺功能,並具有抗炎和促進組織再生的作用。其在術後乾眼中的應用臨床證據仍有限,但有望成為IPL禁忌(如合併色素性病變)或希望更微創治療患者的選擇5)。
KLEx指南中的術後乾眼管理
Section titled “KLEx指南中的術後乾眼管理”Wang等人6)的KLEx(小切口角膜基質透鏡取出術)國際指南中,針對SMILE術後眼表管理提出了基於證據的建議,包括術前乾眼評估和術後積極眼藥水治療。雖然SMILE術後乾眼風險低於LASIK,但最好在術前改善乾眼狀態後再進行手術6)。
角膜擴張症PPP與乾眼的關聯
Section titled “角膜擴張症PPP與乾眼的關聯”AAO角膜擴張症PPP7)認知到,在術後擴張症的管理中,角膜神經損傷常伴隨乾眼症,因此需要同時進行不規則散光矯正(RGP、鞏膜鏡等)和乾眼症治療。鞏膜鏡被認為是既能矯正不規則散光又能改善乾眼症狀的有效選擇7)。
角膜拉伸強度與乾眼症
Section titled “角膜拉伸強度與乾眼症”Reinstein等人8)的數學模型顯示,SMILE可能相對保留前部角膜基質。與術後乾眼症的關聯不僅需要從此力學模型解釋,還需結合涉及角膜神經和淚液指標的臨床研究來綜合解讀4, 8)。
擴張症發生率的比較與乾眼症
Section titled “擴張症發生率的比較與乾眼症”Moshirfar等人9)的系統性回顧整理了術後擴張症的風險評估。在術式選擇中,應分別進行擴張症風險評估和術前乾眼症評估,綜合角膜形態、切削量和淚液狀態進行判斷。
進行性角膜擴張症與乾眼症的合併管理
Section titled “進行性角膜擴張症與乾眼症的合併管理”Gomes等人10)的國際共識指出,角膜擴張症患者乾眼症合併率很高,建議在CXL(角膜交聯)前後積極進行淚液補充和抗炎治療以管理眼表10)。
瑞巴派特有效性的隨機對照試驗
Section titled “瑞巴派特有效性的隨機對照試驗”Igarashi等人11)針對角膜屈光手術後乾眼症進行的隨機對照試驗報告,2%瑞巴派特滴眼液與人工淚液相比,顯著改善了Schirmer值、BUT、角膜染色評分和不規則散光指數。瑞巴派特具有促進黏蛋白分泌和抗炎的雙重作用,對術後乾眼症中的水液缺乏型和黏蛋白減少型均有效11)。
KERALINK試驗對眼表管理的啟示
Section titled “KERALINK試驗對眼表管理的啟示”Larkin等人12)的KERALINK試驗顯示了CXL在年輕圓錐角膜患者中的有效性,試驗中建議持續使用淚液補充劑,再次強調了角膜擴張症與乾眼症合併管理的重要性12)。
PTA(組織改變百分比)與乾眼症風險
Section titled “PTA(組織改變百分比)與乾眼症風險”Santhiago等人13)表明,PTA≥40%是術後擴張症的風險因素。由於深層切削也可能影響角膜神經,因此在術式設計時並行評估擴張症風險和乾眼症風險是合理的4, 13)。
Randleman風險評分與術前乾眼症評估的整合
Section titled “Randleman風險評分與術前乾眼症評估的整合”Randleman等人14)的角膜擴張風險評分系統是一個評估角膜形狀、殘餘基質厚度和近視程度的框架。術前另外透過BUT、Schirmer測試和OSDI評估乾眼,以綜合估計術後併發症的風險。
圓錐角膜頓挫型與乾眼的關聯
Section titled “圓錐角膜頓挫型與乾眼的關聯”Seiler等人15)報告的頓挫型圓錐角膜LASIK術後角膜擴張,是早期報告表明潛伏性角膜擴張的術前評估很重要。乾眼加重風險與角膜形狀風險分開,在術前進行評估。
8. 參考文獻
Section titled “8. 參考文獻”-
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第8版). 日眼会誌. 2024;128(2):135-138.
-
ドライアイ研究会診療ガイドライン作成委員会(島﨑潤ほか). ドライアイ診療ガイドライン. 日本眼科学会雑誌. 2019;123(5):489-592.
-
Jones L, Downie LE, Korb D, et al. TFOS DEWS III: Management and Therapy. Am J Ophthalmol. 2025;279:289-386.
-
Recchioni A, Sisó-Fuertes I, Hartwig A, et al. Short-term impact of FS-LASIK and SMILE on dry eye metrics and corneal nerve morphology. Cornea. 2020;39(7):851-857.
-
Jones L, Craig JP, Markoulli M, et al. TFOS DEWS III: Management and Therapy report. Am J Ophthalmol. 2025;279:289-386.
-
Wang Y, Xie L, Yao K, et al. Evidence-Based Guidelines for Keratorefractive Lenticule Extraction Surgery. Ophthalmology. 2025;132:397-419.
-
American Academy of Ophthalmology Corneal/External Disease Preferred Practice Pattern Panel. Corneal Ectasia Preferred Practice Pattern. San Francisco, CA: AAO; 2024.
-
Reinstein DZ, Archer TJ, Randleman JB. Mathematical model to compare the relative tensile strength of the cornea after PRK, LASIK, and SMILE. J Refract Surg. 2013;29:454-460.
-
Moshirfar M, Tukan AN, Bundogji N, et al. Ectasia after corneal refractive surgery: a systematic review. Ophthalmol Ther. 2021;10:753-776.
-
Gomes JA, Tan D, Rapuano CJ, et al. Global consensus on keratoconus and ectatic diseases. Cornea. 2015;34:359-369.
-
Igarashi T, Ogawa K, Utsugi C, et al. Rebamipide ophthalmic suspension for dry eye after refractive surgery: a randomized controlled trial. Jpn J Ophthalmol. 2015;59(5):349-355.
-
Larkin DFP, Chowdhury K, Burr JM, et al. Effect of corneal cross-linking versus standard care on keratoconus progression in young patients: The Keralink randomized controlled trial. Ophthalmology. 2021;128:1516-1526.
-
Santhiago MR, Smadja D, Gomes BF, et al. Association between the percent tissue altered and post-LASIK ectasia in eyes with normal preoperative topography. Am J Ophthalmol. 2014;158:87-95.e1.
-
Randleman JB, Woodward M, Lynn MJ, Stulting RD. Risk assessment for ectasia after corneal refractive surgery. Ophthalmology. 2008;115:37-50.
-
Seiler T, Quurke AW. Iatrogenic keratectasia after LASIK in a case of forme fruste keratoconus. J Cataract Refract Surg. 1998;24:1007-1009.
