術後早期(1~7天)
視力恢復:從第二天起明顯改善。多數病例從第一天起裸眼即可進行日常生活。
角膜所見:切口(2-3毫米)的上皮通常在1-2天內修復。角膜水腫在數天內消退。
注意事項:過度揉眼會導致切口處上皮損傷。

SMILE(小切口角膜基質透鏡取出術)是一種屈光矯正手術,利用飛秒雷射在角膜基質內形成屈光矯正用的透鏡(透鏡狀角膜組織),並通過2-3mm的小切口將其取出,從而矯正近視和近視散光。它與傳統的LASIK和PRK的根本區別在於不使用準分子雷射,僅用一台飛秒雷射設備即可完成。
自2008年臨床引入以來,它已成為全球最普及的雷射屈光矯正手術之一,截至2023年底全球累計超過800萬例2)。在日本,它於2023年3月22日取得藥事核准1)。最初以大切口的FLEx(飛秒雷射透鏡取出術)形式實施,但切口縮小至2-3mm的SMILE已成為標準術式。自Sekundo等人13)的首個有效性和安全性研究以來,大量研究積累,目前已被確立為高效、安全、預測性高的屈光矯正手術。
該手術的本質特徵在於「不製作角膜瓣」。LASIK首先製作角膜瓣並掀開,然後照射準分子雷射,而SMILE在不製作角膜瓣的情況下僅切除角膜基質內組織。這保持了角膜的結構連續性,保護了前角膜基質。角膜神經切斷也最小化,因此術後乾眼風險低於LASIK2)。
近視矯正範圍為等效球面度數10D(近視≤10D,散光≤3D)1)。適應年齡為18歲以上,且屈光度數穩定為前提條件1)。術前角膜形態評估(包括TBI、CBI等生物力學評估)在所有病例中均為必需,潛伏型圓錐角膜的檢測和排除是影響手術安全性的最重要因素2)。
SMILE手術的適應症為屈光不正(近視、近視性散光),有以下主訴的患者為候選適應者。
術後1~3天可能出現以下情況。通常數日內改善。
術後早期(1~7天)
視力恢復:從第二天起明顯改善。多數病例從第一天起裸眼即可進行日常生活。
角膜所見:切口(2-3毫米)的上皮通常在1-2天內修復。角膜水腫在數天內消退。
注意事項:過度揉眼會導致切口處上皮損傷。
術後1-3個月
術後併發症(需注意)
多數情況下,術後第二天即可進行不戴眼鏡的日常生活。開車通常在術後第二天視力確認後可能,但請遵從醫師指示。劇烈運動和接觸性運動通常在1-2週後允許。游泳、三溫暖等有感染風險的活動建議避免1個月以上。
了解SMILE手術的適應症、禁忌症和風險因素是安全手術的前提。
根據屈光手術指引第8版1),以下為絕對禁忌症:
根據KLEx指引2):
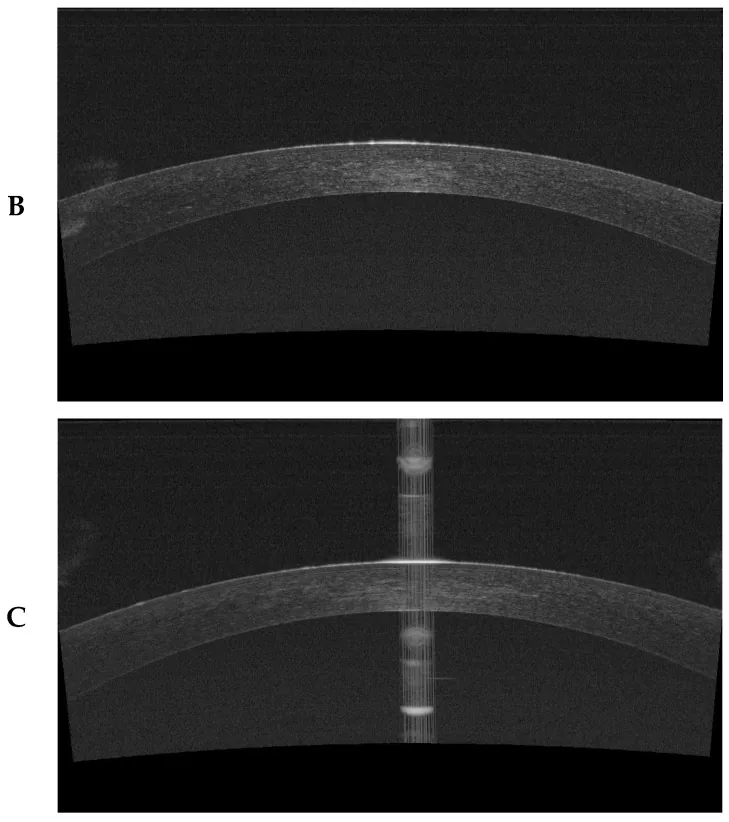
術前進行以下檢查,仔細評估適應症1)。
| 檢查項目 | 目的 | 注意事項 |
|---|---|---|
| 視力檢查(裸眼與矯正) | 基線評估 | 最佳矯正視力也必需 |
| 屈光檢查(自覺、他覺、散瞳下) | 確定矯正量 | 建議睫狀肌麻痺下屈光檢查2) |
| 角膜曲率半徑測量 | 矯正量/手術設計 | — |
| 裂隙燈顯微鏡檢查 | 眼表面及前眼部評估 | 圓錐角膜早期檢測 |
| 角膜地形圖/斷層掃描 | 圓錐角膜篩查 | 最重要檢查。推薦Scheimpflug或OCT |
| 角膜厚度測量(角膜測厚) | RST計算 | 手術設計的基礎 |
| 淚液檢查 | 乾眼評估 | 術後惡化風險評估 |
| 眼底檢查 | 近視性變化的評估 | 高度近視時還需檢查周邊部 |
| 眼壓測量 | 排除青光眼 | 低眼壓為禁忌 |
| 瞳孔直徑測量(暗室) | 光學區設計 | 夜間光暈預測 |
| 角膜直徑測量 | 手術設計 | — |
| 角膜內皮細胞檢查 | 術前基線 | SMILE的必需附加檢查1) |
| 角膜生物力學檢查(Corvis、ORA等) | 擴張症風險評估 | TBI、CBI、CRF具有參考價值2) |
圓錐角膜是絕對禁忌症,若漏診則有術後角膜擴張的風險。TBI(斷層及生物力學指數)診斷準確性最高(SUCRA 96.2%),建議與CBI(83.8%)聯合進行綜合評估2)。必須使用Scheimpflug斷層掃描(Pentacam等)對角膜前後表面及角膜厚度進行三維評估。
安全手術設計的參考標準如下2):
軟性隱形眼鏡通常需在術前1–2週停戴。硬性隱形眼鏡(透氧性、鞏膜鏡)對角膜形態影響較大,需停戴3週至1個月以上。術前檢查必須在停戴隱形眼鏡後進行。這是準確評估角膜形態不可或缺的步驟。
SMILE手術在點眼麻醉下進行,為日間手術。標準步驟如下2):
總手術時間雙眼約1530分鐘。單眼實際雷射照射時間約2540秒,非常短,患者的身心和時間負擔小。
| 分級 | 頻率 | 治療 |
|---|---|---|
| I級(僅周邊) | 1.42%2) | 局部類固醇(氟米龍每日6~8次)+ 觀察 |
| II級(延伸至中心部) | 0.29%2) | 局部類固醇強化(醋酸潑尼松龍每小時一次) |
| III級(融合/局灶性) | 0.08%2) | 高劑量類固醇 + 考慮層間沖洗 |
| IV級(重度) | 0.02%2) | 類固醇層間沖洗(必需)+ 全身性類固醇 |
透過適當的類固醇治療,大多數病例的病灶在一週內改善,約三週後症狀消失2)。
對於矯正不足或屈光回退,術後6個月以上、屈光穩定後考慮增強手術1)。選擇包括:
進行增強時必須確認殘餘角膜厚度(帽、透鏡取出腔、殘餘基質床的總和)符合安全標準(RST ≥ 280μm)2)。透過優化列線圖和AI驅動預測模型,矯正不足發生率持續改善,近年許多機構的增強率低於5%。
如果出現矯正不足、矯正過度或屈光回退,會考慮增強手術。通常在術後6個月以上、屈光穩定後決定。常見方法是用飛秒雷射在原帽面製作角膜瓣並追加準分子雷射照射。必須確認殘餘角膜厚度。
飛秒雷射在角膜基質內聚焦,透過電漿化和微光爆破形成透鏡前表面和後表面的界面。移除夾在這兩個切面之間的角膜基質(透鏡),從而改變角膜曲率,矯正近視。
透鏡的形狀(前表面和後表面的曲率差)根據屈光矯正量設計。移除中央厚、周邊薄的凸透鏡狀基質片,降低角膜屈光力,矯正近視。
透鏡的最小厚度通常認為在1520 μm以上,低於此厚度時安全取出可能困難。在散光矯正中,為了精確定位非對稱透鏡形狀(軸不對稱),角膜緣標記和眼動追蹤系統的精確度很重要6)。SMILE的光學區直徑通常設定為6.07.0 mm,但KLEx指南顯示,較大的光學區(≥6.5 mm)術後高階像差(尤其是彗差)較少,夜間視覺功能較好2),因此在角膜厚度足夠時建議設定較大的光學區。然而,擴大光學區會增加切除量(→RST減少),因此需要個別化設計,平衡生物力學和視覺功能2)。
SMILE比LASIK更好地保持角膜生物力學特性。KLEx指南的統合分析顯示,術後12個月時CRF(角膜阻力因子)的下降量顯著小於FS-LASIK(MD, −1.13; 95%CI −1.36~−0.90; P<0.001)2)。CH(角膜滯後量)的下降也小於FS-LASIK(MD, −1.17; 95%CI −1.45~−0.89; P<0.001)2)。
這一優勢的原因在於帽結構保留了前基質(機械強度最高的部位)。帽(前基質)保持了板層結構的連續性,提供比LASIK瓣更高的生物力學強度2)。
SMILE的帽與LASIK瓣的不同之處在於:①無蒂,全周與角膜保持連續性;②帽下僅有一個小切口(2~3 mm)與外界相通,為封閉結構;③前基質的堅固膠原纖維得以保留。這種設計還帶來了術後外傷不會發生瓣移位的附加好處2)。LT指數(最大透鏡厚度/中央角膜厚度比)≤28%的管理值是維持這一生物力學優勢的重要指標;超過28%時,帽的增強效應被超過,會對生物力學產生不良影響2)。
SMILE僅透過角膜緣附近的小切口(2-3mm)插入器械,從而最大限度地減少對角膜前基質感覺神經(角膜神經叢)的切斷。LASIK在製作360°角膜瓣時會切斷全周的神經。因此,SMILE術後乾眼症狀的發生率和嚴重程度低於LASIK。FS-LASIK與SMILE的比較研究也報告,SMILE術後角膜神經密度恢復更快,對淚液參數的影響更小4)。
使用活體共聚焦顯微鏡(IVCM)對角膜神經密度進行縱向評估顯示,SMILE術後3個月神經叢密度恢復到術前的70-80%左右,而LASIK術後同期通常僅恢復到40-60%左右4)。這一差異被認為與術後乾眼嚴重程度的差異相對應。神經密度完全恢復通常需要6-12個月,部分患者可能需要2年以上。術前合併乾眼的患者神經密度恢復可能延遲,術前積極治療乾眼可能改善術後病程。
術後角膜擴張的主要原因是殘留基質床厚度(RST)不足或透鏡過厚導致的角膜生物力學強度下降,以及術前存在的亞臨床圓錐角膜。KLEx指南2)的分析顯示,65.5%的擴張病例術前角膜形態異常或可疑,52.3%的病例RST < 280 μm。
SMILE術後擴張的發生率低於LASIK(每10萬眼11例 vs 90例)5),但一旦發生,處理方法與LASIK術後擴張相同。如果確認進展,角膜交聯(CXL)是一線治療,自2022年起在日本已納入健保。
不透明氣泡層(OBL)是由水蒸氣和二氧化碳在層間積聚引起的。將室溫控制在18-25°C、濕度30-70%,並設置適當的雷射能量是預防措施2)。如果OBL廣泛發生並覆蓋瞳孔區,建議等待其完全消退後再進行透鏡分離操作。強行繼續操作會增加分離平面錯誤(wrong plane dissection)的風險。
Li等人(2019)的5年比較研究顯示,SMILE組和FS-LASIK組均保持了安全性和有效性,長期角膜生物力學影響無顯著差異3)。SMILE組在5年後仍保持良好的屈光穩定性。兩種術式在5年時的裸眼視力(UDVA)均優異,最佳矯正視力(BCVA)的維持也良好3)。
Moshirfar等人5)的系統性回顧計算出PRK、LASIK和SMILE的角膜擴張發生率分別為每10萬眼20、90和11例。SMILE的角膜擴張發生率約為LASIK的1/8,但SMILE的追蹤時間尚短,可能存在低估5)。該回顧也確認,即使沒有已知風險因素的眼睛也可能發生角膜擴張,因此需要進一步優化術前篩查。
Dishler等人6)報告的美國FDA核准的SMILE前瞻性多中心研究(近視伴散光)顯示,術後12個月平均殘餘等效球鏡度為−0.07 D(±0.38 D SD),95.4%達到20/20或更好的裸眼視力,安全性和有效性均達標。在散光矯正中,使用角膜緣標記校正旋轉誤差可提高精度6)。
Song等人7)的系統性回顧和統合分析比較了SMILE和LASIK的散光矯正效果,在矯正精度、殘餘散光和視力方面無顯著差異,但在高度散光(>2.0 D)病例中,SMILE的旋轉誤差控制影響結果。建議使用角膜緣標記和眼動追蹤系統7)。
Reinstein等人8)通過數學模型比較了PRK、LASIK和SMILE的相對角膜抗張強度。SMILE具有保留前部基質的帽狀結構,在同等矯正量下比LASIK保留更多角膜強度。這一理論依據被認為與SMILE較低的角膜擴張發生率一致8)。
Shetty等人9)的1年追蹤研究顯示,與LASIK相比,SMILE術後角膜生物力學(CRF、CH)的下降顯著較小。這種差異在術後3個月變得明顯,並持續到12個月。有研究指出,前基質的保護可能歸因於帽的生物力學貢獻9)。
AAO角膜擴張症PPP10)明確指出,SMILE的擴張風險低於LASIK,風險特徵與PRK相似。但即使在SMILE中,術前潛伏性圓錐角膜篩查也是必不可少的,建議進行包括CBI和TBI在內的全面生物力學評估10)。
Gomes等人11)的國際共識提出了擴張進展的定義(至少兩項一致變化:角膜前表面變陡、後表面變陡、角膜變薄),該標準適用於包括SMILE在內的屈光手術後擴張的管理。
Santhiago等人12)表明,LASIK術後擴張中PTA(組織改變百分比)≥40%是獨立危險因素。在SMILE(KLEx)中,由於帽與瓣不同,對角膜強度有貢獻,因此直接應用基於LASIK的PTA閾值存在爭議,但LT指數≤28%和RST≥280 μm的管理值共同重要12)。
KLEx指南的薈萃分析證實,與低散光組(<2.0D)相比,高散光組(>2.0D)術後殘餘散光顯著更多,矯正精度降低。使用角膜緣標記或三點定位(triple centration)校正旋轉誤差可提高精度2)。
Sekundo等人13)報告了飛秒雷射透鏡取出術(FLEx)的首個有效性與安全性研究(6個月結果)。FLEx是SMILE的前身技術,該研究為後續SMILE的開發奠定了基礎。通過將切口從FLEx的7mm縮小到SMILE的2-3mm,實現了角膜神經保護和安全性提升。
Jones等人14)的TFOS DEWS III報告指出,多項研究支持SMILE與LASIK相比,對術後乾眼症狀和角膜神經密度的影響顯著較小。在屈光矯正手術後的眼表優化中,建議術前進行MGD治療、使用地夸磷索以及圍手術期使用IPL14)。
有報導稱,結合術前角膜生物力學參數的人工智慧驅動列線圖調整可將屈光預測準確性提高25%以上2)。未來有望利用多模態數據開發個人化列線圖。
Randleman等人15)的圓錐角膜風險評分系統可用於LASIK術後圓錐角膜的術前預測,由五個因素組成:角膜形態異常、殘留基質床厚度低、年齡小、角膜薄和高度近視。在SMILE中,類似因素也會增加術後圓錐角膜的風險,因此該評分概念可用於術前篩查15)。
除SMILE外,還有多種飛秒雷射透鏡取出技術正在開發中,如CLEAR(角膜透鏡取出用於高級屈光矯正)和SILK(平滑切口透鏡角膜磨鑲術),進一步的技術標準化正在進行中2)。CLEAR是SMILE的變體,通過改進切口設計旨在擴大遠視和老視矯正的適應症。SILK旨在平滑切割面並減少氣泡產生,改善透鏡分離的容易度和視力恢復速度。這些新技術繼承了SMILE建立的無瓣和保留生物力學原則,同時旨在擴大適應症、提高精度和減少併發症。
將SMILE中取出的透鏡作為同種異體角膜嵌體再植入遠視、老視或圓錐角膜患者的研究正在進行中。免疫反應可能輕微,但目前仍處於實驗階段,尚未進入常規臨床應用。在將透鏡用於遠視矯正的案例中,原理是冷凍保存取出的透鏡並移植到合適的患者體內,以改變角膜厚度和屈光力,有可能作為角膜庫的替代資源。然而,長期安全性和有效性仍需積累證據。
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第8版). 日眼会誌. 2024;128(2):135-138.
Wang Y, Xie L, Yao K, et al. Evidence-Based Guidelines for Keratorefractive Lenticule Extraction Surgery. Ophthalmology. 2025;132:397-419.
Li M, Li M, Chen Y, et al. Five-year results of small incision lenticule extraction (SMILE) and femtosecond laser LASIK (FS-LASIK) for myopia. Acta Ophthalmol. 2019;97:e373-e380.
Recchioni A, Sisó-Fuertes I, Hartwig A, et al. Short-term impact of FS-LASIK and SMILE on dry eye metrics and corneal nerve morphology. Cornea. 2020;39(7):851-857.
Moshirfar M, Tukan AN, Bundogji N, et al. Ectasia after corneal refractive surgery: a systematic review. Ophthalmol Ther. 2021;10:753-776.
Dishler JG, Slade S, Seifert S, Schallhorn SC. Small-incision lenticule extraction (SMILE) for the correction of myopia with astigmatism: outcomes of the United States Food and Drug Administration premarket approval clinical trial. Ophthalmology. 2020;127:1020-1030.
Song J, Cao H, Chen X, et al. Small incision lenticule extraction (SMILE) versus laser assisted stromal in situ keratomileusis (LASIK) for astigmatism corrections: a systematic review and meta-analysis. Am J Ophthalmol. 2023;247:181-199.
Reinstein DZ, Archer TJ, Randleman JB. Mathematical model to compare the relative tensile strength of the cornea after PRK, LASIK, and SMILE. J Refract Surg. 2013;29:454-460.
Shetty R, Francis M, Shroff R, et al. Corneal biomechanical changes and tissue remodeling after SMILE and LASIK. Invest Ophthalmol Vis Sci. 2017;58:5703-5712.
American Academy of Ophthalmology Corneal/External Disease Preferred Practice Pattern Panel. Corneal Ectasia Preferred Practice Pattern. San Francisco, CA: AAO; 2024.
Gomes JA, Tan D, Rapuano CJ, et al. Global consensus on keratoconus and ectatic diseases. Cornea. 2015;34:359-369.
Santhiago MR, Smadja D, Gomes BF, et al. Association between the percent tissue altered and post-LASIK ectasia in eyes with normal preoperative topography. Am J Ophthalmol. 2014;158:87-95.e1.
Sekundo W, Kunert K, Russmann C, et al. First efficacy and safety study of femtosecond lenticule extraction for the correction of myopia: six-month results. J Cataract Refract Surg. 2008;34:1513-1520.
Jones L, Downie LE, Korb D, et al. TFOS DEWS III: Management and Therapy. Am J Ophthalmol. 2025;279:289-386.
Randleman JB, Woodward M, Lynn MJ, Stulting RD. Risk assessment for ectasia after corneal refractive surgery. Ophthalmology. 2008;115:37-50.