上皮型
樹枝狀角膜炎:伴有末端膨大的特徵性分支狀上皮病變
地圖狀角膜炎:樹枝狀角膜炎遷延導致上皮缺損擴大的病態

單純疱疹角膜炎是由單純疱疹病毒(HSV)感染引起的角膜炎。多數病例的病原體為1型(HSV-1),2型(HSV-2)引起的病例極為罕見。HSV屬於疱疹病毒科α疱疹病毒亞科,是一種嗜神經病毒,在三叉神經節等處潛伏感染並持續終生。
初次感染即發生角膜炎的病例較少。通常,潛伏在三叉神經節的HSV在發燒、感冒、壓力、紫外線照射等誘因下再激活,沿三叉神經到達角膜,引起各種病變。該病最大特徵是復發性,無論何種病型,詳細詢問病史都是確定診斷和治療策略的出發點。
根據2016年基於人口的估計,HSV角膜炎的整體發生率為每10萬人年24.0例,全球每年約有170萬人罹病2)。其中,上皮型約佔每10萬人年16.1例(每年約120萬例),實質型約佔每10萬人年4.9例(每年約37萬例)2)。估計每年約有23萬人新發生HSV角膜炎相關的單眼視力障礙(視力低於6/12)2)。
全球約67%(48.5億人)的人口曾感染HSV-1,特別是在美國和歐洲以外的地區,HSV-1血清陽性率更高,且治療可近性有限,因此實際疾病負擔可能被低估2)。HSV角膜炎是已開發國家角膜性失明的主要原因,尤其是實質型患者中24–42%矯正視力低於6/12,1.5–3.0%進展為重度視力障礙(低於6/60)2)。
作為日本獨有的流行病學調查,全國感染性角膜炎監測顯示,病毒性角膜炎與細菌性、真菌性、棘阿米巴角膜炎一樣佔據重要位置。HSV角膜炎在日本也被視為一種病程慢性、復發、影響視力預後的代表性疾病1)。年齡分佈上,中年以後病例較多,但首次發病可廣泛見於從兒童到老年人的各個年齡段。與年齡相關的細胞免疫下降是增加新發病率的因素6)。
眼疱疹感染症研究會提出的病型分類(Ohashi Yuichi等,1995年)已被感染性角膜炎診療指南第3版採用1)。該分類基於病變的定位和病理差異,是決定治療方針的重要框架。
上皮型
樹枝狀角膜炎:伴有末端膨大的特徵性分支狀上皮病變
地圖狀角膜炎:樹枝狀角膜炎遷延導致上皮缺損擴大的病態
實質型
圓盤狀角膜炎:由遲發型過敏反應引起的圓形實質混濁和水腫
壞死性角膜炎:伴有血管侵入的濃厚實質混濁,有穿孔風險
內皮型
角膜內皮炎:以角膜水腫和角膜後沉著物為主,實質混濁輕微
角膜輪部炎:以角膜輪部為底邊的扇形水腫,伴隨高眼壓
繼發性病變
上皮型是由病毒在上皮細胞中直接增殖引起的病理狀態,而實質型主要以針對病毒的免疫和炎症反應為主。內皮型是直接感染還是免疫反應為主尚未充分闡明。神經營養性角膜潰瘍是不伴隨病毒增殖的傷口癒合異常,並非HSV本身的病變而是繼發症。這些病理差異導致了治療策略的根本性不同。
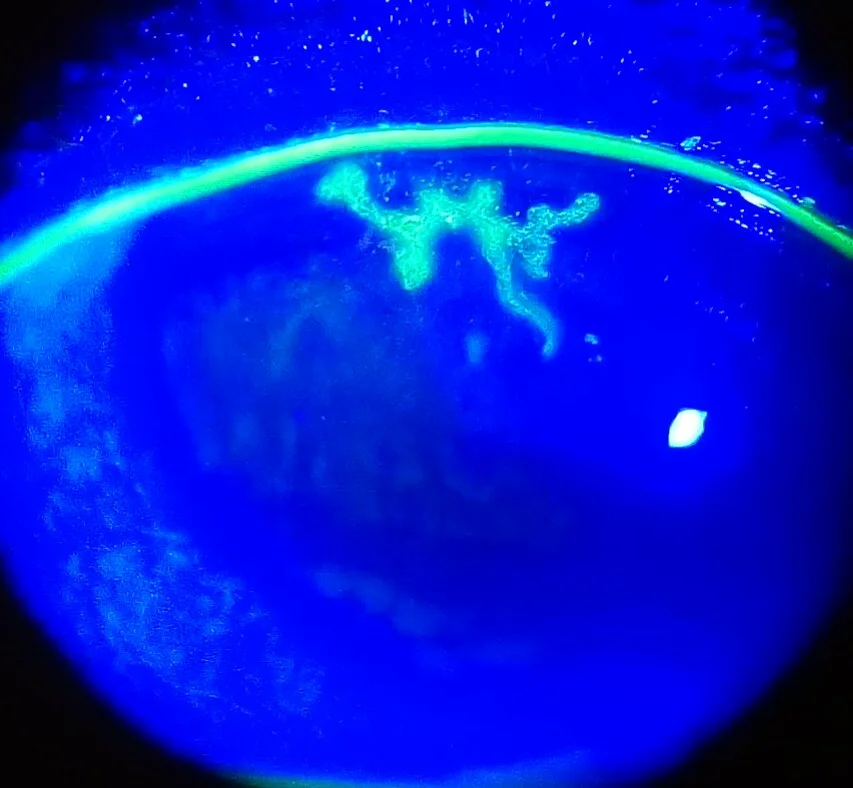
單純疱疹角膜炎的主觀症狀因病型而異。
樹枝狀角膜炎是上皮型角膜疱疹的代表性病變,具有四個對診斷具決定性作用的特徵1)。
螢光素染色下潰瘍底部呈陽性,邊緣腫脹的上皮被玫紅染色。樹突狀角膜炎遷延不癒時,上皮缺損擴大,形成地圖狀角膜炎(geographic keratitis)。在免疫功能不全患者和類固醇使用者中容易進展,邊緣特徵得以保留,出現樹突狀尾(提示樹突狀型態的部分)是診斷的線索。
單純皰疹病毒性角膜炎原則上為單眼性,但文獻報導雙眼病例的發生率為1.3~12%6)。異位性體質、類風濕關節炎(雙眼發生率40%)、免疫抑制狀態、兒童(26%)的雙眼風險較高6)。
盤狀角膜炎是實質型單純皰疹病毒性角膜炎的典型表現,具有以下特徵1)。
隨著反覆發作,混濁變為不規則形,並向深層延伸。除混濁外,還可呈現多種型態的病變,因此僅憑裂隙燈檢查結果難以診斷的病例也很多。
壞死性角膜炎(necrotizing keratitis)是角膜實質內HSV增殖或對抗原的免疫反應過度的病變1)。反覆發作時,在實質內已有血管侵入、疤痕形成、脂肪變性等的眼中容易發生。表現為伴有血管侵入的不規則形濃厚實質混濁,伴有上皮缺損的病例中,實質變薄甚至可導致穿孔。近年來由於早期適當治療,重症病例已很少見。
角膜內皮炎(endotheliitis)是在角膜上皮和實質水腫與病灶部位一致的KP存在,但角膜實質混濁和前房內細胞極為輕微的情況下進行臨床診斷的1)。HSV引起的內皮炎的典型類型是旁中心水腫型,角膜水腫以角膜緣為底邊呈扇形發生,其中央可見KP。可能伴有由於小樑網炎(trabeculitis)導致的高眼壓和角膜緣炎。
角膜葡萄膜炎型是實質炎、內皮炎、虹膜炎併發的重症型,表現為明顯的充血、角膜水腫、Descemet’s membrane folds、KP、前房內細胞,重症病例可出現前房蓄膿。
在反覆發作的病例中,角膜知覺減退變得明顯,是各類型診斷中重要的輔助依據。基質型和內皮型在病毒學診斷上比上皮型更困難,因此角膜知覺檢查的重要性更高。使用Cochet-Bonnet角膜知覺計,透過調整尼龍絲的長度可以分階段評估知覺閾值,也有助於確認左右差異。如果患者有單眼反覆充血的病史,並且患側有明顯知覺減退,則無論為何種類型,都應高度懷疑角膜疱疹。但上皮型復發早期有些病例知覺減退不明顯,僅憑知覺檢查陰性不能排除本病。
文獻報導,雙側HSV角膜炎的發生率為1.3%~12%6)。一項為期30年的回顧性研究顯示,4%的患者在初次發病時為雙側性,另有1%在復發時發展為雙側6)。韓國的一項大規模研究報告為12%,印度的一項研究報告雙側發生率高達25%6)。尤其是類風濕關節炎患者(40%)和兒童(26%)的發生率很高,異位性體質和免疫抑制狀態也容易導致雙側發病,需要特別注意6)。
單純疱疹角膜炎是由HSV(一種雙鏈DNA病毒)引起的。HSV-1主要感染口面部區域,HSV-2主要感染生殖器區域,但兩者均可引起眼部感染。大多數角膜疱疹由HSV-1引起。
初次感染多在兒童期無症狀發生。病毒通過感覺神經軸突到達三叉神經節,建立永久潜伏感染。潜伏病毒在某些誘因下再活化,經三叉神經到達角膜,引起復發性炎症。
以下情況雙側發病的風險較高6)。
角膜移植後HSV角膜炎在中國的一項回顧性研究(411例)中報導發生率為9.73%7)。65%的發病集中在術後1~3個月,術後類固醇使用被認為會促進病毒再活化7)。移植後HSV角膜炎按臨床類型分布為:上皮型27.5%、壞死性基質型20%、混合型42.5%、內皮型10%7)。在有HSV角膜炎病史的眼上進行角膜移植,與圓錐角膜或Fuchs角膜內皮營養不良的移植相比,排斥反應和移植失敗的風險顯著更高7)。
《感染性角膜炎診療指引第3版》1)根據眼疱疹感染症研究會的診斷標準提出以下內容。
但由於病毒分離培養在日常臨床中幾乎不進行,實際診斷需綜合裂隙燈所見、輔助診斷與病毒學檢查結果。
典型病例僅憑裂隙燈檢查即可確診。上皮型可見伴末端膨大之樹枝狀潰瘍,實質型可見盤狀表層混濁與免疫環,內皮炎型可見扇形角膜水腫與KP等各型特異性表現。合併使用伍德燈下螢光素染色與玫瑰紅染色。
角膜知覺檢查是診斷角膜疱疹的重要輔助檢查。建議使用Cochet-Bonnet角膜知覺計,因其操作簡便,可階段性評估知覺減退程度1)。反覆發作的病例可見明顯的知覺減退,但該檢查非特異性檢查,對初發或輕症病例未必有用。
《感染性角膜炎診療指引第3版》有條件地推薦以下檢查1)。
需與假樹枝狀角膜炎及呈現類似病變的疾病進行鑑別,這點非常重要。
| 鑑別疾病 | 鑑別要點 |
|---|---|
| 帶狀疱疹角膜炎(VZV) | 假樹枝狀病變:無末端膨大、螢光素染色弱、Hutchinson徵、伴隨皮疹 |
| 棘阿米巴角膜炎 | 劇烈疼痛、放射狀角膜神經炎、隱形眼鏡配戴史 |
| 復發性角膜糜爛 | 起床時急性發作、劇烈疼痛、外傷史 |
| 藥物毒性角膜病變 | 點眼藥使用史、瀰漫性點狀表層角膜病變 |
| CMV角膜內皮炎 | 錢幣狀病灶、線狀KP、對阿昔洛韋無反應 |
| 角膜移植排斥反應 | KP侷限於移植片後表面、Khodadoust線、對類固醇反應顯著 |
角膜移植術後之內皮炎與排斥反應的鑑別尤為重要。移植後HSV內皮炎中,KP分布於捐贈者-受贈者接合處之外,單用類固醇無法改善,需加用抗病毒藥物方可改善7)。而內皮排斥反應中,KP主要侷限於移植片後表面,Khodadoust線從邊緣向中央進展7)。
角膜知覺檢查是診斷疱疹性角膜炎的有力輔助檢查1)。特別是反覆發作的病例,可觀察到明顯的角膜知覺減退。Cochet-Bonnet角膜知覺計簡單易用且可分級,因此很有用。但該檢查並非特異性檢查,無法單獨用於確診。由於基質型和內皮型的病毒分離及PCR敏感度低於上皮型,因此病史(復發史詢問)和確認角膜知覺減退對診斷更為重要。
單純疱疹角膜炎的治療因病型而根本不同。上皮型由病毒直接增殖引起,因此以抗病毒藥物為中心,禁忌使用類固醇眼藥水。基質型和內皮型以免疫反應為主,因此原則上聯合使用抗病毒藥物和類固醇眼藥水。
第一線治療是阿昔洛韋(ACV,Zovirax®)眼藥膏3%,每日5次給藥1)。由於半衰期短,遵守用藥次數很重要,低劑量存在抗藥株出現的風險。上皮病變消失後減量為每日3次,1〜2週後停藥。為預防混合感染,合併使用抗菌眼藥水(如左氧氟沙星0.5%每日3次等)。
| 藥物 | 劑量 | 特點 |
|---|---|---|
| ACV眼藥膏3%(Zovirax®) | 每日點眼5次 | 第一線治療。因半衰期短,遵守用藥次數很重要 |
| 伐昔洛韋錠(Valtrex®)500mg | 每次2錠,每日2次,飯後 | ACV之前驅藥物。出現副作用或抗藥性菌株時更換 |
| 左氧氟沙星點眼液0.5%(Cravit®) | 每日點眼3次 | 預防混合感染 |
| 三氟胸苷點眼液1%(TFT) | 每日8~9次 | 對ACV耐藥株有效。在美國使用(日本未核准) |
副作用的應對:ACV眼藥膏可能導致角膜下方中心點狀表層角膜病變或眼瞼結膜炎(基劑反應)。輕度時可減量繼續使用,重度時改為口服伐昔洛韋500mg 2錠,分2次飯後服用。連續使用ACV眼藥膏1週無效時,需考慮ACV抗藥株或表現為偽樹枝狀角膜炎的其他疾病。
全身給藥:感染性角膜炎診療指引第3版有條件地推薦上皮型使用抗病毒藥全身給藥(弱推薦,證據強度C)1)。口服阿昔洛韋2,000 mg/天可期待與ACV眼藥膏同等的效果,適用於眼藥膏毒性病例、抗藥株病例及遵醫囑性不良病例。但在日本,HSV角膜炎的口服ACV不在健保給付範圍內1)。
上皮型禁用類固醇眼藥水。類固醇會促進病毒活化,加重病情。
清創術(上皮刮除):為減少病毒量,可與抗病毒藥物合併進行樹枝狀病變的刮除。
實質型角膜炎主要是對病毒的免疫反應所致,因此原則上應採用類固醇眼藥水抑制免疫反應合併ACV眼藥膏進行治療1)。若未使用ACV眼藥膏而單獨使用類固醇治療,初期雖可改善,但容易復發與再燃,且在病程中有誘發上皮型角膜炎的風險1)。
HEDS(疱疹性眼病研究)-1的SKN(未使用類固醇的基質角膜炎)試驗證實,在HSV基質型角膜炎中,局部使用皮質類固醇(磷酸潑尼松龍逐漸減量給藥)與安慰劑相比,可使炎症持續/進展的風險降低68%,並縮短癒合時間3)。在6個月時,用藥組的治療失敗率顯著低於安慰劑組,且視力改善也更早獲得3)。這是基質型角膜炎使用類固醇眼藥水的主要證據,也被日本感染性角膜炎診療指引第3版採納為基質型治療的基礎1)。但HEDS試驗設計並未顯示試驗藥物ACV口服的疊加效果,因此全身抗病毒藥物的合併使用需根據具體病例判斷。
類固醇眼藥水的實際使用:
聯合抗病毒藥物:聯合使用ACV眼膏3%每日5次1)。
口服類固醇:伴有角膜炎葡萄膜炎等嚴重炎症或合併上皮缺損時,在點眼基礎上加服倍他米松(Rinderon®錠0.5mg 2錠 每日1次 早飯後)。
處方示例(重症實質型):
處方示例(合併上皮缺損時):
內皮炎的治療參照實質型角膜炎的方案1)。若與實質型並存,則按照實質型的治療原則進行。對於單純性內皮炎的ACV給藥應為局部或全身使用,目前尚無一致共識。當角膜水腫變成不可逆時,適用角膜內皮移植術。
對於表現為單眼羊脂狀KP、前房發炎及眼壓上升的HSV前部葡萄膜炎,需合併使用抗病毒藥物、類固醇眼藥水、瞳孔管理及眼壓管理。
營養性角膜潰瘍是一種不伴隨病毒增殖的傷口癒合異常,因此治療策略有很大不同。
《感染性角膜炎診療指引》第3版有條件推薦全身性抗病毒藥物投予以預防上皮型角膜疱疹復發(弱推薦,證據等級C)1)。
HEDS-APT試驗中,ACV 400 mg每日兩次、為期12個月的投藥使上皮型及實質型HSV疾病的復發風險幾乎減半,用藥組為19%,對照組為32%4)。超過12個月的長期投藥顯示可進一步延長復發間隔4)。在留意ACV抗藥株出現可能性的同時,對於反覆復發的病例及高風險病例,此為有效的選擇。
當藥物治療無效的瘢痕性角膜混濁殘留時,適用角膜移植術。近年來,由於手術方式的進步和術後抗病毒預防的應用,治療成效大幅提升5)。
全層角膜移植術(PKP)
適應症:角膜穿孔或全層混濁
結果:無抗病毒預防時復發率44%,排斥率46%5)。合併口服ACV可將移植失敗相對風險降至0.35)
問題:免疫排斥反應是移植失敗的主要原因5)
深層前部層狀角膜移植術(DALK)
蘑菇狀角膜移植術(MK)
適應症:DALK術中發生Descemet’s membrane perforation時的轉換術式
結果:10年移植物存活率92%、排斥率9.7%、復發率7.8%5)
特點:9mm前部+6mm後部的雙片式結構。透過最小程度的內皮置換減輕抗原負荷5)
術後抗病毒預防:美國眼科學會(AAO)的Corneal Edema and Opacification Preferred Practice Pattern以及AAO的HSV角膜炎治療指南建議,角膜移植術後抗病毒預防應口服ACV 800 mg每日3次以上,或伐昔洛韋500 mg每日2次,持續至少1年5, 8, 9)。術後1~3個月是復發高峰期,此期間需特別注意7)。移植後HSV角膜炎復發時,應積極進行全身抗病毒治療,並根據上皮狀態、感染嚴重程度和排斥反應活動性謹慎調整類固醇劑量7)。
上皮型(活動性之上皮疾病狀態)禁用類固醇眼藥水。它會激活病毒複製,導致地圖狀潰瘍的進展和病情惡化。另一方面,實質型(如盤狀角膜炎)主要以對病毒的免疫反應為主,因此ACV眼藥膏與類固醇眼藥水的聯合使用是標準治療1, 3)。類固醇眼藥水不應突然停用,而應以月為單位逐漸減量1)。
初次感染:初次感染通常發生於兒童期經由口顏面區域的接觸,大多數為無症狀經過。病毒經由角膜上皮細胞的特異性受體(如Nectin-1、HVEM等)進入細胞內6)。感染後,病毒沿感覺神經軸突到達三叉神經節,建立永續的潛伏感染。
潛伏感染:HSV-1在神經元核內維持其基因組,逃避免疫系統的監視5)。潛伏期產生潛伏相關轉錄本(LAT),維持病毒基因組的完整性並抑制細胞凋亡6)。CD8陽性T細胞和細胞激素抑制病毒基因表現,使病毒維持休眠狀態5)。
再活化:多種誘因導致潛伏病毒再活化,沿三叉神經到達角膜。在COVID-19患者中,免疫抑制和細胞激素風暴症候群的發生導致HSV-1特異性CD8陽性T細胞耗竭,被認為會促進潛伏病毒的再活化6)。
在上皮型單純疱疹病毒性角膜炎中,HSV在角膜上皮細胞中活躍複製。其特徵是病毒在邊緣而非上皮缺損處活躍複製。樹枝狀病變沿角膜神經模式形成。反覆復發會導致角膜感覺神經受損,感覺減退逐漸加重。
HSV實質型角膜炎是以CD4陽性T細胞為主導的免疫反應為中心。攝取HSV抗原的蘭格罕細胞(角膜的抗原呈現細胞)將抗原呈現給CD4陽性T細胞,活化的T細胞釋放細胞激素。這導致嗜中性球浸潤角膜實質,引起組織破壞。小鼠模型顯示,從角膜實質中清除CD4陽性T細胞後不會發生實質炎,證實免疫反應是實質型的核心病理機制。
此外,已證明HSV UL6蛋白與人角膜抗原之間存在分子擬態(molecular mimicry),表明自體免疫機制可能參與實質炎的慢性化和復發。
壞死性與非壞死性的區別:非壞死性(盤狀)角膜炎是純粹的延遲型過敏反應,不伴隨病毒的活躍增殖。而壞死性角膜炎是指在反覆發作的角膜中,新生血管引起的中性粒細胞浸潤作用於實質內積累的抗原抗體複合物,導致更嚴重的組織破壞。
內皮炎究竟是由病毒直接感染引起的細胞損傷為主,還是以免疫學攻擊為主,目前尚無定論。一般認為這兩種病理狀態可能同時存在。HSV引起的內皮炎常伴隨著實質型或上皮型的病程,而單純內皮炎的病理狀態更多見於巨細胞病毒(CMV)1)。
營養性角膜潰瘍是由反覆發作過程中累積的多種因素共同導致的傷口癒合異常。涉及的因素包括實質發炎、角膜感覺神經損傷、上皮基底膜損傷以及抗病毒藥物的副作用等。HSV感染引起的角膜神經損傷會導致“神經營養性角膜病變”狀態,加之淚液分泌減少和眨眼反射減弱,導致上皮癒合延遲。臨床上,伴有病毒複製的地圖狀角膜炎表現為不規則上皮缺損,而營養性角膜潰瘍的特徵是橢圓形上皮缺損,邊緣上皮呈灰白色圓形隆起,與實質層有輕微分離感。雖然無法分離出病毒,但高靈敏度PCR可能檢測到殘留DNA。由於不伴有病毒複製,停止抗病毒眼藥水和促進上皮癒合是治療的基礎。
阿昔洛韋在感染細胞內被病毒來源的胸苷激酶(thymidine kinase:TK)單磷酸化,再被宿主細胞的激酶三磷酸化。這種活性型抑制病毒DNA聚合酶,阻斷病毒DNA合成。由於在正常細胞中不被磷酸化,因此對單純疱疹病毒具有高選擇性,副作用少。ACV抗藥株主要是由於TK活性缺失或突變導致ACV無法磷酸化而產生,免疫缺陷患者的風險尤其高6)。
作為應對ACV抗藥性病毒株的措施,針對HSV-1感染不同階段的多種新型分子的研究正在進行中6)。
BX795和OGT 2115對ACV抗藥性HSV株顯示出有效性,是有前景的候選藥物6)。由於HSV-1難以同時對3種不同的治療機制產生抗藥性,多種分子的聯合用藥有望成為未來的治療策略6)。
在活動性上皮型HSV角膜炎患者的淚液中已鑑定出特異性代謝變化(精氨酸減少、鞘脂代謝改變),提示其作為透過非侵入性淚液採樣進行新型診斷生物標記物的潛力。
隨著DALK和蘑菇形角膜移植的引入,HSV角膜炎的角膜移植效果得到了顯著改善5)。大直徑(9mm)DALK可顯著減少術後散光,據報導44%的患者達到了20/20或更好的視力5)。透過高劑量初始給藥和長期逐漸減量的方案,即使在伴有新生血管的瘢痕眼中也獲得了良好的10年結果5)。
對於伴有嚴重炎症反應、大而深的潰瘍和持續性上皮缺損的HSV角膜炎,已有藥物治療合併羊膜移植的報導7)。羊膜組織有助於促進上皮癒合、減輕炎症反應、抑制纖維母細胞增殖和抑制新生血管形成7)。
旨在預防HSV角膜炎復發的治療性疫苗研究正在進行中,動物實驗已證實可減輕角膜症狀。捐贈者角膜的常規HSV檢測也已被提出,透過檢測、治療和預防有望提高移植片存活率;但由於費用和法律環境的限制,目前尚未普及7)。