上皮型(Epithelial type)
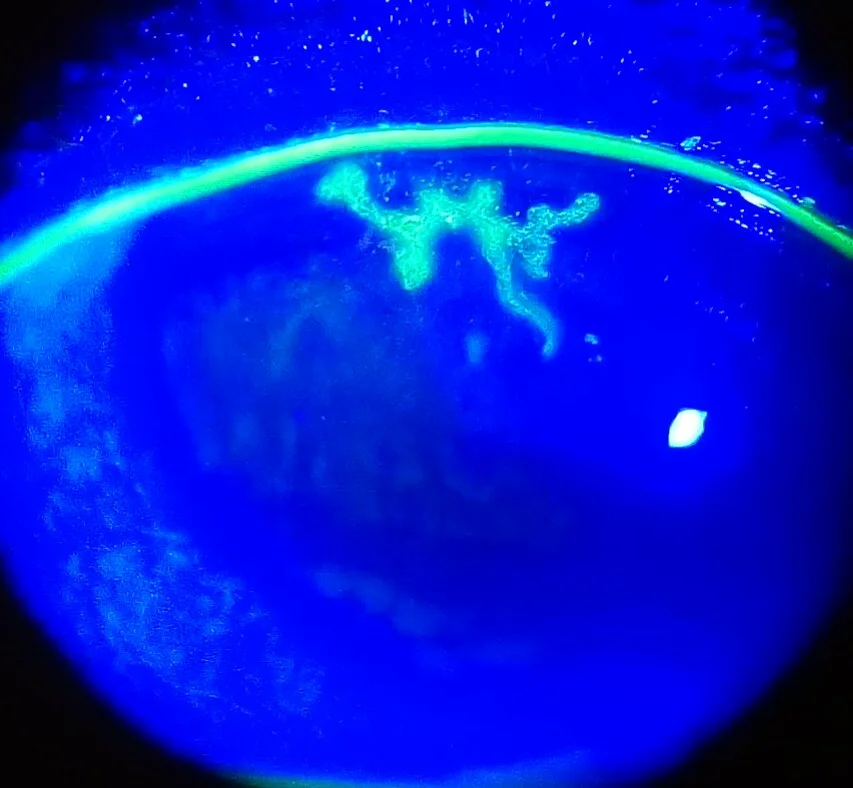
樹枝状角膜炎:末端膨大部を伴う特徴的な枝分かれ状の上皮病変
地図状角膜炎:樹枝状角膜炎の遷延化により上皮欠損が拡大した病態

単純ヘルペス角膜炎は、単純ヘルペスウイルス(herpes simplex virus:HSV)の感染によって生じる角膜炎である。多くの症例で原因ウイルスは1型(HSV-1)であり、2型(HSV-2)による症例は極めて稀である。HSVはヘルペスウイルス科のαヘルペスウイルス亜科に属する神経向性(ニューロトロピック)ウイルスであり、三叉神経節などに潜伏感染して生涯持続する。
初感染で角膜炎を発症する例は少ない。通常は三叉神経節に潜伏したHSVが、発熱・感冒・ストレス・紫外線曝露などの誘因で再活性化し、三叉神経を伝って角膜に到達することで各種の病変を生じる。再発性疾患であることがその最大の特徴であり、病型を問わず病歴の丁寧な聴取が診断・治療方針決定の出発点となる。
2016年の人口に基づく推計では、HSV角膜炎全体の罹患率は10万人あたり24.0人(年間)と推計され、世界で年間約170万人が罹患している2)。このうち上皮型は10万人あたり約16.1人(年間約120万人)、実質型は約4.9人(年間約37万人)を占める2)。年間約23万人が新規に、HSV角膜炎関連の片眼性視力障害(視力6/12未満)を獲得していると推定される2)。
世界人口の約67%(48.5億人)がHSV-1既感染であり、とくに米国・欧州以外の地域ではHSV-1有病率がさらに高く、治療アクセスも限られるため、実際の疾患負担は過小評価されている可能性が高い2)。HSV角膜炎は先進国における角膜性失明の最大の原因であり、とくに実質型は24〜42%で矯正視力6/12未満となり、1.5〜3.0%が重度視力障害(6/60未満)に至る2)。
日本独自の疫学調査としては、感染性角膜炎全国サーベイランスで細菌性・真菌性・アカントアメーバとならびウイルス性角膜炎が重要な位置を占めることが示されており、HSV角膜炎は本邦でも慢性・再発性に経過して視力予後を左右する代表的疾患と位置づけられている1)。年齢分布では中年以降の症例が多いが、初発は小児から高齢者まで幅広く認められ、加齢に伴う細胞性免疫の低下は新規発症率を増加させる要因となる6)。
眼ヘルペス感染症研究会が提唱した病型分類(大橋裕一ら、1995年)は感染性角膜炎診療ガイドライン第3版にも採用されている1)。本病型分類は病変の局在と病態の違いに基づき、治療方針を左右する重要な枠組みである。
上皮型(Epithelial type)
樹枝状角膜炎:末端膨大部を伴う特徴的な枝分かれ状の上皮病変
地図状角膜炎:樹枝状角膜炎の遷延化により上皮欠損が拡大した病態
実質型(Stromal type)
円板状角膜炎:遅延型過敏反応による円形の実質混濁・浮腫
壊死性角膜炎:血管侵入を伴う濃厚な実質混濁、穿孔リスクあり
内皮型(Endothelial type)
角膜内皮炎:角膜浮腫と後面沈着物が主体、実質混濁は軽微
角膜輪部炎:輪部を底辺とした扇型の浮腫と高眼圧を伴う
二次病変
遷延性上皮欠損:創傷治癒遅延による二次的上皮欠損
栄養障害性角膜潰瘍:知覚神経障害と創傷治癒異常による潰瘍
上皮型は上皮細胞でのウイルス直接増殖による病態であり、実質型はウイルスに対する免疫・炎症反応が主体である。内皮型は直接感染と免疫反応のいずれが主体かが十分に解明されていない。栄養障害性角膜潰瘍はウイルス増殖を伴わない創傷治癒異常であり、HSV本来の病変ではなく続発症である。これらの病態の違いが治療戦略の根本的な相違をもたらす。
単純ヘルペス角膜炎の自覚症状は病型によって大きく異なる。
上皮型角膜ヘルペスの代表的病変である樹枝状角膜炎(dendritic keratitis)には、診断の決め手となる4つの特徴がある1)。
フルオレセイン染色では潰瘍底が陽性となり、辺縁の腫脹上皮はローズベンガルで染色される。樹枝状角膜炎が遷延化すると上皮欠損が拡大し、**地図状角膜炎(geographic keratitis)**の形をとる。免疫不全患者やステロイド使用患者で進展しやすく、縁取り所見は保たれ、dendritic tail(樹枝状を疑わせる部分)を認めることが診断の手がかりとなる。
角膜ヘルペスは原則として片眼性であるが、両側性症例の頻度は文献上1.3〜12%とされる6)。アトピー素因、関節リウマチ(両側性頻度40%)、免疫抑制状態、小児(26%)では両側性リスクが高い6)。
実質型角膜ヘルペスの定型例である円板状角膜炎(disciform keratitis)は、以下の所見を特徴とする1)。
再発を繰り返すに従って混濁は不整形となり、深い層にも及ぶ。混濁以外にも多様な形態の病変を呈するため、細隙灯所見のみでは診断が困難な症例も多い。
壊死性角膜炎(necrotizing keratitis)は、角膜実質内でのHSV増殖あるいは抗原に対する免疫反応が過剰になった病態である1)。再発を繰り返し、実質内に血管侵入・瘢痕形成・脂肪変性などがある眼で再燃した場合に生じやすい。血管侵入を伴う不整形の濃厚な実質混濁を呈し、上皮欠損を伴う例では実質の菲薄化から穿孔に至る例もある。近年は早期適切治療により重篤例は稀である。
角膜内皮炎(endotheliitis)は、角膜の上皮・実質浮腫と病巣部に一致したKPを認めるが、角膜実質混濁や前房内細胞がきわめて軽微である場合に臨床的に診断する1)。HSVによる内皮炎の典型型は傍中心部浮腫型であり、角膜浮腫が輪部を底辺とする扇形に生じ、その中央にKPを認める。線維柱帯炎(trabeculitis)による高眼圧と輪部炎を伴うことがある。
角膜ぶどう膜炎型は実質炎・内皮炎・虹彩炎を併発した重症型であり、著明な充血・角膜浮腫・Descemet膜皺襞・KP・前房内細胞を認め、重症例では前房蓄膿を生じる。
再発を繰り返した症例では角膜知覚低下が著明となり、病型を問わず診断の重要な補助所見となる。実質型・内皮型はウイルス学的診断が上皮型より困難なため、角膜知覚検査の重要性がより高い。Cochet-Bonnet 角膜知覚計を用いれば、ナイロン糸の長さを調整することで知覚閾値を段階的に評価でき、左右差の確認にも有用である。片眼性の再発性充血の既往があり、患側で明らかな知覚低下を認める場合は、病型にかかわらず角膜ヘルペスを強く疑う根拠となる。なお、上皮型の再発初期には知覚低下が明瞭でない症例もあり、知覚検査陰性のみで本疾患を除外することはできない。
文献上、両側性HSV角膜炎の発生頻度は1.3〜12%とされています6)。30年間の後方視的研究では全患者の4%が初回発症時に両側性であり、さらに1%が再発時に両側性となりました6)。韓国の大規模研究では12%、インドの研究では最大25%の両側性頻度が報告されています6)。とくに関節リウマチ患者では40%、小児では26%と高率であり、アトピー素因や免疫抑制状態でも両側性になりやすいため注意が必要です6)。
単純ヘルペス角膜炎は二本鎖DNAウイルスであるHSVによって引き起こされる。HSV-1は主に口腔顔面領域に、HSV-2は主に性器領域に感染するが、どちらも眼感染を起こしうる。角膜ヘルペスの大半はHSV-1によるものである。
初感染は多くが小児期に無症状で生じる。ウイルスは感覚神経軸索を通って三叉神経節に到達し、永続的な潜伏感染を確立する。潜伏したウイルスが何らかの誘因で再活性化し、三叉神経を経由して角膜に到達して再発性の炎症を惹起する。
以下の状態では両側性発症のリスクが高い6)。
角膜移植後のHSV角膜炎は、中国の後方視的研究(411例)で発症率9.73%と報告されている7)。発症の65%は術後1〜3ヶ月に集中し、術後のステロイド使用がウイルス再活性化を促進すると考えられる7)。移植後HSV角膜炎の病型別頻度は、上皮型27.5%、壊死性実質型20%、混合型42.5%、内皮型10%であった7)。HSV角膜炎の既往がある眼への角膜移植は、円錐角膜やFuchs角膜ジストロフィへの移植と比較して、拒絶反応と移植片不全のリスクが有意に高い7)。
感染性角膜炎診療ガイドライン第3版1)では、眼ヘルペス感染症研究会の診断基準に基づき以下を提示している。
ただし、ウイルス分離・培養は日常臨床においてほとんど施行されないため、実際には細隙灯所見、補助診断、ウイルス学的検査を総合して診断する。
典型例では細隙灯所見のみで診断可能である。上皮型では末端膨大部を伴う樹枝状潰瘍、実質型では円板状の浅層混濁と免疫輪、内皮炎では扇形の角膜浮腫とKPといった病型に特異的な所見を確認する。ウッドフィルター下でのフルオレセイン染色・ローズベンガル染色を併用する。
角膜知覚検査は角膜ヘルペス診断の有力な補助検査である。Cochet-Bonnet角膜知覚計が簡便で、知覚低下の程度を段階的に評価できるため推奨される1)。再発を繰り返した症例では著明な知覚低下を認めるが、特異性のある検査ではなく、初回症例や軽症例では必ずしも有用ではない点に留意する。
感染性角膜炎診療ガイドライン第3版では、以下の検査を条件付きで推奨している1)。
偽樹枝状角膜炎や類似病変を呈する疾患との鑑別が重要である。
| 鑑別疾患 | 鑑別のポイント |
|---|---|
| 帯状ヘルペス角膜炎(VZV) | 偽樹枝状病変:末端膨大部なし、フルオ染色弱い、Hutchinson徴候、皮疹を伴う |
| アカントアメーバ角膜炎 | 強い疼痛、放射状角膜神経炎、コンタクトレンズ使用歴 |
| 再発性角膜びらん | 起床時の急性発症、強い疼痛、外傷歴 |
| 薬剤毒性角膜症 | 点眼薬使用歴、びまん性点状表層角膜症 |
| CMV角膜内皮炎 | コイン・リージョン、linear KP、アシクロビルに反応せず |
| 角膜移植拒絶反応 | KPがグラフト後面に限局、Khodadoust line、ステロイドに著効 |
角膜移植後の内皮炎と拒絶反応の鑑別はとくに重要である。移植後HSV内皮炎ではKPがドナー・レシピエント接合部を越えて分布し、ステロイド単独では改善せず抗ウイルス薬の追加で改善する7)。一方、内皮拒絶反応ではKPは主にグラフト後面に限局し、Khodadoust lineが辺縁から中心に向かって進行する7)。
角膜知覚検査は角膜ヘルペス診断の有力な補助検査です1)。とくに再発を繰り返す症例では著明な角膜知覚の低下を認めます。Cochet-Bonnet角膜知覚計が簡便で程度を段階づけできるため有用です。ただし特異性のある検査ではないため単独での確定診断はできません。実質型・内皮型は上皮型よりウイルス分離やPCRの感度が低いため、病歴(再発歴の聴取)と角膜知覚低下の確認が診断上より重要になります。
単純ヘルペス角膜炎の治療は病型によって根本的に異なる。上皮型はウイルス直接増殖による病態のため抗ウイルス薬が中心であり、ステロイド点眼は禁忌である。実質型・内皮型は免疫反応が主体のため、抗ウイルス薬とステロイド点眼の併用が原則となる。
第一選択はアシクロビル(ACV、ゾビラックス®)眼軟膏3%の1日5回点入である1)。半減期が短いため回数遵守が重要であり、低用量では耐性株出現のリスクがある。上皮病変が消失したら1日3回に減量し、1〜2週間で中止する。混合感染予防のため抗菌点眼薬(レボフロキサシン0.5%1日3回など)を併用する。
| 薬剤 | 投与量 | 特徴 |
|---|---|---|
| ACV眼軟膏3%(ゾビラックス®) | 1日5回 点入 | 第一選択。半減期が短いため回数遵守が重要 |
| バラシクロビル錠(バルトレックス®)500mg | 2錠 分2 食後 | ACVのプロドラッグ。副作用時や耐性株に変更 |
| レボフロキサシン点眼0.5%(クラビット®) | 1日3回 点眼 | 混合感染予防 |
| トリフルリジン点眼1%(TFT) | 1日8〜9回 | ACV耐性株に有効。米国で使用(日本未承認) |
副作用への対応:ACV眼軟膏により、角膜下方中心の点状表層角膜症や眼瞼結膜炎(基剤反応)が生じることがある。軽度なら減量継続可能であるが、重度の場合はバラシクロビル500mg 2錠分2食後の内服に変更する。ACV眼軟膏を1週間継続して効果が認められない場合は、ACV耐性株や偽樹枝状角膜炎を呈する他疾患を考慮する。
全身投与:感染性角膜炎診療ガイドライン第3版では、上皮型に対する抗ウイルス薬の全身投与を条件付きで推奨している(弱く推奨、エビデンスの強さC)1)。アシクロビル内服2,000 mg/日はACV眼軟膏と同等の効果が期待でき、眼軟膏毒性症例・耐性株症例・アドヒアランス不良例で有用である。ただし日本ではHSV角膜炎に対するACV内服は保険適用外である1)。
上皮型ではステロイド点眼は禁忌である。ステロイドはウイルスの活性化を促進し、病態を悪化させる。
デブリードマン(上皮掻爬):ウイルス量を減少させる目的で、抗ウイルス薬と併用して樹枝状病変の掻爬を行う場合がある。
実質型はウイルスに対する免疫反応が主体であるため、ステロイド点眼による免疫反応の抑制とACV眼軟膏の併用が原則である1)。ACV眼軟膏を使用せずステロイド単独で治療すると、当初は軽快するが再発・再燃が生じやすく、経過中に上皮型を誘発する危険がある1)。
HEDS(Herpetic Eye Disease Study)-1のSKN(Stromal Keratitis Not on steroids)試験では、HSV実質型角膜炎に対する局所ステロイド(リン酸プレドニゾロン漸減投与)がプラセボと比較して、炎症の持続・進行リスクを68%減少させ、治癒時間を短縮することが実証された3)。6ヶ月時点での治療失敗率は実薬群で有意に低く、さらに視力改善も早期に得られることが示された3)。これが実質型角膜炎におけるステロイド点眼使用の主要なエビデンスであり、日本の感染性角膜炎診療ガイドライン第3版でも実質型治療の基本として採用されている1)。ただし、HEDSの試験デザインでは試験薬ACV内服の上乗せ効果は示されなかったため、全身抗ウイルス薬の併用は症例に応じた判断となる。
ステロイド点眼の実際:
抗ウイルス薬の併用:ACV眼軟膏3%1日5回を併用する1)。
ステロイド内服:角膜ぶどう膜炎など強い炎症を伴う場合や上皮欠損を伴う場合は、点眼に加えてベタメタゾン(リンデロン®錠0.5mg 2錠 分1 朝食後)内服を併用する。
処方例(重症実質型):
処方例(上皮欠損合併時):
内皮炎は実質型に準じて治療する1)。実質型に併存している場合は実質型の治療に則る。純粋な内皮炎に対するACV投与が局所か全身かについては一定の見解が得られていない。角膜浮腫が不可逆性となった場合は角膜内皮移植の適応となる。
片眼性の豚脂様KPと前房炎症、眼圧上昇を呈するHSV前部ぶどう膜炎に対しては、抗ウイルス薬とステロイド点眼、瞳孔管理、眼圧管理を組み合わせる。
栄養障害性角膜潰瘍はウイルス増殖を伴わない創傷治癒異常であるため、治療戦略が大きく異なる。
感染性角膜炎診療ガイドライン第3版では、上皮型角膜ヘルペスの再発予防のための抗ウイルス薬全身投与を条件付きで推奨している(弱く推奨、エビデンスC)1)。
HEDS-APT試験では、ACV 400 mg 1日2回の12ヶ月投与により、上皮型・実質型HSV疾患の再発リスクが実薬群19%対プラセボ群32%とほぼ半減した4)。12ヶ月を超える長期投与でさらに再発間隔の延長が示されている4)。ACV耐性株出現の可能性に留意しつつ、再発を繰り返す症例やハイリスク症例では有効な選択肢となる。
薬物療法に反応しない瘢痕性の角膜混濁が残った場合には角膜移植術の適応となる。近年の術式進歩と術後抗ウイルス予防により成績が大幅に向上している5)。
全層角膜移植(PKP)
適応:角膜穿孔や全層の混濁
成績:抗ウイルス予防なしで再発率44%、拒絶率46%5)。経口ACV併用でグラフト不全の相対リスクが0.3に低下5)
問題点:免疫学的拒絶反応が主なグラフト不全の原因5)
深層前部層状角膜移植(DALK)
適応:実質混濁で内皮が健全な症例
成績:再発率6〜10%、拒絶率0〜4.5%、5年生存率96%5)。PKP(5年生存率78.8%)と比較して著明に優れる
利点:宿主内皮を温存するため免疫学的拒絶が少ない5)
マッシュルーム角膜移植(MK)
適応:DALK中のDescemet膜穿孔時の変換術式
成績:10年グラフト生存率92%、拒絶率9.7%、再発率7.8%5)
特徴:9mm前部+6mm後部の2ピース構成。最小限の内皮置換で抗原負荷を軽減5)
術後の抗ウイルス予防:米国眼科学会(AAO)のCorneal Edema and Opacification Preferred Practice Patternおよび AAO の HSV 角膜炎治療ガイドラインでは、角膜移植後の抗ウイルス予防として経口ACV 800 mg 1日3回以上、またはバラシクロビル 500 mg 1日2回を最低1年間継続することを推奨している5, 8, 9)。術後1〜3ヶ月が再発のピークであり、この期間はとくに注意が必要である7)。移植後にHSV角膜炎が再燃した場合には、全身抗ウイルス療法を積極的に行い、ステロイド投与量を上皮の状態・感染重症度・拒絶反応の活動性に応じて慎重に調整する7)。
上皮型(活動性の上皮疾患がある状態)に対してステロイド点眼は禁忌です。ウイルスの増殖を活性化させ、地図状潰瘍への進展や病態悪化を招きます。一方、実質型(円板状角膜炎など)ではウイルスに対する免疫反応が主体のため、ACV眼軟膏とステロイド点眼の併用が標準治療となります1, 3)。ステロイド点眼は急に中止せず月単位で漸減することが重要です1)。
初感染:初感染は通常小児期に口腔顔面領域への接触で生じ、大半は無症状に経過する。ウイルスは角膜上皮細胞の特異的受容体(Nectin-1、HVEMなど)を介して細胞内に侵入する6)。感染後、ウイルスは感覚神経軸索を通って三叉神経節に到達し、永続的な潜伏感染を確立する。
潜伏感染:HSV-1はニューロンの核内にゲノムを維持し、免疫系の監視を回避する5)。潜伏期には潜伏関連転写産物(latency-associated transcript:LAT)を産生し、ウイルスゲノムの完全性を維持するとともに細胞アポトーシスを抑制する6)。CD8陽性T細胞とサイトカインがウイルス遺伝子発現を抑制し、ウイルスを休止状態に維持する5)。
再活性化:各種の誘因により潜伏ウイルスが再活性化し、三叉神経に沿って角膜に到達する。COVID-19患者では免疫抑制とサイトカインストーム症候群が生じ、HSV-1特異的CD8陽性T細胞の疲弊により潜伏ウイルスの再活性化が促進されると考えられている6)。
上皮型角膜ヘルペスでは、HSVが角膜上皮細胞で活発に増殖する。上皮欠損部ではなく、辺縁部でウイルスが活発に増殖しているのが特徴である。樹枝状病変は角膜の神経パターンに沿って形成される。再発を繰り返すと角膜知覚神経が障害され、知覚低下が進行する。
HSV実質型角膜炎はCD4陽性T細胞が主導する免疫反応が中心である。HSV抗原を取り込んだLangerhans細胞(角膜の抗原提示細胞)がCD4陽性T細胞に抗原を提示し、活性化T細胞がサイトカインを放出する。これにより好中球が角膜実質に浸潤し、組織破壊を引き起こす。マウスモデルでは角膜実質からCD4陽性T細胞を除去すると実質炎が発症しないことが示されており、免疫反応が実質型の中心病態であることを裏づける。
また、HSV UL6タンパクとヒト角膜抗原の間に分子擬態(molecular mimicry)が存在することが示されており、自己免疫的機序が実質炎の慢性化・再発に関与する可能性がある。
壊死性と非壊死性の違い:非壊死性(円板状)角膜炎は純粋な遅延型過敏反応であり、ウイルスの活発な増殖は伴わない。一方、壊死性角膜炎は再発を繰り返した角膜で実質内に蓄積した抗原抗体複合物に対して、新生血管を通じた好中球浸潤が生じ、より高度な組織破壊を来す。
内皮炎がウイルスの直接感染による細胞障害か、免疫学的攻撃が主体かについて結論は得られていない。おそらく両者の病態が混在していると考えられている。HSVによる内皮炎は実質型や上皮型を経過中に伴うことが多く、純粋な内皮炎のみの病態はサイトメガロウイルス(CMV)によるものが多いとされる1)。
栄養障害性角膜潰瘍は、再発を繰り返す過程で蓄積した複数の要因が重なって生じる創傷治癒異常である。関与する要因として、実質の炎症、角膜知覚神経の障害、上皮基底膜の障害、抗ウイルス薬の副作用などが挙げられる。HSV感染による角膜神経の障害は「神経栄養性角膜症」の状態を引き起こし、涙液分泌低下と瞬目反射の減弱も相まって上皮治癒が遅延する。臨床的には、ウイルス増殖を伴う地図状角膜炎が不整形の上皮欠損を示すのに対し、栄養障害性角膜潰瘍では上皮欠損が楕円形を示し、辺縁上皮が灰白色に丸く盛り上がり、実質からやや浮いたような所見を呈するのが特徴である。ウイルスは分離されないが、高感度PCR法では残余DNAが検出されることがある。ウイルス増殖を伴わないため、抗ウイルス点眼の中止と上皮治癒促進が治療の基本となる。
アシクロビルは感染細胞内でウイルス由来のチミジンキナーゼ(thymidine kinase:TK)により一リン酸化され、さらに宿主細胞のキナーゼにより三リン酸化される。この活性型がウイルスDNAポリメラーゼを阻害し、ウイルスDNA合成を遮断する。正常細胞ではリン酸化されないため、ヘルペスウイルスに対する選択性が高く副作用が少ない。ACV耐性株は主にTK活性の欠失や変異によりACVがリン酸化されないことで生じ、免疫不全患者でとくにリスクが高い6)。
ACV耐性株への対策として、複数の新規分子がHSV-1感染の異なる段階を標的とする研究が進められている6)。
BX795とOGT 2115はACV耐性HSV株に対して有効性を示しており、有望な候補である6)。HSV-1が3つの異なる治療メカニズムに同時に耐性を獲得することは困難であるため、複数分子の併用が将来の治療戦略として期待される6)。
活動性上皮型HSV角膜炎患者の涙液で特異的な代謝変化(アルギニン減少、スフィンゴ脂質代謝変化)が同定されており、非侵襲的な涙液サンプリングによる新規診断バイオマーカーとしての可能性が示唆されている。
DALKやマッシュルーム角膜移植の導入により、HSV角膜炎に対する角膜移植の成績は飛躍的に向上した5)。大径(9mm)DALKでは術後乱視が有意に軽減され、44%が20/20以上の視力を達成したと報告されている5)。高用量初期投与と長期漸減のプロトコルにより、血管新生を伴う瘢痕眼でも良好な10年成績が報告されている5)。
重度の炎症反応・大きく深い潰瘍・遷延性上皮欠損を伴うHSV角膜炎に対し、薬物療法と羊膜移植の併用が報告されている7)。羊膜組織は上皮治癒の促進、炎症反応の軽減、線維芽細胞増殖の抑制、血管新生の抑制に寄与する7)。
HSV角膜炎の再発予防を目的とした治療的ワクチンの研究が進行中であり、動物実験では角膜症状の軽減が確認されている。またドナー角膜のルーチンHSV検査も提唱されており、検出・治療・予防によるグラフト生存率向上が期待されるが、費用や法的環境の制約から現時点では一般化していない7)。