上皮型
树枝状角膜炎:伴有末端膨大的特征性分支状上皮病变
地图状角膜炎:树枝状角膜炎迁延导致上皮缺损扩大的病态

单纯疱疹角膜炎是由单纯疱疹病毒(HSV)感染引起的角膜炎。多数病例的病原体为1型(HSV-1),2型(HSV-2)引起的病例极为罕见。HSV属于疱疹病毒科α疱疹病毒亚科,是一种嗜神经病毒,在三叉神经节等处潜伏感染并持续终生。
初次感染即发生角膜炎的病例较少。通常,潜伏在三叉神经节的HSV在发热、感冒、压力、紫外线照射等诱因下再激活,沿三叉神经到达角膜,引起各种病变。该病最大特征是复发性,无论何种病型,详细询问病史都是确定诊断和治疗策略的出发点。
根据2016年基于人口的估计,HSV角膜炎的总体发病率为每10万人年24.0例,全球每年约有170万人患病2)。其中,上皮型约占每10万人年16.1例(每年约120万例),实质型约占每10万人年4.9例(每年约37万例)2)。估计每年约有23万人新发HSV角膜炎相关的单眼视力障碍(视力低于6/12)2)。
全球约67%(48.5亿人)的人口曾感染HSV-1,特别是在美国和欧洲以外的地区,HSV-1血清阳性率更高,且治疗可及性有限,因此实际疾病负担可能被低估2)。HSV角膜炎是发达国家角膜盲的首要原因,尤其是实质型患者中24–42%矫正视力低于6/12,1.5–3.0%发展为重度视力障碍(低于6/60)2)。
作为日本独有的流行病学调查,全国感染性角膜炎监测显示,病毒性角膜炎与细菌性、真菌性、棘阿米巴角膜炎一样占据重要位置。HSV角膜炎在日本也被视为一种病程慢性、复发、影响视力预后的代表性疾病1)。年龄分布上,中年以后病例较多,但首次发病可广泛见于从儿童到老年人的各个年龄段。与年龄相关的细胞免疫下降是增加新发病率的因素6)。
眼疱疹感染症研究会提出的病型分类(Ohashi Yuichi等,1995年)已被感染性角膜炎诊疗指南第3版采纳1)。该分类基于病变的定位和病理差异,是决定治疗方针的重要框架。
上皮型
树枝状角膜炎:伴有末端膨大的特征性分支状上皮病变
地图状角膜炎:树枝状角膜炎迁延导致上皮缺损扩大的病态
实质型
圆盘状角膜炎:由迟发型超敏反应引起的圆形实质混浊和水肿
坏死性角膜炎:伴有血管侵入的浓厚实质混浊,有穿孔风险
内皮型
角膜内皮炎:以角膜水肿和角膜后沉着物为主,实质混浊轻微
角膜缘炎:以角膜缘为底边的扇形水肿,伴有高眼压
继发性病变
上皮型是由病毒在上皮细胞中直接增殖引起的病理状态,而实质型主要以针对病毒的免疫和炎症反应为主。内皮型是直接感染还是免疫反应为主尚未充分阐明。神经营养性角膜溃疡是不伴随病毒增殖的伤口愈合异常,并非HSV本身的病变而是继发症。这些病理差异导致了治疗策略的根本性不同。
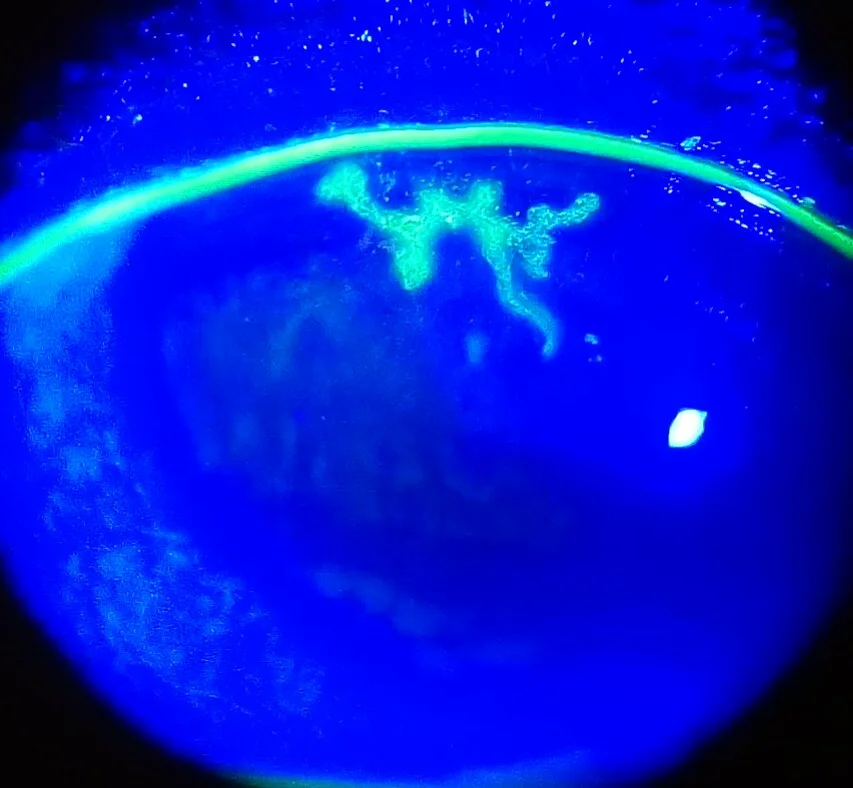
单纯疱疹角膜炎的主观症状因病变类型而异。
树枝状角膜炎是上皮型角膜疱疹的代表性病变,具有四个对诊断起决定性作用的特征1)。
荧光素染色下溃疡底部呈阳性,边缘肿胀的上皮被玫瑰红染色。树突状角膜炎迁延不愈时,上皮缺损扩大,形成地图状角膜炎(geographic keratitis)。在免疫功能不全患者和类固醇使用者中容易进展,边缘特征得以保留,出现树突状尾(提示树突状形态的部分)是诊断的线索。
单纯疱疹病毒性角膜炎原则上为单眼性,但文献报道双眼病例的发生率为1.3~12%6)。特应性体质、类风湿关节炎(双眼发生率40%)、免疫抑制状态、儿童(26%)的双眼风险较高6)。
盘状角膜炎是实质型单纯疱疹病毒性角膜炎的典型表现,具有以下特征1)。
随着反复发作,混浊变为不规则形,并向深层延伸。除混浊外,还可呈现多种形态的病变,因此仅凭裂隙灯检查结果难以诊断的病例也很多。
坏死性角膜炎(necrotizing keratitis)是角膜实质内HSV增殖或对抗原的免疫反应过度的病变1)。反复发作时,在实质内已有血管侵入、瘢痕形成、脂肪变性等的眼中容易发生。表现为伴有血管侵入的不规则形浓厚实质混浊,伴有上皮缺损的病例中,实质变薄甚至可导致穿孔。近年来由于早期适当治疗,重症病例已很少见。
角膜内皮炎(endotheliitis)是在角膜上皮和实质水肿与病灶部位一致的KP存在,但角膜实质混浊和前房内细胞极为轻微的情况下进行临床诊断的1)。HSV引起的内皮炎的典型类型是旁中心水肿型,角膜水肿以角膜缘为底边呈扇形发生,其中央可见KP。可能伴有由于小梁网炎(trabeculitis)导致的高眼压和角膜缘炎。
角膜葡萄膜炎型是实质炎、内皮炎、虹膜炎并发的重症型,表现为明显的充血、角膜水肿、Descemet’s membrane folds、KP、前房内细胞,重症病例可出现前房积脓。
在反复发作的病例中,角膜知觉减退变得明显,是各型诊断中重要的辅助依据。基质型和内皮型在病毒学诊断上比上皮型更困难,因此角膜知觉检查的重要性更高。使用Cochet-Bonnet角膜知觉计,通过调整尼龙丝的长度可以分阶段评估知觉阈值,也有助于确认左右差异。如果患者有单眼反复充血的病史,并且患侧有明显知觉减退,则无论为何种类型,都应高度怀疑角膜疱疹。但上皮型复发早期有些病例知觉减退不明显,仅凭知觉检查阴性不能排除本病。
文献报道,双侧HSV角膜炎的发生率为1.3%~12%6)。一项为期30年的回顾性研究显示,4%的患者在初次发病时为双侧性,另有1%在复发时发展为双侧6)。韩国的一项大规模研究报告为12%,印度的一项研究报告双侧发生率高达25%6)。尤其是类风湿关节炎患者(40%)和儿童(26%)的发生率很高,特应性体质和免疫抑制状态也容易导致双侧发病,需要引起注意6)。
单纯疱疹角膜炎是由HSV(一种双链DNA病毒)引起的。HSV-1主要感染口面部区域,HSV-2主要感染生殖器区域,但两者均可引起眼部感染。大多数角膜疱疹由HSV-1引起。
初次感染多在儿童期无症状发生。病毒通过感觉神经轴突到达三叉神经节,建立永久潜伏感染。潜伏病毒在某些诱因下再激活,经三叉神经到达角膜,引起复发性炎症。
以下情况双侧发病的风险较高6)。
角膜移植后HSV角膜炎在中国的一项回顾性研究(411例)中报道发病率为9.73%7)。65%的发病集中在术后1~3个月,术后类固醇使用被认为会促进病毒再活化7)。移植后HSV角膜炎按临床类型分布为:上皮型27.5%、坏死性基质型20%、混合型42.5%、内皮型10%7)。在有HSV角膜炎病史的眼上进行角膜移植,与圆锥角膜或Fuchs角膜内皮营养不良的移植相比,排斥反应和移植失败的风险显著更高7)。
《感染性角膜炎诊疗指南第3版》1)根据眼疱疹感染症研究会的诊断标准提出了以下内容。
但由于病毒分离培养在日常临床中几乎不进行,实际诊断需综合裂隙灯所见、辅助诊断和病毒学检查结果。
典型病例仅凭裂隙灯检查即可确诊。上皮型可见伴末端膨大的树枝状溃疡,实质型可见盘状浅层混浊和免疫环,内皮炎型可见扇形角膜水肿和KP等各型特异性表现。联合使用伍德灯下荧光素染色和玫瑰红染色。
角膜知觉检查是诊断角膜疱疹的重要辅助检查。推荐使用Cochet-Bonnet角膜知觉计,因其操作简便,可阶段性评估知觉减退程度1)。反复发作的病例可见明显的知觉减退,但该检查并非特异性检查,对初发或轻症病例未必有用。
《感染性角膜炎诊疗指南第3版》有条件地推荐以下检查1)。
需与假树枝状角膜炎及呈现类似病变的疾病进行鉴别,这一点非常重要。
| 鉴别疾病 | 鉴别要点 |
|---|---|
| 带状疱疹角膜炎(VZV) | 假树枝状病变:无末端膨大、荧光素染色弱、Hutchinson征、伴皮疹 |
| 棘阿米巴角膜炎 | 剧烈疼痛、放射状角膜神经炎、隐形眼镜佩戴史 |
| 复发性角膜糜烂 | 起床时急性发作、剧烈疼痛、外伤史 |
| 药物毒性角膜病变 | 滴眼液使用史、弥漫性点状表层角膜病变 |
| 巨细胞病毒性角膜内皮炎 | 钱币状病灶、线状KP、对阿昔洛韦无反应 |
| 角膜移植排斥反应 | KP局限于移植物后表面、Khodadoust线、对类固醇反应显著 |
角膜移植术后内皮炎与排斥反应的鉴别尤为重要。移植后HSV内皮炎中,KP分布于供体-受体交界处之外,单用类固醇无法改善,需加用抗病毒药物方可改善7)。而内皮排斥反应中,KP主要局限于移植物后表面,Khodadoust线从边缘向中央进展7)。
角膜知觉检查是诊断疱疹性角膜炎的有力辅助检查1)。尤其是反复发作的病例,可见明显的角膜知觉减退。Cochet-Bonnet角膜知觉计简便易用且可分级,因此很有用。但该检查并非特异性检查,不能单独用于确诊。由于基质型和内皮型的病毒分离及PCR敏感性低于上皮型,因此病史(复发史询问)和确认角膜知觉减退对诊断更为重要。
单纯疱疹角膜炎的治疗因病型而根本不同。上皮型由病毒直接增殖引起,因此以抗病毒药物为中心,禁忌使用类固醇滴眼液。基质型和内皮型以免疫反应为主,因此原则上联合使用抗病毒药物和类固醇滴眼液。
一线治疗是阿昔洛韦(ACV,Zovirax®)眼膏3%,每日5次给药1)。由于半衰期短,遵守用药次数很重要,低剂量存在耐药株出现的风险。上皮病变消失后减量为每日3次,1〜2周后停药。为预防混合感染,联合使用抗菌滴眼液(如左氧氟沙星0.5%每日3次等)。
| 药物 | 剂量 | 特点 |
|---|---|---|
| ACV眼膏3%(Zovirax®) | 每日滴眼5次 | 一线药物。因半衰期短,遵守用药次数很重要 |
| 伐昔洛韦片(Valtrex®)500mg | 每次2片,每日2次,餐后 | ACV的前体药物。出现副作用或耐药株时更换 |
| 左氧氟沙星滴眼液0.5%(Cravit®) | 每日滴眼3次 | 预防混合感染 |
| 三氟胸苷滴眼液1%(TFT) | 每日8~9次 | 对ACV耐药株有效。在美国使用(日本未批准) |
副作用的应对:ACV眼膏可能导致角膜下方中心点状表层角膜病变或眼睑结膜炎(基质反应)。轻度时可减量继续使用,重度时改为口服伐昔洛韦500mg 2片,分2次饭后服用。连续使用ACV眼膏1周无效时,需考虑ACV耐药株或表现为假树枝状角膜炎的其他疾病。
全身给药:感染性角膜炎诊疗指南第3版有条件地推荐上皮型使用抗病毒药全身给药(弱推荐,证据强度C)1)。口服阿昔洛韦2,000 mg/天可期待与ACV眼膏同等的效果,适用于眼膏毒性病例、耐药株病例及依从性不良病例。但在日本,HSV角膜炎的口服ACV不在医保范围内1)。
上皮型禁用类固醇滴眼液。类固醇会促进病毒活化,加重病情。
清创术(上皮刮除):为减少病毒量,可与抗病毒药联合进行树枝状病变的刮除。
实质性角膜炎主要是对病毒的免疫反应所致,因此原则上应采用糖皮质激素滴眼液抑制免疫反应联合ACV眼膏进行治疗1)。若不使用ACV眼膏而单独使用激素治疗,初期虽可缓解,但易复发和再燃,且在病程中有诱发上皮型角膜炎的风险1)。
HEDS(疱疹性眼病研究)-1的SKN(未使用类固醇的基质角膜炎)试验证实,在HSV基质型角膜炎中,局部使用皮质类固醇(磷酸泼尼松龙逐渐减量给药)与安慰剂相比,可使炎症持续/进展的风险降低68%,并缩短愈合时间3)。在6个月时,用药组的治疗失败率显著低于安慰剂组,且视力改善也更早获得3)。这是基质型角膜炎使用类固醇滴眼液的主要证据,也被日本感染性角膜炎诊疗指南第3版采纳为基质型治疗的基础1)。但HEDS试验设计并未显示试验药物ACV口服的叠加效果,因此全身抗病毒药物的联合使用需根据具体病例判断。
糖皮质激素滴眼液的实际使用:
联合抗病毒药物:联合使用ACV眼膏3%每日5次1)。
口服类固醇:伴有角膜炎葡萄膜炎等严重炎症或合并上皮缺损时,在滴眼基础上加服倍他米松(Rinderon®片0.5mg 2片 每日1次 早饭后)。
处方示例(重症实质型):
处方示例(合并上皮缺损时):
内皮炎的治疗参照实质型角膜炎的方案1)。若与实质型并存,则按照实质型的治疗原则进行。对于单纯内皮炎的ACV给药是局部还是全身使用,目前尚无统一意见。当角膜水肿变为不可逆时,适用角膜内皮移植术。
对于表现为单眼羊脂状KP、前房炎症和眼压升高的HSV前部葡萄膜炎,需联合使用抗病毒药物、类固醇滴眼液、瞳孔管理及眼压管理。
营养性角膜溃疡是一种不伴有病毒增殖的伤口愈合异常,因此治疗策略有很大不同。
《感染性角膜炎诊疗指南》第3版有条件地推荐全身使用抗病毒药物以预防上皮型角膜疱疹的复发(弱推荐,证据等级C)1)。
HEDS-APT试验中,ACV 400 mg每日两次、持续12个月的给药使上皮型和实质型HSV疾病的复发风险几乎减半,用药组为19%,安慰剂组为32%4)。超过12个月的长期给药显示可进一步延长复发间隔4)。在注意ACV耐药株出现可能性的同时,对于反复复发的病例和高危病例,这是一个有效的选择。
当药物疗法无效的瘢痕性角膜混浊残留时,适用角膜移植术。近年来,随着手术方式的进步和术后抗病毒预防的应用,治疗效果显著提高5)。
全层角膜移植术(PKP)
适应证:角膜穿孔或全层混浊
结果:无抗病毒预防时复发率44%,排斥率46%5)。联合口服ACV可将移植失败相对风险降至0.35)
问题:免疫排斥反应是移植失败的主要原因5)
深板层角膜移植术(DALK)
蘑菇状角膜移植术(MK)
适应证:DALK术中发生Descemet’s membrane perforation时的转换术式
结果:10年移植物存活率92%、排斥率9.7%、复发率7.8%5)
特点:9mm前部+6mm后部的双片式结构。通过最小程度的内皮置换减轻抗原负荷5)
术后抗病毒预防:美国眼科学会(AAO)的Corneal Edema and Opacification Preferred Practice Pattern以及AAO的HSV角膜炎治疗指南建议,角膜移植术后抗病毒预防应口服ACV 800 mg每日3次以上,或伐昔洛韦500 mg每日2次,持续至少1年5, 8, 9)。术后1~3个月是复发高峰期,此期间需特别注意7)。移植后HSV角膜炎复发时,应积极进行全身抗病毒治疗,并根据上皮状态、感染严重程度和排斥反应活动性谨慎调整类固醇剂量7)。
上皮型(活动性上皮疾病状态)禁用类固醇滴眼液。它会激活病毒复制,导致地图状溃疡的进展和病情恶化。另一方面,实质型(如盘状角膜炎)主要以对病毒的免疫反应为主,因此ACV眼膏与类固醇滴眼液的联合使用是标准治疗1, 3)。类固醇滴眼液不应突然停用,而应每月逐渐减量1)。
初次感染:初次感染通常发生于儿童期通过口腔颜面区域的接触,大多数为无症状经过。病毒通过角膜上皮细胞的特异性受体(如Nectin-1、HVEM等)侵入细胞内6)。感染后,病毒沿感觉神经轴突到达三叉神经节,建立永久性潜伏感染。
潜伏感染:HSV-1在神经元核内维持其基因组,逃避免疫系统的监视5)。潜伏期产生潜伏相关转录本(LAT),维持病毒基因组的完整性并抑制细胞凋亡6)。CD8阳性T细胞和细胞因子抑制病毒基因表达,使病毒维持静止状态5)。
再激活:多种诱因导致潜伏病毒再激活,沿三叉神经到达角膜。在COVID-19患者中,免疫抑制和细胞因子风暴综合征的发生导致HSV-1特异性CD8阳性T细胞耗竭,被认为会促进潜伏病毒的再激活6)。
在上皮型单纯疱疹病毒性角膜炎中,HSV在角膜上皮细胞中活跃复制。其特征是病毒在边缘而非上皮缺损处活跃复制。树枝状病变沿角膜神经模式形成。反复复发会导致角膜感觉神经受损,感觉减退逐渐加重。
HSV实质型角膜炎是以CD4阳性T细胞为主导的免疫反应为中心。摄取HSV抗原的朗格汉斯细胞(角膜的抗原呈递细胞)将抗原呈递给CD4阳性T细胞,活化的T细胞释放细胞因子。这导致中性粒细胞浸润角膜实质,引起组织破坏。小鼠模型显示,从角膜实质中清除CD4阳性T细胞后不会发生实质炎,证实免疫反应是实质型的核心病理机制。
此外,已证明HSV UL6蛋白与人角膜抗原之间存在分子拟态(molecular mimicry),表明自身免疫机制可能参与实质炎的慢性化和复发。
坏死性与非坏死性的区别:非坏死性(盘状)角膜炎是纯粹的迟发型超敏反应,不伴随病毒的活跃增殖。而坏死性角膜炎是指在反复发作的角膜中,新生血管引起的中性粒细胞浸润作用于实质内积累的抗原抗体复合物,导致更严重的组织破坏。
内皮炎究竟是由病毒直接感染引起的细胞损伤为主,还是以免疫学攻击为主,目前尚无定论。一般认为这两种病理状态可能同时存在。HSV引起的内皮炎常伴随着实质型或上皮型的病程,而单纯内皮炎的病理状态更多见于巨细胞病毒(CMV)1)。
营养性角膜溃疡是由反复发作过程中积累的多种因素共同导致的创面愈合异常。涉及的因素包括实质炎症、角膜感觉神经损伤、上皮基底膜损伤以及抗病毒药物的副作用等。HSV感染引起的角膜神经损伤会导致“神经营养性角膜病变”状态,加之泪液分泌减少和瞬目反射减弱,导致上皮愈合延迟。临床上,伴有病毒复制的地图状角膜炎表现为不规则上皮缺损,而营养性角膜溃疡的特征是椭圆形上皮缺损,边缘上皮呈灰白色圆形隆起,与实质层有轻微分离感。虽然不能分离出病毒,但高灵敏度PCR可能检测到残留DNA。由于不伴有病毒复制,停止抗病毒滴眼液和促进上皮愈合是治疗的基础。
阿昔洛韦在感染细胞内被病毒来源的胸苷激酶(thymidine kinase:TK)单磷酸化,再被宿主细胞的激酶三磷酸化。这种活性型抑制病毒DNA聚合酶,阻断病毒DNA合成。由于在正常细胞中不被磷酸化,因此对单纯疱疹病毒具有高选择性,副作用少。ACV耐药株主要是由于TK活性缺失或突变导致ACV无法磷酸化而产生,免疫缺陷患者的风险尤其高6)。
作为应对ACV耐药株的措施,针对HSV-1感染不同阶段的多种新型分子的研究正在推进6)。
BX795和OGT 2115对ACV耐药HSV株显示出有效性,是有前景的候选药物6)。由于HSV-1难以同时对3种不同的治疗机制产生耐药性,多种分子的联合用药有望成为未来的治疗策略6)。
在活动性上皮型HSV角膜炎患者的泪液中已鉴定出特异性代谢变化(精氨酸减少、鞘脂代谢改变),提示其作为通过无创泪液采样进行新型诊断生物标志物的潜力。
随着DALK和蘑菇形角膜移植的引入,HSV角膜炎的角膜移植效果得到了显著改善5)。大直径(9mm)DALK可显著减少术后散光,据报道44%的患者达到了20/20或更好的视力5)。通过高剂量初始给药和长期逐渐减量的方案,即使在伴有新生血管的瘢痕眼中也获得了良好的10年结果5)。
对于伴有严重炎症反应、大而深的溃疡和持续性上皮缺损的HSV角膜炎,已有药物联合羊膜移植治疗的报道7)。羊膜组织有助于促进上皮愈合、减轻炎症反应、抑制成纤维细胞增殖和抑制新生血管形成7)。
旨在预防HSV角膜炎复发的治疗性疫苗研究正在进行中,动物实验已证实可减轻角膜症状。供体角膜的常规HSV检测也已被提出,通过检测、治疗和预防有望提高移植片存活率;但由于费用和法律环境的限制,目前尚未普及7)。