Forme épithéliale (Epithelial type)
Kératite dendritique : Lésions épithéliales ramifiées caractéristiques avec renflements terminaux
Kératite géographique : Élargissement de la perte épithéliale dû à la persistance d’une kératite dendritique

La kératite herpétique simplex est une inflammation cornéenne causée par l’infection par le virus herpes simplex (HSV). Dans la majorité des cas, le virus en cause est le type 1 (HSV-1), les cas dus au type 2 (HSV-2) étant extrêmement rares. Le HSV est un virus neurotrope appartenant à la sous-famille des Alphaherpesvirinae, famille des Herpesviridae, capable de rester en latence dans le ganglion trigéminé et de persister à vie.
Peu de cas développent une kératite lors de l’infection primaire. Habituellement, le HSV latent dans le ganglion trigéminé est réactivé par des facteurs déclenchants tels que fièvre, rhume, stress, exposition aux UV, puis migre le long du nerf trijumeau jusqu’à la cornée pour provoquer diverses lésions. La caractéristique majeure est qu’il s’agit d’une maladie récurrente, et une anamnèse minutieuse, quel que soit le type de la maladie, constitue le point de départ du diagnostic et de la décision thérapeutique.
Selon les estimations basées sur la population de 2016, l’incidence globale de la kératite herpétique (HSV) est estimée à 24,0 cas pour 100 000 personnes par an, avec environ 1,7 million de personnes touchées chaque année dans le monde2). Parmi celles-ci, la forme épithéliale représente environ 16,1 cas pour 100 000 personnes (environ 1,2 million de cas par an) et la forme stromale environ 4,9 cas (environ 370 000 cas par an)2). On estime qu’environ 230 000 personnes par an développent une nouvelle déficience visuelle unilatérale liée à la kératite herpétique (acuité visuelle inférieure à 6/12)2).
Environ 67 % de la population mondiale (4,85 milliards de personnes) a déjà été infectée par le HSV-1, et la prévalence du HSV-1 est particulièrement plus élevée dans les régions autres que les États-Unis et l’Europe, avec un accès aux traitements limité. Par conséquent, le fardeau réel de la maladie est probablement sous-estimé2). La kératite herpétique est la première cause de cécité cornéenne dans les pays développés. En particulier, la forme stromale entraîne une acuité visuelle corrigée inférieure à 6/12 chez 24 à 42 % des patients et une déficience visuelle sévère (inférieure à 6/60) chez 1,5 à 3,0 % des cas2).
En ce qui concerne les enquêtes épidémiologiques propres au Japon, la surveillance nationale des kératites infectieuses montre que la kératite virale occupe une place importante aux côtés des kératites bactériennes, fongiques et à Acanthamoeba. La kératite herpétique est considérée comme une maladie emblématique qui évolue de manière chronique et récurrente, influençant le pronostic visuel, y compris au Japon1). En termes de répartition par âge, la majorité des patients sont d’âge moyen ou plus âgés, mais la première manifestation peut survenir à tout âge, de l’enfance à la vieillesse. La baisse de l’immunité cellulaire liée à l’âge est un facteur qui augmente l’incidence de nouveaux cas6).
La classification des formes cliniques proposée par le Groupe d’étude des infections oculaires à herpès (Ohashi Yuichi et al., 1995) est également adoptée dans la 3e édition des recommandations pour le traitement de la kératite infectieuse1). Cette classification repose sur la localisation des lésions et les différences pathologiques, constituant un cadre essentiel qui oriente la stratégie thérapeutique.
Forme épithéliale (Epithelial type)
Kératite dendritique : Lésions épithéliales ramifiées caractéristiques avec renflements terminaux
Kératite géographique : Élargissement de la perte épithéliale dû à la persistance d’une kératite dendritique
Type stromal (Stromal type)
Kératite disciforme: Opacité stromale circulaire et œdème dus à une réaction d’hypersensibilité retardée
Kératite nécrosante: Opacité stromale dense avec envahissement vasculaire, risque de perforation
Type endothélial (Endothelial type)
Endothélite cornéenne: Œdème cornéen et dépôts rétro-cornéens prédominants, opacité stromale minime
Kératite limbique: Œdème en éventail avec base au limbe, accompagné d’hypertension oculaire
Lésions secondaires
Déficit épithélial persistant: Déficit épithélial secondaire dû à un retard de cicatrisation
Ulcère cornéen trophique: Ulcère dû à une neuropathie sensitive et à une anomalie de la cicatrisation
Le type épithélial est une pathologie due à la multiplication virale directe dans les cellules épithéliales, tandis que le type stromal est dominé par la réponse immunitaire et inflammatoire au virus. Pour le type endothélial, on ne sait pas encore si l’infection directe ou la réponse immunitaire prédomine. L’ulcère cornéen trophique est une anomalie de la cicatrisation sans multiplication virale, il ne s’agit pas d’une lésion propre au HSV mais d’une complication secondaire. Ces différences pathologiques entraînent des différences fondamentales dans la stratégie thérapeutique.
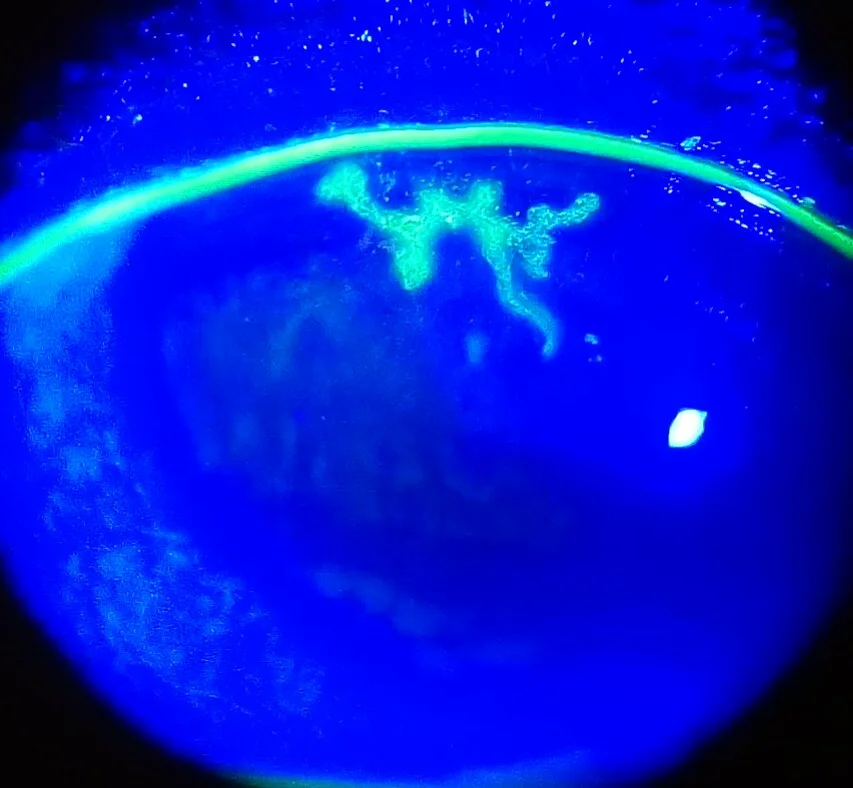
Les symptômes subjectifs de la kératite herpétique simplex varient considérablement selon le type de la maladie.
La kératite dendritique (dendritic keratitis), lésion caractéristique de l’herpès cornéen de type épithélial, présente 4 caractéristiques clés pour le diagnostic1).
La coloration à la fluorescéine est positive au fond de l’ulcère, tandis que l’épithélium œdémateux des bords est coloré au rose bengale. Lorsque la kératite dendritique s’aggrave, la perte de substance épithéliale s’étend et prend la forme d’une kératite géographique (geographic keratitis). Elle progresse plus facilement chez les patients immunodéprimés ou sous stéroïdes. Le liséré demeure intact et la présence d’une queue dendritique (dendritic tail) constitue un indice diagnostique.
L’herpès cornéen est généralement unilatéral, mais la fréquence des cas bilatéraux est de 1,3 à 12 % dans la littérature6). Les patients atopiques, ceux atteints de polyarthrite rhumatoïde (bilatéralité 40 %), les immunodéprimés et les enfants (26 %) présentent un risque bilatéral plus élevé6).
La kératite disciforme (disciform keratitis), forme typique de l’herpès cornéen stromal, se caractérise par les signes suivants1).
Avec les récidives répétées, l’opacité devient irrégulière et s’étend aux couches profondes. Outre l’opacité, les lésions se présentent sous diverses formes, rendant le diagnostic difficile dans de nombreux cas sur la seule base de l’examen à la lampe à fente.
La kératite nécrosante (necrotizing keratitis) est une pathologie caractérisée par une prolifération du HSV dans le stroma cornéen ou une réaction immunitaire excessive contre l’antigène1). Elle survient facilement lors de récidives dans des yeux présentant une invasion vasculaire, une cicatrisation stromale ou une dégénérescence graisseuse. Elle se manifeste par une opacité stromale dense et irrégulière avec invasion vasculaire ; dans les cas accompagnés d’une perte épithéliale, l’amincissement stromal peut conduire à une perforation. Grâce à un traitement précoce et approprié, les cas graves sont devenus rares ces dernières années.
L’endothélite (endotheliitis) est diagnostiquée cliniquement lorsqu’on observe un œdème épithélial et stromal cornéen avec des KP concordant avec la zone lésionnelle, mais que l’opacité stromale ou les cellules de la chambre antérieure sont très minimes1). La forme typique de l’endothélite herpétique est la forme œdémateuse paracentrale, où l’œdème cornéen est en éventail avec la base au limbe et des KP au centre. Elle peut s’accompagner d’une hypertension oculaire due à une trabéculite et d’une inflammation limbique.
La forme kératouvéale est une forme grave associant stromatite, endothélite et iritis, se manifestant par une hyperhémie marquée, un œdème cornéen, des plis de la membrane de Descemet, des KP, des cellules dans la chambre antérieure ; dans les cas graves, un hypopyon peut survenir.
Chez les patients ayant présenté des récidives répétées, l’hypoesthésie cornéenne devient marquée et constitue un signe d’appoint diagnostique important quel que soit le type clinique. Dans les formes stromale et endothéliale, le diagnostic virologique est plus difficile que dans la forme épithéliale, ce qui rend l’examen de la sensibilité cornéenne d’autant plus important. L’utilisation de l’esthésiomètre cornéen de Cochet-Bonnet permet d’évaluer le seuil de sensibilité par paliers en ajustant la longueur du filament de nylon, et est également utile pour confirmer une différence entre les deux yeux. Chez les patients ayant des antécédents d’hyperémie récurrente unilatérale et présentant une hypoesthésie évidente du côté atteint, cela constitue un argument solide pour suspecter un herpès cornéen quel que soit le type clinique. Cependant, au début de la récidive de la forme épithéliale, certains cas ne présentent pas d’hypoesthésie nette, et l’examen de la sensibilité négatif à lui seul ne permet pas d’exclure cette maladie.
Dans la littérature, la fréquence de la kératite HSV bilatérale est rapportée entre 1,3 et 12 %6). Une étude rétrospective sur 30 ans a montré que 4 % de l’ensemble des patients présentaient une atteinte bilatérale dès le premier épisode, et 1 % supplémentaire lors d’une récidive6). Une grande étude coréenne rapporte une fréquence de 12 %, tandis qu’une étude indienne rapporte une fréquence allant jusqu’à 25 %6). Chez les patients atteints de polyarthrite rhumatoïde, cette fréquence atteint 40 %, et chez les enfants, 26 %. Les patients présentant une diathèse atopique ou un état d’immunosuppression sont également plus susceptibles de développer une atteinte bilatérale, nécessitant une attention particulière6).
La kératite herpétique simplex est causée par le HSV, un virus à ADN double brin. Le HSV-1 infecte principalement la région orofaciale, tandis que le HSV-2 infecte principalement la région génitale, mais les deux peuvent provoquer une infection oculaire. La grande majorité des cas d’herpès cornéen est due au HSV-1.
L’infection primaire survient souvent de manière asymptomatique dans l’enfance. Le virus migre le long des axones des nerfs sensoriels jusqu’au ganglion trigéminal et y établit une latence permanente. Le virus latent se réactive sous l’effet de certains déclencheurs, emprunte le nerf trijumeau pour atteindre la cornée et provoque une inflammation récurrente.
Les conditions suivantes présentent un risque élevé d’atteinte bilatérale6) :
La kératite herpétique après greffe de cornée a été rapportée avec une incidence de 9,73 % dans une étude rétrospective chinoise (411 cas)7). 65 % des cas surviennent dans les 1 à 3 mois suivant la chirurgie et l’utilisation de stéroïdes postopératoires est considérée comme favorisant la réactivation virale7). La fréquence des différents types de kératite herpétique post-greffe était : forme épithéliale 27,5 %, forme stromale nécrosante 20 %, forme mixte 42,5 % et forme endothéliale 10 %7). La greffe de cornée sur un œil ayant des antécédents de kératite herpétique présente un risque significativement plus élevé de rejet et d’échec du greffon par rapport à la greffe pour le kératocône ou la dystrophie endothéliale de Fuchs7).
Les recommandations de pratique clinique pour la kératite infectieuse, 3e édition1), présentent les critères diagnostiques suivants basés sur ceux de la Société de recherche sur l’infection herpétique oculaire.
Cependant, comme l’isolement et la culture du virus sont rarement réalisés en pratique clinique courante, le diagnostic repose en pratique sur une combinaison des signes à la lampe à fente, des examens auxiliaires et des tests virologiques.
Dans les cas typiques, le diagnostic peut être posé sur les seuls signes à la lampe à fente. Dans la forme épithéliale, on observe un ulcère dendritique avec terminal bulb ; dans la forme stromale, une opacité superficielle en disque et un anneau immunitaire ; dans l’endothélite, un œdème cornéen en éventail et des précipités rétro-cornéens (KP) — des signes spécifiques à chaque forme. La coloration à la fluorescéine et au rose Bengale sous filtre de Wood est utilisée en complément.
Le test de sensibilité cornéenne est un examen auxiliaire précieux pour le diagnostic de l’herpès cornéen. L’esthésiomètre cornéen de Cochet-Bonnet est recommandé car il est simple d’utilisation et permet une évaluation graduelle du degré d’hypoesthésie1). Chez les patients présentant des récidives répétées, on observe une hypoesthésie marquée, mais il convient de noter qu’il ne s’agit pas d’un test spécifique et qu’il n’est pas toujours utile dans les cas primaires ou les formes légères.
Les recommandations de pratique clinique pour la kératite infectieuse, 3e édition, recommandent sous conditions les examens suivants1).
Il est important de différencier la kératite pseudo-dendritique et les maladies présentant des lésions similaires.
| Diagnostic différentiel | Points clés du diagnostic différentiel |
|---|---|
| Kératite zostérienne (VZV) | Lésions pseudo-dendritiques : pas de renflement terminal, coloration à la fluorescéine faible, signe de Hutchinson, accompagné d’une éruption cutanée |
| Kératite amibienne à Acanthamoeba | Douleur intense, kératonévrite radiaire, antécédent de port de lentilles de contact |
| Érosion cornéenne récidivante | Apparition aiguë au réveil, douleur intense, antécédent de traumatisme |
| Kératopathie toxique médicamenteuse | Antécédent d’utilisation de collyres, kératopathie ponctuée superficielle diffuse |
| Endothélite cornéenne à CMV | Lésion en pièce de monnaie, KP linéaires, sans réponse à l’acyclovir |
| Rejet de greffe de cornée | KP localisés à la face postérieure du greffon, ligne de Khodadoust, excellente réponse aux stéroïdes |
La distinction entre l’endothélite et le rejet après greffe de cornée est particulièrement importante. Dans l’endothélite herpétique post-greffe, les KP se distribuent au-delà de la jonction donneur-receveur et ne s’améliorent pas avec les stéroïdes seuls mais s’améliorent avec l’ajout d’antiviraux7). En revanche, dans le rejet endothélial, les KP sont principalement localisés à la face postérieure du greffon, avec une ligne de Khodadoust progressant du bord vers le centre7).
L’examen de la sensibilité cornéenne est un examen complémentaire utile pour le diagnostic de l’herpès cornéen1). En particulier chez les patients présentant des récidives fréquentes, on observe une diminution marquée de la sensibilité cornéenne. L’esthésiomètre cornéen de Cochet-Bonnet est utile car il est simple d’utilisation et permet de graduer le degré de sensibilité. Cependant, il ne s’agit pas d’un examen spécifique, il ne peut donc pas poser un diagnostic de certitude à lui seul. Étant donné que la sensibilité de l’isolement viral et de la PCR est plus faible dans les formes stromales et endothéliales que dans la forme épithéliale, les antécédents du patient (recherche d’antécédents de récidive) et la confirmation de la diminution de la sensibilité cornéenne deviennent plus importants pour le diagnostic.
Le traitement de la kératite herpétique simplex diffère fondamentalement selon le type de la maladie. Dans la forme épithéliale, due à la multiplication directe du virus, les antiviraux sont au centre du traitement et les collyres stéroïdiens sont contre-indiqués. Dans les formes stromale et endothéliale, à prédominance immuno-allergique, le principe est l’association d’antiviraux et de collyres stéroïdiens.
Le traitement de première intention est la pommade ophtalmique d’acyclovir (ACV, Zovirax®) à 3%, à appliquer 5 fois par jour1). En raison de sa demi-vie courte, le respect de la fréquence d’application est important ; une dose faible comporte un risque d’apparition de souches résistantes. Une fois les lésions épithéliales disparues, réduire à 3 fois par jour et arrêter après 1 à 2 semaines. Associer un collyre antibactérien (lévofloxacine 0,5% 3 fois par jour, etc.) pour prévenir une surinfection.
| Médicament | Posologie | Caractéristiques |
|---|---|---|
| Pommade ophtalmique ACV 3% (Zovirax®) | Application 5 fois/jour | Traitement de première intention. La demi-vie étant courte, le respect du nombre d’administrations est important |
| Comprimé de valacyclovir (Valtrex®) 500 mg | 2 comprimés en 2 prises après les repas | Promédicament de l’ACV. Changer en cas d’effets secondaires ou de souche résistante |
| Levofloxacine collyre 0,5 % (Cravit®) | 3 fois par jour en instillation | Prévention de la surinfection |
| Trifluridine collyre 1 % (TFT) | 8 à 9 fois par jour | Efficace contre les souches résistantes à l’ACV. Utilisé aux États-Unis (non approuvé au Japon) |
Prise en charge des effets secondaires : La pommade ophtalmique d’ACV peut provoquer une kératite ponctuée superficielle au centre inférieur de la cornée ou une conjonctivite palpébrale (réaction au véhicule). En cas de forme légère, la poursuite du traitement à dose réduite est possible, mais en cas de forme sévère, passer au valacyclovir 500 mg, 2 comprimés en 2 prises après les repas. Si aucune amélioration n’est observée après une semaine de pommade ACV, envisager une souche résistante à l’ACV ou une autre pathologie se présentant comme une kératite pseudo-dendritique.
Voie systémique : La 3e édition des recommandations pour la kératite infectieuse recommande sous condition l’administration systémique d’antiviraux pour la forme épithéliale (recommandation faible, niveau de preuve C)1). L’acyclovir oral à 2 000 mg/jour a une efficacité équivalente à celle de la pommade ACV et est utile en cas de toxicité de la pommade, de souche résistante ou de mauvaise observance. Cependant, au Japon, l’ACV oral pour la kératite herpétique n’est pas couvert par l’assurance maladie1).
Les collyres stéroïdiens sont contre-indiqués dans la forme épithéliale. Les stéroïdes favorisent l’activation virale et aggravent la pathologie.
Débridement (grattage épithélial) : Il peut être réalisé en association avec les antiviraux pour réduire la charge virale par grattage des lésions dendritiques.
La forme stromale étant principalement due à une réaction immunitaire contre le virus, le principe est l’association d’un collyre stéroïdien pour supprimer la réaction immunitaire et de la pommade ACV1). Si le traitement est effectué par stéroïdes seuls sans pommade ACV, une amélioration initiale est possible mais les récidives et les rechutes sont fréquentes, avec un risque d’induction de la forme épithéliale en cours de traitement1).
L’essai SKN (Stromal Keratitis Not on steroids) de l’étude HEDS (Herpetic Eye Disease Study)-1 a démontré que les corticostéroïdes topiques (prednisolone phosphate en dégression) réduisaient de 68% le risque de persistance/progression de l’inflammation et raccourcissaient le temps de guérison par rapport au placebo dans la kératite stromale herpétique à HSV3). Le taux d’échec thérapeutique à 6 mois était significativement plus faible dans le groupe traité, et l’amélioration visuelle a également été obtenue plus précocement3). Il s’agit de la preuve principale de l’utilisation des corticoïdes en collyre dans la kératite stromale, et cette approche est adoptée comme traitement de base dans la 3ᵉ édition des recommandations cliniques japonaises pour la kératite infectieuse1). Cependant, comme le design de l’essai HEDS n’a pas démontré de bénéfice additionnel de l’ACV oral, l’utilisation concomitante d’antiviraux systémiques est décidée au cas par cas.
Pratique des corticoïdes en collyre:
Association d’antiviraux:Associer une pommade ophtalmique d’ACV à 3% 5 fois par jour1).
Corticoïdes oraux:En cas d’inflammation sévère avec kératouvéite ou de défaut épithélial, associer de la bétaméthasone orale (Rinderon® comprimés 0,5mg, 2 comprimés en une prise après le petit-déjeuner) en complément des collyres.
Exemple d’ordonnance (kératite stromale sévère):
Exemple d’ordonnance (en cas de perte épithéliale associée) :
L’endothélite est traitée selon les mêmes principes que la kératite stromale1). En cas d’association à une kératite stromale, le traitement suit celui de la forme stromale. Il n’existe pas de consensus clair concernant l’administration locale ou systémique d’ACV pour une endothélite pure. En cas d’œdème cornéen irréversible, une greffe endothéliale de la cornée est indiquée.
L’uvéite antérieure à HSV se manifestant par des KP unilatéraux graisseux, une inflammation de la chambre antérieure et une hypertonie oculaire est traitée par une combinaison d’antiviraux, de corticostéroïdes topiques, de gestion pupillaire et de contrôle de la pression intraoculaire.
L’ulcère cornéen trophique est un trouble de la cicatrisation sans multiplication virale active ; la stratégie thérapeutique est donc radicalement différente.
La troisième édition des recommandations pour la prise en charge des kératites infectieuses recommande sous condition l’administration systémique d’antiviraux pour la prévention des récidives de l’herpès cornéen épithélial (recommandation faible, niveau de preuve C)1).
Dans l’essai HEDS-APT, l’administration d’ACV 400 mg deux fois par jour pendant 12 mois a réduit de près de moitié le risque de récidive de la maladie HSV épithéliale et stromale, avec 19 % dans le groupe traité contre 32 % dans le groupe placebo4). Un traitement prolongé au-delà de 12 mois a montré un allongement supplémentaire de l’intervalle entre les récidives4). Bien qu’il faille tenir compte du risque d’émergence de souches résistantes à l’ACV, cette option reste efficace pour les cas de récidives fréquentes ou à haut risque.
La greffe de cornée est indiquée lorsqu’il persiste une opacité cornéenne cicatricielle ne répondant pas au traitement médical. Les progrès récents des techniques chirurgicales et de la prophylaxie antivirale postopératoire ont considérablement amélioré les résultats5).
Greffe transfixiante de cornée (PKP)
Indications : Perforation cornéenne ou opacité de toute l’épaisseur
Résultats : Taux de récidive de 44 %, taux de rejet de 46 % sans prophylaxie antivirale5). Le risque relatif d’échec du greffon est réduit à 0,3 avec l’ACV oral associé5)
Problèmes : Le rejet immunologique est la principale cause d’échec du greffon5)
Greffe lamellaire antérieure profonde (DALK)
Indications : Cas d’opacité stromale avec endothélium sain
Résultats : Taux de récidive de 6 à 10 %, taux de rejet de 0 à 4,5 %, survie à 5 ans de 96 %5). Nettement supérieur à la PKP (survie à 5 ans de 78,8 %)
Avantages : Préserve l’endothélium de l’hôte, donc moins de rejet immunologique5)
Greffe de cornée en champignon (MK)
Indications : Technique de conversion en cas de perforation de la membrane de Descemet au cours d’un DALK
Résultats : Taux de survie du greffon à 10 ans 92 %, taux de rejet 9,7 %, taux de récidive 7,8 %5)
Caractéristiques : Structure en 2 pièces de 9 mm antérieur + 6 mm postérieur. Remplacement endothélial minimal pour réduire la charge antigénique5)
Prévention antivirale postopératoire : L’American Academy of Ophthalmology (AAO), dans son Corneal Edema and Opacification Preferred Practice Pattern et ses recommandations pour le traitement de la kératite herpétique, préconise une prophylaxie antivirale après greffe de cornée par ACV oral 800 mg 3 fois/jour ou valaciclovir 500 mg 2 fois/jour pendant au moins 1 an5, 8, 9). Le pic de récidive se situe entre 1 et 3 mois après l’opération, période nécessitant une attention particulière7). En cas de récidive d’une kératite herpétique après greffe, un traitement antiviral systémique agressif doit être instauré et la posologie des corticoïdes ajustée prudemment en fonction de l’état de l’épithélium, de la sévérité de l’infection et de l’activité du rejet7).
Les collyres corticostéroïdes sont contre-indiqués dans la forme épithéliale (en présence d’une maladie épithéliale active). Les corticoïdes activent la réplication virale, entraînant une progression vers un ulcère géographique et une aggravation de la pathologie. En revanche, dans la forme stromale (kératite disciforme par exemple), où la réaction immunitaire contre le virus prédomine, l’association d’une pommade ophtalmique d’ACV et de collyres corticostéroïdes constitue le traitement standard1, 3). Il est essentiel de réduire progressivement les collyres corticostéroïdes sur plusieurs mois sans les arrêter brutalement1).
Chez les patients ayant des antécédents de kératite herpétique, il est recommandé de débuter un traitement antiviral oral (acyclovir 800 mg 3 fois/jour ou valacyclovir 500 mg 2 fois/jour) avant la chirurgie et de le poursuivre au moins 1 an après l’opération5, 8). La période de 1 à 3 mois après la chirurgie correspond au pic de récidive, ce qui rend cette période particulièrement importante7). Concernant le choix de la technique chirurgicale, la DALK préserve l’endothélium de l’hôte et présente un taux de survie à 5 ans de 96 %, supérieur à celui de la PKP (78,8 %)5). La greffe de cornée en champignon atteint également un taux de survie du greffon de 92 % à 10 ans5).
Infection primaire : L’infection primaire survient généralement pendant l’enfance par contact avec la région orofaciale et est asymptomatique dans la majorité des cas. Le virus pénètre dans les cellules via des récepteurs spécifiques sur les cellules épithéliales cornéennes (tels que Nectin-1, HVEM)6). Après l’infection, le virus migre le long des axones nerveux sensoriels jusqu’au ganglion trigéminé où il établit une infection latente permanente.
Infection latente : Le HSV-1 maintient son génome dans le noyau des neurones et échappe à la surveillance du système immunitaire5). Pendant la phase de latence, le virus produit des transcrits associés à la latence (LAT) qui maintiennent l’intégrité du génome viral tout en inhibant l’apoptose cellulaire6). Les lymphocytes T CD8+ et les cytokines suppriment l’expression des gènes viraux, maintenant le virus dans un état quiescent5).
Réactivation : Le virus latent est réactivé par divers facteurs déclenchants et atteint la cornée le long du nerf trijumeau. Chez les patients COVID-19, une immunosuppression et un syndrome de tempête cytokinique surviennent, et l’épuisement des lymphocytes T CD8 positifs spécifiques du HSV-1 favoriserait la réactivation du virus latent6).
Dans l’herpès cornéen de forme épithéliale, le HSV se réplique activement dans les cellules épithéliales de la cornée. La caractéristique est que le virus se réplique activement au niveau du limbe, et non au niveau de la zone de perte épithéliale. Les lésions dendritiques se forment le long du trajet des nerfs cornéens. Les récidives répétées endommagent les nerfs sensoriels de la cornée et entraînent une diminution progressive de la sensibilité.
La kératite stromale à HSV est principalement une réaction immunitaire menée par les lymphocytes T CD4 positifs. Les cellules de Langerhans (cellules présentatrices d’antigène de la cornée) qui ont capté l’antigène HSV présentent l’antigène aux lymphocytes T CD4 positifs, et les lymphocytes T activés libèrent des cytokines. Cela entraîne une infiltration de neutrophiles dans le stroma cornéen, provoquant une destruction tissulaire. Des modèles murins ont montré que l’élimination des lymphocytes T CD4 positifs du stroma cornéen empêche le développement de la kératite stromale, confirmant que la réaction immunitaire est le mécanisme pathologique central de la forme stromale.
De plus, il a été démontré qu’il existe un mimétisme moléculaire (molecular mimicry) entre la protéine UL6 du HSV et les antigènes cornéens humains, et un mécanisme auto-immun pourrait être impliqué dans la chronicisation et la récidive de la kératite stromale.
Différence entre les formes nécrosante et non nécrosante : La kératite non nécrosante (disciforme) est une réaction d’hypersensibilité retardée pure, sans réplication virale active. En revanche, dans la kératite nécrosante, les complexes antigène-anticorps accumulés dans le stroma de la cornée lors de récidives répétées entraînent une infiltration de neutrophiles par les néovaisseaux, provoquant une destruction tissulaire plus sévère.
On ne sait pas encore si l’endothélite est due à une lésion cellulaire directe par le virus ou principalement à une attaque immunitaire. Il est probable que les deux mécanismes pathologiques coexistent. L’endothélite herpétique (HSV) est souvent associée à une kératite stromale ou épithéliale au cours de l’évolution, alors que l’endothélite pure est plus souvent causée par le cytomégalovirus (CMV)1).
L’ulcère cornéen trophique est une anomalie de la cicatrisation qui résulte de l’accumulation de multiples facteurs au cours des récidives répétées. Les facteurs impliqués comprennent l’inflammation stromale, les lésions des nerfs cornéens, l’atteinte de la membrane basale épithéliale et les effets secondaires des médicaments antiviraux. Les lésions des nerfs cornéens dues à l’infection par le HSV induisent une « kératopathie neurotrophique » qui, associée à une diminution de la sécrétion lacrymale et une réduction du réflexe de clignement, retarde la cicatrisation épithéliale. Cliniquement, alors que la kératite géographique avec réplication virale présente des pertes de substance épithéliales de forme irrégulière, l’ulcère cornéen trophique se caractérise par une perte de substance épithéliale ovalaire, dont le bord épithélial est surélevé, arrondi et blanc grisâtre, donnant l’impression de flotter légèrement au-dessus du stroma. Le virus n’est pas isolé, mais une PCR très sensible peut parfois détecter de l’ADN résiduel. En l’absence de réplication virale, l’arrêt des collyres antiviraux et la promotion de la cicatrisation épithéliale constituent la base du traitement.
L’aciclovir est d’abord mono-phosphorylé par la thymidine kinase (TK) d’origine virale dans les cellules infectées, puis tri-phosphorylé par les kinases de la cellule hôte. Cette forme active inhibe l’ADN polymérase virale et bloque la synthèse de l’ADN viral. Comme elle n’est pas phosphorylée dans les cellules normales, elle présente une sélectivité élevée pour le virus herpes simplex et peu d’effets secondaires. Les souches résistantes à l’ACV résultent principalement d’une perte ou d’une mutation de l’activité TK, empêchant la phosphorylation de l’ACV, et le risque est particulièrement élevé chez les patients immunodéprimés6).
Pour faire face aux souches résistantes à l’ACV, des recherches sont en cours sur plusieurs nouvelles molécules ciblant différentes étapes de l’infection par le HSV-16).
BX795 et OGT 2115 ont montré leur efficacité contre les souches HSV résistantes à l’ACV et sont des candidats prometteurs6). Étant donné qu’il est difficile pour le HSV-1 d’acquérir simultanément une résistance à trois mécanismes thérapeutiques différents, la combinaison de plusieurs molécules est envisagée comme une stratégie thérapeutique future6).
Des modifications métaboliques spécifiques (diminution de l’arginine, altérations du métabolisme des sphingolipides) ont été identifiées dans les larmes de patients atteints de kératite HSV épithéliale active, suggérant leur potentiel en tant que nouveaux biomarqueurs diagnostiques par prélèvement lacrymal non invasif.
L’introduction de la DALK et de la greffe de cornée en champignon a considérablement amélioré les résultats des greffes de cornée pour la kératite herpétique5). La DALK de grand diamètre (9 mm) a significativement réduit l’astigmatisme postopératoire, 44 % des patients atteignant une acuité visuelle de 20/20 ou plus5). Un protocole de dose initiale élevée suivi d’une diminution progressive à long terme a montré de bons résultats à 10 ans, même dans les yeux cicatriciels avec néovascularisation5).
L’association d’un traitement médicamenteux et d’une greffe de membrane amniotique a été rapportée pour la kératite herpétique accompagnée d’une réaction inflammatoire sévère, d’ulcères profonds et étendus, et de défauts épithéliaux persistants7). Le tissu de la membrane amniotique contribue à la promotion de la cicatrisation épithéliale, à la réduction de l’inflammation, à l’inhibition de la prolifération des fibroblastes et à la suppression de la néovascularisation7).
Des recherches sur un vaccin thérapeutique visant à prévenir la récidive de la kératite herpétique sont en cours et des expériences animales ont confirmé une réduction des symptômes cornéens. Le dépistage systématique du HSV sur les cornées de donneurs est également proposé, ce qui pourrait améliorer le taux de survie des greffons grâce à la détection, au traitement et à la prévention, mais cela ne s’est pas encore généralisé en raison des contraintes de coût et du cadre juridique7).