初期
放射狀角膜神經炎:從角膜緣向角膜中央沿神經分佈的線狀浸潤。這是棘阿米巴角膜炎非常特異的所見。
上皮/上皮下浸潤:點狀、斑狀、線狀混濁聚集。
偽樹枝狀病變:螢光素染色可見邊緣呈鋸齒狀的不規則線狀病變。與皰疹性樹枝狀病變(伴有終端膨大)的鑑別診斷很重要。
睫狀充血和角膜緣水腫:即使角膜病變輕微也可出現。

棘阿米巴角膜炎(Acanthamoeba keratitis;AK)是由棘阿米巴引起的角膜感染性疾病,棘阿米巴是一種廣泛存在於土壤、淡水和自來水中的自由生活阿米巴。該病於1973–74年由Nagington等人首次報告,日本於1988年由石橋等人報告了首例病例。最初,除外傷相關病例外,該病極為罕見,但自2000年代以來,隨著隱形眼鏡(CL)佩戴的普及,病例數不斷增加,目前已成為全球性的重要問題,尤其集中在隱形眼鏡佩戴者中10)。
主要致病菌種為 Acanthamoeba castellanii 和 A. polyphaga 兩種,在基因型中,T4型佔所有病例的94.3%4)。棘阿米巴具有營養體和包囊兩種形態,當生長條件惡化時會形成包囊,並對多種藥物產生抗藥性10)。棘阿米巴角膜炎約佔所有微生物角膜炎的1.5%,發生率估計約為每百萬人2.3眼。根據英國和荷蘭2015年的數據,年發生率約為每1萬隱形眼鏡佩戴者0.31–0.48例,其中約半數患者會發展為視力障礙1)。
棘阿米巴角膜炎是重症隱形眼鏡相關角膜炎的主要原因之一,85~90%的患者為CL佩戴者。日本CL佩戴者重症角膜感染症調查顯示,棘阿米巴角膜炎的發生率僅次於綠膿桿菌角膜潰瘍,位居第二位。延誤治療可能導致角膜穿孔或失明,是一種可在年輕、健康的社會活動族群中造成不可逆視功能損害的疾病。
Carnt等人(2023)的病例對照研究顯示,使用可重複使用的日護理鏡片與拋棄式鏡片相比,罹患棘阿米巴角膜炎的風險高出約3.8倍(OR 3.84; 95% CI 1.75–8.43)1)。嚴重發炎性併發症的發生率也很高,Carnt等人(2018)的194例世代研究中,鞏膜炎約20%、基質環狀浸潤約15%,最終視力0.1以下、穿孔、角膜移植等不良預後占整體的48%2)。作為隱形眼鏡使用者的嚴重角膜感染,這已成為一個公共衛生議題。
雖然CL佩戴者佔大多數,但非CL佩戴者也可能因外傷或接觸污染水而發病。在印度等地,外傷相關病例較多11)。
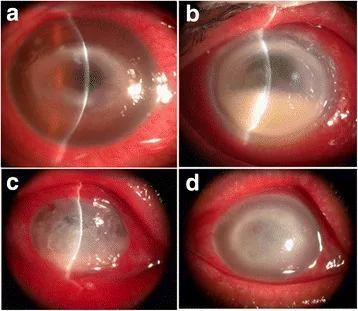
棘阿米巴角膜炎最具特徵性的症狀是與臨床表現不相稱的劇烈眼痛。由於病變在非常輕微的階段就會出現劇烈疼痛,即使就診時角膜表現輕微,也不能排除本病的可能。
症狀進展緩慢,從初發到完成期通常需要數週至1~2個月。但疼痛相對早期即較明顯,患者常因無法忍受而反覆就診。Carnt等(2018)的報告顯示,預後不良病例中症狀持續時間中位數超過37天,對於伴有長期疼痛的隱形眼鏡佩戴者的角膜炎,應始終懷疑本病2)。
棘阿米巴角膜炎緩慢進展,根據病程呈現特徵性臨床所見。根據角膜所見特徵分為初期、移行期、完成期三期。感染性角膜炎診療指引第3版也明確列出了最具特徵的「初期」和「完成期」所見10)。
初期
放射狀角膜神經炎:從角膜緣向角膜中央沿神經分佈的線狀浸潤。這是棘阿米巴角膜炎非常特異的所見。
上皮/上皮下浸潤:點狀、斑狀、線狀混濁聚集。
偽樹枝狀病變:螢光素染色可見邊緣呈鋸齒狀的不規則線狀病變。與皰疹性樹枝狀病變(伴有終端膨大)的鑑別診斷很重要。
睫狀充血和角膜緣水腫:即使角膜病變輕微也可出現。
進展期
在早期與進展期之間的移行階段,病變從上皮下向基質淺層擴展,線狀和斑片狀混濁連接形成不規則的環形。病程中發炎反應始終較為嚴重,病變緩慢進展。從早期到進展期通常約為1至2個月,在此期間能否做出準確診斷並開始治療,對預後影響很大。
除了這種三期分類外,也使用另一種三級分類:「Stage 1:僅上皮病變」「Stage 2:上皮缺損、神經周圍浸潤、實質浸潤」「Stage 3:伴實質環狀浸潤」。Carnt等人(2018)指出,Stage 3的環狀浸潤作為嚴重發炎性併發症(SIC)定義的一部分,與預後不良獨立相關2)。兩種分類一致認為,在實質環狀浸潤出現前的早期診斷是改善預後的關鍵。
棘阿米巴是一種自由生活的阿米巴,廣泛存在於土壤、淡水、自來水、游泳池、淋浴水等各種環境中。它有兩種型態:滋養體(活動型態)和囊體(具有雙層壁的休眠型態)。囊體對冷凍、加熱、放射線和多種藥物具有極強的抵抗力。
與隱形眼鏡佩戴相關的可改變風險因子如下1)。
Carnt等人估計,僅將可重複使用的軟式鏡片更換為日拋型鏡片即可預防30%~62%的棘阿米巴角膜炎病例1)。
多功能保養液(MPS)是最廣泛使用的隱形眼鏡護理產品,但在產品核准過程中並未要求進行針對棘阿米巴的消毒試驗,其消毒效果極低,儘管不同產品之間略有差異。棘阿米巴的增殖需要細菌作為食物,因此透過徹底搓洗來預防細菌污染是預防感染的關鍵。煮沸消毒可以殺死棘阿米巴,但現代的頻繁更換型軟式隱形眼鏡和日拋型鏡片並不採用這種方法。
自來水是棘阿米巴的主要來源之一,用自來水沖洗鏡片或鏡片盒被世界各國公認為隱形眼鏡相關棘阿米巴角膜炎的最大風險因素。在淋浴、溫泉、游泳池、海水、河流等接觸水的環境中配戴鏡片也會透過相同機制增加感染風險。澳洲和英國的病例對照研究顯示,“戴著鏡片淋浴”這一行為的勝算比(OR)持續升高,因此這是對鏡片配戴者進行基本生活指導的重要內容1)。
在非隱形眼鏡佩戴者中,棘阿米巴角膜炎的發病機制主要與外傷相關。由植物碎片、沙子、泥土、農業作業中的異物等污染的自然環境異物引起角膜上皮損傷後發病的病例,在印度等熱帶及發展中國家已有報告。在日本,外傷或眼異物後發生棘阿米巴角膜炎的病例也有零星報告,但目前主流仍然是隱形眼鏡相關感染。
日拋型鏡片的風險比重複使用型鏡片低。但是,如果在淋浴時佩戴或重複使用鏡片,風險就會升高1)。遵守正確的使用方法至關重要。
棘阿米巴角膜炎的診斷較為困難,且常被延遲。根據德國的一項登記研究,47.6%的棘阿米巴角膜炎病例曾被誤診為疱疹性角膜炎4)。準確診斷需正確解讀臨床所見並結合微生物學檢查。
對於配戴隱形眼鏡且表現為治療抵抗性角膜炎的病例,必須將本病列入鑑別診斷。問診時務必確認以下內容:
基於裂隙燈顯微鏡所見進行診斷至關重要。掌握不同病期的特徵性表現(參見「臨床所見」一節),並結合隱形眼鏡配戴史和水暴露史進行臨床懷疑是第一步。
螢光素染色所見有助於鑑別診斷。單純皰疹病毒的樹枝狀病變形成末端膨大(terminal bulb),而棘阿米巴角膜炎的假樹枝狀病變缺乏這種末端膨大,表現為無隆起的、不規則線狀聚集。
在裂隙燈顯微鏡下,隨著病程進展,所見隨時間變化,因此不僅要在初診時,還要每隔數天至1週反覆進行詳細的觀察,這點非常重要。尤其在早期,將螢光素染色、亮光觀察和角膜知覺檢查結合起來,可以提高診斷準確性。角膜知覺隨著放射狀角膜神經炎的進展而下降,但與單純皰疹病毒角膜炎不同,臨床上可通過病變伴隨劇烈疼痛來進行區分。
主要檢查方法的特點如下所示。
| 檢查方法 | 敏感度 | 特異度 |
|---|---|---|
| 培養(大腸桿菌塗布非營養瓊脂培養基) | 33–50% | 100%(黃金標準) |
| 共焦顯微鏡(IVCM) | 約90% | 91.1~100% |
| PCR(18S rRNA基因) | 71~84% | 100% |
專用培養基和抹片鏡檢染色液在一般診所通常不常備,因此一旦懷疑本病,建議及時轉診至專門醫療機構。
多種病原體的混合感染並不罕見,特別是在隱形眼鏡佩戴者中,已有綠膿桿菌等細菌感染與棘阿米巴同時感染的報告。綜合進行塗抹鏡檢、培養及PCR以確定病原微生物至關重要。對於臨床表現類似疱疹但對抗病毒藥物無反應的病例,或按細菌感染開始治療但未見改善的病例,應及時進行包含棘阿米巴在內的重新評估。
早期臨床表現與疱疹病毒性角膜炎相似,假樹枝狀病變容易被誤認為樹枝狀潰瘍。據報告,約半數棘阿米巴角膜炎病例曾被誤診為疱疹4)。對於隱形眼鏡佩戴者中的治療抵抗性角膜炎,應積極懷疑棘阿米巴角膜炎,並及早進行培養和共聚焦顯微鏡檢查。
棘阿米巴角膜炎的治療困難且需長期進行。日本不存在對棘阿米巴有保險給付的藥物,治療需要使用自配點眼液。日本感染性角膜炎診療指引第3版中,針對CQ-7「棘阿米巴角膜炎的治療是否推薦自配點眼液?」提出了**「強烈推薦自配點眼液(證據等級B)」**的建議10)。
在日本,病灶刮除、局部抗棘阿米巴藥物和全身抗真菌藥物聯合的三聯療法為基本治療方案10)。早期診斷與早期開始治療被認為是成功的關鍵。
這是治療中最重要的一項處置。日本感染性角膜炎指南也將其意義歸納如下10)。
被棘阿米巴寄生的角膜上皮與基底膜的附著脆弱,即使看起來健康的上皮,輕輕刮擦也會脫落。原則上應去除所有此類上皮10)。刮除頻率根據病期和所見,一般建議每週1〜2次。
一線藥物是雙胍類消毒劑,需自行配製使用。這些藥物不僅對滋養體有效,對囊體也有效是一大優點,但由於組織滲透性較差,需要頻繁點眼。
在英國進行的一項隨機對照試驗(51眼)報告,0.02% PHMB單藥組(23眼中18眼=78%)與0.02% CHG單藥組(28眼中24眼=85.7%)的2週內臨床改善率無顯著差異,兩者具有同等療效9)10)。Cochrane系統性回顧也將這兩種藥物的單用或併用列為目前最佳證據13)。
以下藥物可能作為輔助治療合併使用。
典型處方例如下。
在初始強化治療階段,需每小時(包括夜間)頻繁點眼,並根據臨床反應逐步減量。通常約1週後從每小時1次減為每2小時1次,之後以每月為間隔逐步減至每3小時1次、每4小時1次。治療療程通常持續數月至半年以上,應避免過快減量以免導致復發。
在《感染性角膜炎診療指引第3版》CQ-7(“棘阿米巴角膜炎的治療是否推薦使用院內調製點眼劑?“)的系統性回顧中,鑑於目前尚無保險給付的藥物治療,判定益處大於危害,並提出「強烈推薦」(證據等級B)的結論10)。CHG點眼液價格相對低廉,但需注意能夠進行院內調製的醫療機構有限。
實施三聯療法時,需同時處理合併的感染與發炎。為預防細菌混合感染,併用新喹諾酮類點眼液(左氧氟沙星1.5%等),虹膜睫狀體炎則併用散瞳藥(阿托品1%)。原則上不使用類固醇,但僅在抗棘阿米巴治療已充分奏效而強烈發炎症狀仍持續的情況下,方可由專科醫師判斷短期、低劑量使用類固醇點眼液。惟其適應症有限,在初診或治療早期屬禁忌。
院內調製點眼液通常由各醫療機構藥局配製,不同機構的濃度與保存期限方案有所不同。一般0.02% CHG的有效期約為4週,0.02% PHMB約為2週。應向患者說明需冷藏保存、使用前搖勻,並嚴格遵守使用期限。
有時會合併使用抗真菌藥物的全身給藥(如口服伊曲康唑)。日本指南指出「全身給藥的有效性尚未明確」,其效果僅為輔助性質10)。
治療效果的判定綜合使用病灶刮取物的定期鏡檢、培養和PCR、裂隙燈檢查中浸潤範圍的縮小、以及自覺症狀(特別是疼痛)的減輕。定期施行IVCM的設施可以非侵入性評估角膜內殘留的囊體。若治療有效,在早期病例中,可預期僅留下輕微疤痕的透明癒合。相反地,即使是相當進展的病例,透過長期治療也能減輕混濁,且角膜形態變化出乎意料地少,這是阿米巴角膜炎的特徵。因此,只要能判斷治療有效(即使進展緩慢),就無需急於進行角膜移植。
另一方面,治療完全無效時,必須在阿米巴向周邊擴散之前進行治療性角膜移植,否則在最壞的情況下可能需要摘除眼球。治療開始後的重要病程指標包括:①疼痛的改善、②浸潤範圍的縮小、③角膜上皮化的進展、④發炎性併發症(前房蓄膿、鞏膜炎、環狀浸潤)的消退。如果這些表現在經過3~4週仍未見改善,則需要考慮更換藥物或進行外科干預。
對於藥物治療無效或發生角膜穿孔的病例,應考慮手術治療10)。
Carnt等(2018)在194例的回顧性研究中報告,抗阿米巴治療開始前使用類固醇會使預後不良風險增加約4倍2)。預後不良病例中25%需要門診就診55次以上、追蹤58個月以上。此外,年齡超過34歲、症狀持續超過37天、存在鞏膜炎或實質環狀浸潤也是獨立的預後不良因子2)。
日本感染性角膜炎診療指引第3版不建議對棘阿米巴角膜炎使用類固醇眼藥水10)。治療前使用類固醇是預後不良因子2)。但對於部分發炎遷延的嚴重病例,在充分進行抗阿米巴治療後,可根據專科醫師判斷有限度地使用。
棘阿米巴的生命週期包括營養體和囊胞兩個階段。營養體(體長20–40 μm)具有偽足和活動性,以細菌和酵母為食,透過二分裂增殖。營養體經由黏附到角膜上皮表面的甘露糖基化醣蛋白上啟動侵入。囊胞(直徑10–20 μm)具有內外雙層囊壁,在不利條件下形成。囊胞具有耐乾燥、耐熱、耐化學品的特性,並對冷凍、加熱、輻射和許多藥物表現出強耐受性。這種囊胞的耐藥性是導致棘阿米巴角膜炎治療困難的最主要原因。
佩戴隱形眼鏡導致的角膜上皮微創傷促進了阿米巴的黏附與侵入。目前,隱形眼鏡護理產品(多功能護理液;MPS)不要求進行針對棘阿米巴的檢測,其消毒效果極低。但由於棘阿米巴的生長需要細菌作為食物來源,徹底揉搓清洗以防止一般性細菌污染是切實可行的預防措施。
感染的進展過程如下。
Kurbanyan 等人使用共軛焦顯微鏡的研究報告指出,在活動性棘阿米巴角膜炎中,角膜神經的密度、長度和分枝顯著降低4)。這種神經變化可能是無痛性棘阿米巴角膜炎的成因之一。
關於角膜塑形鏡片(OK鏡),其發生棘阿米巴角膜炎的風險高於一般RGP鏡片。OK鏡特有的反轉幾何設計被認為會引起角膜上皮變薄和表層細胞損傷,夜間佩戴導致的角膜缺氧以及反轉曲線下的淚液積聚被認為促進了病原體的定植3)。此外,OK鏡佩戴者多為學齡兒童和青少年,經常使用自來水清洗或沖洗鏡片也是風險增加的原因之一。
如前所述,包囊對多種藥物具有抗藥性,這種抗藥性很大程度上歸因於內外雙層包囊壁結構。外壁(外囊)主要成分為無定形蛋白質,內壁(內囊)富含纖維素樣多醣,可阻礙親水性和疏水性藥物的滲透。由於這種結構性抗藥性,抗真菌藥和氨基糖苷類抗菌藥對包囊幾乎無效,而對包囊有效的雙胍類消毒劑(CHG、PHMB)成為治療核心。然而雙胍類消毒劑的組織滲透性也較差,因此必須通過病灶刮除去除上皮屏障。這就是日本三藥聯合療法中病灶刮除備受重視的理論背景。
宿主的免疫反應對棘阿米巴角膜炎的臨床表現有重大影響。實質輪狀浸潤被認為是針對棘阿米巴抗原的延遲型過敏反應導致的中性粒細胞和T細胞浸潤,而鞏膜炎則被推測通過類似於交感性發炎的機制,由阿米巴抗原或T細胞克隆播散至鞏膜引起2)。Carnt等(2018)指出,這些重症炎症性併發症與年齡超過34歲、治療前使用類固醇以及既往疱疹治療史獨立相關,表明免疫反應的個體差異是影響預後的因素之一2)。
與傳統的0.02% PHMB相比,使用4倍濃度0.08% PHMB的單一療法正在研究中。
Di Zazzo等人(2024)對2例對0.02% PHMB+丙帕咪啶0.1%標準療法產生抗藥性4〜6週的患者,全球首次臨床使用了0.08% PHMB單一療法5)。治療方案為:最初5天每小時給藥1次(僅日間16滴/天),之後逐步減量。兩例患者的感染均在15〜30天內消退,7個月以上未觀察到復發。
ODAK試驗(Dart等人2024)報告,PHMB 0.08%單一治療和PHMB 0.02%+丙帕咪啶0.1%聯合治療的治癒率均約為86%5)。
這是一種將核黃素和紫外線A(UVA)交聯技術應用於感染性角膜炎的方法。
Watson等人(2022)報告了1例對最大藥物治療(包括米替福新、伏立康唑、PHMB和氯己定)耐藥的難治性棘阿米巴角膜炎,經PACK-CXL治療後,疼痛在4週內完全消失,浸潤灶在10週內縮小6)。
然而,體外和體內實驗尚未證實核黃素/UVA照射對阿米巴和包囊的殺滅效果6)。推測其間接機制包括:通過膠原穩定化實現組織保護、抑制阿米巴增殖、通過上皮清創減少阿米巴負荷、以及通過降低角膜神經密度產生鎮痛效果。
該藥屬於烷基磷酸膽鹼類,對營養體和包囊均有活性。2016年獲得美國FDA授予治療棘阿米巴角膜炎的孤兒藥資格。作為標準治療4至6週無效的難治性病例的輔助治療6)7)。
Smith等人(2022)的4例病例系列中,含米替福新的聯合治療合併角膜移植術,所有病例最終均獲得疾病控制7)。但部分病例因耐受性問題(消化道症狀)而需要中途停藥。
米替福辛的主要副作用包括消化道症狀(噁心、嘔吐)、致畸性和腎毒性,罕見情況下曾有Stevens-Johnson症候群和嚴重血小板減少的報告7)。用藥期間需要定期監測肝功能。該藥在日本尚未核准,僅限於個人進口或臨床研究使用。這是一個值得關注未來發展趨勢的治療選擇。