革蘭陽性球菌
葡萄球菌:典型表現為小圓形、邊界相對清晰的灰白色局限性膿瘍1)。進展緩慢,但MRSA易重症化,常伴有比感染病灶更大的上皮缺損1)。異位性皮膚炎患者中MRSA檢出率高。
肺炎鏈球菌:表現為特徵性的匐行性角膜潰瘍。病變一端癒合,另一端進展,看起來像在爬行移動1)。莢膜抵抗嗜中性球吞噬,可向深部進展導致角膜穿孔1)。

細菌性角膜炎是細菌侵入角膜實質並增殖所引起的化膿性炎症。也稱為細菌性角膜潰瘍,特別是肺炎鏈球菌引起的稱為匐行性角膜潰瘍(serpiginous corneal ulcer)。它是感染性角膜炎中最常見的類型,若初期診斷和治療不當,可能導致嚴重的視力障礙1)。
在日本,感染性角膜炎患者的年齡分布呈雙峰型,峰值在20多歲和60多歲1)。年輕族群的峰值主要由隱形眼鏡(CL)配戴引起的感染構成。發生率沒有明顯的性別差異,但外傷引起的感染在男性中較常見,而CL相關的感染在女性中較常見1)。
根據大規模世代研究報告,已開發國家的年發生率約為每10萬人中數人到數十人,而開發中國家可達數百人1)。感染性角膜炎的病原微生物中細菌最多,其次是病毒、真菌和棘阿米巴1)。在美國,估計每年發生約71,000例微生物性角膜炎(包括細菌、真菌和棘阿米巴),近年來有增加趨勢7)。從視功能預後的角度來看,有些病例即使治癒後,由於不規則散光或角膜疤痕,視力也無法恢復,尤其是中央部潰瘍容易殘留視功能障礙1)。
在日本,最常見的誘發因素是CL配戴,與其他已開發國家趨勢相同1)。重症CL相關性角膜炎多見於使用兩週頻繁更換型軟性CL(FRSCL)或傳統型SCL的配戴者,護理不當導致的鏡片污染是重要的風險因子1)。還需注意CL配戴引起的感染性角膜炎常為雙眼性。在美國,CL配戴是最大誘因,而在開發中國家,外傷是最大誘因7)。
細菌性角膜炎的四大致病菌是金黃色葡萄球菌、肺炎鏈球菌、綠膿桿菌和莫拉菌。其中葡萄球菌屬的頻率最高,綠膿桿菌是CL相關性角膜炎的主要致病菌1)。近年來國內外莫拉菌的報告增加,眼表疾病、眼手術史和糖尿病是其誘因1)。眼表常駐菌棒狀桿菌也是相對常見的致病菌1)。
混合感染也不容忽視,AAO PPP報告約43%的培養陽性病例檢出兩種或以上細菌7)。混合感染最常見的誘因是外傷,表皮葡萄球菌和鐮刀菌屬的組合較多7)。Ung等人將感染性角膜炎定位為「持續的臨床挑戰」,強調微生物學檢查的快速化、新型抗菌藥物以及抗藥菌株地區差異監測的重要性11)。
「匐行性角膜潰瘍」(serpiginous corneal ulcer)這一名稱自19世紀開始使用,因其病變像爬行一樣在角膜表面移動而得名。在日本,感染性角膜炎診療指引於2007年首次在日本眼科學會雜誌發表,隨後經過2013年第2版12)和2023年第3版的修訂,推動了基於證據的診療標準化1)。
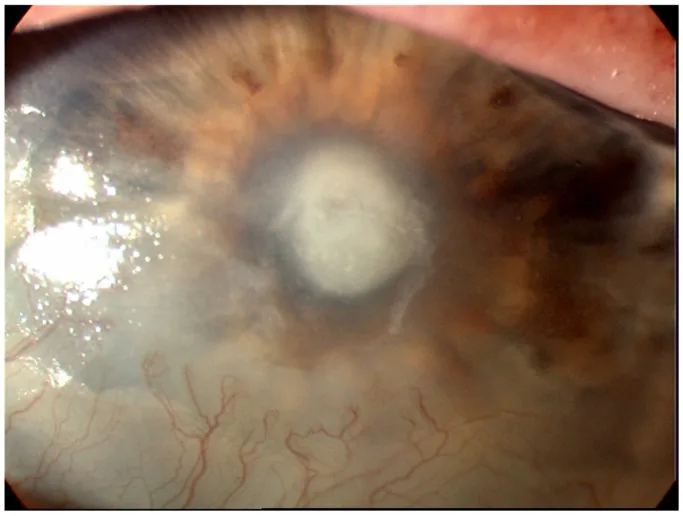
特徵為急性發作的眼痛。輕症表現為眼異物感,重症則主訴劇烈眼痛1)。除疼痛外,還出現充血、視力障礙、流淚、黏液膿性分泌物和畏光1)。症狀進展速度與致病菌的毒力相關,綠膿桿菌可在發病24小時內迅速惡化7)。
細菌性角膜炎的初期病變為浸潤、上皮缺損、前房炎症細胞出現和睫狀充血。但真正的初期病變很少被觀察到,患者通常以圓形膿瘍就診。角膜表現因革蘭陽性球菌和革蘭陰性桿菌而異,是推測致病菌的重要臨床線索1)。
重症病例可見前房蓄膿和纖維蛋白滲出,易發生虹膜後粘連。角膜後沉著物(KP)出現在與角膜浸潤、膿瘍或潰瘍相對應的後表面1)。
裂隙燈顯微鏡檢查時,用擴散光觀察整體混濁,用反光法檢查細胞浸潤狀態和前房炎症(尤其是KP)。用寬裂隙光檢查角膜表面,用窄裂隙光評估病灶深度和前房炎症,並用螢光素染色顯示上皮缺損,此流程很有用。
革蘭陽性球菌
葡萄球菌:典型表現為小圓形、邊界相對清晰的灰白色局限性膿瘍1)。進展緩慢,但MRSA易重症化,常伴有比感染病灶更大的上皮缺損1)。異位性皮膚炎患者中MRSA檢出率高。
肺炎鏈球菌:表現為特徵性的匐行性角膜潰瘍。病變一端癒合,另一端進展,看起來像在爬行移動1)。莢膜抵抗嗜中性球吞噬,可向深部進展導致角膜穿孔1)。
革蘭陰性桿菌
綠膿桿菌:伴有環狀膿瘍,周圍角膜呈毛玻璃樣混濁1)。蛋白酶導致角膜溶解,進展迅速,易穿孔。多與隱形眼鏡相關,有報告稱長期合併使用角膜塑形片和隱形眼鏡可導致環狀潰瘍3)。
莫拉菌:在角膜中央形成局限性、邊界清晰的潰瘍1)。隱形眼鏡佩戴者和糖尿病等基礎疾病是危險因子1)。進展相對緩慢,對多種抗菌藥物敏感。
沙雷菌:表現多樣,從輕度淺表潰瘍到廣泛膿瘍,蛋白酶產生量的多寡與嚴重程度相關1)。
特殊致病菌
革蘭陽性球菌(葡萄球菌、肺炎鏈球菌)表現為小圓形至橢圓形、邊緣整齊的局限性膿瘍。而革蘭陰性桿菌(綠膿桿菌、莫拉菌、沙雷菌)則伴有周圍基質毛玻璃樣混濁和明顯水腫,重症病例因角膜基質溶解形成環狀膿瘍。感染性角膜炎診療指引第2版的角膜炎診斷流程圖中,建議從局限性膿瘍推斷革蘭陽性球菌,從環狀膿瘍推斷革蘭陰性桿菌1)。
正常角膜透過複層鱗狀上皮和淚液中的防禦物質(溶菌酶、乳鐵蛋白、IgA)抵禦感染。因此,細菌性角膜炎發生在創傷、隱形眼鏡佩戴、手術、眼表疾病或全身性疾病導致防禦機制受損的情況下1)。AAO PPP將隱形眼鏡佩戴列為美國最大的危險因子,而世界許多地區創傷是主要原因7)。
隱形眼鏡相關
過夜佩戴:與日間佩戴相比,感染風險顯著增加。包括角膜塑形片在內的夜間佩戴是特別重要的危險因子7)。
不當護理:補充清潔液、污染鏡盒、用自來水儲存或沖洗是典型的誘因1)7)。
鏡片類型:兩週更換型軟式隱形眼鏡和傳統型軟式隱形眼鏡中,綠膿桿菌、莫拉菌、沙雷菌等革蘭氏陰性菌感染較多見1)。
裝飾用隱形眼鏡:未經醫師處方而在網路或商店購買的鏡片感染風險高7)。
外傷與手術相關
眼表與全身因素
眼表疾病:乾眼症、單純疱疹性角膜炎、水疱性角膜病變、Stevens-Johnson症候群、神經營養性角膜病變是易感因素1)。曾有從污染的人工淚液中檢出廣泛抗藥性綠膿桿菌的案例2)。
全身因素:糖尿病、免疫抑制、異位性皮膚炎、膠原病等1)7)。
藥物相關:長期使用類固醇眼藥水、污染眼藥水、非類固醇抗發炎藥眼藥水是危險因素。長期使用氟喹諾酮類抗菌藥眼藥水時,MRSA檢出率升高1)。
非隱形眼鏡相關病例中,角膜移植術後、眼表疾病、長期使用氟喹諾酮類抗菌藥下的MRSA是重要問題1)。長期使用類固醇或免疫抑制劑的患者需與真菌感染(尤其是酵母樣真菌)和疱疹病毒鑑別1)。老年長期臥床患者出現難治性角膜炎時,需考慮綠膿桿菌、MRSA和真菌的可能性1)。
避免過夜佩戴和正確的鏡片護理最為重要。AAO的細菌性角膜炎PPP也將過夜佩戴(包括角膜塑形鏡)列為主要危險因素7)。每3個月更換鏡盒、每日清潔乾燥、避免接觸自來水是基本要求7)。裝飾用鏡片和網購鏡片也易成為感染源,因此建議醫師處方和定期追蹤。
診斷需綜合病史、臨床所見和檢查結果1)。感染性角膜炎診療指引(第3版)臨床問題1(CQ-1)強烈推薦塗片鏡檢和培養檢查用於細菌性角膜炎的診斷(證據等級C)1)。
確認隱形眼鏡佩戴史(類型、使用時間、護理方法、有無誤用)、外傷史、眼科手術史、既存角膜疾病(如角膜皰疹等)、使用中的眼藥水、長期使用類固醇或免疫抑制劑史、全身病史(糖尿病、異位性皮膚炎、MRSA感染史)1)。病程方面,進展迅速時考慮綠膿桿菌或鏈球菌;長期臥床的老年患者若難治,考慮綠膿桿菌、MRSA或真菌1)。
記錄角膜浸潤的部位、大小和深度,並用螢光素染色評估上皮缺損。同時評估前房炎症(細胞、閃輝、纖維蛋白、前房蓄膿)、角膜後面沉著物、角膜知覺、眼瞼閉合不全和淚道系統1)。若後極部觀察困難,則加做超音波B模式檢查。
前眼部光學同調斷層掃描(AS-OCT)可客觀顯示角膜病變深度、角膜厚度增加、變薄、前房炎症細胞、纖維蛋白、KP、內皮斑等1)。通過治療前後比較可評估療效。但感染性角膜炎不在保險給付範圍內1)。
活體共軛焦顯微鏡(IVCM)可非侵入性觀察角膜內細胞、神經纖維、真菌以及棘阿米巴滋養體和囊體1)。
確診需通過角膜病灶刮取進行塗抹鏡檢和培養檢查1)。在抗菌藥物給藥前採集檢體極為重要;感染性角膜炎GL第3版CQ-1報告,檢查前未使用抗菌藥物的病例培養陽性率為77.3%,使用後為37.8%1)。
在點眼麻醉下,用無菌刮匙刮取潰瘍邊緣部。若有穿孔風險,則使用無菌棉棒,並用火焰或酒精固定1)。在檢體採集方法研究中,拭子刮取的培養陽性率為50%,23G針為35%;拭子刮取簡便且推薦使用1)。直接接種於固體培養基的陽性率為61%,通過運送培養基間接接種為44%;可能時首選直接接種於固體培養基1)。
感染性角膜炎GL第3版報告,培養陽性率37.6–74.3%,塗抹鏡檢陽性率58.1–73.7%,細菌塗抹鏡檢的病原菌檢出率60–75%1)。塗抹陽性病例的培養陽性率高達57.1–82.4%,兩者併用較為理想1)。
主要染色方法如下。
| 染色方法 | 檢測對象 | 所需時間 |
|---|---|---|
| 革蘭氏染色(Faber G) | 細菌、真菌、阿米巴 | 3分鐘 |
| 吉姆薩染色(Diff-Quik) | 細菌、真菌、披衣菌 | 15秒 |
| 真菌螢光Y染色 | 真菌和阿米巴囊體 | 螢光顯微鏡 |
革蘭氏染色在懷疑細菌、真菌或棘阿米巴感染時進行1)。簡易快速染色液套組Diff-Quik可在短時間內獲得與吉姆薩染色等效的影像1)。真菌螢光Y染色特異性染色具有β結構的多醣幾丁質和纖維素,靈敏地檢測真菌和阿米巴囊體1)。
培養使用血液瓊脂平板、巧克力瓊脂平板、沙氏瓊脂、液體培養基(硫乙醇酸鹽肉湯)和運送培養基(Seed Swab®、Transwab®)1)。血液瓊脂平板可判斷溶血性,巧克力瓊脂平板含有V因子和X因子,適合嗜血桿菌屬和淋球菌的生長1)。培養判定需要48小時,藥敏結果需要3-4天1)。
需要注意的是,眼表存在常駐菌,因此培養分離出的細菌不一定就是致病菌,需綜合抹片結果、眼部表現、藥敏結果和治療效果進行判斷1)。McLeod等人報告,雖然許多社區獲得性感染僅憑經驗治療即可好轉,但對於中央部大病灶、實質溶解、前房蓄膿、角膜手術史和非典型病例,強烈推薦進行抹片和培養10)。AAO PPP明確推薦在以下情況下進行抹片和培養7):
PCR是一種快速檢測微生物DNA的方法,但日本感染性角膜炎指引第3版不推薦僅憑角膜刮取物的PCR診斷細菌性角膜炎1)。PCR可能檢測到眼表常駐菌,因此被定位為抹片鏡檢和培養檢查的輔助手段1)。
需要與卡他性角膜浸潤(葡萄球菌外毒素引起的III型過敏)、真菌性角膜炎(羽毛狀浸潤、衛星灶、內皮斑)、棘阿米巴角膜炎(放射狀角膜神經炎、環形浸潤、假樹枝狀病灶)和疱疹性角膜炎(末端膨大的樹枝狀病灶)進行鑑別1)。當培養陰性但強烈懷疑感染時,考慮角膜活檢7)。
首先,如果正在使用抗菌藥物,考慮暫時停藥並重新培養。感染性角膜炎指引第3版報告,用藥前培養陽性率為77.3%,用藥後降至37.8%1)。如果仍然陰性,考慮角膜活檢,並重新評估非結核分枝桿菌、諾卡菌、棘阿米巴和真菌等特殊病原體1)。同時繼續使用廣譜抗菌藥物進行經驗性治療,每48小時評估治療反應7)。
感染性角膜炎診療指引(第3版)指出,細菌性角膜炎的治療必須選擇對致病菌有效的抗菌藥物,並要求迅速且準確地鑑定致病菌1)。該指引的治療流程圖(圖10)顯示以下方針1)。
感染性角膜炎GL第3版的初始治療藥物示例如下1)。
| 疑似致病菌 | 首選(兩種藥物併用) |
|---|---|
| 革蘭氏陰性桿菌 | 氟喹諾酮類 + 胺基糖苷類 |
| 革蘭氏陽性球菌 | 氟喹諾酮類 + 頭孢菌素類 |
若無法推測致病菌,則合併使用新喹諾酮類和β-內醯胺類藥物1)。一旦鑑定出致病菌,根據塗片結果、培養結果和藥物敏感性重新評估治療1)。
日本市售的抗菌眼藥水包括氟喹諾酮類(第三代:氧氟沙星[OFLX]、左氧氟沙星[LVFX]、托氟沙星[TFLX];第四代:加替沙星[GFLX]、莫西沙星[MFLX])、頭孢菌素類(鹽酸頭孢甲肟)、胺基糖苷類(妥布黴素、慶大黴素、地貝卡星、新黴素)、大環內酯類(紅黴素)和氯黴素。糖肽類萬古黴素作為院內製劑使用。
第三、四代氟喹諾酮類藥物組織滲透性提高,對鏈球菌的效果也更強。高濃度左氧氟沙星水合物滴眼液對革蘭氏陰性菌的治療效果有所提高1)。而鹽酸頭孢甲肟滴眼液對鏈球菌有效,但對綠膿桿菌效果不佳;胺基糖苷類對綠膿桿菌有效,但對鏈球菌無效1)。需注意第四代氟喹諾酮類對綠膿桿菌的作用較弱。
主要致病菌群與藥物類別的敏感性一般對應關係如下所示。
| 類別 | 葡萄球菌 | 鏈球菌 | 綠膿桿菌 |
|---|---|---|---|
| β-內醯胺類 | 有效 | 有效 | 弱 |
| 氟喹諾酮類 | 有效 | 有效 | 有效 |
| 胺基糖苷類 | 有效 | 無效 | 有效 |
| 巨環內酯類 | 弱 | 有效 | 弱 |
每次點眼1~2滴,根據嚴重程度和藥物的抗生素後效應(PAE)考量 1)。重症病例或刺激導致流淚明顯時,可每30分鐘至1小時頻繁點眼 1)。胺基醣苷類和氟喹諾酮類具有PAE,但頭孢甲肟和氯黴素的PAE較短,需要更頻繁點眼 1)。
美國AAO的細菌性角膜炎PPP(2023)建議,對於伴有中央大病灶或前房蓄膿的視力威脅病例,使用強化抗菌藥物 7)。具體配製方法如下 7)。
重症病例使用頭孢唑林50 mg/mL聯合妥布黴素14 mg/mL;懷疑MRSA時加用萬古黴素25~50 mg/mL 7)。強化抗菌藥物作為院內配製使用,由於配製安全性和保存穩定性問題,感染性角膜炎GL第3版提醒「避免輕易使用」 1)。
如果市售藥物無效,可考慮用生理食鹽水稀釋注射用藥物,配製院內點眼液使用 1)。對於MRSA和MR-CNS,已有報導氯黴素點眼液和院內配製阿貝卡星點眼液(仿單外使用)的有效性 1)。對於廣泛抗藥(XDR)綠膿桿菌,已有報導使用頭孢地爾等新型抗菌藥物全身給藥 2)。
近年來,眼科廣泛使用的氟喹諾酮類藥物感受性下降成為問題,MRSA、MRSE、耐青黴素肺炎鏈球菌等多重抗藥菌的檢出增加 1)。由於點眼液中藥物濃度較高,即使藥敏試驗顯示抗藥,如果臨床有效,有時也可以繼續使用 1)。
感染性角膜炎診療指引(第3版)的CQ-5得出結論:「弱推薦在細菌性角膜炎治療中不併用皮質類固醇點眼液。」 1) 這是基於許多病例未能確定病原菌,且考慮到抗藥菌增加,應謹慎併用類固醇的觀點 1)。
角膜潰瘍類固醇試驗(SCUT)的主要試驗顯示,普賴蘇濃磷酸酯1%點眼液合併廣效抗菌藥物在視力預後上無顯著差異,但次群體分析提示,在綠膿桿菌性和重症病例中早期併用類固醇可改善視力 9)。基於此結果,AAO細菌性角膜炎PPP 2023指出「在確定病原菌並確認對抗菌藥物有反應後(通常48小時後),可考慮併用類固醇」 7)。但棘阿米巴、諾卡菌和真菌感染禁用 7)。
在決定治療方針時,應參考感染性角膜炎診療指引第3版的建議,對於重症病例,需根據個別病情判斷。
AAO PPP建議,若在治療開始後48小時內未觀察到改善趨勢,則應重新考慮治療方案7)。感染性角膜炎GL第3版也要求,若無改善,應重新評估患者背景與治療經過,確認是否存在混合感染(細菌+真菌,罕見細菌+疱疹)的可能性以及患者的點眼藥順從性1)。
對於藥物治療無效或角膜穿孔的病例,進行外科介入。感染性角膜炎GL第3版指出,在不得已的情況下,如前房持續消失,應進行治療性角膜移植,但如果可能,最好在感染平息後進行擇期角膜移植1)。可選擇全層角膜移植(PKP)或深層板層角膜移植(DALK),有報告在嚴重綠膿桿菌角膜炎後透過DALK獲得良好視力恢復6)。對於小穿孔(<2 mm),使用氰基丙烯酸酯角膜黏合劑與治療性角膜接觸鏡。SMILE術後嚴重感染時,有報告將角膜帽轉為角膜瓣,清除壞死組織並以抗菌藥物沖洗的方法5)。對於C. bovis引起的穿孔病例,進行了Gundersen結膜瓣手術4)。
感染性角膜炎診療指引(第3版)CQ-5明確指出:「弱建議在細菌性角膜炎的治療中不併用腎上腺皮質類固醇點眼液」1)。這是基於許多病例未能確定病原菌以及抗藥性菌增加的考量,以安全為重的建議1)。SCUT試驗的次群體分析和AAO PPP認為,僅在確定病原菌並確認對抗菌藥物有反應後(通常48小時後)才可謹慎考慮併用,但棘阿米巴、諾卡菌和真菌感染為禁忌7)。
正常角膜具有由複層鱗狀上皮和Bowman膜構成的屏障,淚液中的溶菌酶、乳鐵蛋白、IgA等防禦物質阻止微生物入侵1)。當這種防禦機制因外傷、隱形眼鏡佩戴、類固醇點眼液或眼表疾病等被破壞時,細菌可侵入角膜基質。
當細菌在角膜內增殖時,以嗜中性球為主的發炎細胞浸潤,形成化膿性病變(浸潤、膿瘍、潰瘍)1)。浸潤的嗜中性球釋放的蛋白分解酶和活性氧導致角膜基質進行性破壞,癒合後殘留組織變薄1)。如果感染長期化或重症化,角膜內皮細胞數量顯著減少,可能發展為水泡性角膜病變1)。
近年來,眼科領域對氟喹諾酮類藥物的感受性下降成為問題,MRSA、MRSE、青黴素抗藥性肺炎鏈球菌等多重抗藥菌正在增加1)。據報導,2005年至2015年間,MRSA和綠膿桿菌的氟喹諾酮抗藥性有所進展7)。抗藥性的背景包括過度使用抗菌藥物、隱形眼鏡佩戴者的污染鏡盒環境以及基因水平轉移等。Austin等人的綜述也指出,基於當地流行病學數據的經驗性治療和快速藥敏試驗對於應對抗藥菌的重要性13)。
綠膿桿菌附著於角膜上皮細胞的細胞表面糖脂(如無唾液酸神經節苷脂),並通過第三型分泌系統將效應分子注入宿主細胞。這引起角膜上皮細胞凋亡和嗜中性球募集。隨後,細菌釋放的彈性蛋白酶、鹼性蛋白酶和蛋白酶IV等蛋白酶降解角膜基質的膠原蛋白和蛋白聚醣,導致快速組織溶解1)11)。同時,宿主嗜中性球來源的基質金屬蛋白酶(MMP-2、MMP-9)也參與角膜破壞,即使在感染控制後也是疤痕形成的主要原因。這種感染建立和組織破壞的級聯反應解釋了為什麼治療不僅要用抗菌藥物清除病原體,還要控制宿主過度炎症11)。
AAO PPP將細菌性角膜炎的病程分為四個階段:進行性浸潤、活動性潰瘍形成、退行和癒合7)。即使接受適當治療,角膜疤痕或不規則散光也可能導致視功能損害,早期診斷和早期使用抗菌藥物是影響預後的最大因素1)。未經治療或重症病例可在24小時內發生角膜穿孔,導致眼內炎甚至眼球喪失7)。
Morelli MK等人報告了一例由市售人工淚液(EzriCare)中分離的廣泛抗藥性(XDR)綠膿桿菌引起的角膜潰瘍,通過全身使用頭孢地爾(一種鐵載體頭孢菌素)聯合局部亞胺培南和多黏菌素B成功治療。全基因組分析鑑定出blaVIM-80和blaGES-92)。
Kikuchi等人報告了一例63歲男性,同時使用角膜塑形鏡和軟性隱形眼鏡10年,發生綠膿桿菌角膜炎。表現為全角膜浸潤和環形潰瘍,使用左氧氟沙星、頭孢甲肟和慶大黴素滴眼液聯合靜脈注射亞胺培南治療後癒合,但殘留角膜混濁3)。
Elsheikh M等人報告了一例89歲女性,有帶狀皰疹角膜炎病史,發生由牛棒狀桿菌引起的嚴重角膜感染並穿孔。推測感染途徑為附近與牛的接觸。採用萬古黴素和環丙沙星聯合治療及Gundersen結膜瓣手術處理4)。
Li J等人報告了SMILE術後發生細菌性角膜炎的5例(7眼)。術後1-3天發病,培養出表皮葡萄球菌和肺炎鏈球菌。重症病例將角膜帽轉為角膜瓣進行壞死組織清除和抗菌藥物沖洗。所有眼最終矯正視力達到20/32或更好5)。
Arun K 和 Georgoudis 報告了一例32歲男性隱形眼鏡佩戴者罹患綠膿桿菌角膜炎,在急性期抗生素治療後進行DALK,獲得了良好的視力恢復 6)。
作為應對抗生素耐藥性問題的方法,光活化角膜交聯(Photoactivated Chromophore for Keratitis-Corneal Cross-linking:PACK-CXL)正受到關注。2008年,圓錐角膜治療的德勒斯登方案(0.1%核黃素滴眼30分鐘 + UVA 3 mW/cm²照射30分鐘,總能量5.4 J/cm²)被應用於感染性角膜炎的治療 8)。2013年的國際會議上正式採用了PACK-CXL的名稱 8)。
Kowalska 等人的範圍綜述分析了233項臨床前研究,總結出PACK-CXL能增強角膜基質對酶降解的抵抗力,並殺滅包括細菌、真菌和阿米巴在內的病原體 8)。在中等程度以下的細菌性角膜潰瘍中報告了良好結果,但德勒斯登方案被認為效果不足,正在向加速型、高能量方案轉變 8)。這是FDA未核准的適應症,在日本也處於研究階段 7)。
耐藥菌的增加是一個全球性問題,需要針對MRSA角膜炎和氟喹諾酮耐藥菌的新治療策略 7)。未來有望建立PACK-CXL的標準方案、現有抗生素的新製備方法以及菌種特異性快速診斷的發展。
對於MRSA,萬古黴素滴眼液(25–50 mg/mL)或院內自製的阿貝卡星滴眼液是選擇之一 1)7)。對於氟喹諾酮耐藥株,考慮更換為氨基糖苷類或頭孢菌素類,或氯黴素滴眼液 1)。對於廣泛耐藥(XDR)綠膿桿菌,已有報告使用頭孢地爾等新型抗生素全身給藥 2)。無論哪種情況,基於藥敏試驗選擇治療藥物都是必不可少的,塗片和培養檢查的重要性再次被強調 1)。PACK-CXL作為耐藥菌的替代療法正在研究中,但並非標準治療 8)。