絲狀菌
羽毛狀潰瘍:表現為邊界不清、毛糙的灰白色浸潤。這是絲狀菌感染的特徵性表現。
隆起性病灶:刮擦時質地硬。
衛星病灶:主病灶周圍散在小浸潤。
內皮斑:在角膜後面形成盤狀白色沉積物。這是菌絲穿過Descemet膜進入前房,或對深層菌絲的強烈免疫反應所致。
前房蓄膿:表明炎症波及前房的嚴重表現。

真菌性角膜炎是真菌感染角膜引起的角膜炎的總稱。也包括無炎症但角膜內真菌增殖的病變,稱為「角膜真菌症」,但日本感染性角膜炎診療指引第3版將伴有炎症的通常病變統一稱為「真菌性角膜炎」1)。
真菌在形態上分為以下兩類。兩者的臨床表現、危險因子和治療策略差異很大。
從流行病學角度來看,絲狀菌感染常由植物表面或土壤中的真菌經由外傷引起,因此被稱為「農村型」;而酵母菌感染與眼表疾病和類固醇眼藥水相關,因此被稱為「都市型」。
井上等人進行的一項多中心前瞻性觀察研究(2016年,《日本眼科學會雜誌》)報告了真菌性角膜炎的患者背景、臨床所見、治療和預後的現況8)。全球範圍內,溫暖地區發生率更高,估計熱帶和亞熱帶地區每年有超過100萬人患病7)。在亞洲溫帶地區,鏈格孢屬是絲狀菌中僅次於念珠菌屬和鐮刀菌屬的第三大分離頻率1)。在溫帶地區,除了鐮刀菌屬外,還有散發性報告的罕見致病菌如彎孢屬6)。
真菌性角膜炎很少發生在沒有危險因子的健康眼中,通常存在外傷、類固醇眼藥水、隱形眼鏡佩戴或眼表疾病等誘因1)。
真菌性角膜炎比細菌性角膜炎進展緩慢,疼痛相對較輕,且對廣譜抗生素無反應。絲狀菌表現為羽毛狀、邊界不清的浸潤,可能出現衛星病灶和內皮斑。確診需要塗片鏡檢或培養證明真菌,治療使用抗真菌藥物。
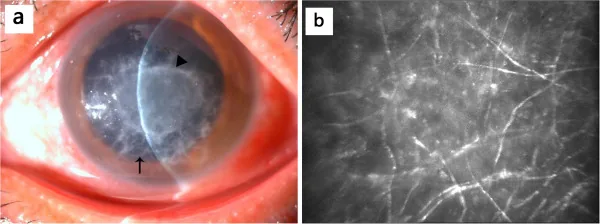
患者主訴的症狀如下。與細菌性角膜炎相比,進展緩慢,早期自覺症狀輕微,容易導致診斷延遲1)。
在極早期,自覺症狀輕微,可能僅有輕微的上皮障礙。疼痛相對較輕、病程緩慢是真菌性角膜炎的特徵,是與細菌性角膜炎鑑別的線索1)。
絲狀菌和酵母菌在裂隙燈顯微鏡下觀察到的臨床影像有很大不同。
絲狀菌
羽毛狀潰瘍:表現為邊界不清、毛糙的灰白色浸潤。這是絲狀菌感染的特徵性表現。
隆起性病灶:刮擦時質地硬。
衛星病灶:主病灶周圍散在小浸潤。
內皮斑:在角膜後面形成盤狀白色沉積物。這是菌絲穿過Descemet膜進入前房,或對深層菌絲的強烈免疫反應所致。
前房蓄膿:表明炎症波及前房的嚴重表現。
酵母菌
侷限性膿瘍:表現為邊界相對清晰的鈕扣狀或類圓形浸潤。
淺層侷限:常侷限於角膜基質淺層。
溶解傾向:病灶周圍可見角膜基質溶解。刮擦時質地軟。
與細菌性角膜炎相似:臨床上難以與葡萄球菌感染區分,必須透過塗片鏡檢和培養進行鑑別。
絲狀菌容易向角膜深層進展,感染擴大後最終導致嚴重的基質溶解,引起角膜穿孔。另一方面,如鏈格孢屬等低溫下易增殖的菌種,傾向於在角膜表面呈面狀擴散。如果使用了類固醇眼藥水,典型表現可能被修飾,導致診斷困難,需注意1)。
在絲狀真菌中,最常見且易導致重症的是鐮刀菌屬,代表菌種為Fusarium solani。此外,麴菌屬、鏈格孢屬、擬青黴屬(現為Purpureocillium lilacinum)、彎孢屬等也可引起角膜感染1)。
在酵母菌中,念珠菌屬佔絕大多數,代表菌種為Candida albicans。近年來,C. parapsilosis的分離頻率增加,而C. glabrata和C. krusei對氟康唑敏感性低,需注意1)。
絲狀真菌和酵母菌共同的真菌性角膜炎風險因素包括發病前使用類固醇眼藥水1)。
植物戳眼或土壤引起的眼外傷是絲狀真菌性角膜炎的最大風險因素。初期自覺症狀較輕,容易被忽視,診斷延遲可能導致角膜穿孔。受傷後如果持續出現充血、異物感、視力下降等症狀,請儘早到眼科就診。
對廣效抗菌藥物無反應的角膜潰瘍、存在衛星病灶、以及大面積潰瘍但分泌物較少,是應懷疑真菌感染的重要表現1)。根據角膜表現可臨床推測是絲狀菌感染還是酵母菌感染,患者背景(外傷史、類固醇使用史、隱形眼鏡佩戴史、眼部手術史)可作為鑑別診斷的參考。
確診需要從病灶部位證明真菌的存在1)。由於真菌生長需要時間,臨床懷疑本病時應不等培養結果即開始治療1)。
真菌性角膜炎需與其他感染性角膜炎鑑別。特別是酵母菌引起的病灶與葡萄球菌感染相似,因此微生物學檢查對鑑別很重要1)。
| 鑑別疾病 | 鑑別要點 |
|---|---|
| 細菌性角膜炎 | 快速進展、膿性分泌物、對廣譜抗生素有反應 |
| 棘阿米巴角膜炎 | 隱形眼鏡佩戴史、放射狀角膜神經炎、環狀浸潤 |
| 疱疹性角膜炎 | 樹枝狀病變、復發史、角膜感覺減退 |
確診需要從角膜病灶刮取物中證明真菌的存在。通過真菌螢光染色或革蘭染色塗片鏡檢確認菌絲,並在沙氏瓊脂培養基上培養。培養至少需要2週,因此如果根據臨床發現懷疑本病,應在等待培養結果前開始治療。
真菌性角膜炎的治療與細菌感染相比反應較差,且治療週期長。根據日本感染性角膜炎診療指南第3版,推薦採用局部和全身抗真菌藥物聯合病灶刮除的多方位治療1)。由於確定致病菌至少需要1週,生長緩慢的真菌可能需要4週,因此如果根據臨床發現懷疑本病,應立即開始治療1)。
根據菌種不同,使用三類抗真菌藥物。在眼科局部用藥中,只有多烯類的匹馬黴素(5%滴眼液、1%眼膏)有健保給付,其他均為臨床使用的院內製劑1)。
感染性角膜炎診療指引第3版建議,將真菌分為酵母樣真菌(念珠菌屬)、鐮刀菌屬和鐮刀菌屬以外的絲狀真菌,分別制定治療策略1)。
酵母菌(念珠菌屬)
第一線:唑類單獨或合併多種藥物使用。
合併治療:也建議唑類與棘白菌素類合併使用。
注意事項:注意氟康唑抗藥性菌株(光滑念珠菌、克柔念珠菌)的增加。也可使用1%匹馬黴素眼藥膏,但需注意藥物毒性引起的角膜上皮損傷。
絲狀真菌
鐮刀菌屬:多烯類匹馬黴素為第一線。考慮到分離頻率高,應從初始治療就考慮包含匹馬黴素的處方。
非鐮刀菌:推薦使用伏立康唑1%眼藥水。尤其考慮用於麴菌屬、擬青黴屬和賽多孢菌屬。
難治病例:如果使用匹馬黴素無改善,考慮加用伏立康唑眼藥水。
重症病例可參考以下合併用藥處方。根據角膜所見,可加用結膜下注射(項目4)。
除點眼外,合併全身給藥抗真菌藥。重症病例合併結膜下注射或基質內注射。使用阿托品消炎,不使用類固醇點眼液。合併抗菌點眼液應對細菌混合感染。
在《感染性角膜炎診療指引第3版》中,CQ-6指出「對於真菌性角膜炎的治療,有條件推薦伏立康唑自配點眼液」,推薦強度為「弱推薦」,證據等級為「B」1)。
支持伏立康唑點眼液的RCT均在海外(印度)進行,主要針對絲狀真菌性角膜炎1)。
基於這些證據,1%伏立康唑點眼液被證明是非鐮刀菌屬絲狀真菌引起的真菌性角膜炎的治療選擇。尤其對於匹馬利星無效的病例,特別是麴菌屬感染,值得考慮使用1)。
關於抗真菌藥物全身性給藥的有效性,尚無明確證據1)。多烯類匹馬利星水溶性差且分子量大,難以滲透至角膜深層,在伴有角膜新生血管的鐮刀菌屬重症病例中,靜脈輸注脂質體兩性黴素B可能彌補藥物滲透不良的問題1)。唑類伏立康唑全身性給藥後可進入前房1)。全身性給藥副作用較多,因此最好在確定致病真菌、目標明確的情況下使用1)。
病灶刮除可提高眼藥水的組織滲透性,並物理性減少菌量1)。由於不同真菌對藥物治療的反應不同,應積極合併使用以增強療效。處方範例中顯示每週刮除約兩次。角膜變薄時需注意穿孔。對於鏈格孢屬等表淺型,作為病灶刮除的延伸,表層角膜切除術也有效1)。
真菌性角膜炎的治療可能持續數週至數月。與細菌性角膜炎相比,對藥物的反應較慢,且眼藥水難以滲透至角膜深層,因此需要長期持續治療。治療期間必須定期追蹤,如果確定了致病菌,根據藥敏試驗結果調整處方也很有用。
當角膜上皮的完整性因外傷或眼表疾病受損時,附著的真菌在組織內增殖並建立感染1)。除外傷外,當存在糖尿病或長期使用類固醇眼藥水等導致眼表易感性增加的情況時,結膜囊或皮膚上常駐的酵母樣真菌(如念珠菌)可能成為病因。在隱形眼鏡佩戴者中,鏡盒內增殖的環境真菌可能成為病因。
一旦真菌附著並增殖於角膜上皮,建立感染,中性白血球遷移並聚集於病灶,形成白色浸潤灶。隨著組織破壞進展,形成膿瘍,並越過鮑曼氏膜形成潰瘍。前房內也發生中性白血球遷移,當發炎細胞增多時,形成前房蓄膿。真菌產生的蛋白質分解酶、抗原和毒素釋放到角膜內,導致壞死和組織結構損傷。
絲狀真菌(尤其是鐮刀菌屬)的菌絲容易向角膜深層延伸,當突破德斯密氏膜並在角膜後表面擴展時,形成內皮斑。即使不突破德斯密氏膜,對深層浸潤的絲狀真菌的強烈免疫反應也可能產生內皮斑。隨著感染擴散,最終發生嚴重溶解,可能導致角膜穿孔。
另一方面,酵母菌往往呈現比絲狀真菌發炎更輕的角膜真菌病形態。病灶侷限於角膜基質淺層,形成邊界清晰的膿瘍,並有溶解傾向。
Dong 等人報告了兩例對局部抗真菌藥耐藥的深層角膜真菌感染,通過單次前房內注射兩性黴素B(10 μg/0.1 mL),兩例患者最終最佳矯正視力均達到20/20 2)。該方法具有將藥物直接遞送至局部或全身給藥難以到達的角膜深層和前房的優勢。
由於抗真菌眼藥水分子量大,難以滲透到角膜基質深層,因此對於難治性深層病變,嘗試了將藥物直接注入病灶的角膜基質內注射。
使用的藥物是伏立康唑(50 μg/0.1 mL)和兩性黴素B(5–10 μg/0.1 mL)。有報導稱,在手術顯微鏡下,將針頭斜面朝下,從無病變部位斜向刺入,在膿瘍周圍分五點注射,形成藥物屏障。注入基質內的藥物作為儲庫存留,可維持有效濃度約7天。動物實驗報告稱,兩性黴素B濃度超過20 μg/0.1 mL會引起角膜水腫、上皮糜爛和新生血管形成,因此需要注意濃度管理。
Ler 等人報告了一例深部絲狀真菌感染(青黴菌屬),通過在病灶周圍環形注射伏立康唑50 μg/0.1 mL,每5天重複一次,共3次,成功治癒 3)。
在一項針對25例對那他黴素和伏立康唑眼藥水無反應的患者的研究中,72%對伏立康唑基質內注射有反應。大多數無反應者的培養結果為鐮刀菌屬陽性。另一項針對20例患者的研究中,14例對注射有反應,平均需要2.65次注射。
在一項針對40例對5%匹馬利辛眼藥水無反應的真菌性角膜炎患者的隨機對照試驗中,比較了加用1%伏立康唑眼藥水與加用伏立康唑基質內注射的效果,結果顯示治癒率無顯著差異,但3個月後的矯正視力在眼藥水加用組更好 1)。儘管該隨機對照試驗病例數有限,但並未顯示基質內注射優於眼藥水。
基質內注射是局部和全身給藥的輔助療法,而非單獨治療。未來的挑戰包括確定最佳注射次數和間隔、驗證不同菌種(尤其是鐮刀菌屬)的療效,以及評估與其他輔助療法聯合使用的效果。
PACK-CXL(光活化角膜交聯術)是一種利用核黃素和紫外線A照射穩定角膜基質並同時滅活病原體的治療方法7)。角膜交聯療法最初是為治療圓錐角膜(德勒斯登方案)而開發,但自2008年起已臨床應用於感染性角膜炎,並於2013年採用PACK-CXL的名稱7)。它具有不依賴抗生素的作用機制,有望成為應對日益增加的抗藥性細菌的新治療選擇。關於真菌感染的臨床前研究也有許多報導,但對於鐮刀菌屬等難治性真菌的最佳方案仍在建立中7)。
Todokoro等人通過DNA序列分析鑑定出與蠶蝕性角膜潰瘍相關的鏈格孢角膜炎的菌種,並通過藥物敏感性試驗確認伏立康唑的MIC為0.5 μg/mL,從而成功治療4)。聯合使用伏立康唑眼藥水和類固醇眼藥水,三個月後視力恢復至0.7。這表明分子診斷與藥物敏感性試驗相結合可能提高個體化治療的精確性。
Chen等人報告了兩例在羊膜移植後10天內發生鐮刀菌角膜炎和Sistotrema biggsiae角膜炎的病例5)。這是文獻中首次報導Sistotrema biggsiae的人類感染。羊膜移植後感染性角膜炎的發病間隔通常為28至347天,因此提醒注意早期發病的病例5)。
井上等人對真菌性角膜炎的患者背景、臨床所見、治療和預後進行了多中心前瞻性觀察研究,並在日本眼科學會雜誌上報告了日本該病的實際情況8)。這提供了日本真菌性角膜炎的病原菌分佈和治療結果的基礎數據,具有重要意義。