丝状菌
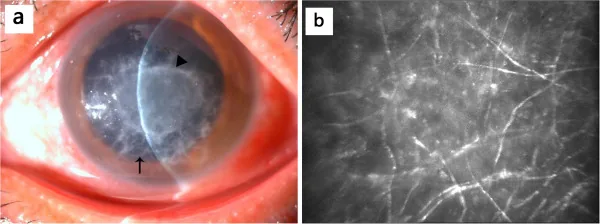
羽毛状溃疡:表现为边界不清、毛糙的灰白色浸润。这是丝状菌感染的特征性表现。
隆起性病灶:刮擦时质地硬。
卫星病灶:主病灶周围散在小浸润。
内皮斑:在角膜后面形成盘状白色沉积物。这是菌丝穿过Descemet膜进入前房,或对深层菌丝的强烈免疫反应所致。
前房积脓:表明炎症波及前房的严重表现。

真菌性角膜炎是真菌感染角膜引起的角膜炎的总称。也包括无炎症但角膜内真菌增殖的病变,称为“角膜真菌症”,但日本感染性角膜炎诊疗指南第3版将伴有炎症的通常病变统一称为“真菌性角膜炎”1)。
真菌在形态上分为以下两类。两者的临床表现、危险因素和治疗策略差异很大。
从流行病学角度看,丝状菌感染常由植物表面或土壤中的真菌通过外伤引起,因此被称为“农村型”;而酵母菌感染与眼表疾病和类固醇滴眼液相关,因此被称为“城市型”。
井上等人进行的一项多中心前瞻性观察研究(2016年,《日本眼科学会杂志》)报告了真菌性角膜炎的患者背景、临床所见、治疗和预后的现状8)。全球范围内,温暖地区发病率更高,估计热带和亚热带地区每年有超过100万人患病7)。在亚洲温带地区,链格孢属是丝状菌中仅次于念珠菌属和镰刀菌属的第三大分离频率1)。在温带地区,除了镰刀菌属外,还有散发性报道的罕见致病菌如弯孢属6)。
真菌性角膜炎很少发生在没有危险因素的健康眼中,通常存在外伤、类固醇滴眼液、隐形眼镜佩戴或眼表疾病等诱因1)。
真菌性角膜炎比细菌性角膜炎进展缓慢,疼痛相对较轻,且对广谱抗生素无反应。丝状菌表现为羽毛状、边界不清的浸润,可能出现卫星病灶和内皮斑。确诊需要涂片镜检或培养证明真菌,治疗使用抗真菌药物。
患者主诉的症状如下。与细菌性角膜炎相比,进展缓慢,早期自觉症状轻微,容易导致诊断延迟1)。
在极早期,自觉症状轻微,可能仅有轻微的上皮损伤。疼痛相对较轻、病程缓慢是真菌性角膜炎的特征,是与细菌性角膜炎鉴别的线索1)。
丝状菌和酵母菌在裂隙灯显微镜下观察到的临床图像有很大不同。
丝状菌
羽毛状溃疡:表现为边界不清、毛糙的灰白色浸润。这是丝状菌感染的特征性表现。
隆起性病灶:刮擦时质地硬。
卫星病灶:主病灶周围散在小浸润。
内皮斑:在角膜后面形成盘状白色沉积物。这是菌丝穿过Descemet膜进入前房,或对深层菌丝的强烈免疫反应所致。
前房积脓:表明炎症波及前房的严重表现。
酵母菌
局限性脓肿:表现为边界相对清晰的纽扣状或类圆形浸润。
浅层局限:常局限于角膜基质浅层。
溶解倾向:病灶周围可见角膜基质溶解。刮擦时质地软。
与细菌性角膜炎相似:临床上难以与葡萄球菌感染区分,必须通过涂片镜检和培养进行鉴别。
丝状菌容易向角膜深层进展,感染扩大后最终导致严重的基质溶解,引起角膜穿孔。另一方面,如链格孢属等低温下易增殖的菌种,倾向于在角膜表面呈面状扩散。如果使用了类固醇滴眼液,典型表现可能被修饰,导致诊断困难,需注意1)。
在丝状真菌中,最常见且易导致重症的是镰刀菌属,代表菌种为Fusarium solani。此外,曲霉菌属、链格孢属、拟青霉属(现为Purpureocillium lilacinum)、弯孢属等也可引起角膜感染1)。
在酵母菌中,念珠菌属占绝大多数,代表菌种为Candida albicans。近年来,C. parapsilosis的分离频率增加,而C. glabrata和C. krusei对氟康唑敏感性低,需注意1)。
丝状真菌和酵母菌共同的真菌性角膜炎风险因素包括发病前使用类固醇滴眼液1)。
植物戳眼或土壤引起的眼外伤是丝状真菌性角膜炎的最大风险因素。初期自觉症状较轻,容易被忽视,诊断延迟可能导致角膜穿孔。受伤后如果持续出现充血、异物感、视力下降等症状,请尽早到眼科就诊。
对广谱抗菌药物无反应的角膜溃疡、存在卫星病灶、以及大面积溃疡但分泌物较少,是应怀疑真菌感染的重要表现1)。根据角膜表现可临床推测是丝状菌感染还是酵母菌感染,患者背景(外伤史、类固醇使用史、隐形眼镜佩戴史、眼部手术史)可作为鉴别诊断的参考。
确诊需要从病灶部位证明真菌的存在1)。由于真菌生长需要时间,临床怀疑本病时应不等培养结果即开始治疗1)。
真菌性角膜炎需与其他感染性角膜炎鉴别。特别是酵母菌引起的病灶与葡萄球菌感染相似,因此微生物学检查对鉴别很重要1)。
| 鉴别疾病 | 鉴别要点 |
|---|---|
| 细菌性角膜炎 | 快速进展、脓性分泌物、对广谱抗生素有反应 |
| 棘阿米巴角膜炎 | 隐形眼镜佩戴史、放射状角膜神经炎、环形浸润 |
| 疱疹性角膜炎 | 树枝状病变、复发史、角膜感觉减退 |
确诊需要从角膜病灶刮取物中证明真菌的存在。通过真菌荧光染色或革兰染色涂片镜检确认菌丝,并在沙氏琼脂培养基上培养。培养至少需要2周,因此如果根据临床发现怀疑本病,应在等待培养结果前开始治疗。
真菌性角膜炎的治疗与细菌感染相比反应较差,且治疗周期长。根据日本感染性角膜炎诊疗指南第3版,推荐采用局部和全身抗真菌药物联合病灶刮除的多方位治疗1)。由于确定致病菌至少需要1周,生长缓慢的真菌可能需要4周,因此如果根据临床发现怀疑本病,应立即开始治疗1)。
根据菌种不同,使用三类抗真菌药物。在眼科局部用药中,只有多烯类的匹马霉素(5%滴眼液、1%眼膏)有医保覆盖,其他均为临床使用的院内制剂1)。
感染性角膜炎诊疗指南第3版建议,将真菌分为酵母样真菌(念珠菌属)、镰刀菌属和镰刀菌属以外的丝状真菌,分别制定治疗策略1)。
酵母菌(念珠菌属)
首选:唑类单用或联合用药。
联合治疗:也推荐唑类与棘白菌素类联合使用。
注意事项:注意氟康唑耐药菌株(光滑念珠菌、克柔念珠菌)的增加。也可使用1%匹马霉素眼膏,但需注意药物毒性引起的角膜上皮损伤。
丝状真菌
镰刀菌属:多烯类匹马霉素为首选。考虑到分离频率高,应从初始治疗就考虑包含匹马霉素的方案。
非镰刀菌:推荐使用伏立康唑1%滴眼液。尤其考虑用于曲霉菌属、拟青霉属和赛多孢菌属。
难治病例:如果使用匹马霉素无改善,考虑加用伏立康唑滴眼液。
重症病例可参考以下联合用药处方。根据角膜所见,可加用结膜下注射(项目4)。
除滴眼外,联合全身给药抗真菌药。重症病例联合结膜下注射或基质内注射。使用阿托品消炎,不使用类固醇滴眼液。联合抗菌滴眼液应对细菌混合感染。
在《感染性角膜炎诊疗指南第3版》中,CQ-6指出“对于真菌性角膜炎的治疗,有条件推荐伏立康唑自配滴眼液”,推荐强度为“弱推荐”,证据等级为“B”1)。
支持伏立康唑滴眼液的RCT均在海外(印度)进行,主要针对丝状真菌性角膜炎1)。
基于这些证据,1%伏立康唑滴眼液被证明是非镰刀菌属丝状真菌引起的真菌性角膜炎的治疗选择。尤其对于匹马利星无效的病例,特别是曲霉菌属感染,值得考虑使用1)。
关于抗真菌药物全身给药的有效性,尚无明确证据1)。多烯类匹马利星水溶性差且分子量大,难以渗透至角膜深层,在伴有角膜新生血管的镰刀菌属重症病例中,静脉输注脂质体两性霉素B可能弥补药物渗透不良的问题1)。唑类伏立康唑全身给药后可进入前房1)。全身给药副作用较多,因此最好在确定致病真菌、目标明确的情况下使用1)。
病灶刮除可提高滴眼液的组织渗透性,并物理性减少菌量1)。由于不同真菌对药物治疗的反应不同,应积极联合使用以增强疗效。处方示例中显示每周刮除约两次。角膜变薄时需注意穿孔。对于链格孢属等表浅型,作为病灶刮除的延伸,表层角膜切除术也有效1)。
真菌性角膜炎的治疗可能持续数周至数月。与细菌性角膜炎相比,对药物的反应较慢,且滴眼液难以渗透至角膜深层,因此需要长期持续治疗。治疗期间必须定期随访,如果确定了致病菌,根据药敏试验结果调整处方也很有用。
当角膜上皮的完整性因外伤或眼表疾病受损时,附着的真菌在组织内增殖并建立感染1)。除外伤外,当存在糖尿病或长期使用类固醇眼药水等导致眼表易感性增加的情况时,结膜囊或皮肤上常驻的酵母样真菌(如念珠菌)可能成为病因。在隐形眼镜佩戴者中,镜盒内增殖的环境真菌可能成为病因。
一旦真菌附着并增殖于角膜上皮,建立感染,中性粒细胞迁移并聚集于病灶,形成白色浸润灶。随着组织破坏进展,形成脓肿,并越过鲍曼膜形成溃疡。前房内也发生中性粒细胞迁移,当炎症细胞增多时,形成前房积脓。真菌产生的蛋白水解酶、抗原和毒素释放到角膜内,导致坏死和组织结构损伤。
丝状真菌(尤其是镰刀菌属)的菌丝容易向角膜深层延伸,当突破德斯密膜并在角膜后表面扩展时,形成内皮斑。即使不突破德斯密膜,对深层浸润的丝状真菌的强烈免疫反应也可能产生内皮斑。随着感染扩散,最终发生严重溶解,可能导致角膜穿孔。
另一方面,酵母菌往往呈现比丝状真菌炎症更轻的角膜真菌病形态。病灶局限于角膜基质浅层,形成边界清晰的脓肿,并有溶解倾向。
Dong 等人报告了两例对局部抗真菌药耐药的真菌性角膜炎,通过单次前房内注射两性霉素B(10 μg/0.1 mL),两例患者最终最佳矫正视力均达到20/20 2)。该方法具有将药物直接递送至局部或全身给药难以到达的角膜深层和前房的优势。
由于抗真菌滴眼液分子量大,难以渗透到角膜基质深层,因此对于难治性深层病变,尝试了将药物直接注入病灶的角膜基质内注射。
使用的药物是伏立康唑(50 μg/0.1 mL)和两性霉素B(5–10 μg/0.1 mL)。有报道称,在手术显微镜下,将针头斜面朝下,从无病变部位斜向刺入,在脓肿周围分五点注射,形成药物屏障。注入基质内的药物作为储库存留,可维持有效浓度约7天。动物实验报告称,两性霉素B浓度超过20 μg/0.1 mL会引起角膜水肿、上皮糜烂和新生血管形成,因此需要注意浓度管理。
Ler 等人报告了一例深部丝状真菌感染(青霉菌属),通过在病灶周围环形注射伏立康唑50 μg/0.1 mL,每5天重复一次,共3次,成功治愈 3)。
在一项针对25例对那他霉素和伏立康唑滴眼液无反应的患者的研究中,72%对伏立康唑基质内注射有反应。大多数无反应者的培养结果为镰刀菌属阳性。另一项针对20例患者的研究中,14例对注射有反应,平均需要2.65次注射。
在一项针对40例对5%匹马利辛滴眼液无反应的真菌性角膜炎患者的随机对照试验中,比较了加用1%伏立康唑滴眼液与加用伏立康唑基质内注射的效果,结果显示治愈率无显著差异,但3个月后的矫正视力在滴眼液加用组更好 1)。尽管该随机对照试验病例数有限,但并未显示基质内注射优于滴眼液。
基质内注射是局部和全身给药的辅助疗法,而非单独治疗。未来的挑战包括确定最佳注射次数和间隔、验证不同菌种(尤其是镰刀菌属)的疗效,以及评估与其他辅助疗法联合使用的效果。
PACK-CXL(光活化角膜交联术)是一种利用核黄素和紫外线A照射稳定角膜基质并同时灭活病原体的治疗方法7)。角膜交联疗法最初是为治疗圆锥角膜(德累斯顿方案)而开发的,但自2008年起已临床应用于感染性角膜炎,并于2013年采用了PACK-CXL的名称7)。它具有不依赖抗生素的作用机制,有望成为应对日益增加的耐药菌的新治疗选择。关于真菌感染的临床前研究也有许多报道,但对于镰刀菌属等难治性真菌的最佳方案仍在建立中7)。
Todokoro等人通过DNA序列分析鉴定出与蚕蚀性角膜溃疡相关的链格孢角膜炎的菌种,并通过药敏试验确认伏立康唑的MIC为0.5 μg/mL,从而成功治疗4)。联合使用伏立康唑滴眼液和类固醇滴眼液,三个月后视力恢复至0.7。这表明分子诊断与药敏试验相结合可能提高个体化治疗的精确性。
Chen等人报告了两例在羊膜移植后10天内发生镰刀菌角膜炎和Sistotrema biggsiae角膜炎的病例5)。这是文献中首次报道Sistotrema biggsiae的人类感染。羊膜移植后感染性角膜炎的发病间隔通常为28至347天,因此提醒注意早期发病的病例5)。
井上等人对真菌性角膜炎的患者背景、临床所见、治疗和预后进行了多中心前瞻性观察研究,并在日本眼科学会杂志上报告了日本该病的实际情况8)。这提供了日本真菌性角膜炎的病原菌分布和治疗结果的基础数据,具有重要意义。