革兰阳性球菌
葡萄球菌:典型表现为小圆形、边界相对清晰的灰白色局限性脓肿1)。进展缓慢,但MRSA易重症化,常伴有比感染病灶更大的上皮缺损1)。特应性皮炎患者中MRSA检出率高。
肺炎链球菌:表现为特征性的匐行性角膜溃疡。病变一端愈合,另一端进展,看起来像在爬行移动1)。荚膜抵抗中性粒细胞吞噬,可向深部进展导致角膜穿孔1)。

细菌性角膜炎是细菌侵入并在角膜实质内增殖引起的化脓性炎症。也称为细菌性角膜溃疡,特别是由肺炎链球菌引起时,称为匐行性角膜溃疡(serpiginous corneal ulcer)。它是感染性角膜炎中最常见的类型,如果初期诊断和治疗不当,可能导致严重的视力障碍1)。
在日本,感染性角膜炎患者的年龄分布呈双峰型,峰值在20多岁和60多岁1)。年轻人群的峰值主要由隐形眼镜(CL)佩戴引起的感染构成。发病率没有明显的性别差异,但外伤引起的感染在男性中更常见,而CL相关的感染在女性中更常见1)。
根据大规模队列研究报告,发达国家的年发病率约为每10万人中数人到数十人,而发展中国家可达数百人1)。感染性角膜炎的病原微生物中细菌最多,其次是病毒、真菌和棘阿米巴1)。在美国,估计每年发生约71,000例微生物性角膜炎(包括细菌、真菌和棘阿米巴),近年来呈增加趋势7)。从视功能预后的角度来看,有些病例即使治愈后,由于不规则散光或角膜瘢痕,视力也无法恢复,尤其是中央部溃疡容易残留视功能障碍1)。
在日本,最常见的诱发因素是CL佩戴,与其他发达国家趋势相同1)。重症CL相关性角膜炎多见于使用两周频繁更换型软性CL(FRSCL)或传统型SCL的佩戴者,护理不当导致的镜片污染是重要的风险因素1)。还需注意CL佩戴引起的感染性角膜炎常为双眼性。在美国,CL佩戴是最大诱因,而在发展中国家,外伤是最大诱因7)。
细菌性角膜炎的四大致病菌是金黄色葡萄球菌、肺炎链球菌、铜绿假单胞菌和莫拉菌。其中葡萄球菌属的频率最高,铜绿假单胞菌是CL相关性角膜炎的主要致病菌1)。近年来国内外莫拉菌的报道增加,眼表疾病、眼手术史和糖尿病是其诱因1)。眼表常驻菌棒状杆菌也是相对常见的致病菌1)。
混合感染也不容忽视,AAO PPP报告称约43%的培养阳性病例检出两种或以上细菌7)。混合感染最常见的诱因是外伤,表皮葡萄球菌和镰刀菌属的组合较多7)。Ung等人将感染性角膜炎定位为“持续的临床挑战”,强调微生物学检查的快速化、新型抗菌药物以及耐药菌株地区差异监测的重要性11)。
“匐行性角膜溃疡”(serpiginous corneal ulcer)这一名称自19世纪开始使用,因其病变像爬行一样在角膜表面移动而得名。在日本,感染性角膜炎诊疗指南于2007年首次在日眼会志上发表,随后经过2013年第2版12)和2023年第3版的修订,推动了基于证据的诊疗标准化1)。
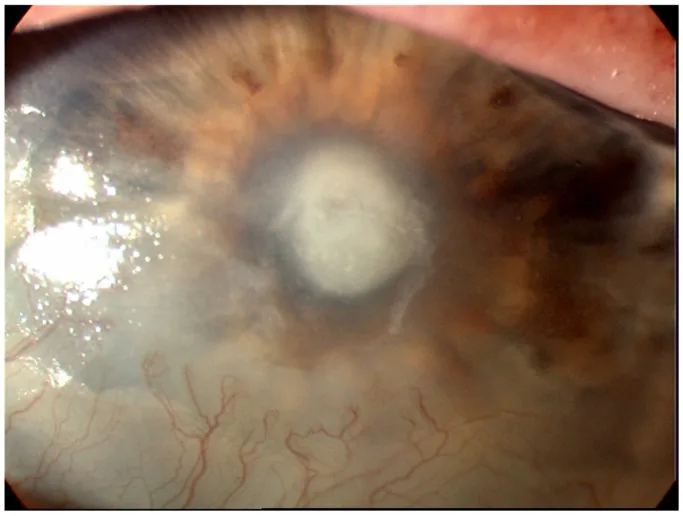
特征为急性发作的眼痛。轻症表现为眼异物感,重症则主诉剧烈眼痛1)。除疼痛外,还出现充血、视力障碍、流泪、黏液脓性分泌物和畏光1)。症状进展速度与致病菌的毒力相关,铜绿假单胞菌可在发病24小时内迅速恶化7)。
细菌性角膜炎的初期病变为浸润、上皮缺损、前房炎症细胞出现和睫状充血。但真正的初期病变很少被观察到,患者通常以圆形脓肿就诊。角膜表现因革兰阳性球菌和革兰阴性杆菌而异,是推测致病菌的重要临床线索1)。
重症病例可见前房积脓和纤维蛋白渗出,易发生虹膜后粘连。角膜后沉着物(KP)出现在与角膜浸润、脓肿或溃疡相对应的后表面1)。
裂隙灯显微镜检查时,用弥散光观察整体混浊,用反光法检查细胞浸润状态和前房炎症(尤其是KP)。用宽裂隙光检查角膜表面,用窄裂隙光评估病灶深度和前房炎症,并用荧光素染色显示上皮缺损,这一流程很有用。
革兰阳性球菌
葡萄球菌:典型表现为小圆形、边界相对清晰的灰白色局限性脓肿1)。进展缓慢,但MRSA易重症化,常伴有比感染病灶更大的上皮缺损1)。特应性皮炎患者中MRSA检出率高。
肺炎链球菌:表现为特征性的匐行性角膜溃疡。病变一端愈合,另一端进展,看起来像在爬行移动1)。荚膜抵抗中性粒细胞吞噬,可向深部进展导致角膜穿孔1)。
革兰阴性杆菌
铜绿假单胞菌:伴有环形脓肿,周围角膜呈毛玻璃样混浊1)。蛋白酶导致角膜溶解,进展迅速,易穿孔。多与接触镜相关,有报道称长期联合使用角膜塑形镜和接触镜可导致环形溃疡3)。
莫拉菌:在角膜中央形成局限性、边界清晰的溃疡1)。接触镜佩戴者和糖尿病等基础疾病是危险因素1)。进展相对缓慢,对多种抗菌药物敏感。
沙雷菌:表现多样,从轻度浅表溃疡到广泛脓肿,蛋白酶产生量的多少与严重程度相关1)。
特殊致病菌
革兰阳性球菌(葡萄球菌、肺炎链球菌)表现为小圆形至椭圆形、边缘整齐的局限性脓肿。而革兰阴性杆菌(铜绿假单胞菌、莫拉菌、沙雷菌)则伴有周围基质毛玻璃样混浊和明显水肿,重症病例因角膜基质溶解形成环形脓肿。感染性角膜炎诊疗指南第2版的角膜炎诊断流程图中,建议从局限性脓肿推断革兰阳性球菌,从环形脓肿推断革兰阴性杆菌1)。
正常角膜通过复层鳞状上皮和泪液中的防御物质(溶菌酶、乳铁蛋白、IgA)抵御感染。因此,细菌性角膜炎发生在创伤、接触镜佩戴、手术、眼表疾病或全身性疾病导致防御机制受损的情况下1)。AAO PPP将接触镜佩戴列为美国最大的危险因素,而世界许多地区创伤是主要原因7)。
接触镜相关
过夜佩戴:与日间佩戴相比,感染风险显著增加。包括角膜塑形镜在内的夜间佩戴是特别重要的危险因素7)。
不当护理:补充清洗液、污染镜盒、用自来水储存或冲洗是典型的诱因1)7)。
镜片类型:两周更换型软性接触镜和传统型软性接触镜中,铜绿假单胞菌、莫拉菌、沙雷菌等革兰阴性菌感染较多见1)。
装饰性接触镜:未经医生处方而在网上或商店购买的镜片感染风险高7)。
外伤与手术相关
眼表与全身因素
眼表疾病:干眼症、单纯疱疹性角膜炎、大疱性角膜病变、Stevens-Johnson综合征、神经营养性角膜病变是易感因素1)。曾有从污染的人工泪液中检出广泛耐药铜绿假单胞菌的案例2)。
全身因素:糖尿病、免疫抑制、特应性皮炎、胶原病等1)7)。
药物相关:长期使用类固醇滴眼液、污染滴眼液、非甾体抗炎药滴眼液是危险因素。长期使用氟喹诺酮类抗菌药滴眼液时,MRSA检出率升高1)。
非接触镜相关病例中,角膜移植术后、眼表疾病、长期使用氟喹诺酮类抗菌药下的MRSA是重要问题1)。长期使用类固醇或免疫抑制剂的患者需与真菌感染(尤其是酵母样真菌)和疱疹病毒鉴别1)。老年长期卧床患者出现难治性角膜炎时,需考虑铜绿假单胞菌、MRSA和真菌的可能性1)。
避免过夜佩戴和正确的镜片护理最为重要。AAO的细菌性角膜炎PPP也将过夜佩戴(包括角膜塑形镜)列为主要危险因素7)。每3个月更换镜盒、每日清洁干燥、避免接触自来水是基本要求7)。装饰性镜片和网购镜片也易成为感染源,因此建议医生处方和定期随访。
诊断需综合病史、临床所见和检查结果1)。感染性角膜炎诊疗指南(第3版)临床问题1(CQ-1)强烈推荐涂片镜检和培养检查用于细菌性角膜炎的诊断(证据等级C)1)。
确认隐形眼镜佩戴史(类型、使用时间、护理方法、有无误用)、外伤史、眼科手术史、既往角膜疾病(如角膜疱疹等)、正在使用的眼药水、长期使用类固醇或免疫抑制剂史、全身病史(糖尿病、特应性皮炎、MRSA感染史)1)。病程方面,进展迅速时考虑铜绿假单胞菌或链球菌;长期卧床的老年患者若难治,考虑铜绿假单胞菌、MRSA或真菌1)。
记录角膜浸润的部位、大小和深度,并用荧光素染色评估上皮缺损。同时评估前房炎症(细胞、闪辉、纤维蛋白、前房积脓)、角膜后沉着物、角膜知觉、眼睑闭合不全和泪道系统1)。若后极部观察困难,则加做超声B超检查。
眼前段光学相干断层扫描(AS-OCT)可客观显示角膜病变深度、角膜厚度增加、变薄、前房炎症细胞、纤维蛋白、KP、内皮斑等1)。通过治疗前后比较可评估疗效。但感染性角膜炎不在医保覆盖范围内1)。
活体共聚焦显微镜(IVCM)可无创观察角膜内细胞、神经纤维、真菌以及棘阿米巴滋养体和包囊1)。
确诊需通过角膜病灶刮片进行涂片镜检和培养检查1)。在抗菌药物给药前采集标本极为重要;感染性角膜炎GL第3版CQ-1报告,检查前未使用抗菌药物的病例培养阳性率为77.3%,使用后为37.8%1)。
在表面麻醉下,用无菌刮匙刮取溃疡边缘部。若有穿孔风险,则使用无菌棉签,并用火焰或酒精固定1)。在标本采集方法研究中,拭子刮取的培养阳性率为50%,23G针为35%;拭子刮取简便且推荐使用1)。直接接种于固体培养基的阳性率为61%,通过运输培养基间接接种为44%;可能时首选直接接种于固体培养基1)。
感染性角膜炎GL第3版报告,培养阳性率37.6–74.3%,涂片镜检阳性率58.1–73.7%,细菌涂片镜检的病原菌检出率60–75%1)。涂片阳性病例的培养阳性率高达57.1–82.4%,两者联合使用较为理想1)。
主要染色方法如下。
| 染色方法 | 检测对象 | 所需时间 |
|---|---|---|
| 革兰染色(Faber G) | 细菌、真菌、阿米巴 | 3分钟 |
| 吉姆萨染色(Diff-Quik) | 细菌、真菌、衣原体 | 15秒 |
| 真菌荧光Y染色 | 真菌和阿米巴包囊 | 荧光显微镜 |
革兰染色在怀疑细菌、真菌或棘阿米巴感染时进行1)。简易快速染色液套装Diff-Quik可在短时间内获得与吉姆萨染色等效的图像1)。真菌荧光Y染色特异性染色具有β结构的多糖几丁质和纤维素,灵敏地检测真菌和阿米巴包囊1)。
培养使用血琼脂平板、巧克力琼脂平板、沙氏琼脂、液体培养基(硫乙醇酸盐肉汤)和运输培养基(Seed Swab®、Transwab®)1)。血琼脂平板可判断溶血性,巧克力琼脂平板含有V因子和X因子,适合嗜血杆菌属和淋球菌的生长1)。培养判定需要48小时,药敏结果需要3-4天1)。
需要注意的是,眼表存在常驻菌,因此培养分离出的细菌不一定就是致病菌,需综合涂片结果、眼部表现、药敏结果和治疗效果进行判断1)。McLeod等人报告,虽然许多社区获得性感染仅凭经验治疗即可好转,但对于中央部大病变、实质溶解、前房积脓、角膜手术史和非典型病例,强烈推荐进行涂片和培养10)。AAO PPP明确推荐在以下情况下进行涂片和培养7):
PCR是一种快速检测微生物DNA的方法,但日本感染性角膜炎指南第3版不推荐仅凭角膜刮取物的PCR诊断细菌性角膜炎1)。PCR可能检测到眼表常驻菌,因此被定位为涂片镜检和培养检查的辅助手段1)。
需要与卡他性角膜浸润(葡萄球菌外毒素引起的III型过敏)、真菌性角膜炎(羽毛状浸润、卫星灶、内皮斑)、棘阿米巴角膜炎(放射状角膜神经炎、环形浸润、假树枝状病变)和疱疹性角膜炎(末端膨大的树枝状病变)进行鉴别1)。当培养阴性但强烈怀疑感染时,考虑角膜活检7)。
首先,如果正在使用抗菌药物,考虑暂时停药并重新培养。感染性角膜炎指南第3版报告,用药前培养阳性率为77.3%,用药后降至37.8%1)。如果仍然阴性,考虑角膜活检,并重新评估非结核分枝杆菌、诺卡菌、棘阿米巴和真菌等特殊病原体1)。同时继续使用广谱抗菌药物进行经验性治疗,每48小时评估治疗反应7)。
感染性角膜炎诊疗指南(第3版)指出,细菌性角膜炎的治疗必须选择对致病菌有效的抗菌药物,并要求迅速且准确地鉴定致病菌1)。该指南的治疗流程图(图10)显示了以下方针1)。
感染性角膜炎GL第3版的初始治疗药物示例如下1)。
| 疑似致病菌 | 首选(两种药物联用) |
|---|---|
| 革兰阴性杆菌 | 氟喹诺酮类 + 氨基糖苷类 |
| 革兰阳性球菌 | 氟喹诺酮类 + 头孢菌素类 |
若无法推测致病菌,则联合使用新喹诺酮类和β-内酰胺类药物1)。一旦鉴定出致病菌,根据涂片结果、培养结果和药敏结果重新评估治疗1)。
日本市售的抗菌眼药水包括氟喹诺酮类(第三代:氧氟沙星[OFLX]、左氧氟沙星[LVFX]、托氟沙星[TFLX];第四代:加替沙星[GFLX]、莫西沙星[MFLX])、头孢菌素类(盐酸头孢甲肟)、氨基糖苷类(妥布霉素、庆大霉素、地贝卡星、新霉素)、大环内酯类(红霉素)和氯霉素。糖肽类万古霉素作为院内制剂使用。
第三、四代氟喹诺酮类药物组织渗透性提高,对链球菌的效果也更强。高浓度左氧氟沙星水合物滴眼液对革兰阴性菌的治疗效果有所提高1)。而盐酸头孢甲肟滴眼液对链球菌有效,但对铜绿假单胞菌效果不佳;氨基糖苷类对铜绿假单胞菌有效,但对链球菌无效1)。需注意第四代氟喹诺酮类对铜绿假单胞菌的作用较弱。
主要致病菌群与药物类别的敏感性一般对应关系如下所示。
| 类别 | 葡萄球菌 | 链球菌 | 铜绿假单胞菌 |
|---|---|---|---|
| β-内酰胺类 | 有效 | 有效 | 弱 |
| 氟喹诺酮类 | 有效 | 有效 | 有效 |
| 氨基糖苷类 | 有效 | 无效 | 有效 |
| 大环内酯类 | 弱 | 有效 | 弱 |
每次滴眼1~2滴,根据严重程度和药物的抗生素后效应(PAE)考虑 1)。重症病例或刺激导致流泪明显时,可每30分钟至1小时频繁滴眼 1)。氨基糖苷类和氟喹诺酮类具有PAE,但头孢甲肟和氯霉素的PAE较短,需要更频繁滴眼 1)。
美国AAO的细菌性角膜炎PPP(2023)建议,对于伴有中央大病变或前房积脓的视力威胁病例,使用强化抗菌药物 7)。具体配制方法如下 7)。
重症病例使用头孢唑林50 mg/mL联合妥布霉素14 mg/mL;怀疑MRSA时加用万古霉素25~50 mg/mL 7)。强化抗菌药物作为院内配制使用,由于配制安全性和保存稳定性问题,感染性角膜炎GL第3版提醒“避免轻易使用” 1)。
如果市售药物无效,可考虑用生理盐水稀释注射用药物,配制院内滴眼液使用 1)。对于MRSA和MR-CNS,已有报道氯霉素滴眼液和院内配制阿贝卡星滴眼液(超说明书使用)的有效性 1)。对于广泛耐药(XDR)铜绿假单胞菌,已有报道使用头孢地尔等新型抗菌药物全身给药 2)。
近年来,眼科广泛使用的氟喹诺酮类药物敏感性下降成为问题,MRSA、MRSE、耐青霉素肺炎球菌等多重耐药菌的检出增加 1)。由于滴眼液中药浓度较高,即使药敏试验显示耐药,如果临床有效,有时也可以继续使用 1)。
感染性角膜炎诊疗指南(第3版)的CQ-5得出结论:“弱推荐在细菌性角膜炎治疗中不联合使用糖皮质激素滴眼液。” 1) 这是基于许多病例未能确定病原菌,且考虑到耐药菌增加,应谨慎联合使用类固醇的观点 1)。
角膜溃疡类固醇试验(SCUT)的主要试验显示,泼尼松龙磷酸酯1%滴眼液联合广谱抗菌药物在视力结局上无显著差异,但亚组分析提示,在铜绿假单胞菌性和重症病例中早期联合使用类固醇可改善视力 9)。基于此结果,AAO细菌性角膜炎PPP 2023指出“在确定病原菌并确认对抗菌药物有反应后(通常48小时后),可考虑联合使用类固醇” 7)。但棘阿米巴、诺卡菌和真菌感染禁用 7)。
在决定治疗方案时,应参考感染性角膜炎诊疗指南第3版的推荐,对于重症病例,需根据个体病情判断。
AAO PPP建议,如果在治疗开始后48小时内未观察到改善趋势,则应重新考虑治疗方案7)。感染性角膜炎GL第3版也要求,如果无改善,应重新评估患者背景和治疗经过,确认是否存在混合感染(细菌+真菌,罕见细菌+疱疹)的可能性以及患者的滴眼药依从性1)。
对于药物治疗无效或角膜穿孔的病例,进行外科干预。感染性角膜炎GL第3版指出,在不得已的情况下,如前房持续消失,应进行治疗性角膜移植,但如果可能,最好在感染平息后进行择期角膜移植1)。可选择全层角膜移植(PKP)或深板层角膜移植(DALK),有报道在重症铜绿假单胞菌角膜炎后通过DALK获得了良好的视力恢复6)。对于小穿孔(<2 mm),使用氰基丙烯酸酯角膜粘合剂和治疗性角膜接触镜。SMILE术后重症感染时,有报道将角膜帽转为角膜瓣,清除坏死组织并用抗菌药物冲洗的方法5)。对于C. bovis引起的穿孔病例,进行了Gundersen结膜瓣手术4)。
感染性角膜炎诊疗指南(第3版)CQ-5明确指出:“弱推荐在细菌性角膜炎的治疗中不联合使用肾上腺皮质激素滴眼液”1)。这是基于许多病例未能确定病原菌以及耐药菌增加的考虑,以安全为重的推荐1)。SCUT试验的亚组分析和AAO PPP认为,仅在确定病原菌并确认对抗菌药物有反应后(通常48小时后)才可谨慎考虑联合使用,但棘阿米巴、诺卡菌和真菌感染为禁忌7)。
正常角膜具有由复层鳞状上皮和Bowman膜构成的屏障,泪液中的溶菌酶、乳铁蛋白、IgA等防御物质阻止微生物入侵1)。当这种防御机制因外伤、隐形眼镜佩戴、类固醇滴眼液或眼表疾病等被破坏时,细菌可侵入角膜基质。
当细菌在角膜内增殖时,以中性粒细胞为主的炎症细胞浸润,形成化脓性病变(浸润、脓肿、溃疡)1)。浸润的中性粒细胞释放的蛋白水解酶和活性氧导致角膜基质进行性破坏,愈合后残留组织变薄1)。如果感染长期化或重症化,角膜内皮细胞数量显著减少,可能发展为大疱性角膜病变1)。
近年来,眼科领域对氟喹诺酮类药物的敏感性下降成为问题,MRSA、MRSE、耐青霉素肺炎球菌等多重耐药菌正在增加1)。据报道,2005年至2015年间,MRSA和铜绿假单胞菌的氟喹诺酮耐药性有所进展7)。耐药性的背景包括过度使用抗菌药物、隐形眼镜佩戴者的污染镜盒环境以及基因水平转移等。Austin等人的综述也指出,基于当地流行病学数据的经验性治疗和快速药敏试验对于应对耐药菌的重要性13)。
铜绿假单胞菌附着于角膜上皮细胞的细胞表面糖脂(如无唾液酸神经节苷脂),并通过III型分泌系统将效应分子注入宿主细胞。这引起角膜上皮细胞凋亡和中性粒细胞募集。随后,细菌释放的弹性蛋白酶、碱性蛋白酶和蛋白酶IV等蛋白酶降解角膜基质的胶原蛋白和蛋白聚糖,导致快速组织溶解1)11)。同时,宿主中性粒细胞来源的基质金属蛋白酶(MMP-2、MMP-9)也参与角膜破坏,即使在感染控制后也是瘢痕形成的主要原因。这种感染建立和组织破坏的级联反应解释了为什么治疗不仅要用抗菌药物清除病原体,还要控制宿主过度炎症11)。
AAO PPP将细菌性角膜炎的病程分为四个阶段:进行性浸润、活动性溃疡形成、退行和愈合7)。即使接受适当治疗,角膜瘢痕或不规则散光也可能导致视功能损害,早期诊断和早期使用抗菌药物是影响预后的最大因素1)。未经治疗或重症病例可在24小时内发生角膜穿孔,导致眼内炎甚至眼球丧失7)。
Morelli MK等人报告了一例由市售人工泪液(EzriCare)中分离的广泛耐药(XDR)铜绿假单胞菌引起的角膜溃疡,通过全身使用头孢地尔(一种铁载体头孢菌素)联合局部亚胺培南和多黏菌素B成功治疗。全基因组分析鉴定出blaVIM-80和blaGES-92)。
Kikuchi等人报告了一例63岁男性,同时使用角膜塑形镜和软性隐形眼镜10年,发生铜绿假单胞菌角膜炎。表现为全角膜浸润和环形溃疡,使用左氧氟沙星、头孢甲肟和庆大霉素滴眼液联合静脉注射亚胺培南治疗后愈合,但残留角膜混浊3)。
Elsheikh M等人报告了一例89岁女性,有带状疱疹角膜炎病史,发生由牛棒状杆菌引起的严重角膜感染并穿孔。推测感染途径为附近与牛的接触。采用万古霉素和环丙沙星联合治疗及Gundersen结膜瓣手术处理4)。
Li J等人报告了SMILE术后发生细菌性角膜炎的5例(7眼)。术后1-3天发病,培养出表皮葡萄球菌和肺炎链球菌。重症病例将角膜帽转为角膜瓣进行坏死组织清除和抗菌药物冲洗。所有眼最终矫正视力达到20/32或更好5)。
Arun K 和 Georgoudis 报告了一例32岁男性隐形眼镜佩戴者患铜绿假单胞菌角膜炎,在急性期抗生素治疗后行DALK,获得了良好的视力恢复 6)。
作为应对抗生素耐药性问题的方法,光活化角膜交联(Photoactivated Chromophore for Keratitis-Corneal Cross-linking:PACK-CXL)正受到关注。2008年,圆锥角膜治疗的德累斯顿方案(0.1%核黄素滴眼30分钟 + UVA 3 mW/cm²照射30分钟,总能量5.4 J/cm²)被应用于感染性角膜炎的治疗 8)。2013年的国际会议上正式采用了PACK-CXL的名称 8)。
Kowalska 等人的范围综述分析了233项临床前研究,总结出PACK-CXL能增强角膜基质对酶降解的抵抗力,并杀灭包括细菌、真菌和阿米巴在内的病原体 8)。在中等程度以下的细菌性角膜溃疡中报告了良好结果,但德累斯顿方案被认为效果不足,正在向加速型、高能量方案转变 8)。这是FDA未批准的适应症,在日本也处于研究阶段 7)。
耐药菌的增加是一个全球性问题,需要针对MRSA角膜炎和氟喹诺酮耐药菌的新治疗策略 7)。未来有望建立PACK-CXL的标准方案、现有抗生素的新制备方法以及菌种特异性快速诊断的发展。
对于MRSA,万古霉素滴眼液(25–50 mg/mL)或院内自制的阿贝卡星滴眼液是选择之一 1)7)。对于氟喹诺酮耐药株,考虑更换为氨基糖苷类或头孢菌素类,或氯霉素滴眼液 1)。对于广泛耐药(XDR)铜绿假单胞菌,已有报告使用头孢地尔等新型抗生素全身给药 2)。无论哪种情况,基于药敏试验选择治疗药物都是必不可少的,涂片和培养检查的重要性再次被强调 1)。PACK-CXL作为耐药菌的替代疗法正在研究中,但并非标准治疗 8)。