急性期治療
人工淚液及眼藥膏:標準處方為0.1%玻尿酸鈉點眼液每日4次,搭配睡前使用歐弗沙辛眼藥膏(0.3%)。
眼罩及睫狀肌麻痺劑:急性期合併使用局部睫狀肌麻痺劑與暫時性眼罩,促進眼表面癒合2)。
抗菌藥物:針對上皮缺損,處方局部抗菌藥物以預防感染。
鎮痛藥:口服非類固醇抗發炎藥(如洛索洛芬60mg需要時服用)可減輕不適感。

復發性角膜糜爛(recurrent corneal erosion:RCE)是由於角膜上皮與基底膜形成的黏附結構異常,導致角膜上皮反覆自然脫落的一種疾病1,2)。發生的上皮糜爛本身在數日內即可癒合,但經過一定時間(1~2週至數月)後會復發。表現為復發性的眼痛和角膜上皮損傷,是嚴重影響患者生活品質(QOL)的代表性角膜疾病之一5)。
發作大多在清晨起床時發生。特點是相對於糜爛的大小,疼痛、異物感等自覺症狀較為劇烈,頻繁反覆發作時,對復發的擔憂可能成為患者的精神壓力。由於多發生於睡眠後,也可能導致失眠。由於表現為單眼性復發性角膜炎,容易被誤診為角膜皰疹,因此問診與徵候的細緻結合是診斷的關鍵。
最常見的病因是機械性外傷,紙邊、指甲、樹枝、睫毛膏前端等造成的切線方向外傷是典型的誘因。另一方面,以上皮基底膜失養症(EBMD)為首的角膜失養症也是重要原因,金屬皰疹性角膜炎、糖尿病性角膜上皮病變、神經麻痺性角膜病變等也可能成為誘因1,5)。
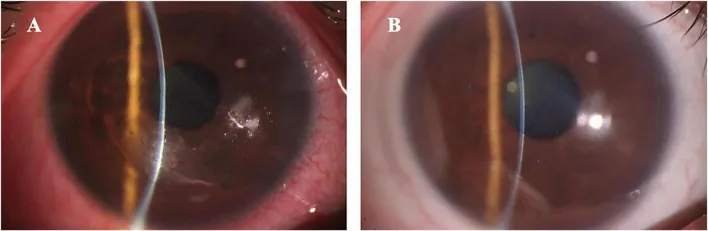
根據Chandler分類,RCE分為以下兩種型態2)。
主要自覺症狀如下。
即使在非發作期,患者也可能主訴起床時的異物感,這具有較高的診斷價值。由於常在睡眠後發病,可能導致失眠,影響患者的日常生活2,5)。
睡眠期間眼瞼閉合,淚液生成減少,角膜上皮與眼瞼直接接觸。黏附不良的上皮容易在眼瞼開閉時被剝離,尤其是起床睜眼時更容易誘發。夜間角膜表面的乾燥與眼瞼的物理接觸共同作用,被認為是起床時發生糜爛發作的原因。
裂隙燈顯微鏡檢查所見範圍廣泛,從正常表現到大面積上皮缺損均可出現2)。
透過角膜圖記錄和照片拍攝,隨時間推移比較糜爛的部位和大小。
使用雷射活體共聚焦顯微鏡(IVCM)對外傷性RCE的觀察發現,基底上皮細胞記憶體在沉積物、上皮下微皺褶和條紋、受損的上皮下神經、異常的基底膜以及前部基質形態改變4)。這些發現提示了臨床黏附不良背後的微細結構變化。
RCE的原因大致分為外傷性和非外傷性兩類1,5)。
這是最常見的原因1)。紙張邊緣、指甲、樹枝、睫毛膏尖端等尖銳物體對角膜的切線方向外傷容易成為誘因。患者本人往往不記得住外傷史,部分病例以不明確主訴遷延經過5)。
以下角膜營養不良可引起RCE1,2)。
糖尿病、乾眼症、瞼板腺功能障礙(MGD)、眼酒渣鼻(ocular rosacea)、帶狀角膜變性、夜間兔眼、過去角膜感染(包括皰疹性角膜炎後的metaherpes)、Salzmann結節狀變性等也參與RCE的病理過程1,2,5)。
並非所有角膜營養不良患者都會發生RCE。上皮基底膜營養不良(EBMD)關聯性最強,但也僅佔RCE病例的19%~29%左右。角膜營養不良的類型、嚴重程度以及環境因素等共同影響。
RCE的診斷主要基於病史詢問和裂隙燈顯微鏡檢查的臨床診斷2,5)。
需注意該病易被誤診為角膜疱疹,因其表現為單眼性、復發性角膜炎5)。
| 鑑別診斷 | 鑑別要點 |
|---|---|
| 角膜疱疹 | 樹枝狀潰瘍、角膜知覺減退、單眼性、復發性 |
| 神經營養性角膜炎 | 角膜知覺顯著減退、難治性上皮缺損 |
| 乾眼症 | 淚液量減少、BUT縮短 |
| 帶狀角膜變性 | 眼瞼裂部帶狀混濁、鈣質沉積 |
| 輪部幹細胞缺乏症 | 角膜緣所見、結膜上皮化 |
| Salzmann結節狀變性 | 角膜表層隆起病變 |
其他需要鑑別的疾病包括角膜潰瘍(細菌性、真菌性、疱疹性)、角膜異物、眼瞼鬆弛症候群等2)。
對於上皮基底膜失養症和RCE,可採用上皮清創術進行管理6)。
RCE的治療需分階段進行。急性期促進糜爛癒合,之後以預防復發為主要目標2,5,11)。
急性期治療
人工淚液及眼藥膏:標準處方為0.1%玻尿酸鈉點眼液每日4次,搭配睡前使用歐弗沙辛眼藥膏(0.3%)。
眼罩及睫狀肌麻痺劑:急性期合併使用局部睫狀肌麻痺劑與暫時性眼罩,促進眼表面癒合2)。
抗菌藥物:針對上皮缺損,處方局部抗菌藥物以預防感染。
鎮痛藥:口服非類固醇抗發炎藥(如洛索洛芬60mg需要時服用)可減輕不適感。
復發預防治療
睡前眼藥膏:即使糜爛發作消失後,也應至少持續使用3個月,最好維持6個月。指導患者起床後立即點用人工淚液,並將點眼瓶放在枕邊。
高張食鹽水:使用5%氯化鈉點眼液或眼藥膏。據報導,睡前使用對於急性期和慢性期均有效2)。
治療性隱形眼鏡:透過連續配戴促進上皮穩定。根據報告,12例連續配戴3個月的患者中,9例(75%)在約1年追蹤時未見復發7)。
淚點封閉術:在伴有乾眼症時考慮。可選擇膠原蛋白塞暫時性封閉或矽膠塞永久性封閉2)。
當保守治療效果不足時加用。
適用於保守治療無效的難治病例。
外科治療選擇
上皮清創術:用棉籤或纖維素海綿去除黏附不良的上皮,暴露Bowman層的平滑面。之後合併使用治療性軟性隱形眼鏡和局部抗菌藥物6)
角膜表層穿刺(anterior stromal puncture:ASP):使用25號細針,在裂隙燈顯微鏡下去除上皮後對淺層基質進行微穿刺。針尖輕微彎曲以防止穿孔。由於穿刺部位會留下點狀混濁,應避開瞳孔區。Zauberman等人的回顧性研究(30例35眼)顯示,單次治療後62.9%的眼睛症狀消失,37.1%的糜爛發作減輕9)
鑽石鑽拋光:去除上皮後,用鑽石鑽拋光Bowman層以改善上皮黏附性。術後配戴治療性隱形眼鏡4~5天2)
PTK(治療性角膜切除術):使用準分子雷射在5~7μm深度均勻切除角膜。O’Brart等人的報告顯示,17眼中13眼在最終追蹤時未見復發10)。可能存在遠視化傾向,且可執行該手術的機構有限。
角膜表層穿刺亦有使用Nd:YAG雷射(0.4~0.5mJ脈衝)進行非接觸式穿刺的報導2)。由於穿刺部位可能形成疤痕,無論何種術式都應避免在瞳孔區操作。
在糜爛發作消失後,繼續使用睡前眼膏和醒來後立即滴用人工淚液至少3個月,最好6個月。有時即使在1年多後仍可能發生糜爛發作,因此持續足夠長的時間很重要。
關於RCE的治療,有2018年Cochrane系統評價,但納入的10項RCT(共505例)在規模和品質上存在局限性,尚未能確立確定的治療演算法11)。在臨床實踐中,通常從保守治療開始逐步升級,對難治性病例考慮手術治療。
正常角膜上皮經由基底細胞的半橋粒(hemidesmosome)附著於基底膜1,2)。基底膜主要由IV型膠原蛋白和層黏連蛋白構成,透過錨定原纖維(VII型膠原蛋白)與下方的Bowman層和基質連接。纖連蛋白-整合素系統所介導的細胞間及細胞-基質間相互作用對維持黏附結構扮演重要角色。
在RCE中,初始損傷後上皮與下方基質的黏附變得不完全且不穩定1)。病理學上,可觀察到基底膜的斷裂或缺失,以及基底細胞黏附結構——半橋粒的減少。
在創傷後RCE中,因某種原因,正常黏附結構的重建受到阻礙。紙張或指甲等造成的切線方向外傷不僅損傷上皮,還損傷Bowman層附近的黏附機制,被認為在癒合過程中無法再生足夠的錨定原纖維5)。另一方面,在伴隨角膜營養不良的RCE中,構成蛋白質成分的基因異常導致黏附結構本身脆弱。
外傷性RCE的IVCM觀察詳細顯示了黏附複合體缺損、基底上皮細胞內沉積物、上皮下微皺褶、上皮下神經損傷、異常基底膜和前部基質形態變化等4)。這些發現反映的不僅是單純的上皮剝離,而是涉及基底膜-Bowman層-前部基質的複合性微細結構異常。
在合併瞼板腺功能障礙(MGD)、眼酒渣鼻和復發性糜爛的患者中,有毒游離脂肪酸、介白素-1(IL-1)和基質金屬蛋白酶-9(MMP-9)的水平升高已被報導2)。這些分子會分解黏附複合體並抑制基底膜形成。
多西環素和局部類固醇均可降低人類角膜上皮培養物中MMP-9的含量和活性。MMP-9抑制可通過減少膠原蛋白和半橋粒的分解,有助於穩定上皮黏附機制8)。
角膜上皮的癒合通過以下三個階段進行2)。
在RCE中,由於第三階段的黏附結構重建不充分,上皮容易持續處於易剝離的狀態。
夜間睡眠時,閉眼導致淚液分泌減少,上皮與眼瞼結膜緊密貼合。黏附薄弱的上皮部分在晨起睜眼的機械應力下容易剝離。此機制解釋了為何RCE發作集中於清晨起床時2,5)。
RCE本質上是一種有較強自癒傾向的疾病2)。但要判定為痊癒,至少需要無發作期持續3個月,最好達到6個月。部分病例即使經過1年以上仍可能再次出現糜爛發作,因此反覆向病人說明復發風險非常重要。
有些病例一旦中斷治療便立即復發。特別是外傷引起的病例,黏附結構的完全重建需要數月至半年以上,因此即使在症狀消失後,也需要鼓勵病人堅持預防性用藥。為防止病人自行判斷「已經好了」而中斷治療,從初診時就告知長期治療的遠景,直接關係到抑制復發。
併發症包括角膜混濁和疤痕形成、治療用隱形眼鏡或長期使用類固醇引起的感染性角膜炎、以及視力下降2)。若能獲得適當治療和及時診斷,預後極佳,因此建議對具有風險因子的患者進行衛教,使其在出現症狀時立即就醫。