眼瞼緣所見
開口部阻塞所見:可見plugging(栓子)、pouting(開口部周圍的尖頂隆起)、ridge(覆蓋多個開口的堤狀結構)。
眼瞼緣血管擴張:開口部周圍的毛細血管擴張・毛細血管擴張症。
黏膜皮膚交界處(MCJ)移位:向前方或後方偏移。通過螢光素染色易於觀察。
眼瞼緣不整:與角膜接觸的線條凹凸不平。

瞼板腺功能障礙(MGD: Meibomian Gland Dysfunction)是瞼板腺的慢性、瀰漫性功能異常。日本MGD工作組(2010年)將其定義為「由於各種原因導致瞼板腺功能發生瀰漫性異常的狀態,並伴有慢性不適感」4)。2023年發布的《瞼板腺功能障礙診療指南(日本眼科學會雜誌127卷2號)》將MGD定位為蒸發亢進型乾眼症的主因,並提供了以實證為基礎的綜合性診療指引3)。
在國際上,國際瞼板腺功能障礙研討會(IWMGD 2011)將其定義為「以終末導管阻塞及/或腺體分泌物質與量的改變為特徵的慢性瀰漫性異常」1), 10)。TFOS DEWS III(2025)也將MGD列為乾眼的主要促成因素,並將熱敷、眼瞼清潔、IPL(強脈衝光)及低強度雷射等物理治療納入其管理流程中8)。日本乾眼研究會制定了《乾眼診療指引》(2019),強調MGD是蒸發過強型乾眼的重要原因9)。
瞼板腺是位於眼瞼瞼板內的一種大型皮脂腺。使用非接觸式瞼板腺成像觀察時,正常眼的上眼瞼有2530條瞼板腺,下眼瞼有1520條5)。每條腺體都有從中央導管分支出來的多個腺泡(acinus),腺泡上皮細胞(meibocyte)透過全分泌(holocrine secretion)方式產生瞼脂(meibum)。瞼脂含有100多種脂質(主要為蠟酯、膽固醇酯、極性磷脂質和鞘脂)和90多種蛋白質,形成淚膜最外層的脂質層,防止水層蒸發,降低表面張力以維持淚膜的擴展1)。淚液脂質層厚度(LLT)正常為60~100 nm,在MGD中會變薄1)。
根據日本眼科學會指引2023 BQ-4引用的一項日本人口基礎研究(對象為6~96歲居民),各年齡層的MGD盛行率如下3)。
| 年齡層 | MGD盛行率 |
|---|---|
| 19歲以下 | 0% |
| 20~29歲 | 11.8% |
| 30~39歲 | 5.6% |
| 40~49歲 | 21.6% |
| 50~59歲 | 32.8% |
| 60~69歲 | 41.9% |
| 70~79歲 | 48.4% |
| 80~89歲 | 63.9% |
許多研究顯示,MGD的發生率與嚴重程度隨年齡增長而增加。就性別而言,男性和停經後女性更為常見3)。Arita等人使用非接觸式瞼板腺攝影的研究報告指出,約86%的乾眼症患者合併有MGD5)。種族差異也已被指出,亞洲人的患病率(3.5%–19.9%)高於白種人1)。在日本,乾眼症研究會估計包含潛在患者在內,共有數千萬名患者,是日常診療中最常遇到的慢性疾病之一3)。
日本MGD工作小組對MGD的分類如下4)。
臨床上,分泌減少型較為常見,其中阻塞性MGD(oMGD)最為普遍。日眼會誌GL 2023 BQ-1將分泌減少型MGD的主要病理機制總結為「導管上皮過度角化和腺泡萎縮」3)。萎縮性MGD是腺泡瀰漫性萎縮的狀態,提出了阻塞繼發性和原發性腺細胞損傷兩種機制。
分泌增加型MGD包括脂漏性MGD(sMGD),它與阻塞性MGD形成對比。輕輕按壓上眼瞼的瞼板部時,正常者會排出透明的瞼脂,但在脂漏性MGD中,分泌異常增加,沿下眼瞼緣的淚液中可見泡沫形成。相關疾病包括後部眼瞼炎、瞼板腺炎和瞼板腺炎相關角結膜上皮症(MRKC),日眼會誌GL 2023 BQ-3強調了統一這些概念的重要性3)。
國際上,IWMGD 2011將MGD分為分泌低下型(low-delivery)和分泌過多型(high-delivery),分泌低下型中以阻塞性最為常見1)。
MGD是蒸發亢進型乾眼最常見的原因。瞼板腺功能下降導致淚液脂質層變薄時,淚液蒸發加劇,淚液滲透壓升高,眼表發生炎症。日本眼科學會指引2023也明確指出MGD可導致乾眼並引起慢性眼部不適。
日本眼科學會指引2023 CQ-2列舉MGD的以下自覺症狀,並強烈建議在問診時採集3)。
表現為「黏糊糊的感覺」的粘稠感也是其特徵之一4)。症狀常在早晨較重,有時患者會主訴視功能波動。但是,目前尚未確定能夠鑑別MGD與其他眼表疾病的特徵性自覺症狀3)。自覺症狀的評估廣泛使用OSDI(Ocular Surface Disease Index)問診表。MGD的症狀不僅對QOL有顯著影響,還會引起眼部刺激和視功能下降,因此系統性地掌握生活障礙程度非常重要1)。
日本眼科學會指引2023 CQ-3推薦以下四項所見有助於MGD的診斷:瞼板腺開口部阻塞、眼瞼緣血管擴張、黏膜皮膚交界處移位以及眼瞼緣不整3)。
眼瞼緣所見
開口部阻塞所見:可見plugging(栓子)、pouting(開口部周圍的尖頂隆起)、ridge(覆蓋多個開口的堤狀結構)。
眼瞼緣血管擴張:開口部周圍的毛細血管擴張・毛細血管擴張症。
黏膜皮膚交界處(MCJ)移位:向前方或後方偏移。通過螢光素染色易於觀察。
眼瞼緣不整:與角膜接觸的線條凹凸不平。
瞼板腺評估
瞼板腺分泌物性狀:正常為透明油脂。MGD中表現為混濁、顆粒狀或牙膏狀。
島崎分類:用拇指中度壓迫評估排出性,分為0~3級,2級及以上為異常。
瞼板腺成像(Meibography):使用紅外線相機觀察腺體缺失(dropout)、縮短和扭曲。
淚膜脂質層變薄:可用干涉儀評估脂質層厚度(LLT)。
島崎的瞼板腺分泌物分級按以下4個等級進行評估4), 12)。
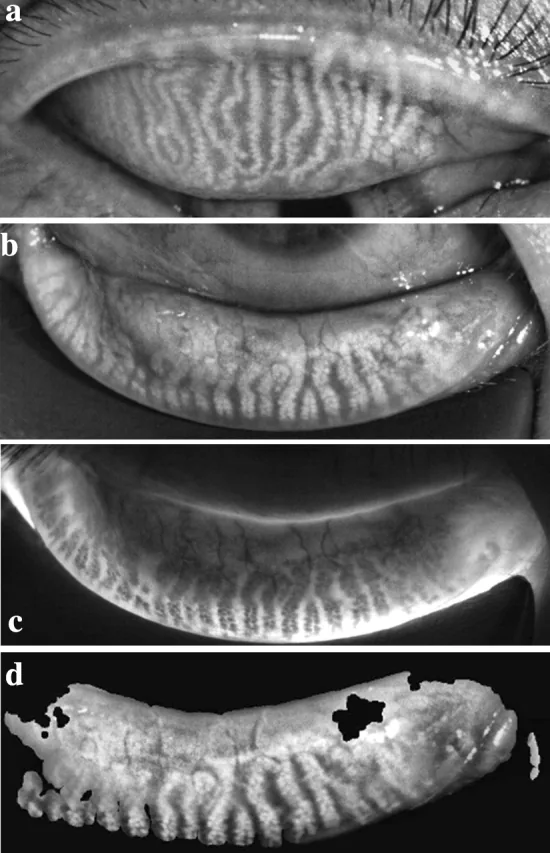
Arita等人於2008年開發的非接觸式麥氏腺攝影(meibography)是一種低侵入性檢查裝置,僅需在裂隙燈顯微鏡上加裝紅外線穿透濾光片(700–850 nm)和小型紅外線CCD攝影機即可5), 11)。紅外光穿透眼瞼板並被瞼脂反射,因此麥氏腺表現為高反射(白色)影像。MGD患者可見瞼板腺消失(dropout)、縮短、彎曲、斑駁狀變化、擴張等多種表現5)。
腺體消失的程度根據Arita麥氏腺評分(meiboscore)分為以下4個等級5)。
| 麥氏腺評分 | 腺體消失面積 |
|---|---|
| 0級 | 無消失 |
| 1級 | 不超過總面積的1/3 |
| 2級 | 1/3至2/3 |
| 第3級 | 2/3以上 |
據報告,隱形眼鏡配戴者比非配戴者出現更多的瞼板腺脫落。配戴年限越長變化越明顯,軟式與硬式隱形眼鏡均可觀察到16)。
日眼會誌GL 2023 BQ-5和BQ-6系統性地整理了與MGD發病相關的因素3)。
老化與荷爾蒙因素
眼部因素與外在因素
全身性疾病
蠕形蟎感染
Demodex folliculorum寄生於睫毛根部,Demodex brevis寄生於瞼板腺和皮脂腺內1)。寄生率隨年齡增長而增加,70歲以上可達100%1)。一項150例的佇列研究顯示,90%的前部瞼緣炎患者和60%的MGD患者中檢出蠕形蟎1)。D. folliculorum直接破壞毛囊基底細胞,引起反應性角化過度,形成圓柱狀皮屑。D. brevis物理性阻塞瞼板腺,誘導肉芽腫反應,促進霰粒腫的發生1)。蠕形蟎還可作為細菌載體引發炎症,在酒渣鼻患者中可能引起遲發型過敏反應1)。Zhang等人報告了一例46歲男性MGD病例,儘管外部表現不明顯,但擠出物中檢出15隻Demodex brevis,證明了擠出物直接鏡檢的實用性6)。
日本眼科學會指引GL 2023明確記載軟性隱形眼鏡配戴是MGD的危險因子。配戴時瞬目產生的機械摩擦可能導致瞼板腺縮短、脫落,開口部閉塞。MGD也可能是CL不耐受的原因之一,MGD治療可改善配戴舒適度。
日本MGD工作組於2010年提出的分泌減少型MGD診斷標準要求以下3項均為陽性4)。日本眼科學會指引GL 2023 CQ-1也記載該標準在日本國內廣泛使用3)。
| 項目 | 內容 |
|---|---|
| 1. 自覺症狀 | 眼部不適感、異物感、乾澀感、壓迫感等 |
| 2. 開口部周圍異常所見 | 血管擴張、黏膜皮膚移行部位移、眼瞼緣不規則中1項以上為陽性 |
| 3. 開口部閉塞所見 | 同時滿足plugging/pouting/ridge等閉塞所見和島崎分級2級以上的壓出降低 |
日眼會誌GL 2023推薦的檢查如下3)。
活體共軛焦顯微鏡(CQ-11)、淚液蒸發量測量(CQ-10)、淚液中發炎性生物標記(CQ-15)、細菌學檢查(CQ-16)以及meibum的生化學分析(CQ-14),目前均尚未被推薦為常規檢查3)。淚液中IL-1α、IL-1β和MMP-9的升高在病理機轉上很重要,但因檢查設備與條件尚未標準化,尚未達到臨床應用階段1)。
在日本的外來診療中,建議將非接觸式瞼板腺攝影整合至裂隙燈顯微鏡的工作流程中5)。
一系列檢查通常在3至5分鐘內完成,患者負擔較小。瞼板腺攝影可為患者提供視覺回饋,有助於提升治療動機5)。
2023年日本眼科學會指引中,13個CQ(CQ-18~CQ-30)以實證醫學評估了MGD的治療方法3)。不存在單一的金標準治療,階段性及合併治療是基本原則1)。日本乾眼診療指引2019也將MGD列為蒸發亢進型乾眼的主因,並提出以溫敷和眼瞼衛生作為第一線選擇的治療演算法9)。TFOS DEWS III管理與治療報告(2025)提出MGD的標準方法為結合溫敷、診間設備治療、IPL、低階光療法(LLLT)、眼瞼清潔、抗蠕形蟎治療和眼瞼去屑的分階段管理8)。
保守治療(第一線選擇)
熱敷療法:日本眼科學會指南 2023 CQ-18「強烈建議實施」。將眼瞼溫度提高到meibum熔點以上以促進分泌。建議使用市售熱敷眼罩,每日2次,每次持續5分鐘以上。
眼瞼清潔:CQ-19中弱推薦。用水浸濕的棉球或市售清潔劑擦拭眼瞼邊緣。原則上應每日持續進行。
Meibum擠壓:CQ-20中弱推薦。使用有田式瞼板腺擠壓鑷,以10天至1個月的間隔作為門診處置實施。閉塞性MGD是良好的適應症。
人工淚液:用於補充淚液和保持眼表濕潤。
藥物治療(注意保險適用範圍)
阿奇黴素水合物滴眼液:CQ-22中弱推薦,但在日本不屬於保險適用範圍。可改善自覺症狀、眼瞼邊緣所見和meibum grade。
四環黴素類口服藥物:CQ-27中弱推薦,不屬於保險適用範圍。用法為多西環素100mg每日2次,3~4個月逐漸減量。
皮質類固醇滴眼液:CQ-24中弱推薦。在日本僅合併眼瞼炎時屬於保險適用範圍。0.1%氟米龍等短期併用。
奧米加-3脂肪酸口服:CQ-26中弱推薦。在日本屬於補充劑,不屬於保險適用範圍。
| 治療 | CQ | 推薦強度 | 日本保險給付 |
|---|---|---|---|
| 熱敷療法 | CQ-18 | 強烈推薦 | 適用 |
| 眼瞼清潔 | CQ-19 | 弱推薦 | 適用 |
| 瞼板脂擠出 | CQ-20 | 弱推薦 | 眼部處置 |
| 地夸磷索點眼液 | CQ-21 | 不推薦(弱) | 不適用 |
| 阿奇黴素眼藥水 | CQ-22 | 弱推薦 | 仿單標示外使用 |
| 類固醇眼藥水 | CQ-24 | 弱推薦 | 僅在合併眼瞼炎時 |
| 環孢素A眼藥水 | CQ-25 | 不執行(弱) | 不適用 |
| 口服Omega-3 | CQ-26 | 弱推薦 | 補充劑 |
| 口服抗生素 | CQ-27 | 弱推薦 | 不適用 |
| IPL | CQ-28 | 弱推薦 | 未核准 |
| 熱脈動治療 | CQ-29 | 弱推薦 | 適應症外使用 |
| 探通術 | CQ-30 | 不實施(弱) | 不適用 |
強脈衝光(IPL)療法(日本眼科學會指南 2023 CQ-28):將500~1200nm的寬頻高亮度非雷射光照射於眼瞼周圍1), 8)。皮膚表面血管內含氧血紅素吸收光能量產生熱能,誘導異常血管熱凝固、細菌減少、蠕形蟎清除、meibum液化、上皮更新抑制、纖維母細胞活化及膠原蛋白合成促進1)。一項88眼的RCT報告,連續3次治療(間隔4週)可顯著降低淚液中IL-17α和IL-6水平1)。多項RCT顯示主觀症狀、瞼板腺開口狀態、meibum grade、BUT及角膜上皮損傷均有改善。儘管證據強烈支持其使用,但本文撰寫時在日本尚未核准且無保險給付,因此日本眼科學會指南 2023僅給予弱推薦3)。不良事件包括眼瞼發紅和腫脹,最高達13%,均為輕度且可逆1)。
熱脈動治療(LipiFlow等)(CQ-29):LipiFlow®(TearScience公司)是一種向量熱脈動(VTP)設備,可從眼瞼結膜側進行42.5°C加熱,同時從外眼瞼側施加由遠端至近端的脈動式壓迫,持續12分鐘1)。它是唯一能直接加熱瞼板內側面的設備,可將上眼瞼溫度從36.9°C升至41.1°C,下眼瞼溫度從37.0°C升至42.0°C1)。單次治療可在1個月後顯著改善瞼板脂分泌評分、OSDI、SPEED及TBUT,並有持續3年的長期療效報告1)。一項400隻眼的RCT顯示,單次LipiFlow治療顯著優於每日2次每次10分鐘熱敷加眼瞼清潔,12個月時86%的患者無需額外治療1)。其療效已被證實優於或等同於口服去氧羥四環素3個月1)。新型半透明啟動器(Activator Clear)易於確認佩戴位置,治療完成率達100%2)。在日本不納入健保。類似設備MiBo Thermoflo®透過42.2°C外部加熱板加溫,但眼瞼升溫效果較小1)。
Intraductal probing(CQ-30):將Maskin探針(1mm→4/6mm,逐步推進)插入阻塞的導管,以物理方式使其再通1)。在一項25例的佇列研究中,96%的患者症狀立即改善,但在49例的隨機對照試驗中,客觀徵象的改善有限1)。由於該操作具侵入性且客觀徵象改善不明顯,日本眼科學會指引2023年提出「弱建議不實施」該操作3)。
在門診進行的主要處置如下。
四環素類:多西環素和米諾環素比四環素脂溶性更高,低劑量即可在眼組織和眼瞼中蓄積1)。主要用於抗炎而非抗菌作用,通過抑制MMP-8、MMP-9、TNF-α、抑制脂肪酶產生和游離脂肪酸產生來控制炎症1)。一項60例RCT報告,與對照組相比,米諾環素聯合組在所有臨床指標以及IL-6、IL-1β、IL-17α、TNF-α、IL-12p70方面均有顯著改善1), 13)。副作用包括光敏反應和消化道症狀,孕婦及兒童禁用14)。
阿奇黴素:大環內酯類抗生素,與50S核糖體23S rRNA結合,抑制細菌蛋白質合成。除抗菌作用外,還能抑制NF-κB、IL-6、IL-8、TNF-α、MMP-9的表現,並誘導抗炎性TGF-β11)。1%滴眼液製劑(AzaSite®,美國)可用於局部給藥,據報導短期用藥後治療效果可持續3個月。口服阿奇黴素的方案包括500mg每日一次×3天,重複3個週期(間隔7天),或每週1次1g×3週。但存在QT間期延長的風險,有心臟病史者需謹慎使用1)。
環孢素A 0.05%點眼液:在美國作為Restasis®核准用於淚液分泌減少型乾眼。藉由抑制T細胞IL-2產生發揮抗發炎作用1)。對單獨MGD的療效有限,日本眼科學會指引2023年弱建議不施行3)。
Lifitegrast 5.0%點眼液:LFA-1拮抗劑,美國FDA核准之乾眼藥物。對MGD的專門證據尚未確立1)。
口服omega-3脂肪酸:補充EPA/DHA可改變meibum的脂肪酸組成1)。DREAM試驗(n=499)於2018年報告,omega-3組與對照組在OSDI、Schirmer試驗、淚膜破裂時間均無顯著差異,證據相互矛盾1)。日本眼科學會指引2023年考量omega-3脂肪酸在日本屬於保健食品,故弱建議使用3)。
蠕形蟎感染隨年齡增長而增加,70歲以上族群感染率達100%1)。Demodex folliculorum 寄生於睫毛根部,Demodex brevis 寄生於瞼板腺和皮脂腺,前者引起反應性角化過度並形成圓柱狀鱗屑(cylindrical dandruff),後者引起腺體阻塞和肉芽腫反應1)。
茶樹油(TTO:源自 Melaleuca alternifolia)的驅蟲治療有效1)。具體而言,每週在診所使用50% TTO眼瞼擦洗一次、每天在家使用10% TTO持續一個月的方案,已被報告可減輕眼瞼緣炎症、降低淚液中IL-1β和IL-17水平、改善眼表刺激症狀1)。TTO的主要殺蟎活性成分為terpinen-4-ol,市售產品如Cliradex®等可供使用1)。也有報告指出,口服伊維菌素200μg/kg單次給藥(第0天和第7天)可改善難治性後部瞼緣炎的蠕形蟎數量、Schirmer試驗和BUT1)。
Zhang等報告了一例46歲男性MGD患者,其外部表現不明顯,睫毛拔取檢查未檢出Demodex,但在眼瞼邊緣消毒後從擠出的瞼板腺分泌物中直接檢出15條短毛囊蠕形螨(D. brevis),經TTO lid scrub治療後症狀緩解6)。這是證明直接顯微鏡檢查meibum對Demodex檢測有用的重要病例。
日本MGD工作小組2010年的診斷標準要求以下3項全部為陽性:(1)眼部不適等自覺症狀,(2)開口部周圍異常所見(血管擴張、MCJ移位、眼瞼邊緣不規則中至少1項),(3)開口部阻塞所見(plugging與島崎2級以上的壓出減少同時存在)。日本眼科學會GL 2023建議進行瞼板腺造影(meibography)與meibum觀察。
將乾淨的毛巾浸濕後用微波爐加熱,或使用市售的熱敷眼罩敷於雙眼5~10分鐘。保持眼瞼溫度在40°C左右至關重要,需注意熱毛巾因蒸發散熱溫度容易下降。日本眼科學會指引2023(CQ-18)建議每日2次、每次持續5分鐘以上。熱敷後輕柔按摩眼瞼可促進融化的瞼脂排出。
日本眼科學會指引2023(BQ-1)將分泌減少型MGD的主要病理生理總結為「導管上皮過度角化和腺泡萎縮」3)。明確指出腺泡萎縮不僅可能繼發於瞼板腺堵塞,也可能由老化等因素導致的腺細胞原發性損傷引起。
從導管堵塞到腺泡萎縮的進展
導管上皮過度角化和瞼脂黏稠度升高導致終末導管堵塞1)。堵塞導致腺泡內壓升高,進而發展為腺泡萎縮和消失。腺泡消失使脂質分泌減少,淚膜脂質層變薄。
瞼脂熔點升高
正常瞼脂的熔點約為19~32°C,在33~37°C的眼表溫度下保持流動狀態1)。在MGD中,神經醯胺等鞘脂的增加使瞼脂熔點升高,重症病例需加熱至40°C以上才能液化1)。這是熱敷和熱脈動治療的理論依據。
性激素的影響
雄激素在瞼板腺細胞中激活脂質合成基因並抑制角化相關基因1)。雄激素缺乏、受體功能障礙及抗雄激素藥物的使用與阻塞性MGD相關。而雌激素則促進脂質分解代謝,並刺激IL-6和TNF-α等發炎性細胞因子的產生1)。停經後荷爾蒙替代療法與乾眼症的關聯可部分歸因於下視丘-腦下垂體-腎上腺軸抑制導致的腎上腺雄激素生成減少1)。
細菌和炎症的作用
眼瞼緣的常駐菌(主要是葡萄球菌)產生的脂肪酶分解瞼板腺脂質,游離脂肪酸的增加引發炎症1)。在眼瞼炎患者中已確認脂肪酶活性增加和基質金屬蛋白酶(MMP)產生增加。MGD患者淚液中IL-1α、成熟型IL-1β、MMP-9、IL-6、IL-8、TNF-α濃度升高,並與眼表面上皮損傷的嚴重程度相關1)。IL-1促進上皮細胞增殖和角化過度,形成阻塞性MGD的惡性循環。
PPAR-γ(過氧化物酶體增殖物激活受體γ)屬於核受體超家族,作為轉錄因子參與脂質合成和瞼板腺細胞分化。它被認為在瞼板腺細胞的細胞分化和脂質合成中扮演重要角色,作為闡明MGD病理生理學的靶點而備受關注3)。
鞘脂與熔點
在MGD中,瞼脂中神經醯胺和鞘脂的比例增加,導致瞼脂脂質膜的穩定性下降1)。神經醯胺含量升高直接導致瞼脂熔點升高,形成只有在40℃以上加熱才能液化的狀態。鞘脂不僅改變瞼脂的物理化學性質,還調控細胞增殖、分化、凋亡和炎症等細胞過程,使MGD的病理機制更加複雜1)。
糖尿病與眼表變化
2型糖尿病是MGD的加重因素。Hao等人對302隻眼的橫斷面研究報告,與單純DED組相比,DED-DM組在上眼瞼緣不規則、瞼緣血管擴張、開口堵塞分級、瞼緣肥厚、上眼瞼麥氏腺缺失、睫狀充血、非侵入性淚膜破裂時間(NIBUT)方面顯著惡化,且血糖水平與NIBUT、瞼緣肥厚、瞼緣不規則呈顯著相關7)。慢性炎症和微血管損傷波及瞼緣和腺組織的病理機制已被提出。
LipiFlow Translucent Activator:LipiFlow的新型半透明活化器(Activator Clear)採用半透明材質,使得安裝位置確認更加容易,Hu等人的研究報告了100%的治療完成率2)。治療後3個月內,自覺症狀和瞼板脂評分均有改善。Blackie等人的長期觀察研究顯示,單次LipiFlow治療可在12個月內持續改善瞼板脂分泌和乾眼症狀,86%的患者無需額外治療15)。
鼻腔內神經刺激(intranasal neurostimulation):鼻腔內前篩骨神經的脈衝刺激透過鼻淚反射途徑誘導淚腺分泌。動物實驗中,每天刺激3分鐘、連續3週可增加淚液量、脂質與蛋白質濃度,並降低淚液滲透壓1)。針對人類的RCT報告顯示,Allergan TrueTear® 鼻腔內淚液神經刺激器(ITN)可誘導結膜杯狀細胞脫顆粒、淚河高度上升、下眼瞼中央瞼板腺溫度上升以及淚液油層厚度增加1)。一項非隨機開放標籤研究報告指出,每天使用4次以上、持續180天,Schirmer值、角結膜染色與主觀症狀均有改善1)。研究亦顯示鼻腔內刺激可引起瞼板腺形態(面積與周長)的即時變化,表明透過神經調節促進瞼脂分泌可能成為一種新的治療策略1)。
性激素療法:Schiffman等人的多中心隨機試驗在ARVO摘要階段報告,局部睪固酮滴眼液(0.03%)治療6個月後,與對照組相比顯著改善了瞼板腺分泌物的黏稠度1)。有研究顯示局部雄激素可增加淚液脂質層厚度和淚膜破裂時間,但目前在包括日本和美國在內的任何國家均無獲批准的滴眼液產品1)。5%睪固酮乳膏在絕經期女性中的應用(改善OSDI)、絕經後患者的經皮DHEA、以及女性激素替代療法的眼科應用雖有討論,但均缺乏充分證據,尚未引入日常臨床實踐1)。
IL-1受體拮抗劑(Anakinra):重組人類IL-1RA(Kineret™)是一種已獲批用於類風濕關節炎的生物製劑,在乾眼中的標籤外使用已顯示出有效性1)。由於MGD患者淚液中IL-1在發病機制中起核心作用,因此它是一個有前景的治療標靶,但針對MGD的臨床試驗結果尚未公布1)。
IPL誘導的腺體形態變化:一項35例佇列研究報告顯示,IPL可誘導腺泡最長直徑增加和單位密度增加,並減少腺體周圍的發炎細胞1)。這表明IPL可能具有超越單純症狀治療的組織修復效果。
瞼板腺基因表達譜:據報導,MGD患者瞼板腺中存在400多種基因表現變化。雄性激素應答基因、角化相關基因和脂質合成相關基因被認為是主要靶點,分子標靶治療的可能性正在探索中1)。
Mibo Thermoflo®、IRPL、低階雷射:外部加熱裝置、IRPL(寬譜光)、低功率雷射等新型設備的比較試驗正在進行中,但目前尚無設備被報告顯示出優於LipiFlow的療效1)。
2023年日本眼科學會指引也在多個臨床問題中指出證據的局限性,透過日本主導的隨機對照試驗累積證據被認為是未來的課題3)。特別是需要:建立日本可行的保守治療標準化方案(熱敷、眼瞼清潔、瞼板腺分泌物擠壓);擴大doxycycline、azithromycin等藥物健保給付範圍的國內試驗;以及IPL和LipiFlow獲得藥事核准所需的多中心試驗。
Sabeti S, Kheirkhah A, Yin J, Dana R. Management of meibomian gland dysfunction: a review. Surv Ophthalmol. 2020;65(2):205-217.
Hu JG, Dang VT, Chang DH, et al. Performance of a Translucent Activator for LipiFlow Vectored Thermal Pulse (VTP) Treatment of Meibomian Gland Dysfunction. Clin Ophthalmol. 2022;16:963-971.
マイボーム腺機能不全診療ガイドライン作成委員会. マイボーム腺機能不全診療ガイドライン. 日眼会誌. 2023;127(2):109-228.
天野史郎ほか(マイボーム腺機能不全ワーキンググループ). マイボーム腺機能不全の定義と診断基準. あたらしい眼科. 2010;27(5):627-631. Available at: https://dryeye.ne.jp/wp/wp-content/themes/dryeye/file/mgd_teigi.pdf
Arita R, Itoh K, Inoue K, Amano S. Noncontact infrared meibography to document age-related changes of the meibomian glands in a normal population. Ophthalmology. 2008;115(5):911-915.
Zhang N, Liang L. Demodex in Meibum. Ophthalmology. 2024.
Hao Y, Wu B, Feng J, et al. Relationship between type 2 diabetes mellitus and changes of the lid margin, meibomian gland and tear film in dry eye patients: a cross-sectional study. 2024.
Jones L, Craig JP, Markoulli M, et al. TFOS DEWS III: Management and Therapy. Am J Ophthalmol. 2025.
ドライアイ研究会. ドライアイ診療ガイドライン. 日眼会誌. 2019;123(5):489-592. Available at: https://journal.nichigan.or.jp/PastContent?mag=0&number=5&vol=123&year=2019
Nelson JD, Shimazaki J, Benitez-del-Castillo JM, et al. The International Workshop on Meibomian Gland Dysfunction: Report of the Definition and Classification Subcommittee. Invest Ophthalmol Vis Sci. 2011;52(4):1930-1937.
Arita R, Minoura I, Morishige N, et al. Development of Definitive and Reliable Grading Scales for Meibomian Gland Dysfunction. Am J Ophthalmol. 2016;169:125-137.
Shimazaki J, Sakata M, Tsubota K. Ocular surface changes and discomfort in patients with meibomian gland dysfunction. Arch Ophthalmol. 1995;113(10):1266-1270.
Lee H, Min K, Kim EK, Kim TI. Minocycline controls clinical outcomes and inflammatory cytokines in moderate and severe meibomian gland dysfunction. Am J Ophthalmol. 2012;154(6):949-957.
Wladis EJ, Bradley EA, Bilyk JR, Yen MT, Mawn LA. Oral antibiotics for meibomian gland-related ocular surface disease: a Report by the American Academy of Ophthalmology. Ophthalmology. 2016;123(3):492-496. PMID: 26707417.
Blackie CA, Coleman CA, Holland EJ. The sustained effect (12 months) of a single-dose vectored thermal pulsation procedure for meibomian gland dysfunction and evaporative dry eye. Clin Ophthalmol. 2016;10:1385-1396. doi:10.2147/OPTH.S109663.
Arita R, Itoh K, Inoue K, Kuchiba A, Yamaguchi T, Amano S. Contact lens wear is associated with decrease of meibomian glands. Ophthalmology. 2009;116(3):379-384. doi:10.1016/j.ophtha.2008.10.012. PMID: 19167077.