ภาวะต่อมไมโบเมียน ทำงานผิดปกติ (MGD ) เป็นสาเหตุที่พบบ่อยที่สุดของโรคตาแห้ง ชนิดระเหยเพิ่มขึ้น
การสำรวจทางระบาดวิทยาในประเทศรายงานว่าชาวญี่ปุ่นอายุ 50 ปีขึ้นไปประมาณ 10–30% เป็น MGD
สาเหตุหลักคือการอุดตันของท่อส่วนปลายจากการมีเคราตินมากเกินไปและการเปลี่ยนแปลงทั้งเชิงคุณภาพและปริมาณของไมบัม
การวินิจฉัยในญี่ปุ่นใช้ 3 เกณฑ์ ได้แก่ อาการทางความรู้สึก ความผิดปกติรอบรูเปิดต่อม และการอุดตันของรูเปิดต่อม
ในปี 2023 สมาคมจักษุแพทย์แห่งญี่ปุ่นและองค์กรอื่นๆ ได้เผยแพร่ ‘แนวทางปฏิบัติทางคลินิกสำหรับภาวะต่อมไมโบเมียน ทำงานผิดปกติ’
การรักษาอันดับแรกคือการประคบอุ่นและการทำความสะอาดเปลือกตา ร่วมกับการบีบไมบัมเป็นหัตถการผู้ป่วยนอก
การรักษาด้วยอุปกรณ์เช่น IPL และ LipiFlow ยังคงอยู่ในขั้นตอนที่ยังไม่ได้รับการอนุมัติหรือไม่ครอบคลุมโดยประกันในญี่ปุ่น
ภาวะต่อมไมโบเมียน ทำงานผิดปกติ (MGD : Meibomian Gland Dysfunction) คือความผิดปกติเรื้อรังแบบกระจายของต่อมไมโบเมียน คณะทำงาน MGD ของญี่ปุ่น (2010) ได้ให้คำจำกัดความว่าเป็น ‘ภาวะที่การทำงานของต่อมไมโบเมียน มีความผิดปกติแบบกระจายจากสาเหตุต่างๆ ร่วมกับมีความรู้สึกไม่สบายตาเรื้อรัง’4) ‘แนวทางปฏิบัติทางคลินิกสำหรับภาวะต่อมไมโบเมียน ทำงานผิดปกติ’ (Nihon Ganka Gakkai Zasshi เล่มที่ 127 ฉบับที่ 2) ซึ่งเผยแพร่ในปี 2023 ได้ระบุให้ MGD เป็นสาเหตุหลักของโรคตาแห้ง ชนิดระเหยเพิ่มขึ้น โดยให้แนวทางปฏิบัติที่ครอบคลุมและอิงหลักฐานเชิงประจักษ์3)
ในระดับสากล คณะทำงานระหว่างประเทศว่าด้วยความผิดปกติของต่อมไมโบเมียน (IWMGD 2011) ได้ให้คำจำกัดความว่าเป็น “ความผิดปกติเรื้อรังแบบกระจายที่มีลักษณะเฉพาะคือการอุดตันของท่อนำส่งส่วนปลาย และ/หรือการเปลี่ยนแปลงเชิงคุณภาพและปริมาณของสารคัดหลั่งของต่อม”1), 10) TFOS DEWS III (2025) ยังระบุว่า MGD เป็นปัจจัยหลักที่ทำให้เกิดโรคตาแห้ง และได้รวมการรักษาด้วยอุปกรณ์ เช่น การประคบอุ่น การทำความสะอาดเปลือกตา IPL และเลเซอร์ระดับต่ำไว้ในอัลกอริทึมการจัดการ8) สมาคมวิจัยโรคตาแห้ง แห่งประเทศญี่ปุ่นได้จัดทำ “แนวทางปฏิบัติทางคลินิกสำหรับโรคตาแห้ง ” (2019) ซึ่งให้ความสำคัญกับ MGD ในฐานะสาเหตุของโรคตาแห้ง ชนิดระเหยเพิ่มขึ้น9) .
ต่อมไมโบเมียน เป็นต่อมไขมันขนาดใหญ่ที่อยู่ในแผ่นทาร์ซัส (tarsal plate) ของเปลือกตา เมื่อตรวจด้วยการตรวจไมโบกราฟีแบบไม่สัมผัส ตาปกติจะมีต่อมไมโบเมียน 25–30 ต่อมที่เปลือกตาบน และ 15–20 ต่อมที่เปลือกตาล่าง5) แต่ละต่อมประกอบด้วยถุงต่อม (acinus) จำนวนมากที่แตกแขนงจากท่อกลาง และเซลล์เยื่อบุถุงต่อม (meibocyte) จะผลิตไมบัม (meibum) โดยวิธีโฮโลไครน์ (holocrine secretion) ไมบัมประกอบด้วยไขมันมากกว่า 100 ชนิด (ส่วนใหญ่เป็น wax ester, cholesterol ester, phospholipid ที่มีขั้ว, sphingolipid) และโปรตีนมากกว่า 90 ชนิด ซึ่งก่อตัวเป็นชั้นไขมันชั้นนอกสุดของฟิล์มน้ำตา ป้องกันการระเหยของชั้นน้ำ ลดแรงตึงผิว และช่วยให้ฟิล์มน้ำตากระจายตัวได้ดี1) ความหนาของชั้นไขมันน้ำตา (LLT) ปกติอยู่ที่ 60–100 นาโนเมตร และจะบางลงใน MGD 1) .
การศึกษาเชิงประชากรในประเทศญี่ปุ่น (อาสาสมัครอายุ 6–96 ปี) ที่อ้างอิงในแนวทางปฏิบัติของวารสารจักษุวิทยาญี่ปุ่น 2023 BQ-4 รายงานความชุกของ MGD จำแนกตามช่วงอายุ ดังนี้3)
ช่วงอายุ ความชุกของ MGD ≤ 19 ปี 0% 20–29 ปี 11.8% 30–39 ปี 5.6% 40–49 ปี 21.6% 50–59 ปี 32.8% อายุ 60 ปี 41.9% อายุ 70 ปี 48.4% อายุ 80 ปี 63.9%
การศึกษาหลายชิ้นพบว่า MGD เพิ่มขึ้นและรุนแรงขึ้นตามอายุ ในแง่ของเพศ พบในผู้ชายและผู้หญิงวัยหมดประจำเดือนมากกว่า3) การศึกษาโดย Arita และคณะโดยใช้เครื่องถ่ายภาพต่อมไมโบมแบบไม่สัมผัสรายงานว่าผู้ป่วยตาแห้ง ประมาณ 86% มี MGD ร่วมด้วย5) ความแตกต่างทางเชื้อชาติก็ถูกชี้ให้เห็น โดยประชากรเอเชียมีความชุกสูงกว่าประชากรคอเคเซียน (3.5–19.9%)1) ในญี่ปุ่น สมาคมวิจัยตาแห้ง ประมาณการว่ามีผู้ป่วยรวมถึงผู้ที่อาจยังไม่ได้รับการวินิจฉัยอีกหลายสิบล้านคน ทำให้ MGD เป็นหนึ่งในโรคเรื้อรังที่พบบ่อยที่สุดในการดูแลผู้ป่วยประจำวัน3) .
การจำแนกประเภท MGD โดยคณะทำงาน MGD ของญี่ปุ่นมีดังนี้4)
ชนิดการหลั่งลดลง (low-delivery type)
ชนิดการหลั่งเพิ่มขึ้น (high-delivery type)
ปฐมภูมิ
ทุติยภูมิ: การติดเชื้อที่ตา, ผิวหนังอักเสบชนิดซีบอร์เฮอิก ฯลฯ
ทางคลินิก ชนิดการหลั่งลดลงพบได้บ่อย โดยเฉพาะ MGD ชนิดอุดตัน (oMGD : obstructive MGD ) พบได้บ่อยที่สุด JOS Guideline 2023 BQ-1 สรุปพยาธิสภาพหลักของ MGD ชนิดหลั่งลดลงว่าเป็น “การเกิดเคอราติไนเซชันมากเกินไปของเยื่อบุท่อนำไข่และการฝ่อของต่อมอะซินาร์”3) MGD ชนิดฝ่อคือภาวะที่ต่อมอะซินาร์ฝ่อแบบกระจาย และมีการเสนอทั้งกลไกการอุดตันทุติยภูมิและความเสียหายของเซลล์ต่อมปฐมภูมิ
MGD ชนิดหลั่งมาก (hypersecretory MGD ) รวมถึงต่อมไมโบเมียน อักเสบชนิดซีบอร์รีอิก (seborrheic MGD : sMGD ) และได้รับการยอมรับว่าแตกต่างจากต่อมไมโบเมียน อักเสบชนิดอุดกั้น เมื่อกดเบาๆ ที่แผ่นทาร์ซัสของเปลือกตาบน ในคนปกติจะมีไมบัม (meibum) ใสๆ ออกมา แต่ใน MGD ชนิดซีบอร์รีอิก การหลั่งจะเพิ่มขึ้นอย่างผิดปกติ โดยพบฟองอากาศในน้ำตาตามขอบเปลือกตาล่าง โรคที่เกี่ยวข้องได้แก่ เปลือกตาอักเสบ ส่วนหลัง (posterior blepharitis), ต่อมไมโบเมียน อักเสบ (meibomianitis), และโรคกระจกตา และเยื่อบุตาอักเสบ ที่เกี่ยวข้องกับต่อมไมโบเมียน อักเสบ (meibomitis-related keratoconjunctivitis: MRKC) โดย แนวทางของสมาคมจักษุวิทยาญี่ปุ่น 2023 BQ-3 ได้เน้นย้ำถึงความสำคัญของการรวมแนวคิดเหล่านี้เข้าด้วยกัน3)
ในระดับสากล IWMGD 2011 ได้จัดประเภทตามกรอบของชนิดหลั่งน้อย (low-delivery) และชนิดหลั่งมาก (high-delivery) โดยชนิดอุดกั้นเป็นชนิดที่พบบ่อยที่สุดในกลุ่มหลั่งน้อย1)
Q
MGD และโรคตาแห้งมีความสัมพันธ์กันอย่างไร?
A
MGD เป็นสาเหตุที่พบบ่อยที่สุดของโรคตาแห้ง ชนิดระเหยเพิ่มขึ้น (evaporative dry eye) เมื่อชั้นไขมันของน้ำตาบางลงเนื่องจากการทำงานของต่อมไมโบเมียน ลดลง จะทำให้น้ำตาระเหยเพิ่มขึ้น ค่าออสโมลาริตีของน้ำตาสูงขึ้น และเกิดการอักเสบบนผิวดวงตา แนวทางของสมาคมจักษุวิทยาญี่ปุ่น 2023 ยังระบุชัดเจนว่า MGD ทำให้เกิดโรคตาแห้ง และอาการไม่สบายตาอย่างเรื้อรัง
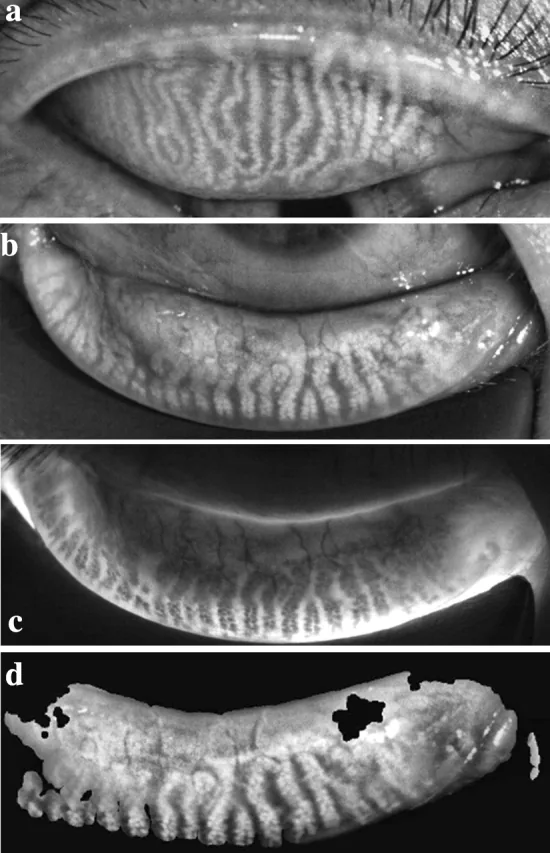
ภาพไมโบกราฟี (meibography) ของต่อมไมโบเมียนทำงานผิดปกติ พบความคดเคี้ยว การเปลี่ยนรูป และการสูญเสียของต่อมไมโบเมียนในเปลือกตาบนและล่าง Li B, et al. Comparison of the therapeutic effect of Meibomian Thermal Pulsation LipiFlow® on obstructive and hyposecretory meibomian gland dysfunction patients. Int Ophthalmol. 2020. Figure 1. PM
CI D: PMC7669766. License: CC BY.
ภาพไมโบกราฟีของเปลือกตาบนและล่างแสดงให้เห็นความคดเคี้ยว การจัดเรียงตัวผิดปกติ และการสูญเสียต่อมบางส่วนของ
ต่อมไมโบเมียน ซึ่งเป็นความผิดปกติของรูปร่างที่มีลักษณะเฉพาะของ
MGD และเหมาะสมสำหรับอธิบายอาการแสดงทางคลินิกหลัก
แนวทางของสมาคมจักษุวิทยาญี่ปุ่น 2023 CQ-2 ระบุอาการที่ผู้ป่วยรับรู้ได้ของ MGD ดังต่อไปนี้ และแนะนำอย่างยิ่งให้สอบถามอาการเหล่านี้3)
อาการไม่สบายตาและความรู้สึกมีสิ่งแปลกปลอมในตา : อาการพบบ่อยที่สุดความรู้สึกแห้งและกดดัน : มักรุนแรงขึ้นในตอนเช้าปวดและแสบร้อน : อาจมีอาการแสบร้อนตามขอบเปลือกตาน้ำตาไหลและล้าตา : เนื่องจากการหลั่งน้ำตาแบบรีเฟล็กซ์ที่เพิ่มขึ้นตาพร่า มัว / ความผันผวนของการมองเห็น อาการคัน / ขี้ตา / กลัวแสง : อาการร่วมที่เกิดจากการอักเสบ
ความรู้สึกเหนียวหนืด (“เหนียวหนืด”) ก็เป็นลักษณะเฉพาะเช่นกัน4) อาการมักรุนแรงในตอนเช้า และบางครั้งผู้ป่วยอาจบ่นว่าการมองเห็น มีความผันผวน อย่างไรก็ตาม ปัจจุบันยังไม่มีการระบุอาการทางความรู้สึกที่จำเพาะเจาะจงในการแยก MGD ออกจากโรคผิวตาอื่นๆ3) แบบสอบถาม OSDI (Ocular Surface Disease Index) ถูกนำมาใช้กันอย่างแพร่หลายในการประเมินอาการทางความรู้สึก อาการของ MGD ส่งผลกระทบอย่างมากต่อคุณภาพชีวิต ไม่เพียงแต่ก่อให้เกิดการระคายเคืองตาแต่ยังทำให้การมองเห็น ลดลง ดังนั้นจึงเป็นสิ่งสำคัญที่จะประเมินระดับความบกพร่องในการใช้ชีวิตอย่างเป็นระบบ1)
แนวทางเวชปฏิบัติ JOS GL 2023 CQ-3 แนะนำว่าสัญญาณ 4 ประการ ได้แก่ การอุดตันของช่องเปิดต่อมไมโบเมียน การขยายตัวของหลอดเลือดที่ขอบเปลือกตา การเคลื่อนตัวของรอยต่อเยื่อเมือกกับผิวหนัง และความไม่เรียบของขอบเปลือกตา มีประโยชน์ในการวินิจฉัย MGD 3)
ลักษณะที่ขอบเปลือกตา
ลักษณะการอุดตันของช่องเปิด : plugging (สิ่งอุด), pouting (ตุ่มนูนแหลมรอบช่องเปิด), ridge (สันนูนครอบคลุมหลายช่องเปิด)
การขยายตัวของหลอดเลือดที่ขอบเปลือกตา : การขยายตัวของเส้นเลือดฝอย / telangiectasia รอบช่องเปิดต่อม
การเคลื่อนตัวของรอยต่อเยื่อเมือกกับผิวหนัง (MCJ) : การเบี่ยงเบนไปทางด้านหน้าหรือด้านหลัง สังเกตได้ง่ายด้วยการย้อมฟลูออเรสซีน
ความไม่เรียบของขอบเปลือกตา : ความไม่สม่ำเสมอของแนวที่สัมผัสกับกระจกตา
การประเมิน meibum และต่อมไมโบเมียน
ลักษณะของ meibum : ปกติเป็นน้ำมันใส ใน MGD จะมีลักษณะขุ่น เป็นเม็ด หรือคล้ายยาสีฟัน
การจำแนกของ Shimazaki : ประเมินการไหลของ meibum เมื่อกดด้วยนิ้วหัวแม่มือระดับปานกลางเป็น grade 0-3 โดย grade 2 ขึ้นไปถือว่าผิดปกติ
Meibography : สังเกตการสูญหาย (dropout) การสั้นลง และการโค้งงอของต่อมด้วยกล้องอินฟราเรด
การบางลงของชั้นไขมันในน้ำตา : สามารถประเมินความหนาของชั้นไขมัน (LLT) ได้ด้วย interferometer
Meibum grade ของ Shimazaki แบ่งการประเมินเป็น 4 ระดับดังนี้4), 12)
grade 0 : สามารถบีบ meibum ใสออกได้ง่ายเมื่อกดเบา ๆgrade 1 : บีบ meibum ขุ่นออกได้เมื่อกดเบา ๆgrade 2 : บีบ meibum ขุ่นออกได้เมื่อกดปานกลางถึงแรงgrade 3 : ไม่สามารถบีบ meibum ออกได้แม้กดแรง
Meibography แบบไม่สัมผัสที่พัฒนาโดย Arita และคณะในปี 2008 เป็นอุปกรณ์ที่มีการรุกรานต่ำ เพียงติดฟิลเตอร์อินฟราเรด (700–850 นาโนเมตร) และกล้อง CCD อินฟราเรดขนาดเล็กเข้ากับกล้องจุลทรรศน์ชีวภาพแบบกรีด5), 11) แสงอินฟราเรดทะลุแผ่นเยื่อตาและสะท้อนจาก meibum ทำให้ต่อมไมโบเมียน มองเห็นเป็นสีขาวสะท้อนแสงสูง ในผู้ป่วย MGD พบการสูญเสียต่อม (dropout) การหดสั้น การคดงอ การเป็นหย่อม ๆ และการขยายตัวของต่อมไมโบเมียน ปนกันไป5)
ระดับการสูญเสียต่อมแบ่งออกเป็น 4 ระดับตาม Arita Meiboscore ดังต่อไปนี้5) :
Meiboscore พื้นที่ต่อมสูญเสีย grade 0 ไม่สูญเสีย grade 1 ≤ 1/3 ของทั้งหมด grade 2 1/3–2/3 grade 3 ≥ 2/3
มีรายงานว่าผู้ใช้คอนแทคเลนส์มีการสูญเสียต่อมไมโบเมียน มากกว่าผู้ที่ไม่ใช้คอนแทคเลนส์ ยิ่งระยะเวลาการใช้นานขึ้น การเปลี่ยนแปลงจะยิ่งเด่นชัด และพบได้ทั้งในคอนแทคเลนส์ชนิดอ่อนและชนิดแข็ง16)
แนวทางของสมาคมจักษุวิทยาญี่ปุ่น 2023 BQ-5 และ BQ-6 ได้รวบรวมปัจจัยที่เกี่ยวข้องกับการเกิด MGD อย่างเป็นระบบ3)
อายุและปัจจัยฮอร์โมน
อายุ : ปัจจัยเสี่ยงที่สำคัญที่สุด ทำให้ต่อมฝ่อและการทำงานลดลงผู้ชายและผู้หญิงหลังหมดประจำเดือน : มีความชุกของโรคสูงการขาดแอนโดรเจน : แอนโดรเจนส่งเสริมการสังเคราะห์ไขมันของต่อมไมโบเมียน และยับยั้งการสร้างเคราติน การขาดแอนโดรเจน ความผิดปกติของตัวรับ และยายับยั้งแอนโดรเจนสัมพันธ์กับ MGD ชนิดอุดตัน1) เอสโตรเจน : ยับยั้งการหลั่งไขมันและมีฤทธิ์ส่งเสริมการอักเสบบนผิวตา1)
ปัจจัยทางตาและปัจจัยภายนอก
การใช้คอนแทคเลนส์ชนิดอ่อน : ส่งเสริมการอุดตันทางกลของช่องเปิดต่อมการทำงานกับอุปกรณ์แสดงผล (VDT) : การระเหยเพิ่มขึ้นเนื่องจากการกระพริบตาลดลงการสูบบุหรี่ การอาศัยในชนบท เชื้อชาติเอเชีย : ระบุเป็นปัจจัยเสี่ยงใน แนวทางของสมาคมจักษุวิทยาญี่ปุ่น 20233) การใช้ยาหยอดตารักษาโรคต้อหิน เป็นเวลานาน : พิษจากสารกันเสียและตัวยาเองประวัติการผ่าตัดตา : มีรายงานการกำเริบของ MGD หลังการผ่าตัดต้อกระจก และการผ่าตัดแก้ไขสายตายา : ไอโซเทรติโนอิน ยาแก้แพ้ ยาต้านเศร้า เป็นต้น
โรคทางระบบ
โรคเบาหวาน : ระบุเป็นปัจจัยเสี่ยงของ MGD ใน Jpn J Ophthalmol Soc GL 20233) การศึกษาภาคตัดขวางในตาแห้ง 302 ตาที่มีเบาหวานชนิดที่ 2 ร่วม พบว่ากลุ่ม DED -DM มีความรุนแรงมากกว่ากลุ่ม DED เพียงอย่างเดียวอย่างมีนัยสำคัญใน grade การอุดตันของช่องเปิดต่อม (P<0.0001) การขยายหลอดเลือดที่ขอบเปลือกตา (P<0.0001) การสูญเสียต่อมไมโบเมียน ที่เปลือกตาบน (P=0.003) และ BUT แบบไม่รุกล้ำ (P=0.011)7) ความผิดปกติของเมแทบอลิซึมของไขมัน・ความดันโลหิตสูง・ภาวะต่อมไทรอยด์ทำงานเกิน : ระบุใน Jpn J Ophthalmol Soc GL 2023 BQ-63) โรครอบปาก (Rosacea)・กลุ่มอาการโจเกรน・กลุ่มอาการสตีเวนส์-จอห์นสัน ・โรคกราฟต์เวอร์ซัสโฮสต์ : เกี่ยวข้องกับ MGD ผ่านทางการอักเสบของตา3)
การติดเชื้อ Demodex
Demodex folliculorum อาศัยอยู่ที่โคนขนตา ส่วน Demodex brevis อาศัยอยู่ในต่อมไมโบเมียน และต่อมไขมัน1) อัตราการอาศัยเพิ่มขึ้นตามอายุ โดยสูงถึง 100% ในผู้ที่มีอายุ 70 ปีขึ้นไป1) การศึกษาตามกลุ่มประชากร 150 รายพบ Demodex ในผู้ป่วยเยื่อบุตาอักเสบ ส่วนหน้าถึง 90% และในผู้ป่วย MGD ถึง 60%1) D. folliculorum ทำลายเซลล์ฐานของรากขนตาโดยตรง ทำให้เกิดการสร้างเคราตินมากเกินไปและการเกิดขุยรูปทรงกระบอก D. brevis อุดตันต่อมไมโบเมียน ทางกายภาพและกระตุ้นปฏิกิริยาแกรนูโลมา ส่งเสริมการเกิดกุ้งยิง ใน1) Demodex ยังก่อให้เกิดการอักเสบโดยเป็นพาหะนำแบคทีเรีย และอาจทำให้เกิดปฏิกิริยาภูมิไวเกินแบบ delayed-type ในผู้ป่วยโรครอบปาก1) Zhang และคณะรายงานผู้ป่วย MGD ชายอายุ 46 ปีที่พบ Demodex brevis จำนวน 15 ตัวใน meibum ที่บีบออกมาแม้ไม่มีอาการภายนอกชัดเจน แสดงให้เห็นประโยชน์ของการตรวจ meibum โดยตรง6)
ในชีวิตประจำวัน การดูแลตนเองด้วยการอบอุ่นเปลือกตา (การประคบอุ่น) มีประสิทธิภาพ ใช้มาส์กตาอุ่นที่มีจำหน่ายทั่วไป ครั้งละ 5 นาทีขึ้นไป วันละ 2 ครั้ง หลังจากนั้นนวดเปลือกตาเบาๆ การเช็ดเปลือกตาด้วยสำลีชุบน้ำหรือน้ำยาทำความสะอาดก็มีประสิทธิภาพเช่นกัน ขณะทำงานกับ VDT ควรกระพริบตาอย่างมีสติ และผู้ใช้คอนแทคเลนส์ชนิดอ่อนควรทบทวนระยะเวลาในการใส่
Q
คอนแทคเลนส์สัมพันธ์กับ MGD หรือไม่?
A
ตามจักษุวิทยาสารญี่ปุ่น GL 2023 ระบุว่าการใส่คอนแทคเลนส์ชนิดอ่อนเป็นปัจจัยเสี่ยงของ MGD การเสียดสีเชิงกลขณะกระพริบตาระหว่างใส่เลนส์อาจทำให้ต่อมไมโบเมียน สั้นลงและหายไป และช่องเปิดอุดตันได้ MGD อาจเป็นสาเหตุหนึ่งของการไม่ทนต่อ CL และการรักษา MGD อาจช่วยให้การใส่เลนส์สบายขึ้น
เกณฑ์การวินิจฉัย MGD ชนิดหลั่งลดลงที่คณะทำงาน MGD ญี่ปุ่นเสนอในปี 2010 กำหนดให้ทั้ง 3 ข้อต่อไปนี้เป็นบวกทั้งหมด4) จักษุวิทยาสารญี่ปุ่น GL 2023 CQ-1 ก็ระบุว่าเกณฑ์นี้ใช้กันอย่างแพร่หลายในประเทศ3)
ข้อ เนื้อหา 1. อาการทางความรู้สึก มีความรู้สึกไม่สบายตา ความรู้สึกมีสิ่งแปลกปลอม ตาแห้ง ความรู้สึกกดทับ เป็นต้น 2. ความผิดปกติบริเวณรอบช่องเปิด การขยายตัวของหลอดเลือด การเคลื่อนของรอยต่อเยื่อเมือก-ผิวหนัง ขอบเปลือกตาไม่เรียบ: 1 ข้อขึ้นไปเป็นบวก 3. อาการอุดตันของช่องเปิด อาการอุดตันเช่น plugging/pouting/ridge และการหลั่งลดลงระดับ Shimazaki 2 ขึ้นไป
การตรวจที่จักษุวิทยาสารญี่ปุ่น GL 2023 แนะนำมีดังนี้3)
การสังเกต meibum ด้วยกล้องจุลทรรศน์ชนิดกรีด (CQ-6, แนะนำ): ประเมินคุณภาพและปริมาณของ meibum แบบกึ่งปริมาณการสังเกตทางกายวิภาคของขอบเปลือกตา (CQ-3, มีประโยชน์): ยืนยัน 4 สิ่งที่พบดังกล่าวไมโบกราฟี (CQ-8, แนะนำ): ชนิดไม่สัมผัสเป็นมาตรฐานสากล ใช้เวลาสั้น บาดเจ็บน้อย5) วัดปริมาณด้วย Meiboscoreเวลาการแตกตัวของชั้นน้ำตา (BUT ) (CQ-4): ลดลงใน MGD แต่ไม่ใช่การตรวจที่จำเพาะการย้อมฟลูออเรสซีน กระจกตา และเยื่อบุตา การวัดความหนาชั้นน้ำมันของน้ำตา (LLT) (CQ-9): Interferometer แสดงให้เห็นว่า LLT ในผู้ป่วย MGD บางกว่า แต่ยังไม่มีการกำหนดค่าตัดแบ่งการวัดความดันออสโมซิสของน้ำตา (CQ-12): ในปัจจุบันประโยชน์ทางคลินิกยังจำกัด
กล้องจุลทรรศน์คอนโฟคัลชนิดชีวภาพ (CQ-11), การวัดอัตราการระเหยของน้ำตา (CQ-10), เครื่องหมายการอักเสบในน้ำตา (CQ-15), การตรวจทางแบคทีเรียวิทยา (CQ-16), การวิเคราะห์ทางชีวเคมีของ meibum (CQ-14) ล้วนยังไม่ถึงระดับคำแนะนำให้เป็นการตรวจประจำในปัจจุบัน3) การเพิ่มขึ้นของ IL-1α, IL-1β และ MMP-9 ในน้ำตามีความสำคัญในเชิงกลไกพยาธิสภาพ แต่เนื่องจากอุปกรณ์และเงื่อนไขการตรวจยังไม่ได้มาตรฐานจึงยังไม่นำไปใช้ทางคลินิก1)
ในคลินิกผู้ป่วยนอกของญี่ปุ่น แนะนำให้นำการตรวจไมโบกราฟีชนิดไม่สัมผัสเข้ามาใช้ในขั้นตอนการทำงานของกล้องจุลทรรศน์ชนิดกรีด5)
ให้ผู้ป่วยวางหน้าบนที่วางคางของกล้องจุลทรรศน์ชนิดกรีด
สังเกตสภาพรอบรูเปิดของต่อมไมโบมและขอบเปลือกตาด้วยแสงกระจาย (plugging/pouting/ridge, หลอดเลือดขยาย, การเคลื่อนของ MCJ, ขอบเปลือกตาไม่เรียบ)
ทำการย้อมฟลูออเรสซีน วัดความเสียหายของเยื่อบุผิวกระจกตา และเยื่อบุตา (SPK ) และเวลาการแตกตัวของชั้นน้ำตา (BUT ) ด้วยฟิลเตอร์สีน้ำเงิน
เปลี่ยนเป็นฟิลเตอร์ผ่านอินฟราเรด สังเกตต่อมไมโบมบนและล่างด้วยไมโบกราฟี และบันทึกเป็นภาพนิ่งหรือวิดีโอ ประเมิน Meiboscore
กลับไปใช้แสงกระจาย กดตรงกลางเปลือกตาด้วยนิ้วหัวแม่มือหรือคีมกดเพื่อประเมินคุณภาพและการไหลของ meibum (การจำแนกของ Shimazaki)
การตรวจต่างๆ มักจะเสร็จภายใน 3–5 นาที และไม่เป็นภาระต่อผู้ป่วยมากนัก การตรวจไมโบกราฟีช่วยให้ผู้ป่วยเห็นภาพสะท้อนและเพิ่มแรงจูงใจในการรักษา5)
ภาวะตาแห้ง ชนิดน้ำตาเสื่อม (ADDE) : ร่วมกับการประเมินค่า Schirmer ที่ลดลงและกลุ่มอาการ Sjögren ตาม TFOS DEWS II พบว่าส่วนใหญ่เป็นชนิดระเหยเพิ่มขึ้นและชนิดผสมมะเร็งต่อมไขมัน มะเร็งต่อมไขมัน เป็นที่ทราบกันดีว่าสามารถแอบแฝงเป็นเปลือกตาอักเสบ ดื้อยาหรือ Chalazionเปลือกตาอักเสบ ส่วนหลัง – ไมโบเมียนอักเสบMGD ความสำคัญของการรวมแนวคิดให้เป็นหนึ่งเดียวยังถูกเน้นย้ำใน แนวทางของสมาคมจักษุวิทยาญี่ปุ่น 2023 BQ-33) โรคเยื่อบุผิวกระจกตา และเยื่อบุตา ที่เกี่ยวข้องกับไมโบเมียนอักเสบ (MRKC) : ชื่อโรคที่ใช้บ่อยในญี่ปุ่น หมายถึงความผิดปกติของเยื่อบุผิวกระจกตา และเยื่อบุตา ที่เกิดตามหลังไมโบเมียนอักเสบเยื่อบุตาอักเสบจากภูมิแพ้ – เปลือกตาอักเสบ ติดเชื้อMGD ขนตางอกผิดทาง – หนังตาหงิก : อาจเป็นสาเหตุของอาการสิ่งแปลกปลอม จึงต้องตัดออกด้วยการตรวจด้วยหลอดกรีดChalazion : ยังถือเป็นรูปแบบรอยโรคเฉพาะที่ของ MGD 3)
ใน GL 2023 ของวารสารจักษุวิทยาญี่ปุ่น CQ จำนวน 13 ข้อ (CQ-18~CQ-30) ได้ประเมินวิธีการรักษา MGD ตามหลักฐานเชิงประจักษ์3) ไม่มีการรักษาเดี่ยวใดที่เป็นมาตรฐานทองคำ แนวทางพื้นฐานคือการรักษาแบบเป็นขั้นตอนและร่วมกัน1) แนวทางปฏิบัติทางคลินิกโรคตาแห้ง ของญี่ปุ่นปี 2019 ยังระบุว่า MGD เป็นสาเหตุหลักของโรคตาแห้ง ชนิดระเหยน้ำมากเกินไป และแสดงอัลกอริทึมการรักษาโดยให้การประคบอุ่นและสุขอนามัยขอบตาเป็นตัวเลือกแรก9) รายงาน TFOS DEWS III ด้านการจัดการและการรักษา (2025) เสนอการจัดการแบบเป็นขั้นตอนที่ผสมผสานการประคบอุ่น การรักษาด้วยอุปกรณ์ในคลินิก IPL การบำบัดด้วยแสงระดับต่ำ (LLLT) การทำความสะอาดขอบตา การบำบัดต้าน Demodex และ blepharoexfoliation เป็นแนวทางมาตรฐานสำหรับ MGD 8)
การรักษาแบบประคับประคอง (ทางเลือกแรก)
การประคบอุ่น : CQ-18 ของ GL 2023 วารสารจักษุวิทยาญี่ปุ่นแนะนำอย่างยิ่งให้ปฏิบัติ การเพิ่มอุณหภูมิของเปลือกตาให้สูงกว่าจุดหลอมเหลวของ meibum เพื่อส่งเสริมการหลั่ง แนะนำให้ใช้หน้ากากอุ่นที่มีจำหน่ายทั่วไป วันละ 2 ครั้ง ครั้งละอย่างน้อย 5 นาที
การทำความสะอาดขอบตา : CQ-19 แนะนำอย่างอ่อน ทำความสะอาดขอบตาด้วยสำลีชุบน้ำหรือน้ำยาทำความสะอาดที่มีจำหน่ายทั่วไป หลักการคือต้องทำอย่างสม่ำเสมอทุกวัน
การบีบ meibum : CQ-20 แนะนำอย่างอ่อน ดำเนินการเป็นหัตถการผู้ป่วยนอกโดยใช้คีมบีบต่อม meibomian แบบ Arita ห่างกัน 10 วันถึง 1 เดือน MGD ชนิดอุดตันเป็นข้อบ่งชี้ที่ดี
น้ำตาเทียม : ใช้เพื่อทดแทนน้ำตาและให้ความชุ่มชื้นแก่ผิวตา
การรักษาด้วยยา (โปรดสังเกตเรื่องการครอบคลุมของประกัน)
ยาหยอดตา azithromycin hydrat : CQ-22 แนะนำอย่างอ่อน แต่ไม่ครอบคลุมโดยประกันในญี่ปุ่น ช่วยปรับปรุงอาการทาง subjective, อาการแสดงที่ขอบตา และระดับ meibum
Tetracycline ชนิดรับประทาน : CQ-27 แนะนำอย่างอ่อน ไม่ครอบคลุมโดยประกัน สูตรที่ใช้คือ doxycycline 100mg วันละ 2 ครั้ง ลดขนาดลง gradually ใน 3-4 เดือน
การหยอดตาคอร์ติโคสเตียรอยด์ : แนะนำอย่างอ่อนที่ CQ-24 ในประเทศญี่ปุ่นครอบคลุมประกันเฉพาะเมื่อมีเกล็ดกระดี่ร่วมด้วย ใช้ฟลูออโรเมโธโลน 0.1% และอื่นๆ ร่วมกันในระยะสั้น
การรับประทานกรดไขมันโอเมก้า-3 : แนะนำอย่างอ่อนที่ CQ-26 ในประเทศญี่ปุ่นถือเป็นผลิตภัณฑ์เสริมอาหารและไม่ครอบคลุมประกัน
วิธีการรักษา CQ ระดับความเข้มข้นของคำแนะนำ ประกันภัยในญี่ปุ่น การประคบอุ่น CQ-18 แนะนำอย่างยิ่ง ครอบคลุม การทำความสะอาดเปลือกตา CQ-19 แนะนำอย่างอ่อน ครอบคลุม การบีบเหมย์บัม CQ-20 แนะนำอย่างอ่อน หัตถการทางตา ยาหยอดตาไดควาโฟซอล CQ-21 ไม่แนะนำให้ทำ (อ่อน) นอกเหนือข้อบ่งใช้ ยาหยอดตาอะซิโทรมัยซิน CQ-22 แนะนำอย่างอ่อน นอกเหนือข้อบ่งใช้ ยาหยอดตาสเตียรอยด์ CQ-24 แนะนำอย่างอ่อน เฉพาะเมื่อมีเกล็ดกระดี่ร่วมด้วย ยาหยอดตาไซโคลสปอรีน เอ CQ-25 ไม่ดำเนินการ (ระดับอ่อน) ไม่มีข้อบ่งใช้ รับประทานโอเมก้า-3 CQ-26 แนะนำระดับอ่อน อาหารเสริม ยาปฏิชีวนะชนิดรับประทาน CQ-27 แนะนำระดับอ่อน ไม่มีข้อบ่งใช้ IPL CQ-28 แนะนำระดับอ่อน ไม่ได้รับการอนุมัติ Thermal pulsation CQ-29 แนะนำอย่างอ่อน ไม่ครอบคลุม การตรวจด้วยหัววัด CQ-30 ไม่ควรทำ (อ่อน) ไม่ครอบคลุม
การรักษาด้วย Intense pulsed light (IPL) (แนวทางของสมาคมจักษุวิทยาญี่ปุ่น 2023 CQ-28): ฉายแสงไม่ใช่เลเซอร์ความเข้มสูงแบบกว้างสเปกตรัม 500–1200nm รอบเปลือกตา1), 8) พลังงานแสงถูกดูดซับโดยออกซีฮีโมโกลบินในหลอดเลือดที่ผิวหนัง ทำให้เกิดความร้อน นำไปสู่การจี้แข็งตัวของหลอดเลือดผิดปกติ ลดแบคทีเรีย กำจัด Demodex ทำให้ meibum เหลว ยับยั้งการหมุนเวียนของเยื่อบุผิว กระตุ้นไฟโบรบลาสต์ และส่งเสริมการสังเคราะห์คอลลาเจน1) การศึกษา RCT ใน 88 ดวงตารายงานว่าการรักษาต่อเนื่อง 3 ครั้ง (ห่างกัน 4 สัปดาห์) ลด IL-17α และ IL-6 ในน้ำตาลงอย่างมีนัยสำคัญ1) การศึกษา RCT หลายชิ้นแสดงให้เห็นถึงการปรับปรุงของอาการ อาการแสดงที่รูเปิด meibum grade BUT และรอยโรคที่กระจกตา ตามหลักฐานแล้วแนะนำอย่างยิ่ง แต่ ในญี่ปุ่น ณ เวลาที่เขียนต้นฉบับ ยังไม่ได้รับการอนุมัติและไม่ครอบคลุมสิทธิประโยชน์ ดังนั้น แนวทางของสมาคมจักษุวิทยาญี่ปุ่น 2023 จึงแนะนำอย่างอ่อนเท่านั้น3) อาการไม่พึงประสงค์ ได้แก่ เปลือกตาแดง และบวมสูงสุด 13% ซึ่งทั้งหมดไม่รุนแรงและสามารถกลับคืนได้1)
การบำบัดด้วยการสั่นพ่นความร้อน (LipiFlow ฯลฯ) (CQ-29): LipiFlow® (TearScience) เป็นอุปกรณ์เวกเตอร์เทอร์มอลพัลเซชัน (VTP) ที่ให้ความร้อน 42.5°C จากด้านเยื่อบุตา และกดเป็นจังหวะจากด้านนอกเปลือกตาในทิศทางจากส่วนปลายไปยังส่วนต้นพร้อมกันเป็นเวลา 12 นาที1) เป็นอุปกรณ์เดียวที่สามารถให้ความร้อนโดยตรงกับผิวด้านในของเปลือกตา โดยเพิ่มอุณหภูมิเปลือกตาบนจาก 36.9°C เป็น 41.1°C และเปลือกตาล่างจาก 37.0°C เป็น 42.0°C1) การรักษาครั้งเดียวช่วยให้คะแนนการหลั่ง meibum, OSDI, SPEED และ TBUT ดีขึ้นอย่างมีนัยสำคัญหลังจาก 1 เดือน และมีรายงานผลลัพธ์ระยะยาวนานถึง 3 ปี1) การทดลองแบบสุ่มที่มีกลุ่มควบคุมใน 400 ตาพบว่า LipiFlow ครั้งเดียวมีประสิทธิภาพเหนือกว่าการประคบอุ่นครั้งละ 10 นาทีวันละ 2 ครั้งร่วมกับการเช็ดทำความสะอาดเปลือกตาอย่างมีนัยสำคัญ โดย 86% ไม่จำเป็นต้องรักษาเพิ่มเติมเมื่อติดตามผลที่ 12 เดือน1) ผลการศึกษายืนยันว่ามีประสิทธิภาพเทียบเท่าหรือดีกว่า doxycycline ชนิดรับประทานนาน 3 เดือน1) ด้วย Activator Clear รุ่นใหม่ที่โปร่งแสง ทำให้สามารถตรวจสอบตำแหน่งการวางได้ง่ายขึ้น และมีรายงานอัตราการรักษาสำเร็จ 100%2) ไม่ครอบคลุมโดยประกันในญี่ปุ่น อุปกรณ์ใกล้เคียงกันคือ MiBo Thermoflo® ซึ่งให้ความร้อนด้วยแผ่นให้ความร้อนภายนอกที่ 42.2°C แต่ผลการเพิ่มอุณหภูมิเปลือกตาน้อยกว่า1)
การสวนท่อต่อมไขมัน (Intraductal probing) (CQ-30): สอดหัววัด Maskin (เพิ่มขนาดจาก 1mm เป็น 4/6mm ตามลำดับ) เข้าไปในท่อที่อุดตันเพื่อเปิดทางกายภาพ1) ในกลุ่มตัวอย่าง 25 ราย 96% มีอาการดีขึ้นทันที แต่ในการทดลองแบบสุ่มที่มีกลุ่มควบคุม 49 ราย การเปลี่ยนแปลงของอาการแสดงทางกายภาพพบว่ามีจำกัด1) เนื่องจากเป็นวิธีการที่รุกล้ำและให้ผลการเปลี่ยนแปลงอาการแสดงทางกายภาพจำกัด แนวทางปฏิบัติ GL 2023 ของวารสารจักษุวิทยาญี่ปุ่นจึงแนะนำแบบอ่อนว่าไม่ควรทำหัตถการนี้3)
หัตถการหลักที่ทำในผู้ป่วยนอกมีดังนี้
การบีบ meibum : ทำเพื่อขับสิ่งอุดตันและปรับปรุงการทำงานของต่อม ปากคีบกดต่อม Meibomian แบบ Arita (บริษัท Inami) ออกแบบมาเพื่อช่วยลดความเจ็บปวดขณะบีบ ทำอย่างต่อเนื่องทุก 10 วันถึง 1 เดือน ร่วมกับการประคบอุ่นและทำความสะอาดขอบเปลือกตาที่บ้าน Meibum ที่ถูกบีบออกมาจะมีลักษณะขุ่นหรือคล้ายยาสีฟันใน MGD ชนิดหลั่งลดการนำ plugging ออก : หากมี plugging ขนาดใหญ่ทำให้รู้สึกไม่สบาย ให้นำออกด้วยปากคีบหลังจากหยดยาชาเฉพาะที่ หากอุดตันลึกในช่องเปิด ให้ใช้สำลีก้านกดขอบเปลือกตาหรือใช้ปากคีบกด meibum หาก Meibomian infarction ยื่นออกมาเป็นลักษณะคล้ายขี้ผึ้ง ให้กรีดด้วยเข็มฉีดยาและนำออกการเจาะกุ้งยิง ภายใน : หากมีหัวหนองชัดเจน ให้เจาะด้วยเข็มฉีดยา 21~25G ใช้สำลีก้านบีบหนองออก จากนั้นจ่ายยาปฏิชีวนะการฉีดสเตียรอยด์ รักษาก้อนที่เปลือกตา (chalazion) : ใช้กระบอกฉีดยา 1mL และเข็ม 2728G ฉีด triamcinolone acetonide 2mg (Kenacort-A® 40mg/mL ปริมาณ 0.05mL) เข้าไปในก้อนจากด้านเยื่อบุตา อัตราการหายขาดอยู่ที่ 6090% หลังฉีด 1~2 ครั้ง มีประสิทธิภาพเทียบเท่าการผ่าตัดนำก้อนออก ระยะเวลาจนหายดีประมาณ 5 วันถึง 2.5 สัปดาห์ การฉีดจากด้านเยื่อบุตา แทนการฉีดจากด้านผิวหนังช่วยป้องกันการสะสมสีขาวของยาและการสูญเสียสีผิว หากไม่ดีขึ้นหลังฉีด 2 ครั้ง ให้พิจารณาการรักษาด้วย IPL หากสงสัยมะเร็งต่อมไขมัน ให้ทำการผ่าตัดและตรวจทางพยาธิวิทยาค่าตอบแทนทางการแพทย์ : การประคบอุ่น การบีบ meibum การนำ plugging ออก และการเจาะกุ้งยิง ภายใน คิดเป็น “หัตถการทางตา” การบีบ meibum และการนำ plugging ออก ใส่รหัสวินิจฉัย “Meibomian gland infarction” Kenacort-A® ไม่มีสิทธิ์เบิกประกันสำหรับการวินิจฉัย “chalazion” แต่สามารถเบิกได้ในฐานะ “การรักษาตามอาการของโรคอักเสบบริเวณภายนอกดวงตา”
กลุ่มเตตราไซคลิน : ด็อกซีไซคลิน และไมโนไซคลินมีคุณสมบัติละลายในไขมันได้ดีกว่าเตตราไซคลิน สะสมในเนื้อเยื่อตาและเปลือกตาได้ในขนาดต่ำ1) ใช้โดยมีวัตถุประสงค์หลักในการต้านการอักเสบมากกว่าต้านเชื้อแบคทีเรีย ควบคุมการอักเสบผ่านการยับยั้ง MMP-8, MMP-9, TNF -α, ยับยั้งการผลิตไลเปส และยับยั้งการผลิตกรดไขมันอิสระ1) การศึกษา RCT ในผู้ป่วย 60 รายรายงานว่ากลุ่มที่ใช้ไมโนไซคลินร่วมมีตัวชี้วัดทางคลินิกทั้งหมดและ IL-6, IL-1β, IL-17α, TNF -α, IL-12p70 ดีขึ้นอย่างมีนัยสำคัญเมื่อเทียบกับกลุ่มควบคุม1), 13) ผลข้างเคียงคืออาการไวต่อแสง และอาการทางเดินอาหาร ห้ามใช้ในหญิงตั้งครรภ์และเด็ก14)
อะซิโธรมัยซิน : เป็นกลุ่มแมคโครไลด์ จับกับ 50S ไรโบโซม 23S rRNA และยับยั้งการสังเคราะห์โปรตีนของแบคทีเรีย นอกเหนือจากฤทธิ์ต้านเชื้อแบคทีเรียแล้ว ยังมีฤทธิ์ยับยั้งการแสดงออกของ NF -κB, IL-6, IL-8, TNF -α, MMP-9 และเหนี่ยวนำ TGF-β1 ที่ต้านการอักเสบ1) ยาหยอดตา 1% (AzaSite®, สหรัฐอเมริกา) มีจำหน่าย โดยรายงานว่ามีประสิทธิภาพในการรักษาที่ยาวนานถึง 3 เดือนหลังการใช้ระยะสั้น อะซิโธรมัยซินชนิดรับประทานใช้ในขนาด 500 มก. × 3 วัน จำนวน 3 รอบ (ห่างกัน 7 วัน) หรือสัปดาห์ละครั้ง 1 กรัม × 3 สัปดาห์ แต่มีความเสี่ยงต่อการยืดช่วง QT ต้องระมัดระวังในผู้ป่วยที่มีประวัติโรคหัวใจ1)
Cyclosporine A 0.05% ยาหยอดตา : ได้รับการรับรองจาก FDA สหรัฐฯ ในชื่อ Restasis® สำหรับโรคตาแห้ง ชนิดขาดน้ำตา ยับยั้งการผลิต IL-2 ของเซลล์ทีและออกฤทธิ์ต้านการอักเสบ1) ประสิทธิภาพใน MGD เพียงอย่างเดียวยังมีจำกัด แนวทางปฏิบัติของวารสารจักษุวิทยาญี่ปุ่นปี 2023 แนะนำอย่างอ่อนให้ไม่ควรทำ3)
Lifitegrast 5.0% ยาหยอดตา : ยาต้าน LFA -1 ที่ได้รับการรับรองจาก FDA สหรัฐฯ สำหรับโรคตาแห้ง หลักฐานเฉพาะสำหรับ MGD ยังไม่เป็นที่ยอมรับ1)
การรับประทานกรดไขมันโอเมก้า-3 : การเสริม EPA/DHA ช่วยเปลี่ยนองค์ประกอบกรดไขมันของ meibum1) การทดลอง DREAM (n=499) รายงานในปี 2018 ว่าไม่มีความแตกต่างอย่างมีนัยสำคัญของ OSDI, Schirmer และ BUT ระหว่างกลุ่มโอเมก้า-3 และกลุ่มควบคุม หลักฐานจึงยังขัดแย้งกัน1) แนวทางปฏิบัติ GL 2023 ของวารสารจักษุวิทยาญี่ปุ่นแนะนำอย่างอ่อน เนื่องจากถือเป็นผลิตภัณฑ์เสริมอาหารในญี่ปุ่น3)
การติดเชื้อ Demodex เพิ่มขึ้นตามอายุและสูงถึง 100% ในผู้ที่มีอายุมากกว่า 70 ปี1) Demodex folliculorum อาศัยอยู่ที่โคนขนตา ส่วน Demodex brevis อาศัยอยู่ในต่อม meibomian และต่อมไขมัน ชนิดแรกทำให้เกิด keratinization เพิ่มขึ้นแบบปฏิกิริยาและเกิดรังแคทรงกระบอก (cylindrical dandruff) ส่วนชนิดหลังทำให้เกิดการอุดตันของต่อมและปฏิกิริยา granuloma1)
น้ำมันทีทรี (TTO: จาก Melaleuca alternifolia ) มีประสิทธิภาพในการกำจัดปรสิต1) โดยเฉพาะอย่างยิ่ง โปรโตคอลการใช้ TTO 50% ขัดขอบเปลือกตาที่คลินิกสัปดาห์ละ 1 ครั้ง และ TTO 10% ที่บ้านทุกวันเป็นเวลา 1 เดือน มีรายงานว่าช่วยลดการอักเสบของขอบเปลือกตา ลด IL-1β และ IL-17 ในน้ำตา และปรับปรุงอาการระคายเคืองของผิวลูกตา1) สารออกฤทธิ์ฆ่า Demodex ใน TTO คือ terpinen-4-ol และมีผลิตภัณฑ์การค้าเช่น Cliradex® ให้ใช้ได้1) นอกจากนี้ยังมีรายงานว่า ivermectin ชนิดรับประทาน 200 μg/kg ครั้งเดียว (วันที่ 0 และวันที่ 7) ช่วยปรับปรุงจำนวน Demodex, Schirmer และ BUT ในโรคขอบเปลือกตาอักเสบ ส่วนหลังที่ดื้อต่อการรักษา1)
Zhang และคณะรายงานผู้ป่วย MGD ชายอายุ 46 ปี ที่มีอาการแสดงภายนอกน้อย และไม่พบ Demodex จากการตรวจขนตาดึง หลังจากฆ่าเชื้อขอบเปลือกตา พบ D. brevis 15 ตัวโดยตรงใน meibum ที่บีบออก และอาการดีขึ้นหลังจาก TTO lid scrub6) เป็นกรณีสำคัญที่แสดงให้เห็นว่าการตรวจ meibum โดยตรงมีประโยชน์ในการตรวจหา Demodex
การประคบอุ่นและการเช็ดทำความสะอาดเปลือกตาทุกวันเป็นกุญแจสำคัญสู่ความสำเร็จในการรักษา แม้อาการจะดีขึ้น อย่าหยุดการรักษาด้วยตนเอง ควรมาตรวจตามนัดอย่างสม่ำเสมอ Doxycycline แบบรับประทานอาจทำให้เกิดอาการไวต่อแสง และอาการทางเดินอาหาร ห้ามใช้ในหญิงตั้งครรภ์และเด็ก Azithromycin แบบรับประทานมีความเสี่ยงต่อการยืดช่วง QT ต้องระวังในผู้ที่มีประวัติโรคหัวใจ การรักษาด้วยอุปกรณ์เช่น IPL, LipiFlow ไม่มีสิทธิ์เบิกประกันในญี่ปุ่นและเป็นการรักษานอกระบบ จึงควรตรวจสอบค่าใช้จ่ายและสถานที่ให้บริการล่วงหน้า
Q
การตรวจใดบ้างที่ใช้ในการวินิจฉัย MGD?
A
ตามเกณฑ์การวินิจฉัยของ MGD Working Group ญี่ปุ่น 2010 ต้องมีผลบวกทั้ง 3 ข้อ: (1) อาการทางความรู้สึก เช่น รู้สึกไม่สบายตา (2) ความผิดปกติรอบต่อม meibomian (หลอดเลือดขยาย การเคลื่อนของ MCJ ขอบเปลือกตาไม่เรียบ อย่างน้อย 1 ข้อ) (3) การอุดตันของต่อม (plugging และการหลั่ง meibum ลดลงตั้งแต่ grade 2 ขึ้นไปตาม Shimazaki) แนวทาง GL 2023 ของวารสารจักษุวิทยาญี่ปุ่นแนะนำให้ทำ meibography และสังเกต meibum
Q
การประคบอุ่นควรทำอย่างไร?
A
ทำให้ผ้าสะอาดชุ่มน้ำแล้วอุ่นในไมโครเวฟ หรือใช้หน้ากากอุ่นตาที่มีจำหน่ายทั่วไปวางบนตาทั้งสองข้างนาน 5–10 นาที สิ่งสำคัญคือต้องรักษาอุณหภูมิขอบเปลือกตาประมาณ 40°C ควรระวังว่าผ้าร้อนมีแนวโน้มลดอุณหภูมิลงเนื่องจากการระเหย แนวทาง GL 2023 CQ-18 ของวารสารจักษุวิทยาญี่ปุ่นแนะนำให้ทำวันละ 2 ครั้ง ครั้งละอย่างน้อย 5 นาที การนวดขอบเปลือกตาเบาๆ หลังจากประคบอุ่นช่วยขับ meibum ที่หลอมเหลวออกมา
วารสารจักษุวิทยาญี่ปุ่น GL 2023 BQ-1 สรุปพยาธิสภาพหลักของ MGD ชนิดที่มีการหลั่งลดลงว่า “ภาวะเยื่อบุท่อขับหนาตัวผิดปกติและการฝ่อของต่อมแอซินัส”3) โดยระบุว่าการฝ่อของต่อมแอซินัสสามารถเกิดขึ้นได้ไม่เพียงแต่เป็นผลทุติยภูมิจากการอุดตันของต่อมไมโบเมียน แต่ยังเกิดจากความเสียหายปฐมภูมิของเซลล์ต่อมจากอายุที่มากขึ้นอีกด้วย
การดำเนินโรคจากการอุดตันของท่อขับไปสู่การฝ่อของต่อมแอซินัส
ภาวะเยื่อบุท่อขับหนาตัวผิดปกติและความหนืดของ meibum ที่เพิ่มขึ้นทำให้เกิดการอุดตันของท่อส่วนปลาย1) การอุดตันทำให้ความดันภายในต่อมแอซินัสเพิ่มขึ้น นำไปสู่การฝ่อและการสูญเสียต่อมแอซินัส การสูญเสียต่อมแอซินัสทำให้การหลั่งไขมันลดลง และชั้นไขมันของฟิล์มน้ำตาบางลง
การเพิ่มขึ้นของจุดหลอมเหลวของ meibum
Meibum ปกติมีจุดหลอมเหลวประมาณ 19–32°C และคงสภาพเป็นของเหลวที่อุณหภูมิผิวตาประมาณ 33–37°C1) ใน MGD การเพิ่มขึ้นของสฟิงโกลิปิด เช่น เซราไมด์ ทำให้จุดหลอมเหลวของ meibum สูงขึ้น ในกรณีรุนแรง meibum จะไม่กลายเป็นของเหลวเว้นแต่จะได้รับความร้อนสูงกว่า 40°C1) นี่คือเหตุผลในการรักษาด้วยการประคบอุ่นและการให้ความร้อนแบบพัลส์
อิทธิพลของฮอร์โมนเพศ
แอนโดรเจนกระตุ้นยีนสังเคราะห์ไขมันใน meibocyte (เซลล์ต่อมไมโบเมียน ) และยับยั้งยีนที่เกี่ยวข้องกับการหนาตัวผิดปกติของเยื่อบุ1) การขาดแอนโดรเจน ความผิดปกติของตัวรับ หรือการใช้ยาต้านแอนโดรเจนสัมพันธ์กับ MGD ชนิดอุดกั้น ในทางกลับกัน เอสโตรเจนส่งเสริมการสลายไขมันและกระตุ้นการผลิตไซโตไคน์อักเสบ เช่น IL-6 และ TNF -α1) ความสัมพันธ์ระหว่างการบำบัดด้วยฮอร์โมนทดแทนในวัยหมดประจำเดือนกับภาวะตาแห้ง สามารถอธิบายได้ส่วนหนึ่งจากการลดลงของการผลิตแอนโดรเจนจากต่อมหมวกไตผ่านการยับยั้งแกนไฮโปทาลามัส–ต่อมใต้สมอง–ต่อมหมวกไต1)
บทบาทของแบคทีเรียและการอักเสบ
ไลเปสที่ผลิตโดยแบคทีเรียประจำถิ่นที่ขอบเปลือกตา (ส่วนใหญ่เป็นเชื้อสแตฟิโลค็อกคัส) จะย่อยสลายไขมันใน meibum ทำให้กรดไขมันอิสระเพิ่มขึ้นและก่อให้เกิดการอักเสบ1) ในผู้ป่วยโรคเปลือกตาอักเสบ พบว่ามีการเพิ่มขึ้นของกิจกรรมไลเปสและการผลิตเมทริกซ์เมทัลโลโปรตีเนส (MMP) ในน้ำตาของผู้ป่วย MGD พบว่าความเข้มข้นของ IL-1α, IL-1β ที่เจริญเต็มที่, MMP-9, IL-6, IL-8, TNF -α สูงขึ้น และสัมพันธ์กับความรุนแรงของความเสียหายของเยื่อบุผิวผิวตาดำ1) IL-1 กระตุ้นการเพิ่มจำนวนและการสร้างเคราตินมากเกินไปของเซลล์เยื่อบุผิว ทำให้เกิดวงจรอุบาทว์ของ MGD ชนิดอุดตัน
PPAR-γ (peroxisome proliferator-activated receptor γ) อยู่ในกลุ่มซูเปอร์แฟมิลีของตัวรับนิวเคลียร์ ทำหน้าที่เป็นปัจจัยถอดรหัสที่เกี่ยวข้องกับการสังเคราะห์ไขมันและการเปลี่ยนแปลงของเซลล์ต่อมไขมัน ใน meibocyte เชื่อว่ามีบทบาทสำคัญในการเปลี่ยนแปลงของเซลล์และการสังเคราะห์ไขมัน และกำลังได้รับความสนใจในฐานะเป้าหมายในการทำความเข้าใจพยาธิสภาพของ MGD 3)
สฟิงโกลิปิดและจุดหลอมเหลว
ใน MGD สัดส่วนของเซราไมด์และสฟิงโกลิปิดใน meibum เพิ่มขึ้น ทำให้ความเสถียรของฟิล์มไขมัน meibum ลดลง1) การเพิ่มขึ้นของปริมาณเซราไมด์ส่งผลโดยตรงต่อการเพิ่มขึ้นของจุดหลอมเหลวของ meibum ทำให้ไม่กลายเป็นของเหลวเว้นแต่จะได้รับความร้อนสูงกว่า 40°C สฟิงโกลิปิดไม่เพียงเปลี่ยนแปลงคุณสมบัติทางเคมีกายภาพของ meibum แต่ยังควบคุมกระบวนการของเซลล์ เช่น การเพิ่มจำนวน การเปลี่ยนแปลง การตายของเซลล์แบบโปรแกรม และการอักเสบ ซึ่งทำให้พยาธิสภาพของ MGD ซับซ้อนยิ่งขึ้น1)
เบาหวานและการเปลี่ยนแปลงของผิวตาดำ
โรคเบาหวานชนิดที่ 2 เป็นปัจจัยที่ทำให้ MGD รุนแรงขึ้น การศึกษาแบบภาคตัดขวางใน 302 ตาโดย Hao และคณะรายงานว่ากลุ่ม DED -DM มีความผิดปกติของขอบเปลือกตาบน, หลอดเลือดขยายที่ขอบเปลือกตา, ระดับการอุดตันของต่อม, ขอบเปลือกตาหนา, การสูญเสียต่อมไมโบเมียน ของเปลือกตาบน, ภาวะคั่งเลือดของขนตา, และค่า NIBUT (non-invasive BUT ) แย่ลงอย่างมีนัยสำคัญเมื่อเทียบกับกลุ่ม DED เพียงอย่างเดียว และระดับน้ำตาลในเลือดมีความสัมพันธ์อย่างมีนัยสำคัญกับค่า NIBUT , ขอบเปลือกตาหนา และความผิดปกติของขอบเปลือกตา7) มีการเสนอว่ากลไกพยาธิสภาพคือการอักเสบเรื้อรังและความเสียหายของหลอดเลือดขนาดเล็กที่ลุกลามไปยังขอบเปลือกตาและเนื้อเยื่อต่อม
เนื้อหาต่อไปนี้อยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิก และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับความก้าวหน้าทางการแพทย์ในอนาคต
LipiFlow Translucent Activator : Activator Clear ซึ่งเป็นตัวกระตุ้นกึ่งโปร่งใสแบบใหม่ของ LipiFlow ช่วยให้การยืนยันตำแหน่งที่วางทำได้ง่ายขึ้นเนื่องจากวัสดุกึ่งโปร่งใส การศึกษาของ Hu และคณะรายงานอัตราการรักษาสำเร็จ 100%2) มีการยืนยันการปรับปรุงของอาการและคะแนน meibum นานถึง 3 เดือนหลังการรักษา การศึกษาติดตามระยะยาวของ Blackie และคณะพบว่าการรักษาด้วย LipiFlow ครั้งเดียวช่วยรักษาการหลั่ง meibum และอาการตาแห้ง ให้นานขึ้น 12 เดือน โดย 86% ไม่ต้องการการรักษาเพิ่มเติม15)
การกระตุ้นประสาทภายในโพรงจมูก (intranasal neurostimulation): การกระตุ้นเส้นประสาทเอทมอยด์ส่วนหน้าภายในโพรงจมูกแบบพัลส์เหนี่ยวนำให้เกิดการหลั่งน้ำตาจากต่อมน้ำตาผ่านรีเฟล็กซ์จมูก-น้ำตา ในการทดลองในสัตว์ การกระตุ้นวันละ 3 นาที ติดต่อกัน 3 สัปดาห์ช่วยเพิ่มปริมาณน้ำตา ความเข้มข้นของไขมันและโปรตีน และลดความดันออสโมซิสของน้ำตา1) การทดลองแบบสุ่มที่มีกลุ่มควบคุมในมนุษย์รายงานว่า Allergan TrueTear® Intranasal Tear Neurostimulator (ITN) เหนี่ยวนำให้เกิดการสลายแกรนูลของเซลล์กอบเล็ตเยื่อบุตา เพิ่มความสูงของวงเดือนน้ำตา เพิ่มอุณหภูมิบริเวณต่อมไมโบเมียน ส่วนกลางของเปลือกตาล่าง และเพิ่มความหนาของชั้นไขมันฟิล์มน้ำตา1) การศึกษาแบบเปิดไม่สุ่มรายงานว่าการใช้ 4 ครั้งขึ้นไปต่อวันนาน 180 วันช่วยให้ค่า Schirmer การย้อมสีกระจกตา และเยื่อบุตา และอาการทางคลินิกดีขึ้นทั้งหมด1) รูปร่างของต่อมไมโบเมียน (พื้นที่ เส้นรอบวง) เปลี่ยนแปลงทันทีเมื่อกระตุ้นภายในโพรงจมูก ซึ่งอาจเป็นกลยุทธ์การรักษาใหม่ที่ส่งเสริมการหลั่งไมบัมผ่านการปรับระบบประสาท1)
การบำบัดด้วยฮอร์โมนเพศ: การทดลองแบบสุ่มหลายศูนย์ของ Schiffman และคณะในรายงานระดับบทคัดย่อ ARVO พบว่ายาหยอดตาเทสโทสเตอโรนเฉพาะที่ (0.03%) หลังการรักษา 6 เดือนช่วยปรับปรุงความหนืดของสารคัดหลั่งต่อมไมโบเมียน อย่างมีนัยสำคัญเมื่อเทียบกับกลุ่มควบคุม1) มีการศึกษาที่พบว่าแอนโดรเจนเฉพาะที่เพิ่มความหนาของชั้นไขมันน้ำตาและ BUT แต่ปัจจุบันยังไม่มีการรับรองยาหยอดตานี้ทั้งในญี่ปุ่นและสหรัฐอเมริกา1) ครีมเทสโทสเตอโรน 5% ในสตรีวัยหมดประจำเดือน (การปรับปรุง OSDI) DHEA ผ่านผิวหนังในผู้ป่วยหลังหมดประจำเดือน และการประยุกต์ใช้การบำบัดด้วยฮอร์โมนทดแทนในสตรีทางจักษุวิทยาก็ถูกกล่าวถึงเช่นกัน แต่ทั้งหมดยังมีหลักฐานไม่เพียงพอและยังไม่ถูกนำมาใช้ในเวชปฏิบัติประจำวัน1)
สารต้านตัวรับ IL-1 (Anakinra) :Kineret™ (IL-1RA recombinant ของมนุษย์) เป็นชีววัตถุที่ได้รับการอนุมัติสำหรับโรครูมาตอยด์ และได้แสดงประสิทธิภาพในการใช้นอกเหนือข้อบ่งชี้สำหรับโรคตาแห้ง 1) เนื่องจาก IL-1 ในน้ำตาของผู้ป่วย MGD มีบทบาทสำคัญในการก่อโรค จึงเป็นเป้าหมายการรักษาที่มีแนวโน้มดี แต่ผลการทดลองทางคลินิกใน MGD ยังไม่ได้รับการตีพิมพ์1)
การเปลี่ยนแปลงรูปร่างของต่อมโดย IPL :การศึกษาตามกลุ่มตัวอย่าง 35 รายรายงานว่า IPL ทำให้เส้นผ่านศูนย์กลางยาวที่สุดของ acinus เพิ่มขึ้นและความหนาแน่นของหน่วยเพิ่มขึ้น พร้อมลดเซลล์อักเสบรอบต่อม1) ผลนี้ชี้ให้เห็นถึงความเป็นไปได้ของผลการซ่อมแซมเนื้อเยื่อที่เหนือกว่าการรักษาตามอาการเพียงอย่างเดียว
โปรไฟล์การแสดงออกของยีนต่อมไมโบเมียน :ใน MGD มีรายงานการเปลี่ยนแปลงการแสดงออกของยีนมากกว่า 400 ยีนในต่อมไมโบเมียน ยีนที่ตอบสนองต่อแอนโดรเจน ยีนที่เกี่ยวข้องกับการสร้างเคราติน และยีนที่เกี่ยวข้องกับการสังเคราะห์ไขมันถูกระบุเป็นเป้าหมายหลัก และกำลังมีการศึกษาความเป็นไปได้ของการรักษาแบบมุ่งเป้าระดับโมเลกุล1)
Mibo Thermoflo®・IRP L・เลเซอร์ระดับต่ำ :การทดลองเปรียบเทียบอุปกรณ์ใหม่ เช่น อุปกรณ์ให้ความร้อนภายนอก IRP L (แสงความกว้างแถบกว้าง) และเลเซอร์กำลังต่ำกำลังดำเนินการอยู่ แต่ยังไม่มีรายงานอุปกรณ์ใดที่แสดงประสิทธิภาพเหนือกว่า LipiFlow ณ เวลาปัจจุบัน1)
แนวทางปฏิบัติทางคลินิกของจักษุวิทยาญี่ปุ่นปี 2023 ก็ชี้ให้เห็นข้อจำกัดของหลักฐานใน CQ จำนวนมาก และการสะสมหลักฐานผ่าน RCT ที่นำโดยญี่ปุ่นถือเป็นความท้าทายในอนาคต3) โดยเฉพาะอย่างยิ่งจำเป็นต้องมีการกำหนดโปรโตคอลมาตรฐานสำหรับการรักษาแบบอนุรักษ์นิยมที่สามารถทำได้ในญี่ปุ่น (การประคบอุ่น การทำความสะอาดเปลือกตา การบีบ meibum) การทดลองในประเทศเพื่อขยายการครอบคลุมของประกันสำหรับ doxycycline, azithromycin ฯลฯ และการทดลองแบบหลายศูนย์เพื่อขออนุมัติยาสำหรับ IPL และ LipiFlow
Sabeti S, Kheirkhah A, Yin J, Dana R. Management of meibomian gland dysfunction: a review. Surv Ophthalmol. 2020;65(2):205-217.
Hu JG, Dang VT, Chang DH, et al. Performance of a Translucent Activator for LipiFlow Vectored Thermal Pulse (VTP) Treatment of Meibomian Gland Dysfunction. Clin Ophthalmol. 2022;16:963-971.
マイボーム腺機能不全診療ガイドライン作成委員会. マイボーム腺機能不全診療ガイドライン. 日眼会誌. 2023;127(2):109-228.
天野史郎ほか(マイボーム腺機能不全ワーキンググループ). マイボーム腺機能不全の定義と診断基準. あたらしい眼科. 2010;27(5):627-631. Available at: https://dryeye.ne.jp/wp/wp-content/themes/dryeye/file/mgd_teigi.pdf
Arita R, Itoh K, Inoue K, Amano S. Noncontact infrared meibography to document age-related changes of the meibomian glands in a normal population. Ophthalmology. 2008;115(5):911-915.
Zhang N, Liang L. Demodex in Meibum. Ophthalmology. 2024.
Hao Y, Wu B, Feng J, et al. Relationship between type 2 diabetes mellitus and changes of the lid margin, meibomian gland and tear film in dry eye patients: a cross-sectional study. 2024.
Jones L, Craig JP, Markoulli M, et al. TFOS DEWS III: Management and Therapy. Am J Ophthalmol. 2025.
ドライアイ研究会. ドライアイ診療ガイドライン. 日眼会誌. 2019;123(5):489-592. Available at: https://journal.nichigan.or.jp/PastContent?mag=0&number=5&vol=123&year=2019
Nelson JD, Shimazaki J, Benitez-del-Castillo JM, et al. The International Workshop on Meibomian Gland Dysfunction: Report of the Definition and Classification Subcommittee. Invest Ophthalmol Vis Sci. 2011;52(4):1930-1937.
Arita R, Minoura I, Morishige N, et al. Development of Definitive and Reliable Grading Scales for Meibomian Gland Dysfunction. Am J Ophthalmol. 2016;169:125-137.
Shimazaki J, Sakata M, Tsubota K. Ocular surface changes and discomfort in patients with meibomian gland dysfunction. Arch Ophthalmol. 1995;113(10):1266-1270.
Lee H, Min K, Kim EK, Kim TI. Minocycline controls clinical outcomes and inflammatory cytokines in moderate and severe meibomian gland dysfunction. Am J Ophthalmol. 2012;154(6):949-957.
Wladis EJ, Bradley EA, Bilyk JR, Yen MT, Mawn LA. Oral antibiotics for meibomian gland-related ocular surface disease: a Report by the American Academy of Ophthalmology. Ophthalmology. 2016;123(3):492-496. PMID: 26707417.
Blackie CA, Coleman CA, Holland EJ. The sustained effect (12 months) of a single-dose vectored thermal pulsation procedure for meibomian gland dysfunction and evaporative dry eye. Clin Ophthalmol. 2016;10:1385-1396. doi:10.2147/OPTH.S109663.
Arita R, Itoh K, Inoue K, Kuchiba A, Yamaguchi T, Amano S. Contact lens wear is associated with decrease of meibomian glands. Ophthalmology. 2009;116(3):379-384. doi:10.1016/j.ophtha.2008.10.012. PMID: 19167077.