上方型

点状表層角膜炎(SPK)
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 点状表層角膜炎(SPK)とは
Section titled “1. 点状表層角膜炎(SPK)とは”点状表層角膜炎(superficial punctate keratitis / superficial punctate keratopathy:SPK)は、角膜上皮の最表層細胞が種々の原因により点状に脱落した状態である。フルオレセイン生体染色を行うと、上皮欠損部が点状または集簇した染色像として観察される。基底細胞層は保たれており、障害がさらに深層に及べば角膜びらん、実質まで及べば角膜潰瘍と呼ばれる。
重要な前提として、SPK はあくまで「所見」であり独立した疾患名ではない。眼科外来で異物感を主訴とする患者の所見として最も高頻度に認められ、その背景には多彩な原因疾患が潜んでいる。したがって SPK の診療では原因検索が治療方針決定の第一歩となる。
一方で、例外的に独立した疾患単位として扱われるのが Thygeson 点状表層角膜炎(Thygeson superficial punctate keratitis:TSPK)である。TSPK は1950年に Phillips Thygeson により報告された両眼性・再発性の角膜上皮炎であり、明確な原因疾患が同定できない特発性の表層角膜炎として別項で記述される。
主な原因カテゴリ
Section titled “主な原因カテゴリ”- 涙液関連:ドライアイ(涙液分泌減少型・BUT 短縮型)、マイボーム腺機能不全(MGD)1)
- 物理・機械的要因:コンタクトレンズ障害、睫毛乱生、眼瞼内反、結膜弛緩症
- 化学的要因:点眼薬の薬剤毒性(防腐剤ベンザルコニウム塩化物を含む)、全身抗腫瘍薬の涙液移行
- 炎症・アレルギー:アレルギー性結膜炎、春季カタル、上輪部角結膜炎(SLK)
- 感染性:単純ヘルペスウイルス、アデノウイルス
- 神経・眼瞼障害:三叉神経麻痺、顔面神経麻痺、兎眼
- 特発性:Thygeson 点状表層角膜炎
SPK は病名ではなく、角膜上皮が何らかの原因で障害された結果として観察される「所見」である。原因を特定しない限り根本的な治療はできないため、SPK を認めたら必ず原因検索を行う。Thygeson 点状表層角膜炎だけは例外的に独立した疾患単位として扱われる。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”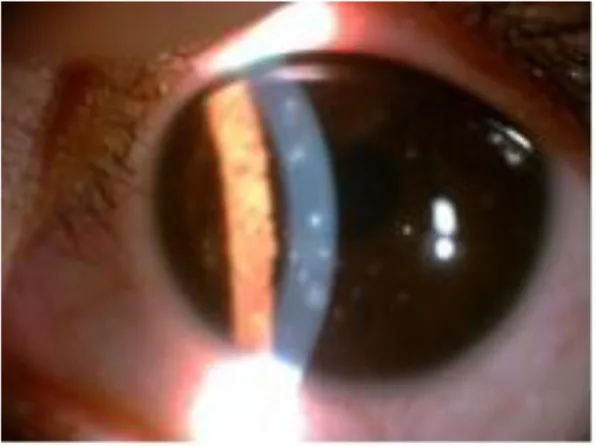
患者が訴える症状は多彩であり、眼科疾患で生じるほとんどすべての症状が SPK により出現しうる。
- 異物感:最も高頻度で、異物感を主訴とする外来患者の背景病態として最多である。
- 疼痛・眼痛:上皮障害の程度により軽度〜中等度の痛みを伴う。
- 視力低下・霧視:瞳孔領に病変が及ぶと生じる。
- 羞明:光に対する過敏性。増悪期に顕著となる。
- 乾燥感:涙液機能低下型で顕著。
- 充血:結膜充血の合併。
- 疲労感・眼精疲労:慢性経過で持続する。
- 眼脂・瘙痒感:アレルギー性や感染性で顕著。
臨床所見(医師が診察で確認する所見)
Section titled “臨床所見(医師が診察で確認する所見)”細隙灯顕微鏡検査では肉眼的に病変を観察できない例が多く、フルオレセイン生体染色による評価が診断の中核となる。染色像は点状・渦巻き状・クラックライン様など多様な形態を呈し、障害の程度により染色性は異なる。
染色部位による原因推定
Section titled “染色部位による原因推定”染色部位は原因疾患の推定に有用であり、日常診療の基本アプローチである。
中央型
主な起因疾患:神経麻痺性角膜症、Thygeson 点状表層角膜炎、睫毛による機械的障害、ハードコンタクトレンズ(HCL)障害、ドライアイ。
観察のポイント:角膜知覚検査と睫毛の状態を確認する。
下方・瞼裂部型
主な起因疾患:ドライアイ、結膜弛緩症、兎眼、マイボーム腺機能不全(MGD)、ソフトコンタクトレンズ(SCL)障害、眼瞼内反、薬剤性。
観察のポイント:瞼裂幅、マイボーム腺開口部、涙液メニスカスを観察する。
びまん性・局所型
びまん性:薬剤毒性(点眼薬毒性、抗腫瘍薬副作用)、重症ドライアイ、SCL 障害、角膜上皮関連ジストロフィ(Meesmann など)。
局所型:結膜異物、ヘルペス感染、CL 装用者の3時9時ステイニング。
進行度の目安
Section titled “進行度の目安”- 軽症 SPK:散在する点状染色。自覚症状軽度〜中等度。
- レイトステイニング(バスクリン角膜症):点眼後しばらくしてフルオレセインが染み込む所見。上皮バリア機能障害を示す。薬剤毒性で高頻度。
- ハリケーン角膜上皮症:角膜中央部に渦巻き状の染色パターン。薬剤毒性の中等度所見。
- 上皮クラックライン(epithelial crack line):ひび割れ様の線状欠損。薬剤毒性の重症型。
- 遷延性上皮欠損:SPK が進展し広範な上皮欠損へ移行した状態。
Thygeson 点状表層角膜炎の所見
Section titled “Thygeson 点状表層角膜炎の所見”TSPK は一般的な原因別 SPK とは異なる独立疾患であり、特徴的な臨床像を示す。
- 両眼性・再発性:通常両眼性で、増悪と寛解を繰り返す経過をとる。
- 角膜中央部の隆起病変:灰白色で類円形、わずかに隆起した点状混濁が散在する。各病巣は顆粒状変化の集合体であり、通常各眼に約20個、最大で50個程度認められる。
- 結膜の静穏性:結膜充血や炎症反応を欠く点が鑑別の重要な手がかりである。
- フルオレセイン染色:病巣中心部が点状に染色される。病変周辺の角膜上皮は正常である。
- 角膜知覚:正常またはわずかに低下する程度にとどまる。
- 自覚症状の頻度:異物感 48.8%、羞明 41.9%、霧視 36.0%、流涙 15.1%。眼痛はまれ。
- 病悩期間:1回のエピソードは1〜2ヶ月持続し、寛解までに約6週間を要する。再発は数年〜数十年続くことがあり、最長41年の記録もある。最終的には瘢痕を残さず消退する傾向にある。
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”SPK の原因は多岐にわたる。以下に臨床的に頻度の高いものから順に列挙する。
- 涙液分泌減少型ドライアイ:涙液の基礎分泌低下により生じる。Schirmer 第Ⅰ法で5mm 以下、BUT で5秒以下が診断基準の目安である3)。加齢、Sjögren 症候群、関節リウマチ、抗コリン薬内服などがリスク因子となる。
- BUT 短縮型ドライアイ:涙液量は保たれるが涙液層の安定性が低下し、まばたき直後から涙液層が破壊される病型である。VDT 作業、エアコン、コンタクトレンズ装用などと関連する3)。
- マイボーム腺機能不全(MGD):マイボーム腺開口部の閉塞や脂質分泌異常により涙液油層が障害され、蒸発亢進型のドライアイと難治性 SPK を呈する1,4)。下方〜瞼裂部の SPK が典型的である。
物理・機械的要因
Section titled “物理・機械的要因”- ハードコンタクトレンズ障害:角膜中央部に限局した SPK を生じる。装用時間の延長やレンズフィッティング不良がリスクとなる。
- ソフトコンタクトレンズ障害:びまん性または下方の SPK を呈する。レンズ汚染、装用時間延長、酸素透過性不足が関連する9)。3時9時ステイニングは円形状の局所 SPK で CL 特有の所見である。
- 睫毛乱生・眼瞼内反:睫毛が角膜面を擦過し機械的障害を生じる。
- 結膜弛緩症:下方瞼裂部に弛緩結膜が入り込み瞬目時の摩擦を増加させる。
- 薬剤毒性角膜症:点眼薬の防腐剤(ベンザルコニウム塩化物:BAC)が主たる原因で、主成分の毒性により生じる場合もある。抗緑内障薬、抗菌薬、抗真菌薬、抗ウイルス薬、NSAIDs 点眼、β遮断薬、点眼麻酔薬で報告が多い。軽症ではドライアイ類似の瞼裂部〜下方 SPK を呈し、重症化するとハリケーン角膜上皮症、上皮クラックライン、遷延性上皮欠損へと進行する。長期間の点眼毒性負荷は輪部機能不全や偽眼類天疱瘡の誘因となる。TS-1 などの抗癌薬全身投与では角膜上方の輪部から上皮障害が生じる。
炎症・アレルギー
Section titled “炎症・アレルギー”- アレルギー性結膜炎・春季カタル:上方型 SPK の代表であり、巨大乳頭や粘液性眼脂を伴う5)。
- 上輪部角結膜炎(SLK):50歳以上に好発する上輪部の慢性炎症で、上方型 SPK と糸状角膜炎を生じる。
- フリクテン角膜炎(マイボーム腺炎角結膜上皮症):マイボーム腺炎と関連する IV 型アレルギーによる両眼性再発性角膜炎。
- 単純ヘルペスウイルス角膜炎(上皮型):片眼性、角膜知覚低下、樹枝状潰瘍が典型的である。初期には点状や星芒状の上皮所見を示すこともあり SPK との鑑別を要する7)。
- アデノウイルス角膜炎:流行性角結膜炎に伴う多発性上皮下浸潤として観察される。先行する結膜炎の既往が鑑別点となる。
神経・眼瞼障害
Section titled “神経・眼瞼障害”- 神経麻痺性角膜症:三叉神経の障害により角膜知覚が低下し、上皮修復機能が破綻して中央型 SPK を生じる。角膜ヘルペス後、帯状疱疹眼症、三叉神経手術後、脳幹病変などが原因となる。
- 兎眼性角膜症:閉瞼不全により角膜下方が乾燥する。顔面神経麻痺、甲状腺眼症、眼窩腫瘍、睡眠時閉瞼不全、昏睡などが背景疾患となる。
- 糖尿病角膜症:糖尿病による神経障害と上皮接着性低下により生じる。
特発性:Thygeson 点状表層角膜炎
Section titled “特発性:Thygeson 点状表層角膜炎”原因不明の再発性両眼性角膜上皮炎である。HLA-DR3 との関連が報告されており、免疫学的機序の関与が示唆されている2)。セリアック病との合併が HLA-DR3 の共有を介して報告されている2)。シクロスポリン A やタクロリムスなどの免疫抑制薬が奏功することから、T 細胞介在性の免疫反応が推定されている。ウイルス関与説も提唱されたが、PCR による検討では原因ウイルスは同定されていない。
全身疾患との関連
Section titled “全身疾患との関連”関節リウマチなどの膠原病、糖尿病、アトピー性皮膚炎は SPK の背景疾患となりうる。治療方針を立てる際には全身疾患の聴取が重要である。
4. 診断と検査方法
Section titled “4. 診断と検査方法”SPK の診療は、所見の確認にとどまらず「何が原因で上皮が障害されているか」を体系的に検索することが治療方針決定の鍵となる。
診断プロセス
Section titled “診断プロセス”- 問診:発症の急性/慢性、片眼性/両眼性、CL 装用歴、使用点眼薬・内服薬、外傷・異物暴露、全身疾患歴(関節リウマチ、糖尿病、アトピー、Sjögren 症候群など)を聴取する。急性・片眼性であれば外因性(異物・化学物質)、慢性・両眼性であれば内因性(ドライアイ・MGD・薬剤毒性)の可能性が高い。
- 細隙灯顕微鏡検査:上皮下浸潤などの炎症所見の有無、結膜充血、前房内炎症の有無を確認する。
- フルオレセイン生体染色:染色部位・パターンから原因を推定する(セクション2の CardGrid 参照)。
- 環境因子評価(6項目):涙液機能、眼瞼、角膜知覚、結膜、使用薬剤、全身疾患の各項目を評価する。
- 定量評価:SPK の重症度を客観化するため、AD 分類またはフルオレセイン染色スコアを用いる。
- Schirmer テスト第Ⅰ法:涙液の基礎分泌および反射性分泌を測定する。5分後の測定値が10mm 以上であれば正常、5mm 以下であれば涙液分泌減少型ドライアイを疑う。
- 涙液層破壊時間(BUT):フルオレセイン点眼後に開瞼を維持し、涙液層に乾燥斑が出現するまでの時間を測定する。5秒以下で異常と判定し、BUT 短縮型ドライアイの診断根拠となる3,8)。
- 涙液メニスカス観察:下眼瞼縁の涙液三日月の高さを評価する。減少型ドライアイでは低値を示す。
- Cochet-Bonnet 角膜知覚計:角膜ヘルペスや糖尿病角膜症、LASIK 術後、CL 長期装用者、顔面神経麻痺などで低下する。知覚低下は涙液の反射性分泌を低下させ、SPK を悪化させる。
- 共焦点顕微鏡検査:Thygeson SPK では表層・基底上皮細胞層に星芒状の高反射性堆積物、基底上皮層へのランゲルハンス細胞侵入、前部実質混濁が認められる。疾患の持続期間が長い眼ほど変化が重度となる。
- 涙液検査:ラクトフェリン定量、MMP-9 検査などが補助的に用いられる。
- 全身疾患スクリーニング:抗 SS-A/SS-B 抗体、HbA1c、血清 IgE などを必要に応じて評価する。
- AD 分類:SPK の面積(Area:A0〜A3)と密度(Density:D0〜D3)を各3点満点で評価し、例えば A2D2 のように表現する。
- フルオレセイン染色スコア:角膜を3領域に分け、各領域を0〜3点で評価し合計9点満点で表現する。経時的変化の追跡に用いられる。
- NEI スケール:角膜を5領域に分け、各領域を0〜3点で評価し合計15点満点で表現する国際的な指標である。
| 鑑別対象 | 鑑別のポイント |
|---|---|
| 角膜ヘルペス(上皮型) | 片眼性、知覚低下、樹枝状潰瘍 |
| アデノウイルス角膜炎 | 先行結膜炎、多発性上皮下浸潤 |
| Thygeson SPK | 両眼・中央・結膜静穏・隆起病変 |
| ドライアイ/MGD | 下方 SPK、BUT 短縮、涙液異常 |
| 薬剤毒性角膜症 | 点眼歴、瞼裂部 SPK、レイト染 |
| アレルギー性角結膜炎 | 上方 SPK、巨大乳頭、瘙痒 |
| 神経麻痺性角膜症 | 中央 SPK、角膜知覚低下 |
| 兎眼性角膜症 | 閉瞼不全、下方 SPK |
代表的な定量評価法として、SPK の範囲(Area)と密度(Density)を各3点満点で表現する AD 分類と、角膜を3領域に分け0〜3点で評価する9点満点のフルオレセイン染色スコアがある。国際的には角膜を5領域に分ける NEI スケール(15点満点)も用いられる。いずれも経時的変化の追跡と治療効果判定に有用である。
5. 標準的な治療法
Section titled “5. 標準的な治療法”SPK の治療の大原則は 「原因の除去」と「角膜上皮の保護・修復」の併用である。原因疾患によって治療戦略が大きく異なるため、原因別のアプローチを以下に示す。
涙液補充・保護
ヒアルロン酸ナトリウム点眼:ヒアレイン点眼液(0.1%)1日4〜6回。自覚症状・涙液安定性・角膜障害のいずれも改善し、ドライアイ診療ガイドラインでも使用が推奨されている3)。
人工涙液:防腐剤フリー製剤が望ましい。軽症例や薬剤毒性例で第一に選択する。
眼軟膏:就寝前の角膜保護に用いる。タリビッド眼軟膏(0.3%)などが代表である。
涙液動態の改善
ジクアホソルナトリウム点眼:ジクアス点眼液(3%)1日6回。膜結合型ムチン発現と水分分泌を促進し、BUT 短縮型ドライアイに有効である。臨床試験により自覚症状と上皮障害の改善が示されており、ドライアイ診療ガイドラインで推奨されている3)。
レバミピド点眼:ムコスタ点眼液UD(2%)1日4回。ムチン産生促進と抗炎症作用を併せ持つ。自覚症状と上皮障害の改善が示されており、同じく推奨されている3)。
原因別の治療プロトコル
Section titled “原因別の治療プロトコル”ドライアイによる SPK
Section titled “ドライアイによる SPK”- 第一選択:ヒアレイン点眼液(0.1%)1日4〜6回。
- BUT 短縮型での併用:
- ジクアス点眼液(3%)1日6回、または
- ムコスタ点眼液UD(2%)1日4回。
- 重症例:涙点プラグ挿入または涙点縫合術を行う。従来の点眼治療と比較して自覚症状・涙液安定性・上皮障害のいずれも有意に改善させる3)。
- 補助:副腎皮質ステロイド点眼は自覚症状と涙液安定性の改善に有用だが、眼圧上昇に留意して使用する3)。
マイボーム腺機能不全(MGD)による SPK
Section titled “マイボーム腺機能不全(MGD)による SPK”- 温罨法・眼瞼清拭:ホットパック(40℃・5分間)と眼瞼マッサージを1日1〜2回行う1)。
- 眼軟膏:タリビッド眼軟膏(0.3%)をごく少量眼瞼縁に薄く塗布する。
- 点眼:ヒアレイン点眼液(0.1%)を適宜使用する。
- 炎症が強い場合:
- クラリス錠(200mg)2錠 分2(クラリスロマイシン内服)
- ベストロン点眼用(0.5%)1日4回
- フルメトロン点眼液(0.1%)1日4回
アレルギー性結膜炎による SPK
Section titled “アレルギー性結膜炎による SPK”重症度に応じて段階的に追加する5)。
- アレジオン点眼液(0.05%)1日4回(朝・昼・夕・眠前)
- タリムス点眼液(0.1%)1日2回
- 炎症が強い場合:フルメトロン点眼液(0.1%)1日4回
薬剤毒性角膜症
Section titled “薬剤毒性角膜症”- 原因薬剤の中止または変更:抗緑内障薬、NSAIDs、抗菌薬などの候補点眼を中止する。
- 防腐剤無添加製剤への変更:同一薬効で防腐剤フリー製剤がある場合はそちらを選択する。
- 補充療法:防腐剤フリーの人工涙液を頻回点眼する。
- 補助:充血や濾胞性結膜炎が顕著な場合は低濃度ステロイド点眼を考慮するが、創傷治癒遅延に留意する。
神経麻痺性角膜症・糖尿病角膜症・兎眼性角膜症
Section titled “神経麻痺性角膜症・糖尿病角膜症・兎眼性角膜症”- 強制閉瞼(メパッチクリアなど)、保護用ソフトコンタクトレンズの装用を行う。
- ヒアレイン点眼液(0.1%)1日4〜6回。
- タリビッド眼軟膏(0.3%)1日2〜4回点入。
- 重症・遷延例では羊膜移植、自家血清点眼、神経栄養因子関連治療などが検討される。
睫毛乱生・眼瞼内反
Section titled “睫毛乱生・眼瞼内反”- 定期的な睫毛抜去、電気分解を行う。
- 根治のため眼瞼形成手術を施行する。
Thygeson 点状表層角膜炎
Section titled “Thygeson 点状表層角膜炎”- 軽症例:自覚症状が軽ければ経過観察で足りる。
- 有症状例:フルメトロン点眼液(0.1%)1日4回。
- 漸減:再燃を繰り返すため、症状消退後も数ヶ月かけてステロイド点眼を漸減し、週1回〜隔週の維持量まで減量する。
- 代替療法:
- シクロスポリン A 2% 点眼 1日3回、6ヶ月かけて漸減した症例報告があり、3年間の追跡で再発を認めなかった2)。
- タクロリムス点眼・軟膏。
- 治療用ソフトコンタクトレンズ(隆起病変の機械的被覆)。
- 禁忌・無効:イドクスウリジンはゴースト混濁や前部実質瘢痕を引き起こすため使用しない。抗菌薬は無効である。表層角膜切除術(PTK)は部分的改善にとどまり再発率が高いため推奨されない。
いずれもドライアイ診療ガイドラインで使用が推奨されている点眼薬であるが、作用機序が異なる。ジクアホソルナトリウム(ジクアス点眼液3%)は膜結合型ムチン発現と水分分泌を促進し涙液油層伸展を助けるため、BUT 短縮型ドライアイで第一に検討される。レバミピド(ムコスタ点眼液UD 2%)はムチン産生促進に加えて抗炎症作用を有し、眼表面炎症を伴う症例で有用である。いずれもヒアルロン酸ナトリウム点眼と併用され、症例に応じて主治医が選択する3)。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”角膜上皮ターンオーバーの破綻
Section titled “角膜上皮ターンオーバーの破綻”角膜上皮は基底細胞層からのターンオーバーにより恒常的に更新されている。SPK は、最表層細胞の脱落亢進 または 基底細胞からの細胞供給低下 によりターンオーバーのバランスが崩れた初期状態として理解される。実際には多くの症例で前者、すなわち脱落亢進が主因となる。
原因別の分子・細胞機序
Section titled “原因別の分子・細胞機序”- ドライアイ:涙液層の不安定化により眼表面が乾燥し、上皮細胞にストレスが加わる。炎症性サイトカイン(IL-1、TNF-α)と MMP-9 の活性化が上皮バリアを破壊する6)。
- マイボーム腺機能不全:マイボーム腺脂質の質的・量的異常により涙液油層が機能低下し、蒸発亢進と涙液層不安定化を生じる1)。慢性炎症により瞼板内脂腺の閉塞が進行する悪循環が形成される。
- 薬剤毒性:防腐剤ベンザルコニウム塩化物(BAC)が角膜上皮細胞膜のリン脂質層を破壊し、バリア機能を障害する。軽度の上皮障害でもフルオレセインが染み込みやすくなるレイトステイニング像として可視化される。長期暴露は輪部幹細胞機能低下を招く。
- 神経麻痺性角膜症:三叉神経支配の喪失により神経栄養因子(サブスタンス P、CGRP、NGF)の供給が途絶え、上皮の接着性と創傷治癒能が低下する。
Thygeson 点状表層角膜炎の免疫学的機序
Section titled “Thygeson 点状表層角膜炎の免疫学的機序”Thygeson SPK の病巣では、上皮内へのリンパ球を主体とする単核球浸潤が認められる。免疫学的機序を支持する所見として以下が挙げられる。
- HLA-DR3 との関連:罹患者で HLA-DR3 の保有率が有意に高いことが報告されている2)。HLA-DR3 はクラス II 主要組織適合遺伝子複合体(MHC)分子であり、T 細胞への抗原提示を担う。
- ランゲルハンス細胞の侵入:共焦点顕微鏡で基底上皮層へのランゲルハンス細胞侵入が一貫して認められる。抗原提示細胞の活性化が病態形成に関与する。
- 自己免疫疾患との合併:セリアック病、アジソン病、Sjögren 症候群、全身性エリテマトーデスなど HLA-DR3 関連自己免疫疾患との併存例が報告されている2)。
- 免疫抑制薬の奏功:低濃度副腎皮質ステロイド、シクロスポリン A、タクロリムスが有効であり、T 細胞介在性の免疫反応が推定される。
組織学的変化と長期経過
Section titled “組織学的変化と長期経過”Thygeson SPK では細胞内および細胞間浮腫、上皮下神経叢・ボーマン膜・前部実質への微細な変化を認める。これらの変化は疾患の持続期間が長い眼ほど重度となる。ただし通常は病変消退後に瘢痕を残さず、視力予後は良好である。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”Thygeson SPK とセリアック病の免疫遺伝学的関連
Section titled “Thygeson SPK とセリアック病の免疫遺伝学的関連”Tagmouti らは、4年間のセリアック病歴を有する20歳女性に Thygeson SPK が発症した症例を報告した2)。セリアック病は HLA-DQ2 および HLA-DQ8 と強く関連し、患者の90%以上が HLA-DR3 アレルを保有する自己免疫疾患である。Thygeson SPK においても HLA-DR3 との関連が以前から指摘されており、両疾患の免疫遺伝学的関連が示唆される。
Tagmouti らは「Thygeson 点状表層角膜炎の症例では、共通の遺伝的素因を考慮してセリアック病のスクリーニングを検討すべきである」と述べている2)。
この症例ではシクロスポリン A 2% 点眼 1日3回の6ヶ月漸減投与により完全寛解が達成され、3年間の追跡で再発を認めなかった2)。免疫調節療法としてのシクロスポリン点眼の有効性が改めて確認されるとともに、Thygeson SPK と自己免疫疾患の関連を探る今後の研究の重要性が示されている。
ドライアイ治療の進展
Section titled “ドライアイ治療の進展”涙液油層・水層・ムチン層の各層に対する標的治療の発展により、SPK を主訴とする症例に対しても病態ベースの治療選択が広がりつつある。TFOS DEWS III(2025年)では、涙液層の機能的評価と個別化治療戦略が提唱されている6,10)。生物学的製剤、温熱・光治療(IPL)、新規ムチン分泌促進薬などが研究開発中である。
8. 参考文献
Section titled “8. 参考文献”- 天野史郎, 有田玲子, 横井則彦, ほか. マイボーム腺機能不全診療ガイドライン. 日本眼科学会雑誌. 2010;114(6):557-587.
- Tagmouti A, Lazaar H, Benchekroun M, et al. Association Between Thygeson Superficial Punctate Keratitis and Celiac Disease. Cureus. 2025;17(3):e80252.
- ドライアイ研究会診療ガイドライン作成委員会. ドライアイ診療ガイドライン. 日本眼科学会雑誌. 2019;123(4):489-592.
- 有田玲子, 天野史郎, 島﨑潤, ほか. マイボーム腺機能不全の定義と診断基準. あたらしい眼科. 2010;27(5):627-631.
- 日本眼科アレルギー学会. アレルギー性結膜疾患診療ガイドライン(第3版). 日本眼科学会雑誌. 2021;125(7):739-776.
- Jones L, Downie LE, Korb D, et al. TFOS DEWS II Management and Therapy Report. Ocular Surface. 2017;15(3):575-628.
- 日本眼感染症学会 感染性角膜炎診療ガイドライン改訂委員会. 感染性角膜炎診療ガイドライン(第3版). 日本眼科学会雑誌. 2023;127(2):117-204.
- 島﨑潤. ドライアイの定義と診断基準(2016年版). あたらしい眼科. 2017;34(3):309-313.
- Carnt N, Keay L, Willcox M, et al. Contact lens-related adverse events: A review of the literature. Contact Lens and Anterior Eye. 2018;41(5):395-405.
- Craig JP, Nichols KK, Akpek EK, et al. TFOS DEWS II Definition and Classification Report. Ocular Surface. 2017;15(3):276-283.
