眼瞼症状

甲状腺眼症(バセドウ病眼症の眼窩病変)
1. 甲状腺眼症とは
Section titled “1. 甲状腺眼症とは”甲状腺眼症(thyroid eye disease: TED)は甲状腺機能異常に伴う免疫機能異常が眼窩内部組織の炎症を誘発し、眼窩脂肪織と外眼筋の容積を増大させる自己免疫疾患である。球後組織圧の上昇により眼球突出が生じる。甲状腺機能亢進症(Graves病/バセドウ病)に伴う発症が最多だが、甲状腺機能が正常な euthyroid ophthalmopathy としても発症しうる。甲状腺眼症は甲状腺ホルモンとは無関係に進行し、甲状腺関連自己抗体が関与する自己免疫疾患の1つである。
Graves病(バセドウ病)患者の約40〜50%に眼症状が生じる。重症型眼窩病変は全Graves病患者の5〜10%と比較的まれである。
有病率は女性で16/100,000人年、男性で2.9/100,000人年とされる1)。発症年齢は40〜50歳代と60〜70歳代に二峰性のピークを有する1)。喫煙は甲状腺眼症の最大のリスク因子であり、発症リスクを有意に高める2)。若年者は眼球突出が主徴となり、高齢者は複視が主徴となる年齢別パターンが認められる。
甲状腺眼症の自然経過はRundle曲線に従い、活動期(炎症期、通常1〜3年)を経て安定期(非炎症期)へ移行する3)。治療介入のタイミングはこの曲線に基づいて決定される。
4大症状の概観
Section titled “4大症状の概観”眼球突出
若年者に多い(眼窩支持組織の脆弱性)。
Hertel眼球突出計で評価。日本人正常値は10〜15mm(平均13mm)。左右差2mm以内が正常。
複視
高齢者に多い。外眼筋の炎症・線維化による拘束性斜視が原因。
下直筋が最多罹患 → 上転障害が最多。次いで内直筋罹患による外転障害。
視力障害
甲状腺機能が正常な状態でも euthyroid ophthalmopathy として発症しうる。甲状腺眼症は甲状腺ホルモン値とは独立に進行する自己免疫疾患であり、甲状腺関連自己抗体(TRAb, TSAb)が陽性であれば発症しうる。眼瞼後退・眼球突出の所見があれば、甲状腺機能が正常でも甲状腺関連自己抗体の検査が必要である。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”自覚症状の段階的進行
Section titled “自覚症状の段階的進行”早期には乾燥感・刺激感・流涙・羞明が主体である。病態の進行とともに眼窩周囲腫脹・眼球突出・複視・眼瞼後退が顕在化し、重症例では角膜潰瘍・圧迫性視神経症に至る。
甲状腺眼症に特徴的な眼瞼所見を以下に示す。
| 徴候名 | 英語名 | 所見 |
|---|---|---|
| Dalrymple徴候 | Dalrymple sign | 上眼瞼後退による瞼裂開大。上方角膜輪部上方に白目が露出する |
| von Graefe徴候 | lid lag | 下方視時に上眼瞼の追従が遅れる現象 |
| Stellwag徴候 | Stellwag sign | 瞬目の減少と不完全な閉瞼 |
| Gifford徴候 | Gifford sign | 上眼瞼の反転困難 |
眼球突出の評価
Section titled “眼球突出の評価”眼球突出はHertel眼球突出計で測定する。日本人の正常値は10〜15mm(平均13mm)であり、左右差2mm以内が正常である。Hertel値18mm超では眼球突出を示唆する1)。
圧迫性視神経症(DON)
Section titled “圧迫性視神経症(DON)”肥厚した外眼筋が眼窩先端部(orbital apex)で視神経を圧迫することで生じる。全症例の約5%に発症し1)、緊急性が高い。RAPD(相対的求心性瞳孔散大)陽性・CFF(臨界融合頻度)低下・視野障害が早期徴候となる。色覚異常も重要な所見である。
QOLへの影響
Section titled “QOLへの影響”疼痛・複視・外見変化が主たるQOL低下要因である。甲状腺眼症患者の不安・うつ併存率は36%と、一般人口(18.9%)の約2倍に上る5)。中等症患者の62%・重症患者の89%が高いQOL障害(スコア≥4/7点)を有する5)。糖尿病・肺気腫・心不全と同等以下のQOL低下が報告されている。
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”免疫学的機序
Section titled “免疫学的機序”甲状腺機能異常に伴う免疫機能異常が眼窩内部組織の炎症を誘発する。TSH受容体(TSHR)に対する自己抗体(TRAb)が眼窩線維芽細胞上のTSHRを活性化し、炎症性サイトカイン(TNF-α、IL-6、IL-1β等)の産生が惹起される。CD4+/CD8+ T細胞が眼窩組織に浸潤して炎症反応を増幅させる。
活性化した線維芽細胞はグリコサミノグリカン(GAG)・ヒアルロン酸の合成を亢進させ、組織浮腫・保水を引き起こす。線維芽細胞の脂肪細胞・筋線維芽細胞への分化により眼窩脂肪の膨張と外眼筋の線維化が進行する3)。
IGF-1受容体(IGF-1R)はTSHRと複合体を形成し、眼窩線維芽細胞の活性化に相乗的に関与する4)。この機序がテプロツムマブ(IGF-1R阻害薬)の治療標的となっている。
喫煙が最大のリスク因子であり、発症リスク・重症化・治療抵抗性のいずれとも関連する2)。そのほか甲状腺機能の不安定化、放射性ヨード治療後の急性期、高齢・男性も重症化リスクに関与する。
4. 診断と検査方法
Section titled “4. 診断と検査方法”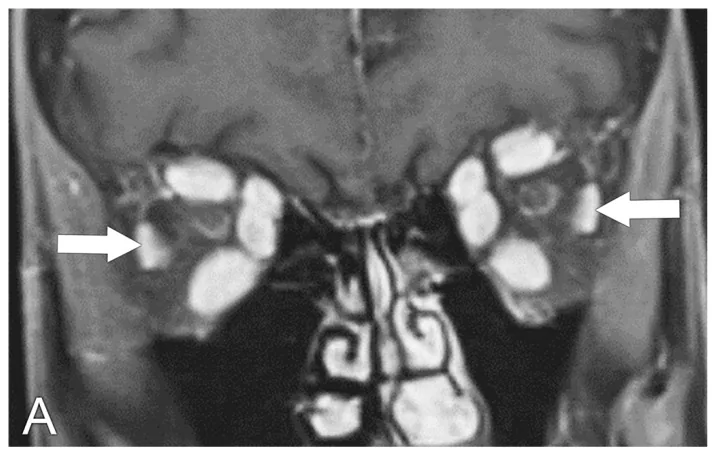
診断のアプローチ
Section titled “診断のアプローチ”眼瞼後退・眼球突出・複視の3徴が揃えば臨床的にTEDを強く示唆する。甲状腺機能が正常であっても甲状腺関連自己抗体が陽性の場合はTEDと診断しうる。
甲状腺ホルモン(FT₄、FT₃)・TSH・甲状腺自己抗体を測定する。測定対象は TRAb(TSH受容体抗体)・TSAb(甲状腺刺激抗体)・抗TG抗体(抗サイログロブリン抗体)・抗TPO抗体(抗甲状腺ペルオキシダーゼ抗体)である。これらのいずれかが陽性となる。
MRI(第一選択):T1強調画像で外眼筋の形態を評価する。STIR(short-TI inversion recovery)法では炎症の部位が高信号領域として描出され、炎症活動性の評価に有用である。冠状断は下斜筋以外の全外眼筋を同時評価できるため必須である。軸位断では内外直筋を評価する。
CT:外眼筋肥厚(腱部は温存され筋腹が肥大するパターンがTED特有)を確認し、眼窩骨壁の評価に骨窓を用いる。
B-scan超音波:外眼筋肥大の評価に補助的に使用する。
CAS(Clinical Activity Score)
Section titled “CAS(Clinical Activity Score)”Mouritsらが1989年に提案した炎症活動性評価の7項目スコアリングシステム(0〜7点)である6)。
評価7項目:①自発性球後部痛、②眼球運動時痛、③眼瞼発赤、④眼瞼腫脹、⑤結膜発赤、⑥結膜浮腫、⑦涙丘/半月ひだ腫脹。
CAS≥3/7で活動期と判定し、ステロイドパルス療法の適応となる。CAS≥4/7がテプロツムマブのRCT組み入れ基準である。
EUGOGO重症度分類と治療方針
Section titled “EUGOGO重症度分類と治療方針”| 重症度 | 基準 | 治療方針 |
|---|---|---|
| 軽症 | 日常生活への影響軽微 | セレニウム補充+経過観察 |
| 中等症〜重症 | 眼瞼後退≥2mm、突出≥3mm over normal、複視あり | ステロイドパルス・テプロツムマブ |
| 視力脅威型 | 圧迫性視神経症・角膜潰瘍 | 緊急眼窩減圧術 or 高用量ステロイド |
EUGOGO(欧州Graves眼症グループ)の2021年版臨床診療ガイドラインによる分類である1)。NOSPECS分類(0〜6クラス)およびVISA分類(Vision・Inflammation・Strabismus・Appearance)も重症度評価に用いられる。
| 鑑別疾患 | 鑑別ポイント | 画像所見 |
|---|---|---|
| IgG4関連眼疾患 | 涙腺腫大+外眼筋腫大、血清IgG4高値 | 涙腺+外眼筋びまん性腫大 |
| 外眼筋炎(眼窩筋炎) | 急性発症、疼痛が強い | 腱部からの肥厚(甲状腺眼症は筋腹肥厚で腱部は温存) |
| 眼窩腫瘍・転移性腫瘍 | 片眼性・進行性 | 腫瘤形成 |
甲状腺眼症の炎症活動性を評価する7項目のスコアリングシステム(0〜7点)である。①自発性球後部痛、②眼球運動時痛、③眼瞼発赤、④眼瞼腫脹、⑤結膜発赤、⑥結膜浮腫、⑦涙丘/半月ひだ腫脹の7項目を評価し、3点以上で活動期と判定する。治療選択の重要な指標となり、ステロイドパルス療法やテプロツムマブの適応判断に用いる。
5. 標準的な治療法
Section titled “5. 標準的な治療法”5-1. 一般管理
Section titled “5-1. 一般管理”甲状腺機能正常化が必須条件であり、内分泌科との連携が不可欠である。禁煙指導は病態増悪・治療抵抗性の最大リスク因子である喫煙を排除するために全症例で実施する。
セレニウム補充:軽症TEDに対し、セレニウム200μg/日を6ヶ月間補充することが疾患活動性改善に有益であり推奨される10)。
角膜・眼表面保護:人工涙液・角膜保護点眼の頻回使用および就眠前眼軟膏点入を基本とする。重度兎眼では外側足根縫合(lateral tarsorrhaphy)を考慮する。
5-2. ステロイド療法(活動期の標準治療)
Section titled “5-2. ステロイド療法(活動期の標準治療)”ステロイドパルス療法(第一選択):メチルプレドニゾロン500〜1,000mg/週を6〜12週間投与する1)。経口ステロイドより静注ステロイドのほうが有効性が高い9)。累積投与量は8g以内を推奨(肝障害リスク軽減)。
標準プロトコル:メチルプレドニゾロン1g×3日間を1クールとして施行する。
経口プレドニゾロン:静注が困難な中等症〜重症例には1mg/kg/日から開始する。
局所ステロイド注射:上眼瞼浮腫・炎症性眼瞼後退に対し、トリアムシノロンアセトニド(ケナコルト-A® 1アンプル)の局所注射が有効である。
5-3. 生物学的製剤・免疫調節療法
Section titled “5-3. 生物学的製剤・免疫調節療法”テプロツムマブ(IGF-1R阻害薬):活動性中等症〜重症TEDに対し、眼球突出・複視の改善が期待できる治療薬である。5つのRCT(計411例)のメタ解析では、眼球突出の有意な減少・24週時CAS 0〜1の達成率の有意な改善・複視改善率の有意な向上が確認されており4)、重篤な有害事象の有意な増加はなかった。Smith et al.(2017年、42例vs45例)7)およびDouglas et al.(2020年、41例vs42例)8)の2つの主要RCTでエビデンスが構築されている。
リツキシマブ(抗CD20モノクローナル抗体):難治性の中等症〜重症TEDで疾患活動性を低下させる可能性が多施設無作為化試験で示されている12)。
トシリズマブ(IL-6受容体阻害薬):ステロイド・リツキシマブ難治例への使用が検討されている。
5-4. 眼窩放射線療法
Section titled “5-4. 眼窩放射線療法”中等症〜重症TEDでは免疫抑制療法との併用として施行する。通常20Gy/10回を2週間かけて照射する。ステロイドとの併用が単独投与より有効とされる。
5-5. 外科的治療(非炎症期)
Section titled “5-5. 外科的治療(非炎症期)”手術は原則としてRundle曲線の安定期に入り炎症が沈静化した後に計画する。施行順序は厳守すべきであり、先行する手術の結果が後続の手術計画に直接影響する。
Step 1: 眼窩減圧術
適応: 重度眼球突出・圧迫性視神経症(緊急適応)
術式と効果: 内側壁・床・外側壁+脂肪の組み合わせによる5種類の術式がある。1壁減圧で-1.4〜-2.3mm、3壁+脂肪減圧で-4.6〜-5.0mmの眼球突出改善が得られる。
633眼の多施設研究で、同一術式間の術者間に有意差なく安定した再現性が確認されている11)。
Step 2: 斜視手術
Step 3: 眼瞼手術
IGF-1受容体(IGF-1R)を阻害するモノクローナル抗体である。眼窩線維芽細胞上のIGF-1RとTSHRの複合体シグナルを遮断し、炎症・組織膨張を抑制する。5つのRCT(計411例)のメタ解析で眼球突出・複視・CASの有意な改善が確認されている。重篤な有害事象の有意な増加はないが、長期安全性(聴覚障害・高血糖等)については引き続き評価中である。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”眼窩組織の病態
Section titled “眼窩組織の病態”甲状腺機能異常に伴う免疫機能異常が眼窩内部組織の炎症を誘発し、眼窩脂肪織と外眼筋の容積を増大させる。球後組織圧の上昇により眼球突出が生じる。
眼窩脂肪織の病態:脂肪細胞の腫大と間質のリンパ球浸潤が生じ、慢性炎症による浮腫と瘢痕形成がみられる。グリコサミノグリカン(GAG)・ヒアルロン酸の合成亢進が組織の液体貯留・腫脹を引き起こす。
外眼筋の病態:横紋筋線維間にリンパ球主体の炎症細胞浸潤がみられ、筋線維は変性壊死を起こす。間質には炎症による浮腫と肥厚が生じ、筋線維間に結合織が増生して外眼筋肥大が形成される。外眼筋が侵される頻度は下直筋が最も多く、内直筋・上直筋・外直筋の順に減少する。このため上転障害が最も多くみられ、次いで外転障害が多い。
上眼瞼後退の発生機序
Section titled “上眼瞼後退の発生機序”2つの機序が複合して生じる。
①上眼瞼挙筋の病態:炎症のため筋細胞に浮腫が生じ眼瞼浮腫となる。筋線維間には脂肪織が侵入し、筋細胞は壊死・瘢痕化して挙筋機能が変化する。
②Müller筋の病態:交感神経支配の平滑筋であるMüller筋は、甲状腺機能亢進症に伴う交感神経亢進により持続収縮し、瞼板を挙上させて瞼裂を開大させる。
免疫シグナル経路
Section titled “免疫シグナル経路”TSH受容体(TSHR)に対する自己抗体(TRAb)が眼窩線維芽細胞上のTSHRを活性化し、下流シグナルを介して炎症性サイトカイン(TNF-α、IL-6、IL-1β)が産生される。CD4+/CD8+ T細胞が眼窩組織に浸潤して炎症反応を増幅させる。活性化された線維芽細胞は脂肪細胞と筋線維芽細胞に分化し、それぞれ眼窩脂肪の膨張と外眼筋の線維化を引き起こす3)。
IGF-1R(IGF-1受容体)はTSHRと複合体を形成し、眼窩線維芽細胞の活性化に相乗的に関与する4)。この複合体シグナルの遮断がテプロツムマブの作用機序である。
Rundle曲線と病期
Section titled “Rundle曲線と病期”炎症活動期(通常1〜3年)から安定期(非炎症期)へ移行する自然経過は、Rundle曲線として概念化されてきた13)。実際の治療介入は、活動性と重症度を評価したうえで選択する1)。活動期には炎症抑制治療を優先し、非炎症安定期に手術計画を立てる。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”テプロツムマブの長期エビデンス
Section titled “テプロツムマブの長期エビデンス”FDA承認後も継続的にデータが蓄積されている。5つのRCT(計411例)のメタ解析4)で有効性・安全性が確認されているが、長期安全性(聴覚障害・高血糖等の長期転帰)についてはPhase IV試験の結果が注目される。非活動期TEDへの適応拡大の可能性も検討されている。
眼窩減圧術の精度向上
Section titled “眼窩減圧術の精度向上”7施設・7術者・633眼の多施設研究11)では、同一術式を施行した場合に術者間の有意差がないことが確認された。これは多施設RCTの統計的妥当性を支持する重要な知見である。内視鏡的内側壁減圧は開放術と比較して内側壁+床減圧において有意に大きな突出度改善(-3.67mm vs -2.97mm、p=0.008)が報告されている。術前の眼球突出度が術後の突出度変化と統計的に有意に関連する(p<0.001)ことも示されており、術前評価の重要性が再確認されている。
バイオマーカーと個別化治療
Section titled “バイオマーカーと個別化治療”TRAb・TSAbの活動期における変動がCASと相関するとされ、バイオマーカーに基づく治療選択の研究が進行中である。トシリズマブ(IL-6阻害薬)についても難治性症例への大規模RCTが待たれる。
8. 参考文献
Section titled “8. 参考文献”-
Bartalena L, Kahaly GJ, Baldeschi L, et al. The 2021 European Group on Graves’ Orbitopathy (EUGOGO) clinical practice guidelines for the medical management of Graves’ orbitopathy. Eur J Endocrinol. 2021;184(4):G43-G67.
-
Prummel MF, Wiersinga WM. Smoking and risk of Graves’ disease. JAMA. 1993;269(4):479-482.
-
Bahn RS. Graves’ ophthalmopathy. N Engl J Med. 2010;362(8):726-738.
-
Cong X, Pei L, Hu H. Teprotumumab for treating active thyroid eye disease: a meta-analysis. Medicine. 2024;103(18):e38059.
-
Wang Y, Sharma A, Padnick-Silver L, et al. Physician-perceived impact of thyroid eye disease on patient quality of life in the United States. Ophthalmol Ther. 2021;10(1):75-87.
-
Mourits MP, Koornneef L, Wiersinga WM, et al. Clinical criteria for the assessment of disease activity in Graves’ ophthalmopathy: a novel approach. Br J Ophthalmol. 1989;73(8):639-644.
-
Smith TJ, Kahaly GJ, Ezra DG, et al. Teprotumumab for thyroid-associated ophthalmopathy. N Engl J Med. 2017;376(18):1748-1761.
-
Douglas RS, Kahaly GJ, Patel A, et al. Teprotumumab for the treatment of active thyroid eye disease. N Engl J Med. 2020;382(4):341-352.
-
Kahaly GJ, Pitz S, Hommel G, et al. Randomized, single blind trial of intravenous versus oral steroid monotherapy in Graves’ orbitopathy. J Clin Endocrinol Metab. 2005;90(9):5234-5240.
-
Marcocci C, Kahaly GJ, Krassas GE, Bartalena L, Prummel M, Stahl M, et al.; European Group on Graves’ Orbitopathy. Selenium and the course of mild Graves’ orbitopathy. N Engl J Med. 2011;364(20):1920-1931. PMID: 21591944. doi:10.1056/NEJMoa1012985.
-
Hong A, Shoji MK, Villatoro GA, et al. Intersurgeon variability in proptosis reduction after orbital decompression for thyroid eye disease: a multicenter analysis. Ophthalmic Plast Reconstr Surg. 2024;40(3).
-
Salvi M, Vannucchi G, Campi I, et al. Rituximab treatment in active moderate-to-severe Graves’ orbitopathy: an international, multicenter, single-blind, randomized placebo-controlled study. J Clin Endocrinol Metab. 2015;100(11):422-431.
-
Rundle FF, Wilson CW. Development and course of exophthalmos and ophthalmoplegia in Graves’ disease with special reference to the effect of thyroidectomy. Clin Sci. 1945;5(3-4):177-194. PMID: 21011937.
