眼窩先端部型
好発部位:眼窩先端部(視神経孔・上眼窩裂周囲)
主症状:視力低下・強い疼痛・眼球運動障害
特記事項:5型中最重症。視神経に近接するため視神経障害のリスクが高い。感染症(特に真菌)との鑑別が必須。

眼窩組織には、感染症ではない非特異的な急性〜亜急性の炎症性病変がしばしば発生する。この病態は以下の3条件を同時に満たすことを特徴とする。
この病態は従来「眼窩炎性偽腫瘍」と呼ばれてきた。腫瘍を形成したかのように眼球突出・眼瞼腫脹をきたすことから名付けられた古い時代の用語である。画像診断技術が限られていた時代の名称であり、MRIを駆使すれば炎症性病変を見抜くことが比較的容易となった現在では不適切な用語とされ、特発性眼窩炎症(idiopathic orbital inflammation; IOI) という診断名に置き換えられつつある1)。
眼窩原発腫瘍の中で最多を占めるのはリンパ増殖性疾患群であり、眼窩腫瘍全体の50〜60%を占める。このリンパ増殖性疾患群には悪性リンパ腫、反応性リンパ過形成、IgG4関連眼疾患(IgG4-ROD)、そして特発性眼窩炎症が含まれる。IOIは全眼窩腫瘤性病変の約8〜10%を占めると報告されている1,2)。
近年、IgG4関連眼疾患が独立した疾患として確立されたことにより、かつてIOIに含まれていた症例群が再分類され、IOIの疾患概念は縮小・精緻化されている。現在のIOIは、これらの特異的疾患を除外した後に残る「真の非特異的炎症」を指す3,4)。
急性〜亜急性に発症することが多く、以下の症状を呈する。
病巣は眼窩内をびまん性に広がることはまれで、涙腺・外眼筋・眼球周囲・眼窩先端部を中心とし、比較的境界不鮮明に広がることが多い。
CT/MRI画像所見をもとに、炎症の発生部位によって前部眼窩型・びまん性型・眼窩先端部型・筋組織型・涙腺型の5型に分類される1,2)。
眼窩先端部型
好発部位:眼窩先端部(視神経孔・上眼窩裂周囲)
主症状:視力低下・強い疼痛・眼球運動障害
特記事項:5型中最重症。視神経に近接するため視神経障害のリスクが高い。感染症(特に真菌)との鑑別が必須。
筋組織型(眼窩筋炎)
涙腺型
局在型別の特徴を以下に示す。
| 型 | 好発部位 | 主症状 | 特記事項 |
|---|---|---|---|
| 前部眼窩型 | 眼球周囲 | 眼瞼腫脹・結膜充血 | — |
| びまん性型 | 眼窩脂肪組織 | 眼球突出 | びまん性病巣。まれ |
| 先端部型 | 眼窩先端部 | 視力低下・強い疼痛 | 最重症。感染との鑑別必須 |
| 筋組織型 | 外眼筋 | 眼球運動障害・複視 | 予後良好 |
| 涙腺型 | 涙腺 | 涙腺腫脹・疼痛 | IgG4-RODとの鑑別 |
眼窩先端部型が最も重症である。視神経に近接するため視力低下のリスクが高く、強い疼痛を伴う。また慢性型(特発性硬化性眼窩炎症)は高度な線維化のためステロイド反応性が乏しく難治性となる。外眼筋に局在する筋組織型は一般に予後が良好である。
眼窩原発腫瘍の中でリンパ増殖性疾患群(悪性リンパ腫・反応性リンパ過形成・IgG4関連眼疾患・IOIを含む)は最多を占め、眼窩腫瘍全体の50〜60%を占める。その中で特発性眼窩炎症は成人の良性眼窩疾患の代表的疾患の一つである。
IgG4関連眼疾患が独立疾患として確立された結果、従来IOIと診断されていた症例の一部が再分類され、純粋なIOIの頻度は縮小している。海外の報告では中年成人(40〜60歳代)に好発するとされているが、日本国内での詳細な疫学データは限られている。性差についても一定の傾向を示す大規模なデータは乏しい。
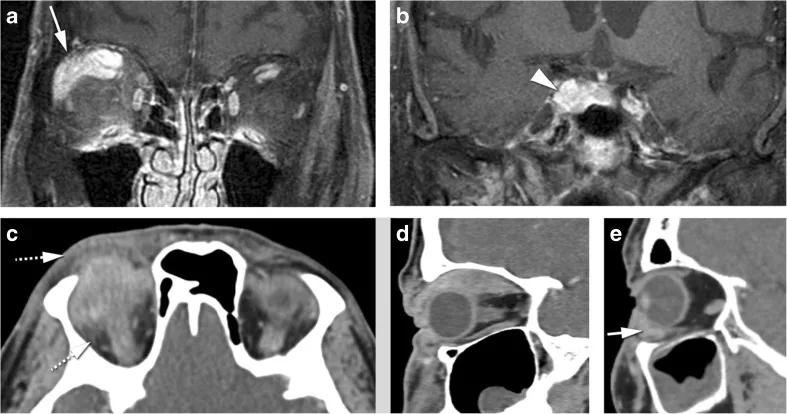
急性〜亜急性に発生する眼瞼腫脹・眼球突出・眼球偏位が認められた場合、CTおよびMRIによる画像診断を行う。
臨床的には、画像診断で特発性眼窩炎症が疑われた場合にステロイドの試験的投与を行い、著効すれば臨床診断が確定する方針が一般的である。
急性期・治療前の生検は、治療後に眼球運動障害などの後遺症を起こしやすいため、避けるのが一般的である。ただし以下の場合には生検を検討する。
特に感染性疾患(眼窩蜂巣炎)と悪性疾患(MALTリンパ腫)との鑑別が重要である。Aryasitら(2021)の報告では、IOIと初期診断された45例のうち21例(46.7%)の組織にIgG4陽性形質細胞浸潤が確認されており、組織学的再評価とIgG4免疫染色が強く推奨されている4)。
| 鑑別疾患 | 鑑別のポイント |
|---|---|
| 眼窩蜂巣炎 | 感染性。発熱・白血球増多。CT/血液検査で鑑別 |
| IgG4関連眼疾患 | IgG4陽性形質細胞の浸潤。血清IgG4高値。組織学的に鑑別 |
| 甲状腺眼症 | 甲状腺機能異常。外眼筋腫大(筋腹のみ、腱付着部は温存)。亜急性経過 |
| 多発血管炎性肉芽腫症(GPA) | ANCA陽性。壊死性肉芽腫。多臓器病変 |
| MALTリンパ腫 | 緩慢な経過。生検で確定。IgH遺伝子再構成検査 |
| 副鼻腔囊胞穿破 | 急性発症。CT画像で副鼻腔病変を確認 |
感染症である眼窩蜂巣炎や副鼻腔囊胞の眼窩内穿破は、急性に眼瞼腫脹・眼球突出・眼球偏位をきたす疾患として鑑別が重要である。血液検査所見やCT等の画像検査で鑑別を進める。亜急性に進行する眼窩疾患としては、甲状腺眼症や多発血管炎性肉芽腫症などの特異的な眼窩炎症性疾患が鑑別に挙げられる。
第一選択はステロイド内服療法である。ただし疼痛などの症状が強くなければ、自然寛解がみられることもあるため経過観察という選択肢もある。
ステロイド開始前に感染症(特に眼窩先端部の真菌感染)を十分に除外することが必須である。
プレドニゾロン 0.25〜1.0 mg/kg/日で開始し、3〜6ヶ月の投薬中止を目処に漸減する1,3)。漸減中の再発はしばしば経験される。漸減を急ぐと再発リスクが高まるため、十分な期間をかけて緩やかに漸減することが重要である。
処方例を以下に示す。
| 薬剤 | 用法・用量 | 備考 |
|---|---|---|
| プレドニゾン錠 5mg | 1日6錠 分2(朝4錠・昼2錠 食後) | 経過をみて漸減。3〜6ヶ月で中止目標 |
| カスターD錠 10mg(アルファカルシドール) | 1日2錠 分2(朝夕食後) | ステロイド性骨粗鬆症予防として併用 |
再発を繰り返す難治例には以下の治療が試みられる。
ステロイドに対する反応性は良好である。十分な治療により再発なく鎮静化できる場合が多い。ただし漸減を急ぐと再発しやすいため、十分な経過観察が必要である。外眼筋に局在するもの(特発性眼窩筋炎)は一般に予後が良好である。まれに遷延性の難治例となることがある。
本疾患は原因不明の非特異的炎症であり、ステロイドは炎症を抑制するが根本原因を除去しない。そのため漸減に伴い炎症が再燃しやすい。3〜6ヶ月をかけて緩やかに漸減することが再発予防に重要である。難治例や頻回再発例では放射線治療や免疫抑制薬への変更を検討する。
特発性眼窩炎症の病因は不明である。眼窩組織への原因不明の非特異的炎症として位置づけられる。
組織学的には非特異的な炎症細胞浸潤(リンパ球・形質細胞主体)を示す。特定の原因微生物や特異的な自己抗体は同定されていないが、自己免疫的機序の関与が推測されている。
炎症は眼窩内をびまん性に広がることはまれで、涙腺・外眼筋・眼球周囲・眼窩先端部など特定の部位に好発し、比較的境界不鮮明に広がることが多い。この部位選択性の機序については未解明の部分が多い。
特発性硬化性眼窩炎症は、高度な線維化を伴う慢性型の亜型である。線維芽細胞の活性化と膠原線維の過剰沈着が病変の主体であり、ステロイド反応性が乏しく予後不良となる。
歴史的に「眼窩偽腫瘍」として一括されていた病変群から、IgG4関連眼疾患とMALTリンパ腫が独立疾患として確立され、残った非特異的炎症が狭義のIOIとして位置づけられている。現在のIOIは、これら特異的疾患を除外した後に残る「真の非特異的炎症」を指す概念である。
反応性リンパ過形成との区別も課題であり、特にIgG4関連眼疾患が独立疾患として確立されたことで、リンパ増殖性病変のほとんどはIgG4-RODまたはMALTリンパ腫として再分類されるようになった。
IgG4関連疾患の独立疾患化に伴い、IOIの疾患概念は縮小・精緻化されている。分子生物学的手法(フローサイトメトリー・免疫組織化学・IgH遺伝子再構成検査など)の進歩により、以前はIOIに分類されていた症例がより精密に鑑別・分類されるようになった。今後、IOIの病因解明につながる分子マーカーの同定が期待される。
特発性硬化性眼窩炎症(sclerosing variant)はステロイド抵抗性を示すことが多く、治療に難渋する。メトトレキサートやミコフェノール酸モフェチルなどの免疫抑制薬の有効性に関するエビデンス蓄積が進んでいる。
リツキシマブ(抗CD20抗体)などの生物学的製剤がIOIの難治例に試みられている。Suhlerら(2014)の第1/2相無作為化臨床試験では、ステロイドおよび他の免疫抑制薬抵抗性の眼窩炎症10例中7例で24週時点での改善が確認され、ステロイド減量にも成功している6)。ただしIgG4-RODとの診断的重複もあり、IOI単独での大規模なエビデンスは蓄積途上である。今後の臨床研究による有効性の検証が必要である。