炎症期の評価
CAS(Clinical Activity Score)1)
7項目: 自発性球後痛・注視時疼痛・眼瞼発赤・結膜充血・結膜浮腫・涙丘腫脹・眼瞼浮腫
CAS≥3/7: 活動期と判定。ステロイドパルス療法の適応。
画像: MRI STIR法で高信号(炎症活動性の指標)

眼窩減圧術(orbital decompression surgery)は、甲状腺眼症(thyroid eye disease: TED)に伴う眼球突出や圧迫性視神経症に対して行う手術である。眼窩壁(内側壁・下壁・外側壁)を骨削除し、眼窩内の脂肪組織を必要に応じて切除することで眼窩容積を拡大し、眼球を後方に復位させる。
甲状腺眼症は甲状腺機能亢進症(Graves病/バセドウ病)に伴い発症する場合と、甲状腺機能が正常なeuthyroid ophthalmopathyとして発症する場合がある。甲状腺眼症は基本的に甲状腺ホルモンとは無関係に進行し、甲状腺関連自己抗体が関与する自己免疫疾患の1つである。眼窩脂肪組織と外眼筋の容積増大により眼窩内圧が上昇し、眼球突出が生じる。
眼窩減圧術には大きく2つの目的がある。
整容的目的:薬物療法でも改善が得られない著明な眼球突出の軽減。容貌の変化や社会生活への支障が適応の判断基準となる。
視機能保存:肥大した外眼筋が眼窩先端部(orbital apex)で視神経を圧迫する圧迫性視神経症(dysthyroid optic neuropathy: DON)の解除。緊急適応となりうる最重要の手術目的である。
眼窩減圧術は薬物治療に反応しない視神経障害や著明な眼球突出に対して行われる。炎症期(活動期)においては、ステロイドパルス療法や放射線療法を先行させるのが原則である。圧迫性視神経症が高度な場合は炎症期であっても緊急に眼窩減圧術を施行するが、術後にステロイド治療を継続して消炎を図る。
すべての眼球突出に手術が必要なわけではない。炎症期にはステロイドパルス療法(メチルプレドニゾロン500〜1,000mg/日×3日間を1クール)や放射線療法が第一選択であり、多くの症例で炎症の鎮静化と症状の改善が得られる。眼窩減圧術は薬物治療に反応しない視神経障害や著明な眼球突出に対して行われる確立した治療選択肢である。
甲状腺眼症の臨床症状は眼瞼症状・眼球突出・複視・視力障害の4つに分類される。若年者では眼球突出が主体となり、高齢者では眼球運動障害・複視が生じやすい。
視力障害には、角膜障害による視力低下と肥大した外眼筋による圧迫性視神経症による視力低下の2種類がある。下直筋と内直筋が罹患筋となることが多いため、上下斜視と内斜視をきたしやすい。
| 徴候名 | 所見 |
|---|---|
| Graefe(グレーフェ)徴候 | 下方視時の上眼瞼下降不全(lid lag) |
| Dalrymple(ダルリンプル)徴候 | 上眼瞼後退による瞼裂開大 |
| Stellwag(ステルヴァーク)徴候 | 瞬目の減少と不完全な閉瞼 |
| Gifford(ギフォード)徴候 | 上眼瞼の反転困難 |
炎症期(活動期):球後組織の浮腫・炎症が主体。ステロイドパルス療法・放射線療法が優先される。眼窩減圧術は圧迫性視神経症が高度な緊急時のみ適応となる。
非炎症期(慢性期):炎症が沈静化し、固定した眼球突出・眼球運動障害・視神経症が残存する時期。眼窩減圧術の主たる適応時期である。
CAS(Clinical Activity Score)は甲状腺眼症の炎症活動性を評価する7項目のスコアリングシステムである1)。7項目中3点以上で活動期と判定し、薬物治療の適応となる。
EUGOGO(欧州Graves眼症グループ)の重症度分類では、軽症・中等症〜重症・視力脅威型(sight-threatening)の3段階に分類される8)。視力脅威型は圧迫性視神経症または角膜潰瘍を指し、緊急介入の対象となる。
眼窩内球後組織の線維芽細胞内に存在するTSH受容体(TSHR)が抗原となって眼窩組織にリンパ球の浸潤を促し、マクロファージを活性化させ、眼局所でのサイトカインネットワークにより炎症反応が活性化する。これにより眼窩内容積が増大し、眼球突出・眼窩内圧上昇・圧迫性視神経症が生じる。
甲状腺眼症はGraves病(バセドウ病)患者の25〜50%に合併する3)。視力を脅かす圧迫性視神経症は全症例の約3〜5%に発症する。
下直筋と内直筋が最も高頻度に罹患する。外眼筋の侵犯は下直筋が最多であり、内直筋・上直筋・外直筋の順に減少する。このため上転障害が最も多くみられ、次いで外転障害が多い。
喫煙は甲状腺眼症の最大のリスク因子であり、発症リスク・重症化・治療抵抗性のいずれとも関連する。633眼・386名の多施設研究では喫煙率が16.2〜71.1%と施設間で幅広いが、喫煙は眼症の重症度を増悪させるものの、減圧術の突出度減少効果自体には有意な影響がなかった4)。
甲状腺関連自己抗体のいずれかが陽性の場合に診断が確立される。測定対象はTSH受容体抗体(TRAb)・甲状腺刺激抗体(TSAb)・抗TG抗体(TgAb)・抗TPO抗体(TPOAb)である。甲状腺機能が正常であっても、眼球突出・眼瞼後退・複視の所見があれば検査を行う。
Hertel眼球突出計にて眼球突出度を測定する。日本人の正常値は10〜15mm(平均13mm)であり、それを超えるものを眼球突出と判定する。左右差は2mm以内が正常である。術前・術後の評価に標準的に用いられる。
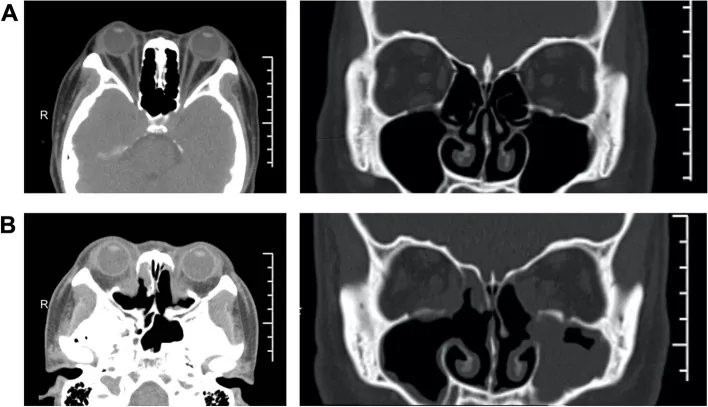
MRI(第一選択):T1強調画像で外眼筋の形態を評価する。STIR(short-TI inversion recovery)法は炎症の部位が高信号領域として描出され、炎症活動性の評価に有用である。冠状断では下斜筋以外の全外眼筋を同時評価できるため必須である。
CT:外眼筋の肥厚を確認する(腱の肥厚は軽度で筋腹が肥厚するため全体に紡錘形を呈する)。眼窩骨壁の評価・手術計画に骨窓CTを用いる。減圧術前の眼窩断面積(上眼窩裂前方約1.5cmの冠状断CT断面積)の測定が術後突出度変化の予測に用いられる4)。
RAPD(relative afferent pupillary defect)陽性・CFF(critical flicker frequency:限界フリッカ値)の低下・色覚異常・視野障害が圧迫性視神経症の早期徴候となる。これらが確認された場合は緊急の対応が必要である。
炎症期の評価
CAS(Clinical Activity Score)1)
7項目: 自発性球後痛・注視時疼痛・眼瞼発赤・結膜充血・結膜浮腫・涙丘腫脹・眼瞼浮腫
CAS≥3/7: 活動期と判定。ステロイドパルス療法の適応。
画像: MRI STIR法で高信号(炎症活動性の指標)
非炎症期の評価
甲状腺機能亢進症があれば甲状腺ホルモンの正常化が必須前提であり、内分泌科との緊密な連携が求められる。手術はRundle曲線の安定期(非炎症期)に入り炎症が沈静化した後に計画する。施行順序は眼窩減圧術→斜視手術→眼瞼手術であり、先行する手術の結果が後続の手術計画に直接影響するため、この順序を厳守する。
ステロイドパルス療法(第一選択):メチルプレドニゾロン500〜1,000mg/日×3日間を1クールとして施行する。症状を見ながら1週間おきに2〜3クール行った後、点滴や内服で漸減する。
局所ステロイド注射:肥大した外眼筋周囲のTenon囊下にステロイド注射を行う。上眼瞼浮腫・炎症による眼瞼後退に対しては、トリアムシノロンアセトニド(ケナコルト-A® 1アンプル)の局所注射が有効である。
放射線療法:ステロイド治療が行えない場合や再燃した場合に適応となる。球後組織に1.5〜2.0Gy/日を10日間照射する。
テプロツムマブ(IGF-1R抗体):海外で眼球突出の有意な改善が報告された生物学的製剤である5)。IGF-1受容体を阻害し、眼窩線維芽細胞の活性化を抑制する機序を持つ。現時点では日本未承認であり、研究段階の治療選択肢に位置づけられる。
眼窩壁の切除範囲と脂肪切除の組み合わせにより、主に5つの術式に分類される。633眼の多施設研究(7術者)による術式別の突出度減少量は以下のとおりである4)。
| 術式 | 壁数 | 突出度減少量(平均) |
|---|---|---|
| 内側壁のみ | 1壁 | 1.4〜2.3mm |
| 脂肪+外側壁 | 2壁 | 2.9〜3.6mm |
| 内側壁+下壁 | 2壁 | 2.6〜3.7mm |
| 脂肪+外側壁+内側壁 | 3壁 | 3.1〜3.9mm |
| 脂肪+外側壁+内側壁+下壁 | 3壁+脂肪 | 4.6〜5.0mm(最大効果) |
壁数の増加に伴い突出度減少量が増大する。重症度に応じた段階的減圧(graded decompression)が術式選択の基本原則であり2)6)、整容目的か視神経保護目的かによっても術式が決定される。術前突出度が高いほど術後の改善量も大きくなることが統計的に有意に示されている(p<0.001)4)。
| 順序 | 手術 | 時期 |
|---|---|---|
| 1 | 眼窩減圧術 | 非炎症期(圧迫性視神経症では緊急施行も) |
| 2 | 斜視手術 | 減圧術後の斜視が安定した後 |
| 3 | 眼瞼手術 | 最後に行う |
斜視手術:慢性期に固定した斜視に対し、肥厚した直筋の後転を主体に施行する。眼窩減圧術後に新規複視が出現する場合があり、斜視が安定した後に手術計画を立てる。
眼瞼手術:眼瞼後退に対し、炎症による場合はトリアムシノロンアセトニド局所注射を行う。非炎症安定期の固定した眼瞼後退には後退修正術(Müller筋切除術・上眼瞼挙筋後転術)を施行する。
術式により異なる。1壁減圧(内側壁のみ)で1.4〜2.3mm、3壁+脂肪減圧(最大術式)で4.6〜5.0mmの突出度減少が期待できる4)。壁数増加に伴い効果が増大し、術前の突出度が高いほど術後の改善量も大きくなる傾向がある。重症度に応じた段階的減圧(graded decompression)が推奨される6)。
眼窩内球後組織の線維芽細胞内に存在するTSH受容体が抗原となって眼窩組織にリンパ球の浸潤を促し、マクロファージを活性化させ、眼局所でのサイトカインネットワークにより炎症反応が活性化する。炎症性サイトカイン(IL-1、IL-6、TNF-α)が産生され、眼窩内容積の増大が進行する。
脂肪組織の変化:脂肪細胞の腫大と間質のリンパ球浸潤が生じ、慢性炎症による浮腫と瘢痕形成がみられる。グリコサミノグリカン(GAG)・ヒアルロン酸の合成亢進が組織の液体貯留・腫脹を引き起こす。
外眼筋の変化:横紋筋線維間にリンパ球主体の炎症細胞浸潤がみられ、筋線維は変性壊死を起こす。間質には炎症による浮腫と肥厚が生じ、筋線維間に結合織が増生して外眼筋肥大が形成される。CT/MRI上では腱の肥厚は軽度で筋腹が肥大するため全体に紡錘形を呈する。
眼窩内容積の増大による眼窩内圧上昇と外眼筋の肥厚が、眼窩先端部(orbital apex)で視神経を圧迫する。RAPD陽性・CFF低下・視野障害が徴候となる。この機序が眼窩減圧術(眼窩容積拡大)による視神経圧迫解除の根拠となる。
IGF-1受容体(IGF-1R)は眼窩線維芽細胞上でTSHRと複合体を形成し、眼窩線維芽細胞の活性化に相乗的に関与する5)。この複合体シグナルの遮断がテプロツムマブの作用機序であり、海外での眼球突出改善という治療成果の理論的基盤となっている。
眼窩壁を削除することで眼窩と隣接する副鼻腔(篩骨洞・上顎洞・蝶形骨洞)の間の骨隔壁がなくなり、眼窩内脂肪が副鼻腔側に脱出して眼窩内容積が拡大する。これにより眼窩内圧が低下し、眼球が後方に移動する。脂肪切除を組み合わせることで減圧効果をさらに高めることができる。
Hong et al.(2025)の7施設・7術者・633眼を対象とした多施設後方視的研究では、同一術式を施行した場合の術者間突出度減少量に有意差がないことが確認された4)(標準誤差0.14〜0.56mm)。標準化された術式の再現性が多施設レベルで示されたことは、多施設RCTの統計的妥当性を支持する重要な知見である。
また、術前眼球突出度が術後の突出度変化を予測する最も有意な因子であることが示されており(p<0.001)、術前評価の重要性が再確認されている4)。
同研究では術式ごとにアプローチ法の効果も検討された。内側壁+下壁減圧においては内視鏡群が開放術より有意に大きい突出度減少を示した(-3.67mm vs -2.97mm、p=0.008)。一方、脂肪+外側壁+内側壁減圧では内視鏡と開放術の間に有意差はなかった4)。
テプロツムマブ(IGF-1R抗体)は海外での眼球突出の有意な改善が報告されている生物学的製剤である5)。日本では現時点で未承認であるが、国際的には活動期中等症〜重症甲状腺眼症に対する薬物療法として位置づけられている。長期安全性(聴覚障害・高血糖等)についてはPhase IV試験の結果が注目される。
減圧術後の新規複視発生を予測するモデルが開発されており7)、術前カウンセリングや術式選択に活用されることが期待される。
喫煙は甲状腺眼症の重症度を増悪させる最大のリスク因子であるが、633眼の研究では減圧術による突出度減少効果自体には喫煙の有意な影響がなかった4)。治療効果の予測において喫煙の役割が精緻化されている。
Mourits MP, Prummel MF, Wiersinga WM, et al. Clinical activity score as a guide in the management of patients with Graves’ ophthalmopathy. Clin Endocrinol (Oxf). 1997;47:9-14.
Mourits MP, Bijl H, Altea MA, et al; European Group on Graves’ Orbitopathy (EUGOGO). Outcome of orbital decompression for disfiguring proptosis in patients with Graves’ orbitopathy using various surgical procedures. Br J Ophthalmol. 2009;93:1518-1523.
Bahn RS, Heufelder AE. Pathogenesis of Graves’ ophthalmopathy. N Engl J Med. 1993;329:1468-1475.
Hong A, Shoji MK, Villatoro GA, et al. Intersurgeon variability in proptosis reduction after orbital decompression for thyroid eye disease: a multicenter analysis. Ophthalmic Plast Reconstr Surg. 2025. [Epub ahead of print].
Rootman DB. Orbital decompression for thyroid eye disease. Surv Ophthalmol. 2018;63:86-104.
Kikkawa DO, Pornpanich K, Cruz RC Jr, Levi L, Granet DB. Graded orbital decompression based on severity of proptosis. Ophthalmology. 2002;109(7):1219-1224. doi:10.1016/S0161-6420(02)01068-0.
Nair AA, Ediriwickrema LS, Dolman PJ, et al. Predictive modeling of new-onset postoperative diplopia following orbital decompression for thyroid eye disease. Ophthalmic Plast Reconstr Surg. 2022;38(6):551-557. PMID:35551414. doi:10.1097/IOP.0000000000002196.
Bartalena L, Kahaly GJ, Baldeschi L, Dayan CM, Eckstein A, Marcocci C, et al; EUGOGO. The 2021 European Group on Graves’ orbitopathy (EUGOGO) clinical practice guidelines for the medical management of Graves’ orbitopathy. Eur J Endocrinol. 2021;185(4):G43-G67. PMID:34297684. doi:10.1530/EJE-21-0479.