甲状腺眼症(最多)
機序: 上眼瞼挙筋への炎症性脂肪浸潤→筋細胞壊死瘢痕化+Müller筋の交感神経過緊張による異常持続収縮。
特徴: 両眼性または片眼性。甲状腺機能の異常がない場合も発症しうる。
鑑別要点: 眼球突出・外眼筋障害・甲状腺自己抗体陽性。

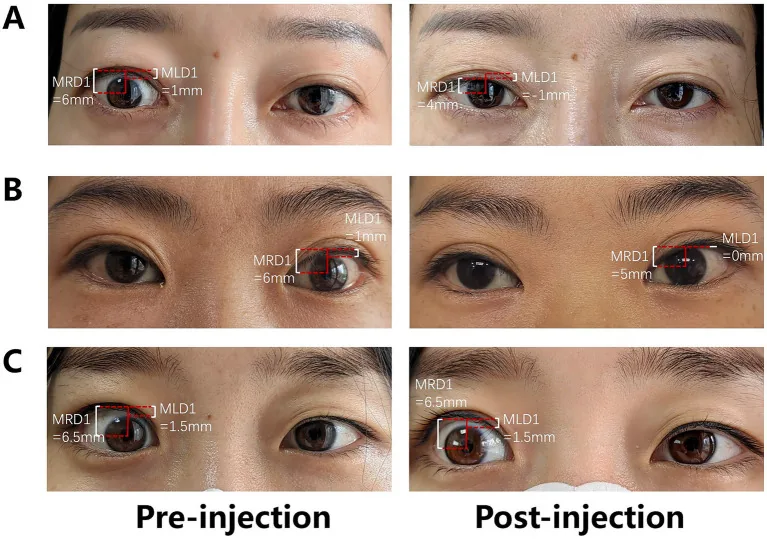
第1眼位において通常、上眼瞼縁は角膜上方輪部から1〜2mm下の位置にある。上眼瞼縁と角膜上方輪部の間に強膜が確認できた状態を上眼瞼後退という。MRD-1(角膜中央光反射から上眼瞼縁までの距離)が5.5mmを超える場合を上眼瞼後退の目安とする。下眼瞼後退はMRD-2の増大として評価する。眼瞼後退が生じると角膜の露出が問題となり、対症療法だけでなく手術が必要となることもある。
眼瞼後退は甲状腺眼症(thyroid eye disease: TED)の最も多い徴候である6)。TEDの有病率は女性で16/100,000人/年、男性で2.9/100,000人/年とされる1)。発症年齢は40〜50歳代と60〜70歳代に二峰性のピークを有し3)、喫煙が重要なリスク因子として知られている5)。甲状腺眼症患者の過半数に眼瞼後退が合併すると推定され、視機能・整容の両面でQOLに大きな影響を与える1)。
眼瞼後退(MRD-1 > 5.5mm)と眼瞼下垂(MRD-1 < 3.5mm)は正反対の病態である。甲状腺眼症では患眼に眼瞼後退が生じる一方、片側性の眼瞼下垂があるとHeringの法則により対側の眼瞼が相対的に後退して見えることがある。この偽性眼瞼後退との鑑別は治療方針決定に不可欠である。
甲状腺眼症の経過はRundle曲線に従い、炎症活動期から安定期へと移行する6)。早期には眼周囲の乾燥感・刺激感が主体であり、中間期に眼瞼後退・眼球突出・複視が顕在化し、重症例では角膜露出・圧迫性視神経症に至る3)。炎症活動性の評価にはCAS(Clinical Activity Score)が用いられ、7項目中3点以上を活動期と判定する1)。
| 徴候 | 甲状腺眼症 | 中脳性 | 瘢痕性 |
|---|---|---|---|
| 眼瞼後退 | ○(両眼/片眼) | ○(両眼性が多い) | ○(術後・外傷眼) |
| Dalrymple徴候 | ○ | − | − |
| von Graefe徴候 | ○ | − | − |
| 上方注視麻痺 | − | ○(Parinaud症候群) | − |
| 眼球突出 | ○ | − | − |
| 既往 | 甲状腺疾患 | 頭蓋内疾患 | 眼瞼手術・外傷 |
甲状腺眼症(最多)
機序: 上眼瞼挙筋への炎症性脂肪浸潤→筋細胞壊死瘢痕化+Müller筋の交感神経過緊張による異常持続収縮。
特徴: 両眼性または片眼性。甲状腺機能の異常がない場合も発症しうる。
鑑別要点: 眼球突出・外眼筋障害・甲状腺自己抗体陽性。
瘢痕性
中脳性
機序: 中脳上背側の疾患(松果体腫瘍・水頭症)による後交連圧迫→Collier’s sign。
特徴: 両眼性眼瞼後退+上方注視麻痺(Parinaud症候群の一部)。
鑑別要点: MRI/CT で頭蓋内病変を確認する。緊急対応が必要な場合がある。
随意的・その他
EUGOGO(欧州Graves眼症グループ)による重症度分類では、軽症・中等症〜重症・視力脅威の3段階に分類する1)。NOSPECS分類では0〜6クラスで評価し、外眼筋障害・角膜障害・視神経障害の有無が重症度を規定する4)。視力脅威型(圧迫性視神経症・角膜分解)は緊急介入の対象となる。
MRD-1測定は上眼瞼後退の基本的定量法である。角膜中央光反射から上眼瞼縁までの距離を計測し、5.5mmを超える場合に上眼瞼後退と判定する。前頭筋の代償を排除するため前額部を軽く固定して測定する。MRD-2は角膜中央光反射から下眼瞼縁までの距離であり、下眼瞼後退の評価に用いる。
Hertel眼球突出計では正常18mm未満とされるが、TED患者では21mmを超えることが多い3)。眼球突出の程度は眼瞼後退の重症度と相関する傾向がある。
フルオレセイン染色による点状表層角膜炎(SPK)の評価を行う。兎眼による角膜下方の露出部位に一致したSPKが特徴的であり、治療必要性と緊急度の判断に用いる。
甲状腺眼症が疑われる場合、MRIまたはCTによる眼窩検査を行う。CT所見では外眼筋の紡錘形腫大が特徴的であり、筋腹が肥大して腱付着部は温存されることがTED特有のパターンである4)。MRIはMüller筋・上眼瞼挙筋の評価、炎症活動性の評価(T2強調画像での高信号)に有用である。中脳性が疑われる場合は頭部MRI/CT(松果体腫瘍・水頭症の除外)を施行する。
甲状腺機能検査(FT4、FT3、TSH)および自己抗体検査(TRAb、TSAb、TgAb、TPOAb)を実施する。眼瞼後退を呈する患者の一部は甲状腺機能が正常であってもTEDである場合があり、自己抗体の確認は不可欠である6)。
臨床診断が基本であり、眼瞼後退+眼球突出+複視の三徴が揃えばTEDを強く示唆する6)。
Dalrymple徴候は第1眼位(正面視)での瞼裂開大であり、上方角膜輪部上方に強膜が露出する。von Graefe徴候は下方視時に上眼瞼の追従が遅れる現象(lid lag)である。いずれも甲状腺眼症に特徴的な所見であり、MRD-1測定と組み合わせて眼瞼後退の診断・重症度評価に用いる。
角膜保護が治療の基本である。
炎症による眼瞼後退に対し、ステロイド治療が有効である。
局所注射:上眼瞼浮腫・炎症性眼瞼後退にはトリアムシノロンアセトニド(ケナコルト-A® 1アンプル)の局所注射が有効である。
ステロイドパルス療法:炎症期の適応であり、メチルプレドニゾロン1g×3日間を1クールとして施行する。
静注ステロイド(IV methylprednisolone):500〜1000mgを週1回、6〜12週間投与する方法は経口ステロイドより有効性が高い5)。炎症活動期(CAS ≥ 3)の中等症〜重症TEDに適応となる。
近年、TEDに対する生物学的製剤が登場している。
テプロツムマブ(IGF-1R阻害薬):中等症〜重症の活動性TEDを対象とした第2相試験2)および第3相RCT7)で眼球突出・複視の有意な改善が示された。眼瞼後退の改善も報告されており、炎症活動期の有望な治療選択肢である。
リツキシマブ(抗CD20モノクローナル抗体):中等症〜重症TEDへの使用で疾患活動性の低下が報告されている3)。B細胞を標的とした免疫抑制により炎症を抑制する。
トシリズマブ(IL-6受容体阻害薬):ステロイドおよびリツキシマブ難治例を対象とした報告で有益性が示されている3)。
手術適応の時期:炎症期が沈静化し、Rundle曲線でプラトーに達した非炎症期に手術を計画する。通常、発症から1〜3年で炎症が安定する。
術式の選択:
重度の眼球突出・圧迫性視神経症に対して眼窩内壁または下壁の骨切除による眼窩減圧術が行われる5)。眼瞼後退単独の一次適応ではないが、眼球突出の減少に伴い眼瞼後退が改善する例がある。
炎症期(活動期)が沈静化し、非炎症期に安定してから手術を計画する。通常Rundle曲線のプラトー到達(発症から1〜3年程度)を待つ。CAS(臨床活動性スコア)が3点未満で安定した時期が手術に適している。炎症期に手術を行うと術後の変動・再発リスクが高まる。
甲状腺眼症による眼瞼後退は上眼瞼挙筋とMüller筋の二つの病態が複合して生じる。
上眼瞼挙筋の病態:炎症性細胞浸潤→筋線維間への脂肪組織侵入→筋細胞の壊死・瘢痕化→挙筋機能低下。筋組織が後方に引き締められることで眼瞼が上方に後退する。
Müller筋の病態:交感神経支配の平滑筋であるMüller筋は、甲状腺機能亢進症による交感神経過緊張状態で異常持続収縮を起こす。これが瞼板の上方挙上を引き起こし、瞼裂を開大させる。
TEDの病態の中心はTSH受容体(TSHR)に対する自己抗体による眼窩線維芽細胞の活性化である4)。CD4+およびCD8+ T細胞が眼窩組織に浸潤して炎症反応を惹起し5)、活性化された眼窩線維芽細胞は脂肪細胞および筋線維芽細胞へと分化する5)。脂肪細胞への分化は眼窩脂肪の拡大をもたらし、筋線維芽細胞への分化は外眼筋・挙筋の線維化を引き起こす。
ヒアルロン酸(GAG)の産生増大により眼窩組織の液体貯留・腫脹が生じる5)。TNF-α・IL-6・IL-1β等の炎症性サイトカインが持続的に産生され、組織傷害と線維化が進行する4)。
IGF-1受容体(IGF-1R)はTSHRと複合体を形成し、眼窩線維芽細胞の活性化に相乗的に関与する7)。テプロツムマブがIGF-1Rを標的とする根拠がここにある。
中脳上背側疾患(松果体腫瘍・水頭症)による後交連への圧迫が、上眼瞼挙筋を神経支配する動眼神経核の上眼瞼下制ニューロンを障害することで眼瞼後退が生じる。Collier’s sign(両眼性眼瞼後退)とParinaud症候群(上方注視麻痺・輻湊退縮眼振・瞳孔光反射障害)の組み合わせは中脳上背側病変の特徴的な徴候群である。
甲状腺眼症の自然経過はRundle曲線6)に従い、発症後6〜18カ月の炎症活動期を経てプラトーに達し、その後徐々に安定する。炎症期には眼瞼後退・眼球突出・複視が変動しながら進行し、安定期には軽度改善することもあるが、瘢痕性変化が固定した場合は自然改善が期待しにくい。
テプロツムマブによる活動性TED治療では眼球突出・複視の有意な改善が示されており7)、これに伴う眼瞼後退の改善も報告されている。手術療法(挙筋後転術・Müller筋切除術)は非炎症安定期に施行することで安定した成績が得られる。術後の矯正不足・過矯正には再手術が必要になることがある。
圧迫性視神経症(DON)はTED患者の約5%に発生し、緊急の眼窩減圧術または高用量ステロイド治療を要する5)。色覚異常・相対的求心性瞳孔散大(RAPD)・視野欠損が早期徴候であり、定期的なフォローアップが重要である。長期にわたる眼瞼後退・兎眼による角膜潰瘍・角膜瘢痕は視力障害を引き起こすことがある。QOLへの影響は大きく、整容的問題・複視・視機能障害が複合する1)。