上方型

點狀表層角膜炎(SPK)
一目瞭然重點
Section titled “一目瞭然重點”1. 什麼是點狀表層角膜炎(SPK)?
Section titled “1. 什麼是點狀表層角膜炎(SPK)?”點狀表層角膜炎(superficial punctate keratitis / superficial punctate keratopathy:SPK)是指角膜上皮最表層細胞因各種原因呈點狀脫落的狀態。進行螢光素活體染色時,上皮缺損部位呈現點狀或聚集的染色影像。基底細胞層得以保留,損傷進一步加深時稱為角膜糜爛,累及實質時稱為角膜潰瘍。
一個重要前提是,SPK 僅是一種「所見」,而非獨立的疾病名稱。在眼科門診中,以異物感為主訴的患者中最常觀察到這一所見,其背後潛藏著多種多樣的原因疾病。因此,在 SPK 的診療中,尋找病因是確定治療方針的第一步。
另一方面,被例外地作為獨立疾病單元處理的是 Thygeson 點狀表層角膜炎(Thygeson superficial punctate keratitis:TSPK)。TSPK 是1950年由 Phillips Thygeson 報告的雙側性、復發性角膜上皮炎,作為無法明確病因的特發性表層角膜炎,將在另節中描述。
主要原因類別
Section titled “主要原因類別”- 淚液相關:乾眼症(淚液分泌減少型、BUT 縮短型)、瞼板腺功能障礙(MGD)1)
- 物理和機械因素:隱形眼鏡相關損傷、睫毛亂生、眼瞼內翻、結膜鬆弛症
- 化學因素:點眼藥物的毒性(包括防腐劑苯扎氯銨)、全身性抗腫瘤藥物的淚液移行
- 炎症和過敏:過敏性結膜炎、春季角結膜炎、上輪部角結膜炎(SLK)
- 感染性:單純皰疹病毒、腺病毒
- 神經和眼瞼障礙:三叉神經麻痺、顏面神經麻痺、兔眼
- 特發性:Thygeson 表層點狀角膜炎
SPK 並非疾病名稱,而是角膜上皮因某種原因受損後觀察到的「徵象」。除非明確病因,否則無法進行根本性治療,因此一旦發現 SPK 必須進行病因排查。僅 Thygeson 表層點狀角膜炎被視為獨立的疾病單元。
2. 主要症狀與臨床徵象
Section titled “2. 主要症狀與臨床徵象”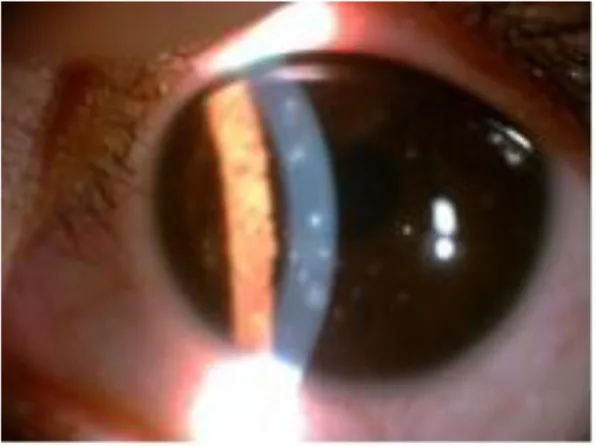
患者主訴的症狀多種多樣,眼科疾病中可能出現的幾乎所有症狀均可由 SPK 引起。
- 異物感:最常見的症狀,是以異物感為主訴的門診患者中最常見的背景疾病。
- 疼痛/眼痛:根據上皮損傷程度伴有輕度至中度疼痛。
- 視力下降/視物模糊:當病變累及瞳孔區時出現。
- 畏光:對光敏感。在惡化期尤為顯著。
- 乾澀感:在淚液功能減退型中尤為顯著。
- 充血:伴有結膜充血。
- 疲勞感/眼疲勞:在慢性病程中持續存在。
- 眼部分泌物與搔癢感:在過敏性與感染性疾病中顯著。
臨床所見(醫師在檢查中確認的所見)
Section titled “臨床所見(醫師在檢查中確認的所見)”裂隙燈顯微鏡檢查時常無法以肉眼觀察到病變,螢光素活體染色評估是診斷的核心。染色型態多樣,可呈點狀、漩渦狀、裂紋線樣等,染色性因損傷程度而異。
根據染色部位推斷病因
Section titled “根據染色部位推斷病因”染色部位有助於推斷病因,是日常診療的基本方法。
中央型
主要病因:神經麻痺性角膜病變、Thygeson 點狀表層角膜炎、睫毛機械性損傷、硬式隱形眼鏡(HCL)損傷、乾眼。
觀察要點:檢查角膜知覺和睫毛狀態。
下方/眼瞼裂部型
瀰漫性/局部型
瀰漫性:藥物毒性(點眼藥毒性、抗腫瘤藥物副作用)、嚴重乾眼症、SCL相關疾病、角膜上皮相關失養症(Meesmann等)。
局部型:結膜異物、疱疹感染、CL佩戴者的3點和9點染色。
嚴重程度參考
Section titled “嚴重程度參考”- 輕度SPK:散在的點狀染色。自覺症狀輕度至中度。
- 晚期染色(沐浴劑角膜病變):點眼後一段時間螢光素滲入的表現。顯示上皮屏障功能障礙。藥物毒性中常見。
- 颶風角膜上皮病變:角膜中央部出現漩渦狀染色模式。藥物毒性的中度表現。
- 上皮裂縫線:龜裂樣的線狀缺損。藥物毒性的重症型。
- 持續性上皮缺損:SPK 進展為廣泛上皮缺損的狀態。
Thygeson 點狀表層角膜炎的所見
Section titled “Thygeson 點狀表層角膜炎的所見”TSPK 是一種與常見原因性 SPK 不同的獨立疾病,具有特徵性臨床表現。
- 雙眼性、復發性:通常為雙眼性,病程呈反覆惡化與緩解。
- 角膜中央部隆起病變:灰白色、類圓形、輕微隆起的點狀混濁散在分布。每個病灶是顆粒狀變化的集合體,通常每眼約20個,最多可達50個左右。
- 結膜無充血:缺乏結膜充血或炎症反應是鑑別診斷的重要線索。
- 螢光素染色:病灶中心部呈點狀染色。病變周圍的角膜上皮正常。
- 角膜知覺:正常或僅輕度下降。
- 自覺症狀頻率:異物感 48.8%、畏光 41.9%、視力模糊 36.0%、流淚 15.1%。眼痛罕見。
- 病程持續時間:單次發作持續1~2個月,緩解約需6週。復發可持續數年至數十年,最長有持續41年的記錄。最終傾向於不留疤痕而消退。
3. 病因與風險因素
Section titled “3. 病因與風險因素”SPK 的病因多種多樣。以下按臨床頻率從高到低列舉。
- 淚液分泌減少型乾眼症:由基礎淚液分泌減少引起。Schirmer I 試驗 ≤5 mm、淚膜破裂時間 ≤5 秒是診斷參考標準3)。年齡增長、Sjögren 症候群、類風濕性關節炎、服用抗膽鹼藥物等是危險因素。
- BUT縮短型乾眼:淚液量正常,但淚膜穩定性下降,眨眼後淚膜立即破裂的類型。與VDT作業、空調、隱形眼鏡佩戴等相關3)。
- 瞼板腺功能障礙(MGD):瞼板腺開口阻塞或脂質分泌異常導致淚膜油層受損,表現為蒸發過強型乾眼和難治性SPK1,4)。下方至眼裂區SPK較典型。
物理及機械因素
Section titled “物理及機械因素”- 硬式隱形眼鏡損傷:導致侷限於角膜中央部的SPK。佩戴時間延長和鏡片配適不良為風險因素。
- 軟式隱形眼鏡損傷:表現為瀰漫性或下方SPK。與鏡片汙染、佩戴時間延長、透氧性不足相關9)。3點和9點鐘方向染色是圓形局部SPK,為隱形眼鏡特有表現。
- 倒睫和眼瞼內翻:睫毛摩擦角膜表面,造成機械性損傷。
- 結膜鬆弛症:鬆弛的結膜陷入下方眼裂區,增加眨眼時的摩擦。
- 藥物毒性角膜病變:眼藥水中的防腐劑(苯扎氯銨,BAC)是主要原因,有時也可由主成分的毒性引起。抗青光眼藥物、抗菌藥、抗真菌藥、抗病毒藥、NSAIDs滴眼液、β受體阻斷劑、表面麻醉滴眼液報告較多。輕症表現為類似乾眼的瞼裂部至下方SPK,重症則進展為颶風角膜上皮病變、上皮裂紋線、遷延性上皮缺損。長期滴眼液毒性負荷可誘發角膜緣幹細胞缺乏和假性類天疱瘡。TS-1等抗癌藥全身給藥時,角膜上方的角膜緣會出現上皮障礙。
- 過敏性結膜炎·春季角結膜炎:上方型SPK的代表,伴有巨大乳頭和黏液性眼部分泌物5)。
- 上角膜緣角結膜炎(SLK):好發於50歲以上族群的角膜上緣慢性發炎,引起上方型SPK和絲狀角膜炎。
- 泡性角膜炎(瞼板腺炎角結膜上皮病變):與瞼板腺炎相關的IV型過敏性雙側復發性角膜炎。
- 單純皰疹病毒性角膜炎(上皮型):典型的表現為單眼發病、角膜知覺減退、樹枝狀潰瘍。早期可出現點狀或星芒狀上皮病變,需與SPK進行鑑別7)。
- 腺病毒角膜炎:表現為流行性角結膜炎伴隨的多發性上皮下浸潤。先前的結膜炎病史是鑑別要點。
神經·眼瞼障礙
Section titled “神經·眼瞼障礙”- 神經營養性角膜病變:因三叉神經損傷導致角膜知覺下降,上皮修復功能破壞,產生中央型SPK。常見於角膜皰疹後、帶狀皰疹眼症、三叉神經手術後、腦幹病變等。
- 兔眼性角膜病變:因眼瞼閉合不全導致角膜下方乾燥。顏面神經麻痺、甲狀腺眼症、眼眶腫瘤、睡眠時眼瞼閉合不全、昏迷等為背景疾病。
- 糖尿病性角膜病變:由糖尿病引起的神經病變和上皮黏附性下降導致。
特發性:Thygeson 淺層點狀角膜炎
Section titled “特發性:Thygeson 淺層點狀角膜炎”原因不明的復發性雙眼角膜上皮炎。已報告與HLA-DR3相關,提示免疫學機制的參與2)。與乳糜瀉的合併報告透過共享HLA-DR3媒介2)。環孢素A和他克莫司等免疫抑制劑有效,推測為T細胞媒介的免疫反應。曾提出病毒參與學說,但PCR研究未鑑定出致病病毒。
與全身疾病的關聯
Section titled “與全身疾病的關聯”類風濕關節炎等膠原病、糖尿病、異位性皮膚炎可能成為SPK的背景疾病。制定治療方針時,詢問全身疾病史非常重要。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”SPK的診療不僅在於確認所見,更重要的是系統性地探究“是什麼原因導致了上皮損傷”,這是決定治療方針的關鍵。
- 問診:詢問發病為急性/慢性、單眼/雙眼、隱形眼鏡佩戴史、使用之眼藥水及口服藥、外傷或異物暴露史、全身疾病史(類風濕性關節炎、糖尿病、異位性皮膚炎、Sjögren症候群等)。急性單眼發病提示外源性原因(異物、化學物質),慢性雙眼發病提示內源性原因(乾眼、MGD、藥物毒性)。
- 裂隙燈顯微鏡檢查:檢查有無上皮下浸潤等發炎表現、結膜充血、前房發炎。
- 螢光素活體染色:根據染色部位和模式推斷原因(參見第2節的CardGrid)。
- 環境因素評估(6項):評估淚液功能、眼瞼、角膜知覺、結膜、使用藥物和全身疾病。
- 定量評估:使用AD分類或螢光素染色評分客觀評估SPK嚴重程度。
主要檢查方法
Section titled “主要檢查方法”- Schirmer試驗Ⅰ法:測量基礎淚液分泌及反射性分泌。5分鐘後測量值≥10mm為正常,≤5mm提示淚液分泌減少型乾眼。
- 淚膜破裂時間(BUT):螢光素點眼後維持睜眼,測量淚膜出現乾燥斑的時間。≤5秒判斷為異常,為BUT縮短型乾眼的診斷依據3,8)。
- 淚河觀察:評估下眼瞼緣淚液半月板的高度。在分泌減少型乾眼中呈低值。
- Cochet-Bonnet 角膜知覺計:在角膜疱疹、糖尿病角膜病變、LASIK 術後、長期配戴隱形眼鏡者、顏面神經麻痺等情況下下降。知覺下降會減少淚液的反射性分泌,加重 SPK。
- 共聚焦顯微鏡檢查:在 Thygeson SPK 中,表層和基底上皮細胞層可見星芒狀高反射沉積物、基底上皮層的蘭格漢氏細胞浸潤以及前部基質混濁。病程越長的眼睛,變化越嚴重。
- 淚液檢查:乳鐵蛋白定量、MMP-9 檢測等作為輔助手段使用。
- 全身疾病篩查:根據需要進行抗 SS-A/SS-B 抗體、HbA1c、血清 IgE 等評估。
定量評估方法
Section titled “定量評估方法”- AD 分類:對 SPK 的面積(Area:A0~A3)和密度(Density:D0~D3)分別進行 3 分制評估,例如表示為 A2D2。
- 螢光素染色評分:將角膜分為 3 個區域,每個區域評估 0~3 分,總分 9 分。用於隨時間變化的追蹤。
- NEI 量表:將角膜分為 5 個區域,每個區域評估 0~3 分,總分 15 分的國際指標。
| 鑑別對象 | 鑑別要點 |
|---|---|
| 角膜疱疹(上皮型) | 單眼性、知覺減退、樹枝狀潰瘍 |
| 腺病毒角膜炎 | 先行結膜炎、多發性上皮下浸潤 |
| Thygeson SPK | 雙眼、中央、結膜靜穩、隆起病變 |
| 乾眼症/MGD | 下方SPK、BUT縮短、淚液異常 |
| 藥物毒性角膜病變 | 點眼史、眼瞼裂部SPK、晚期染色 |
| 過敏性角結膜炎 | 上方SPK、巨大乳頭、搔癢 |
| 神經麻痺性角膜病變 | 中央SPK、角膜知覺減低 |
| 兔眼性角膜病變 | 眼瞼閉合不全、下方SPK |
典型的定量評估方法包括:AD分類法(將SPK的範圍和密度分別按3分制評分)和螢光素染色評分(將角膜分為3個區域,各評0〜3分,滿分9分)。國際上還採用將角膜分為5個區域的NEI量表(滿分15分)。兩者均有助於追蹤隨時間的變化和評估治療效果。
5. 標準治療方法
Section titled “5. 標準治療方法”SPK 治療的基本原則是 「去除病因」與「角膜上皮的保護和修復」相結合。由於治療策略因病因不同而有很大差異,以下按病因分別說明。
淚液補充與保護
玻尿酸鈉滴眼液:Hyalein 滴眼液(0.1%)每日4~6次。可改善自覺症狀、淚膜穩定性及角膜障礙,乾眼症診療指引亦建議使用3)。
人工淚液:優先選用不含防腐劑的製劑。在輕症或藥物毒性病例中優先選擇。
眼藥膏:用於睡前保護角膜。代表藥物有 Tarivid 眼藥膏(0.3%)等。
改善淚液動力學
依病因分類的治療方案
Section titled “依病因分類的治療方案”乾眼症引起的 SPK
Section titled “乾眼症引起的 SPK”- 第一線治療:希亞霖點眼液(0.1%)每日4-6次。
- BUT縮短型的併用治療:
- 地夸磷索點眼液(3%)每日6次,或
- 瑞巴派特點眼液UD(2%)每日4次。
- 重症病例:進行淚點栓塞術或淚點縫合術。與傳統點眼治療相比,兩者在自覺症狀、淚膜穩定性及上皮病變方面均有顯著改善3)。
- 輔助治療:皮質類固醇點眼液有助於改善自覺症狀和淚膜穩定性,但使用時需注意眼壓升高3)。
瞼板腺功能障礙(MGD)引起的 SPK
Section titled “瞼板腺功能障礙(MGD)引起的 SPK”- 熱敷與眼瞼清潔:使用熱敷(40°C,5分鐘)和眼瞼按摩,每日1-2次1)。
- 眼藥膏:將極少量氧氟沙星眼藥膏(0.3%)薄薄塗抹於眼瞼緣。
- 點眼液:依情況使用海露點眼液(0.1%)。
- 發炎較嚴重時:
- 克拉霉素錠(200mg)2錠,分2次口服
- 貝斯特隆點眼液(0.5%)每日4次
- 氟美童點眼液(0.1%)每日4次
過敏性結膜炎引起的 SPK
Section titled “過敏性結膜炎引起的 SPK”依嚴重程度逐步加用5)。
- 愛立爽點眼液(0.05%)每日4次(早、中、晚、睡前)
- 塔利姆斯點眼液(0.1%)每日2次
- 發炎較嚴重時:氟美童點眼液(0.1%)每日4次
藥物毒性角膜病變
Section titled “藥物毒性角膜病變”- 停用或更換致病藥物:停止使用可疑的眼藥水,如抗青光眼藥、NSAIDs、抗菌藥等。
- 改用不含防腐劑的製劑:在相同療效範圍內如有不含防腐劑的製劑,應優先選擇。
- 補充治療:頻繁點用不含防腐劑的人工淚液。
- 輔助治療:若充血或濾泡性結膜炎明顯,可考慮低濃度類固醇眼藥水,但需注意傷口癒合延遲的風險。
神經營養性角膜病變、糖尿病性角膜病變及兔眼性角膜病變
Section titled “神經營養性角膜病變、糖尿病性角膜病變及兔眼性角膜病變”- 強制閉瞼(如使用眼墊等),並配戴保護性軟性角膜接觸鏡。
- Hyalein點眼液(0.1%)每日4~6次。
- Tarivid眼藥膏(0.3%)每日塗眼2~4次。
- 重症或遷延病例可考慮羊膜移植、自體血清點眼液、神經營養因子相關治療等。
睫毛亂生與眼瞼內翻
Section titled “睫毛亂生與眼瞼內翻”- 定期進行睫毛拔除和電解治療。
- 為根治施行眼瞼成形手術。
Thygeson點狀表層角膜炎
Section titled “Thygeson點狀表層角膜炎”- 輕症病例:自覺症狀輕微者僅需觀察。
- 有症狀病例:氟米龍滴眼液(0.1%)每日4次。
- 逐漸減量:由於容易復發,症狀消退後也需數月逐步減少類固醇滴眼液,減至每週1次至隔週的維持劑量。
- 替代療法:
- 有病例報告使用環孢素A 2%滴眼液每日3次、在6個月內逐漸減量,追蹤3年未見復發2)。
- 他克莫司滴眼液/軟膏。
- 治療用軟式隱形眼鏡(機械性覆蓋隆起病變)。
- 禁忌・無效:碘苷(Idoxuridine)可能引起鬼影混濁及前基質疤痕,故不應使用。抗生素無效。表層角膜切除術(PTK)僅能部分改善且復發率高,故不建議。
這兩種眼藥水均為乾眼診療指引建議使用的藥物,但作用機制不同。地夸磷索鈉(地夸斯點眼液3%)可促進膜結合型黏蛋白表現和水分分泌,並有助於淚液油脂層延展,因此在BUT縮短型乾眼中作為首選考量。瑞巴派特(穆科斯塔點眼液UD 2%)除促進黏蛋白生成外還具有抗發炎作用,適用於伴有眼表發炎的病例。兩者均與玻尿酸鈉點眼液併用,由主治醫師根據病例情況選擇3)。
6. 病理生理學及詳細發病機轉
Section titled “6. 病理生理學及詳細發病機轉”角膜上皮更替障礙
Section titled “角膜上皮更替障礙”角膜上皮經由基底細胞層的更替持續更新。SPK可理解為因最表層細胞脫落亢進或基底細胞供應減少而導致更替平衡被破壞的初期狀態。實際上,多數病例以前者即脫落亢進為主因。
各病因的分子及細胞機轉
Section titled “各病因的分子及細胞機轉”- 乾眼:淚膜不穩定導致眼表乾燥,上皮細胞承受壓力。發炎性細胞激素(IL-1、TNF-α)與MMP-9的活化破壞上皮屏障6)。
- 麥粒腺功能障礙:麥粒腺脂質的質與量異常導致淚膜脂質層功能下降,引起淚液蒸發增加和淚膜不穩定1)。慢性炎症形成惡性循環,瞼板腺管阻塞逐漸惡化。
- 藥物毒性:防腐劑苯扎氯銨(BAC)破壞角膜上皮細胞膜的磷脂層,損害屏障功能。即使輕微的上皮損傷,螢光素也易於滲入,表現為遲染(late staining)影像。長期暴露會導致角膜緣幹細胞功能下降。
- 神經營養性角膜病變:三叉神經支配喪失導致神經營養因子(P物質、CGRP、NGF)供應中斷,上皮黏附性和傷口癒合能力下降。
Thygeson 淺層點狀角膜炎的免疫學機轉
Section titled “Thygeson 淺層點狀角膜炎的免疫學機轉”在 Thygeson SPK 的病灶中,可見上皮內以淋巴細胞為主的單核球浸潤。支持免疫學機轉的證據如下。
- 與 HLA-DR3 的相關性:根據報告,患者中 HLA-DR3 的攜帶率顯著較高2)。HLA-DR3 是第二類主要組織相容性複合體(MHC)分子,負責向 T 細胞呈遞抗原。
- 蘭格漢氏細胞浸潤:共軛焦顯微鏡一致觀察到蘭格漢氏細胞侵入基底上皮層。抗原呈遞細胞的活化參與了疾病的發病機制。
- 與自體免疫疾病的關聯:已有報告指出可與乳糜瀉、艾迪生氏病、修格連氏症候群、全身性紅斑性狼瘡等 HLA-DR3 相關自體免疫疾病合併存在2)。
- 免疫抑制劑的療效:低濃度皮質類固醇、環孢素 A、他克莫司有效,推測為 T 細胞媒介性免疫反應。
組織學變化與長期病程
Section titled “組織學變化與長期病程”Thygeson SPK 可見細胞內及細胞間水腫、上皮下神經叢、鮑曼氏膜及前部基質的細微變化。這些變化在病程較長的眼睛中更為嚴重。但通常病變消退後不留疤痕,視力預後良好。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”Thygeson SPK 與乳糜瀉的免疫遺傳學關聯
Section titled “Thygeson SPK 與乳糜瀉的免疫遺傳學關聯”Tagmouti 等人報告了一名有4年乳糜瀉病史的20歲女性出現 Thygeson SPK 的病例2)。乳糜瀉是一種與 HLA-DQ2 和 HLA-DQ8 密切相關的自體免疫疾病,90%以上的患者帶有 HLA-DR3 等位基因。此前已有研究指出 Thygeson SPK 與 HLA-DR3 存在關聯,提示這兩種疾病之間存在免疫遺傳學聯繫。
Tagmouti 等人指出「在 Thygeson 點狀表層角膜炎病例中,應考慮共同遺傳易感因素,對乳糜瀉進行篩查」2)。
該病例透過環孢素 A 2% 點眼液每日3次、6個月漸減給藥實現了完全緩解,追蹤3年未見復發2)。這再次證實了環孢素點眼液作為免疫調節療法之有效性,並凸顯了探索 Thygeson SPK 與自體免疫疾病關係之未來研究的重要性。
乾眼症治療的進展
Section titled “乾眼症治療的進展”隨著針對淚膜脂質層、水液層和黏蛋白層各層的標靶治療的發展,即使是主訴為SPK的病例,基於病理狀態的治療選擇也在不斷擴大。TFOS DEWS III(2025年)提出了淚膜層的功能評估和個體化治療策略6,10)。生物製劑、強脈衝光(IPL)治療、新型黏蛋白分泌促進劑等正處於研究開發中。
8. 參考文獻
Section titled “8. 參考文獻”- 天野史郎, 有田玲子, 横井則彦, ほか. マイボーム腺機能不全診療ガイドライン. 日本眼科学会雑誌. 2010;114(6):557-587.
- Tagmouti A, Lazaar H, Benchekroun M, et al. Association Between Thygeson Superficial Punctate Keratitis and Celiac Disease. Cureus. 2025;17(3):e80252.
- ドライアイ研究会診療ガイドライン作成委員会. ドライアイ診療ガイドライン. 日本眼科学会雑誌. 2019;123(4):489-592.
- 有田玲子, 天野史郎, 島﨑潤, ほか. マイボーム腺機能不全の定義と診断基準. あたらしい眼科. 2010;27(5):627-631.
- 日本眼科アレルギー学会. アレルギー性結膜疾患診療ガイドライン(第3版). 日本眼科学会雑誌. 2021;125(7):739-776.
- Jones L, Downie LE, Korb D, et al. TFOS DEWS II Management and Therapy Report. Ocular Surface. 2017;15(3):575-628.
- 日本眼感染症学会 感染性角膜炎診療ガイドライン改訂委員会. 感染性角膜炎診療ガイドライン(第3版). 日本眼科学会雑誌. 2023;127(2):117-204.
- 島﨑潤. ドライアイの定義と診断基準(2016年版). あたらしい眼科. 2017;34(3):309-313.
- Carnt N, Keay L, Willcox M, et al. Contact lens-related adverse events: A review of the literature. Contact Lens and Anterior Eye. 2018;41(5):395-405.
- Craig JP, Nichols KK, Akpek EK, et al. TFOS DEWS II Definition and Classification Report. Ocular Surface. 2017;15(3):276-283.
