裂隙灯显微镜所见
颗粒状浸润:瓣下散在白色至灰白色细小颗粒状浸润。呈“沙”样外观。
分布变化:1级以周边部为主。2级以上向中心部进展。
边界特征:病灶边界不清,有从瓣边缘向中心扩展的趋势。
前房炎症:前房炎症通常轻微或缺如。若前房炎症严重,应优先与感染性角膜炎鉴别。

弥漫性层间角膜炎(diffuse lamellar keratitis, DLK)是LASIK术后在瓣膜与角膜基质床之间的界面(层间)发生的非感染性弥漫性炎症反应。其特征是瓣膜下散在的细小白色颗粒状浸润,被形容为“撒哈拉沙漠”。
屈光矫正手术指南(第8版)中,DLK被列为准分子激光手术和SMILE两种术式的术后并发症,需要适当处理1)。LASIK总体发生率报道约为0.1-1%2)。即使在飞秒激光制作瓣膜成为主流后,DLK仍有一定发生率,SMILE术后也观察到DLK样层间炎症。根据KLEx(小切口角膜基质透镜取出术)指南,SMILE术后DLK总体发生率为0.84%,其中I级(周边局限)1.42%,II级(中央扩展)0.29%,III级(融合/灶状)0.08%,IV级(重度)0.02%3)。
弥漫性层间角膜炎(DLK)的病理与感染性角膜炎完全不同,其本质是没有细菌参与。另一方面,与外观相似的炎症性疾病IFS(界面液综合征/PISK)的鉴别是最重要的临床课题,因为治疗方案会180度改变。
DLK最常见于LASIK术后,但也可能发生在SMILE(小切口角膜基质透镜取出术)后。屈光矫正手术指南(第8版)也将DLK列为准分子激光手术和SMILE的术后并发症。PRK不制作角膜瓣,因此不会发生DLK。即使在飞秒激光普及后,DLK的发生率也并未降至零,术后1-5天的细致观察和早期干预是良好预后的关键。特别是早期发现1-2级并迅速开始类固醇治疗,对于预防进展至3-4级最为重要。需要注意的是,PRK虽然不制作角膜瓣而不发生DLK,但存在术后haze(上皮下混浊)的风险,有时会使用丝裂霉素C进行预防性处理。需要充分了解手术特点后对患者进行个体化说明。
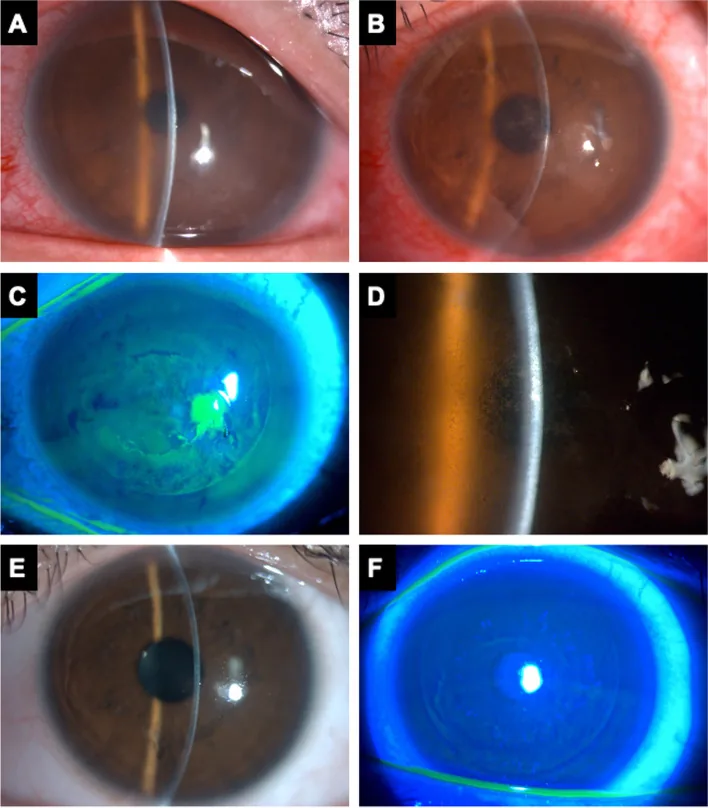
DLK的自觉症状取决于严重程度(分级)。
典型发病时间为术后1-5天,认为炎症介质在角膜瓣制作后立即积累并显现。但也有术后数周至数月的迟发型报道,部分病例在停用类固醇滴眼液后复发。
裂隙灯显微镜下的反光(retroillumination)观察为DLK的诊断提供了最重要的发现。通过反光观察,光线从后方照射,更容易评估瓣下细胞浸润的情况。初学者可能觉得“沙暴样外观”这一描述难以直观理解,但随着经验积累,可以将其识别为非常特征性的表现。在1~2级时,颗粒状浸润主要分布于周边部,2级以上则向中央部进展。“撒哈拉沙漠之沙(Sands of Sahara)”这一术语被用作准确描述细小白色颗粒状浸润扩散方式的临床表达。
裂隙灯显微镜所见
颗粒状浸润:瓣下散在白色至灰白色细小颗粒状浸润。呈“沙”样外观。
分布变化:1级以周边部为主。2级以上向中心部进展。
边界特征:病灶边界不清,有从瓣边缘向中心扩展的趋势。
前房炎症:前房炎症通常轻微或缺如。若前房炎症严重,应优先与感染性角膜炎鉴别。
眼前节OCT所见
高反射区:瓣下界面可见点状至线状高反射区。
无瓣分离:与IFS不同,未见瓣的物理分离或液体蓄积(4级除外)。
基质融解监测:在3~4级,可通过眼前节OCT随时间评估基质床的融解状态。
与IFS的鉴别:IFS在瓣下可见均匀的液体层(低反射带),而DLK以点状高反射区为主。
DLK的发生涉及多种诱因。它们都通过共同的机制:“炎症诱导物质被封闭在瓣下密闭空间内”。
内源性诱因:
外源性诱因:
环境与设施因素: DLK的聚集性发生(设施内短期集中多发)常提示手术室内存在污染物(有机挥发物、内毒素等)6)。通过监测整个设施的DLK发生率来识别原因并采取环境改善措施非常重要。已有报告指出与特定批次的清洁剂、灭菌液或滴眼液相关。
感染性炎症(细菌、真菌、棘阿米巴)根据DLK定义被排除,但感染可能诱发DLK样反应。
影响发生率的因素:
DLK的严重程度按1-4级评估。该分类直接决定治疗方案2)。
| 分级 | 裂隙灯所见 | 对视力影响 | 治疗方案 |
|---|---|---|---|
| 1级 | 仅周边部有白色颗粒状浸润(中央部正常) | 几乎无影响 | 频繁使用类固醇滴眼液并观察 |
| 2级 | 浸润向包括瞳孔区的中央部扩展 | 轻度视力下降 | 增加类固醇滴眼液用量,次日复诊 |
| 3级 | 重度浸润达中央区,基质融解的早期迹象 | 中度视力下降 | 强烈考虑类固醇滴眼液+掀瓣冲洗 |
| 4级 | 中央基质融解(角膜溶解)和瘢痕形成 | 显著视力下降 | 紧急掀瓣冲洗(考虑全身使用类固醇) |
DLK最重要的鉴别诊断是以下两种疾病。
与IFS(界面液综合征/PISK)的鉴别:
IFS是由于类固醇引起的眼压升高导致的瓣下液体聚集,不伴有炎症细胞,本质是眼压升高。如果将DLK误诊为IFS并继续使用类固醇,眼压会进一步升高,加重IFS 4)。反之,如果将IFS误诊为DLK而停用类固醇,DLK可能进展为角膜基质融解。
| 鉴别要点 | DLK | IFS(PISK) |
|---|---|---|
| 发病时间 | 术后1~5天 | 术后数天至数月(可有迟发) |
| 炎症细胞 | 多核白细胞浸润 | 无炎症细胞(仅水肿) |
| 眼压 | 正常 | 升高(Goldmann测量假性偏低) |
| 眼前节OCT | 点状高反射区 | 均匀低反射液体层(瓣膜分离) |
| 类固醇反应 | 有效(1~2级) | 恶化 |
| 治疗 | 增加类固醇滴眼液 | 停用类固醇+降眼压药物 |
与感染性角膜炎的鉴别:
感染性角膜炎(细菌、真菌、棘阿米巴)常伴有前房炎症。强毒力细菌或真菌引起的基质炎可能出现前房纤维蛋白渗出。非感染性角膜炎(包括DLK)通常前房炎症轻微。如果出现局部浸润、充血和分泌物,应怀疑感染。
| 检查 | 目的 | DLK中的表现 |
|---|---|---|
| 裂隙灯显微镜(后照法) | 评估颗粒状浸润 | 瓣下点状白色浸润 |
| 眼前段OCT | 鉴别瓣下液体与炎症细胞 | 点状高反射区(IFS表现为均匀液体层) |
| 眼压测量 | 排除IFS | 正常(IFS时升高) |
| 角膜培养/涂片 | 排除感染性角膜炎 | 阴性 |
| 角膜地形图分析 | 评估基质溶解导致的不规则散光 | 进展期呈不规则模式 |
屈光手术指南(第8版)1)规定术后次日必须进行裂隙灯显微镜检查,但对于DLK管理,建议以下观察频率:
大多数12级DLK在术后2周内完全消退,但34级可能因基质溶解而留下永久性不规则散光,因此建议治疗完成后进行3~6个月的角膜地形图随访9)。
区分DLK和IFS(界面液综合征)最关键的是“眼压”。IFS时眼压升高,但Goldmann压平眼压计的中央测量可能因液体垫效应出现假性低值,因此建议周边部或动态轮廓眼压计测量。前节OCT中,DLK表现为点状高反射区,IFS表现为均匀的低反射液体层将瓣膜抬起。DLK在术后早期(1~5天)出现疼痛和白色颗粒浸润,而IFS主要表现为雾视和眼压升高,缺乏炎症细胞。由于治疗完全相反(DLK→增加类固醇,IFS→停用类固醇+降眼压),误诊会导致严重后果。
根据分级决定治疗。
频繁滴用类固醇眼药水是首选治疗。
在继续使用类固醇眼药水的同时,强烈考虑掀瓣和生理盐水冲洗。
SMILE中的III级除了高剂量类固醇外,还需考虑层间冲洗3)。SMILE术后层间冲洗比LASIK更难操作,因此应由经验丰富的手术医生进行。
必须紧急进行瓣膜提起和冲洗。
| 分级 | 初始处理 | 复诊间隔 | 干预阈值 |
|---|---|---|---|
| 1 | 泼尼松龙1%滴眼液,每1-2小时一次 | 次日到2天后 | 若进展至2级或以上,考虑掀瓣 |
| 2 | 同上,增加剂量。次日复诊确认 | 次日 | 若无改善,次日掀瓣 |
| 3 | 类固醇滴眼液+掀瓣及冲洗 | 当日至次日 | 原则上实施掀瓣 |
| 4 | 紧急掀瓣及冲洗(考虑全身类固醇) | 当日紧急 | 立即干预 |
DLK的治疗因分级而异。对于12级,使用1%泼尼松龙滴眼液频繁滴眼,每12小时一次。大多数病例在1~2周内改善。对于3级,除了滴眼液外,可能需要进行瓣膜掀开(重新打开角膜瓣)和生理盐水冲洗。4级(基质溶解)需要紧急瓣膜掀开和冲洗,并考虑全身使用类固醇。不要自行停止滴眼液;如果术后出现视力下降或严重畏光,请立即联系主治医生。
DLK是一种以多形核白细胞(中性粒细胞)为主的非感染性炎症反应。当角膜瓣制作过程中产生的碎屑、手术器械来源的微粒或生物源性刺激物被封闭在角膜界面的闭合空间内时,局部会产生细胞因子(IL-1β、IL-6、TNF-α等)和趋化因子(IL-8、MCP-1等),导致中性粒细胞聚集。与感染性炎症不同,这种炎症反应不伴有细菌或真菌增殖。
由于术后角膜瓣并未完全愈合,界面作为一个半封闭空间发挥作用。这种将炎症细胞和炎症介质“封闭”起来的结构特性,使得DLK局限于角膜瓣下。
由于角膜瓣界面与正常角膜基质接触的部分较少,中性粒细胞的募集途径主要被认为通过角膜缘血管网和角膜基质内的现有细胞(角膜细胞、朗格汉斯细胞)。从发病到重症化(1级→4级)的速度个体差异很大;部分病例在术后1~2天内迅速进展至4级。这就是术后数天内密切观察对于DLK管理绝对不可或缺的原因。
在重症DLK(4级)中,中性粒细胞来源的大量基质金属蛋白酶(MMP-8、MMP-9等)被释放,降解胶原纤维,导致角膜基质溶解。如果溶解波及中央区,会导致永久性视力下降和不规则散光。早期干预(瓣膜掀开和冲洗)以物理清除产生MMP的中性粒细胞,是阻止溶解进展的重要依据。
DLK在病理学上可见炎症性多形核白细胞和单核细胞在层间积聚,而IFS则缺乏炎症细胞,仅见基质水肿4)。这一病理学差异是区分两种疾病治疗策略的根本依据。
飞秒激光制作角膜瓣相比微型角膜刀提高了瓣的精确度,但激光照射形成的不透明气泡层(OBL)可能引起一过性界面反应。光爆破产生的等离子体和微气泡可能诱发局部炎症反应5)。虽然尚未证实飞秒激光特有地增加DLK,但鉴别OBL相关炎症与DLK被认为很重要。
使用飞秒激光时,10%–30%的病例出现OBL,多数在术后数小时至数天内自然消退。但广泛的OBL会干扰准分子激光的眼球追踪,导致照射精度下降,因此术中若发现,常等待其消退。OBL本身不被认为会引起炎症,但当OBL与DLK同时观察到时,反光照明对评估DLK进展特别有用。
SMILE术后DLK发生在帽(相当于瓣)下的层间,但适用与LASIK相同的病理和治疗原则3)。然而,由于通过2–3mm的小切口插入器械,层间冲洗难度高于LASIK。KLEx指南指出,通过适当的类固醇治疗,多数病例病灶在一周内改善,约三周症状消失3)。
SMILE术后DLK的发生率(0.84%)与LASIK术后DLK的发生率(0.1%–1%)大致相似,提示瓣/帽界面的存在是共同诱因,而非术式本身。SMILE不会发生瓣相关并发症(如瓣移位、游离瓣),但在DLK管理中需要同样谨慎,术后1–5天的观察尤为重要。对SMILE术后3–4级DLK进行层间冲洗,前提是主治医生具有足够的SMILE术后管理经验3)。
DLK是屈光矫正手术的并发症之一,通过早期诊断和适当治疗可显著改善视力预后。制定细致的术后早期观察计划,并充分指导患者在症状恶化时尽早就诊,是预防DLK导致视力损害的基本且最重要的管理策略。
已知通过改善手术环境可降低DLK的发生率。具体措施包括:冲洗液的质量控制(蒸馏水、BSS等的纯度)、更换外科手套(使用无滑石粉手套)、加强器械的超声波清洗、维持手术室正压以防止内毒素污染等6)。持续监测设施层面的DLK发生率对于确定原因和制定对策至关重要。
2022年《巴西眼科档案》的一篇综述提出了一种扩展分类,补充了现有的1-4级分级系统,引入了纤维化反应(5级)和伴有前房浸润的重症型(相当于6级)的概念7)。但目前国际共识仍以1-4级分类为标准。
有报告称,术前或术中使用局部类固醇(如泼尼松龙)可能降低DLK的发生率8)。然而,对类固醇敏感的患者存在眼压升高的风险,因此需要进行个体风险评估。
DLK是屈光手术后需要诊断和治疗决策的代表性并发症之一。Swanson等人9)的综述总结了屈光手术后DLK、上皮植入和瓣相关并发症的发生率、危险因素和治疗结果,确认DLK是最常见的并发症(LASIK术后0.1-1%)。Phipps等人10)的综述系统整理了DLK的病理生理学、分级分类、鉴别诊断和治疗的最新证据,强调1-2级通过保守治疗90%以上可恢复,而3-4级早期瓣掀开和冲洗对视力预后至关重要。
Moshirfar等人11)的瓣并发症综述显示,DLK在微型角膜刀和飞秒激光两种设备中发生率相似,论证了瓣界面的存在本身就是DLK的必要条件。还讨论了飞秒激光特有的不透明气泡层(OBL)形成可能诱发DLK的可能性11)。
Venkataraman等人12)报告了一系列迟发性IFS病例,包括LASIK术后10年以上发病的病例,表明IFS可在LASIK术后任何时间发生。他们指出,眼压测量(使用周边测量或动态轮廓眼压计)和前段OCT对鉴别诊断至关重要12)。
Slade13)讨论了飞秒激光瓣定制(瓣厚度、铰链角度、侧切角)对瓣安全性和并发症谱的影响,表明适当的瓣设计(均匀厚度、适当铰链宽度、锐角侧切)有助于降低术后瓣移位和DLK的发生率13)。
Randleman等人14)的圆锥角膜风险评分系统确定了术后圆锥角膜的五个预测因子:角膜形态异常、残留基质床厚度低、年轻、角膜薄、高度近视。虽然圆锥角膜和DLK是独立的并发症,但当3-4级DLK发生基质溶解时,角膜的结构脆弱性增加,可能增加潜在圆锥角膜的风险14)。
AAO角膜扩张PPP15)建议将CXL(角膜交联)作为术后圆锥角膜管理的一线治疗,并指出即使在DLK导致基质溶解进展的病例中,也可考虑CXL适应症。但CXL仅适用于确认进展的情况,单独的DLK不是CXL的适应症15)。
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第8版). 日眼会誌. 2024;128(2):135-138.
Johnson JD, Harissi-Dagher M, Pineda R, et al. Diffuse lamellar keratitis: incidence, associations, outcomes, and a new classification system. J Cataract Refract Surg. 2001;27(10):1560-1566.
Wang Y, Xie L, Yao K, et al. Evidence-Based Guidelines for Keratorefractive Lenticule Extraction Surgery. Ophthalmology. 2025;132:397-419.
Vera-Duarte GR, Guerrero-Becerril J, Müller-Morales CA, et al. Delayed-onset pressure-induced interlamellar stromal keratitis (PISK) and interface epithelial ingrowth 10 years after laser-assisted in situ keratomileusis. Am J Ophthalmol Case Rep. 2023;32:101874.
Kymionis GD, Naoumidi TL, Aslanides IM, Pallikaris IG, Siganos CS. Diffuse lamellar keratitis after laser in situ keratomileusis with the IntraLase femtosecond laser. J Cataract Refract Surg. 2007;33(8):1471-1473.
Stulting RD, Randleman JB, Cowan LA, Thompson KP, Bradley EV, Lynn MJ. The epidemiology of diffuse lamellar keratitis. Cornea. 2004;23(7):680-688.
Rosa DS, de Macedo ELS, Leal LA, et al. Diffuse lamellar keratitis after LASIK: literature review and proposed new grading. Arq Bras Oftalmol. 2022;85(2):198-204.
Linebarger EJ, Hardten DR, Lindstrom RL. Diffuse lamellar keratitis: diagnosis and management. J Cataract Refract Surg. 2000;26(7):1072-1077.
Swanson ME, Naidoo KS. Corneal complications following refractive surgery: a review. Cont Lens Anterior Eye. 2016;39(4):268-278.
Phipps MD, Nassiri N. Diffuse lamellar keratitis. StatPearls. 2023.
Moshirfar M, Anderson E, Hsu M, et al. LASIK flap complications. StatPearls. 2024.
Venkataraman P, Shroff A, Prabu S, Senthilkumar N. Behind the blur: Understanding interface fluid syndrome in post-LASIK patients. Indian J Ophthalmol. 2025.
Slade SG. The use of the femtosecond laser in the customization of corneal flaps in laser in situ keratomileusis. Curr Opin Ophthalmol. 2007;18(4):314-317.
Randleman JB, Woodward M, Lynn MJ, Stulting RD. Risk assessment for ectasia after corneal refractive surgery. Ophthalmology. 2008;115:37-50.
American Academy of Ophthalmology Corneal/External Disease Preferred Practice Pattern Panel. Corneal Ectasia Preferred Practice Pattern. San Francisco, CA: AAO; 2024.