微型角膜刀相关
不完全角膜瓣:角膜刀中途停止导致不完全切开。复位角膜瓣后,考虑3~6个月后再次手术。
游离瓣(free cap):未形成铰链,角膜瓣完全分离。微型角膜刀的发生率报道为0.004~1.31%3)。如果基质床平整,可继续激光照射,用BSS保持湿润后复位,并用治疗性角膜接触镜固定。
纽扣孔(buttonhole):角膜瓣中央穿孔。发生率约为0.2%3)。复位角膜瓣,将再次手术推迟3~6个月。
薄/厚/不规则角膜瓣:与计划角膜瓣厚度的偏差。过薄的角膜瓣有降低角膜强度的风险。

LASIK是一种屈光矫正手术,在表面麻醉下制作约100微米的角膜瓣,对其下的角膜基质进行准分子激光照射,然后将瓣复位。瓣并发症是与瓣制作、复位及术后过程相关的结构性、炎症性和感染性障碍的总称。
屈光手术指南(第8版)将“瓣异常”和“弥漫性层间角膜炎(DLK)”列为LASIK术后并发症,并指出“可能发生各种瓣问题,需要适当处理”1)。
瓣并发症按发生时间分为术中(瓣制作至复位时)和术后(术后即刻至晚期)。也可按病理分为结构性、炎症性和上皮性。
瓣制作设备包括传统微型角膜刀和飞秒激光。目前大多数瓣由飞秒激光制作,提高了瓣的精度,显著减少了游离瓣、不规则瓣等术中并发症。然而,飞秒激光特有的并发症(如OBL、垂直气体突破)也已知。
SMILE是一种在角膜内制作透镜并取出而不制作角膜瓣的手术方式,因此原则上不会发生角膜瓣相关并发症。在基于证据的KLEx(小切口角膜基质透镜取出术)国际指南中,无角膜瓣被视为SMILE的安全性优势之一2)。
飞秒激光的引入大大提高了角膜瓣的精度,显著减少了游离瓣、不规则瓣等微型角膜刀特有的问题。然而,飞秒激光特有的并发症(OBL:不透明气泡层、纵向气体突破等)仍可能发生。此外,DLK、角膜瓣移位、上皮植入即使在飞秒激光使用时也可能发生。并发症并未完全消除,适当的术前评估和术中、术后管理仍然重要。
术中角膜瓣并发症主要源于角膜瓣制作设备的特性。微型角膜刀和飞秒激光使用时具有不同的并发症特征。及时识别和处理术中并发症对最终视力结果影响很大。术者需要在术前熟悉并发症应对方案,并做好术中果断判断的准备1)。
微型角膜刀相关
不完全角膜瓣:角膜刀中途停止导致不完全切开。复位角膜瓣后,考虑3~6个月后再次手术。
游离瓣(free cap):未形成铰链,角膜瓣完全分离。微型角膜刀的发生率报道为0.004~1.31%3)。如果基质床平整,可继续激光照射,用BSS保持湿润后复位,并用治疗性角膜接触镜固定。
纽扣孔(buttonhole):角膜瓣中央穿孔。发生率约为0.2%3)。复位角膜瓣,将再次手术推迟3~6个月。
薄/厚/不规则角膜瓣:与计划角膜瓣厚度的偏差。过薄的角膜瓣有降低角膜强度的风险。
飞秒激光相关
OBL(不透明气泡层):激光切开时产生的气泡滞留在角膜基质内的现象。多数自然消退,但侵入瞳孔区可能干扰眼球追踪。
纵向气体突破:气泡从切开面向房方向逸出。前房内气泡可能导致一过性眼压升高。
角膜瓣边缘不规则:激光参数设置问题导致边缘不规则。
点状切割错误:由于局部激光切割失败导致的不完全瓣变形。
发生游离瓣时,术者需判断是否继续激光照射。若基质床平整,可继续照射。游离瓣应在滴注BSS(平衡盐溶液)的湿润环境中处理,以防干燥变形。照射完成后,将游离瓣上皮面朝上,按正确轴向复位。术前的不对称标记对于确认正确方向至关重要。若基质床不平整,则不应进行激光照射,将瓣复位。
复位后常佩戴治疗性角膜接触镜(BCL)。角膜内皮泵功能可使瓣牢固再附着。术后约30分钟用胶带闭合眼睑可有效防止脱落。扁平角膜(低于40D)和吸引不足是游离瓣的主要危险因素,术前角膜曲率测量和选择合适的吸引环是预防的基础。
术后早期(术后1个月内)发生的瓣并发症可分为结构性、炎症性和上皮相关三类。
瓣结构性并发症
瓣移位:术后早期因外伤或揉眼发生。需紧急掀瓣、BSS冲洗和复位。术后1周内需特别注意。据报道,术后1周内发生率为0.1-0.3%4)。
瓣皱褶(条纹/皱褶):宏观皱褶(肉眼可见的皱褶)可能影响视功能,若随时间未减轻,应早期进行瓣复位。微观皱褶通常对视功能影响较小。
炎症性并发症
上皮相关并发症
上皮植入:上皮细胞从瓣边缘侵入界面并增殖。发生率报道为0.5%~2%(增效术后高达20%)6)。轻症观察。若进展超过2mm或视力下降,则行掀瓣、刮除及边缘处理。
瓣边缘上皮病变:瓣边缘上皮不规则或台阶。多数保守治疗可缓解。
基于Linebarger/Goodman分类的四级分级用于决定治疗方案5)。
| 分级 | 表现 | 对视力影响 | 治疗方案 |
|---|---|---|---|
| 1级 | 仅周边部白色颗粒状浸润(中央部正常) | 几乎无影响 | 1%泼尼松龙眼药水每1~2小时频繁滴眼 |
| 2级 | 浸润向中央扩展 | 轻度下降 | 继续或增加类固醇眼药水;次日复诊 |
| 3级 | 严重浸润到达中央;基质融解的早期迹象 | 中度下降 | 继续使用类固醇眼药水;强烈考虑掀瓣和冲洗 |
| 4级 | 中央基质融解(角膜溶解)和瘢痕形成 | 显著下降 | 紧急掀瓣和冲洗;考虑全身使用类固醇 |
术后1个月或更晚发生的瓣相关问题被归类为术后晚期并发症。
晚期瓣移位:由于LASIK瓣在术后多年仍不能完全愈合,外伤(如车祸、运动时直接眼部外伤等)可能导致术后数年甚至更晚发生瓣移位4)。一旦发现瓣移位,治疗原则是掀瓣、冲洗和复位;时间越长,上皮植入的风险越高。已有术后5年以上的外伤病例报告,从患者教育的角度强调告知主治医生屈光手术史的重要性1)。
晚期上皮植入进展:术后早期发现的轻度上皮植入可能在数年内增大,导致瓣融解和不规则散光。增效手术(再次矫正手术)已知是增加上皮植入风险的因素,对于有此类病史的眼,建议缩短术后观察间隔6)。掀瓣和刮除后的复发率据报道为5-20%,边缘酒精处理或瓣边缘缝合(爱惜邦)等附加措施被认为有效6)。
持续性干眼:LASIK术后角膜神经切断导致的反射性泪液分泌减少在大多数病例中于术后6-12个月恢复,但部分病例会持续为顽固性干眼7)。屈光手术指南(第8版)明确将干眼列为LASIK术后并发症,要求术前评估和积极的术后治疗1)。SMILE与FS-LASIK的比较研究表明,SMILE术后角膜神经密度恢复更快,对泪液参数的影响更小7),这成为术式选择的一个考虑因素。
瓣边缘坏死:作为一种罕见并发症,可能发生瓣边缘缺血性坏死。在角膜地形图上表现为特征性的边缘起伏。
术后角膜扩张:由于制作瓣后残留基质床(RST)不足或术前潜伏性圆锥角膜显现,术后可能发生角膜扩张。LASIK术后角膜扩张的患病率据报道约为每10万眼90例14),约为PRK(约20例)的4.5倍14)。RST < 280 μm是角膜扩张风险急剧增加的阈值,PTA(组织改变百分比)≥ 40%也被认为是独立危险因素13)。Randleman评分系统通过综合评估角膜形态异常、RST低值、年轻、角膜薄和高度近视这五个因素,可实现术前风险分层11)。
屈光手术指南(第8版)规定,术后次日必须进行裂隙灯显微镜检查以检查异常,并持续随访至术后6个月1)。
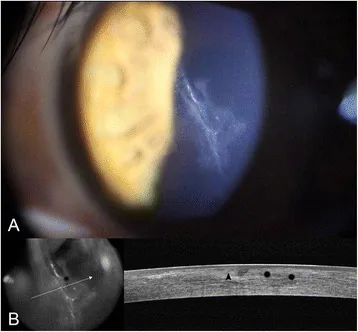
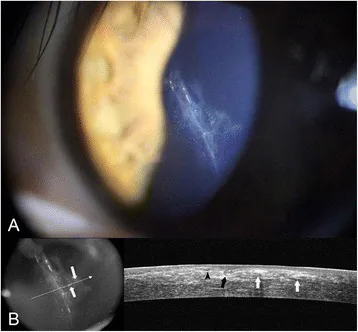
裂隙灯显微镜检查:对瓣并发症的诊断和监测最为重要。通过后部照明评估瓣下浸润和界面状态。1~2级DLK的特征是周边部细点状浸润,及时识别向中央扩展是治疗决策的依据。上皮植入表现为从瓣边缘向内侧的白色混浊,定量记录从边缘到中央的距离(mm)很重要。
眼前节OCT(AS-OCT):对于评估瓣厚度和残留基质床、确认上皮植入的深度和范围、以及鉴别DLK与界面液综合征(IFS)至关重要。IFS中瓣下可见均匀的低亮度液体层,而DLK主要表现为点状或线状高亮度区域8)。眼前节OCT还可量化瓣移位的程度(移位距离和深度),有助于判断治疗的紧急程度。
眼压测量:鉴别DLK和IFS所必需。Goldmann压平眼压计中央测量可能因液体垫效应出现假性低值,因此推荐周边测量或动态轮廓眼压计测量8)。
角膜地形图:用于评估瓣皱褶、不规则散光和扩张症。通过术后系列观察可捕捉变化。4级DLK导致基质溶解后,需使用Pentacam等断层成像检查后表面高度变化,评估是否发生圆锥角膜。
角膜培养和涂片:若怀疑瓣下感染(如前房炎症、充血、致密浸润、瓣边缘脓性分泌物等),应在瓣掀起的同时采集培养以鉴定菌种和药敏。感染性角膜炎在临床上可能与DLK相似,因此怀疑时应尽早进行微生物学检查。
| 并发症 | 治疗 | 紧急程度 |
|---|---|---|
| 1~2级DLK | 泼尼松龙1%滴眼液每1~2小时一次 | 半紧急(次日复诊) |
| 3级DLK | 类固醇滴眼液 + 考虑瓣膜提起和冲洗 | 紧急(当天至次日) |
| 4级DLK | 紧急瓣膜提起和冲洗(考虑全身使用类固醇) | 紧急(当天) |
| 瓣膜移位(早期) | 瓣膜提起、BSS冲洗、复位、气泡固定 | 紧急(当天) |
| 瓣膜移位(晚期) | 瓣膜提起、冲洗、复位(同时去除上皮植入) | 紧急(发现当天) |
| 瓣膜皱褶(影响视功能) | 瓣膜提起、复位、再固定 | 亚紧急(数日内) |
| 上皮植入(≥2mm/视力下降) | 掀瓣、刮除、边缘酒精处理 | 计划(观察后) |
| 游离帽(术中) | 用BSS保护、消融后准确复位、BCL固定 | 术中处理 |
| 不完全瓣/纽扣孔 | 瓣复位、手术延期 | 3-6个月后考虑再次手术 |
DLK的治疗方案根据分级(严重程度)而不同。1-2级时,使用泼尼松龙1%滴眼液每1-2小时频繁滴眼治疗。大多数病例通过这种类固醇滴眼治疗可缓解。3级时,在上述基础上考虑掀瓣冲洗。4级(中央基质溶解)需要紧急掀瓣冲洗,并考虑全身使用类固醇。不要自行判断,如果术后感觉瓣下混浊或视力下降,请立即联系您的眼科医生。
瓣并发症的发生率因手术方式(微型角膜刀 vs. 飞秒激光)、机构经验和患者选择标准而有很大差异。以下为主要文献中得出的发生率3)12)。
| 并发症 | 发生率 | 设备 |
|---|---|---|
| 游离帽 | 0.004%~1.31% | 微型角膜刀(飞秒激光极为罕见) |
| 纽扣孔 | 约0.2% | 微型角膜刀 |
| OBL(不透明气泡层) | 10%~30% | 飞秒激光(多数自行消退) |
| 角膜瓣移位(术后1周内) | 0.1%~0.3% | 两种设备均常见 |
| DLK(所有分级) | 0.1%~1% | 两种设备均常见 |
| 上皮植入 | 0.5%~2%(增强术后可达20%) | 两种设备通用 |
| 术后角膜扩张 | 每10万眼约90例 | LASIK总体 |
随着飞秒激光的普及,游离帽、纽扣孔等严重术中并发症显著减少。但需注意,即使使用飞秒激光,DLK、瓣移位、上皮植入仍可能发生12)。
DLK 3~4级、伴瓣融解的严重上皮植入、大面积瓣皱褶,若治疗延迟可导致永久性视力下降。Stulting等12)的流行病学调查显示,约0.1%的DLK进展为基质融解(4级),即使接受适当治疗,仍有部分残留不规则散光的报道。LASIK术后高危早期建议术后1周内每日或隔日复查1)。
LASIK瓣通过使用微型角膜刀或飞秒激光在角膜前表面下约100μm处进行板层切开制作。飞秒激光通过光致破裂形成等离子体和微气泡线性排列来形成切面。微型角膜刀通过机械切削进行切开。对于有角膜混浊或曾行放射状角膜切开术(RK)的病例,可选择使用微型角膜刀或选择PRK。
DLK是一种非感染性界面炎症反应。角膜基质切削碎屑、手术器械残留物、上皮来源刺激物等在瓣界面诱导多形核白细胞浸润。通常为一过性炎症,可自然缓解,但进展至4级时会发生基质融解(角膜溶解),成为永久性不规则散光的原因。术后1~3天内复查,早期发现和早期干预对预后至关重要。
瓣缘的上皮细胞侵入瓣下界面并增殖。侵入的上皮细胞在瓣下形成细胞巢,随着增大,导致瓣融解、不规则散光和视力下降。进行瓣提升的增强手术后风险增加。瓣边缘位置和既往手术史是危险因素6)。
LASIK术后,角膜瓣与角膜基质未完全愈合,瓣对角膜结构强度几乎没有贡献。瓣越厚,残留基质床(RST)越薄,对角膜生物力学的影响越大9)。残留基质床变薄与角膜扩张风险增加相关,当RST < 280 μm时风险急剧上升2)。与SMILE相比,LASIK术后角膜生物力学脆弱性更大,术后12个月时角膜阻力因子(CRF)降低量有显著差异(MD, −1.13; 95% CI −1.36〜−0.90; P<0.001)2)。
有限元分析模拟研究定量显示了瓣厚度对生物力学的影响9)。随着瓣厚度增加,角膜后表面的前移量增加,较薄的瓣更有利于后表面稳定性。但过薄的瓣容易出现制作精度问题(不均匀、OBL等)。飞秒激光可以±10 μm的精度制作瓣,因此可以安全制作100〜120 μm左右的薄瓣,建议在生物力学和瓣可靠制作之间取得平衡。术后残留基质床(RST)的绝对值是LASIK中扩张风险评估的最重要指标,当RST < 280 μm时建议重新考虑手术适应证2)15)。
瓣下的封闭空间需要与普通角膜感染不同的管理。应根据致病菌选择抗生素滴眼液,重症病例需进行瓣提升和冲洗。屈光矫正手术指南(第8版)指出“术者必须严格遵守高级屏障预防措施,严格进行器械灭菌、术野消毒和铺巾”1)。
界面液综合征(IFS)是由类固醇引起的眼压升高导致的瓣下液体聚集,与DLK的鉴别是使治疗方案发生180度转变的关键问题。IFS表现为眼压升高(注意Goldmann压平眼压计可能出现假性低值),前段OCT显示均匀的低反射液体层。由于继续使用类固醇会加重IFS,因此必须通过前段OCT和眼压测量进行鉴别8)。迟发性IFS可能在术后数月至数年发生,一旦发现瓣下液体聚集,必须进行眼压测量(尤其是周边或动态轮廓眼压计)8)。
通过改变瓣制作角度(垂直和水平斜面角度)以及调整瓣蒂的宽度和角度,提高了瓣的稳定性,降低了术后瓣移位的风险。特别是有报告称,上方蒂比鼻侧蒂具有更好的术后稳定性10)。也有观点认为,将瓣边缘侧切角设计为锐角(侧切角≥90°)可降低边缘上皮植入的风险10)。此外,飞秒激光在瓣厚度均匀性方面优于微型角膜刀,有限元分析已量化了瓣厚度对生物力学的影响9)。
由于SMILE不制作瓣,因此本节所述的瓣相关并发症(瓣移位、DLK、上皮植入、游离帽、纽扣孔)原则上不会发生。KLEx指南显示,LASIK的角膜膨隆发生率为每10万眼90例,而SMILE为11例,表明SMILE的术后角膜膨隆风险较低2)。然而,SMILE也有其特有的并发症,如层间炎症(DLK样)、透镜残留和帽切开等。
当术后角膜扩张进展时,角膜交联术(CXL)是一线治疗。标准方法是德累斯顿方案,即滴用0.1%核黄素后照射UVA(3 mW/cm²,30分钟),大多数病例的进展会停止15)。加速CXL(9 mW/cm²×10分钟)可缩短治疗时间15)。CXL对LASIK术后角膜扩张的有效性略低于对圆锥角膜的有效性,但早期干预可改善预后15)。在日本,自2022年起CXL已纳入医保。通过使用Randleman评分系统进行术前风险评估11)以及AAO角膜扩张PPP17)推荐的术前筛查,最大限度地预防角膜扩张的发生至关重要。
监测设施层面的DLK发生率并识别聚集性发生(短期内多例集中出现)非常重要。聚集性发生通常提示手术室污染、器械灭菌不充分或清洗液问题16)。如果发生率超过0.5%,建议对手术室、器械和清洗液进行全面检查。
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第8版). 日眼会誌. 2024;128(2):135-138.
Wang Y, Xie L, Yao K, et al. Evidence-Based Guidelines for Keratorefractive Lenticule Extraction Surgery. Ophthalmology. 2025;132:397-419.
Moshirfar M, Anderson E, Hsu M, et al. LASIK flap complications. StatPearls. 2024.
Ursea R, Feng MT, Zhou M, Cain W, Weikert MP. Temporal analysis of LASIK flap displacement presenting as late complication. Clin Ophthalmol. 2011;5:1535-1538.
Johnson JD, Harissi-Dagher M, Pineda R, et al. Diffuse lamellar keratitis: incidence, associations, outcomes, and a new classification system. J Cataract Refract Surg. 2001;27(10):1560-1566.
Jabbur NS, Chicani CF, Kuo IC, O’Brien TP. Risk factors in interface epithelial ingrowth after LASIK. J Refract Surg. 2004;20(4):343-348.
Recchioni A, Sisó-Fuertes I, Hartwig A, et al. Short-term impact of FS-LASIK and SMILE on dry eye metrics and corneal nerve morphology. Cornea. 2020;39(7):851-857.
Vera-Duarte GR, Guerrero-Becerril J, Müller-Morales CA, et al. Delayed-onset pressure-induced interlamellar stromal keratitis (PISK) and interface epithelial ingrowth 10 years after laser-assisted in situ keratomileusis. Am J Ophthalmol Case Rep. 2023;32:101874.
Fang L, Wang Y, Yang R, et al. Effects of the LASIK flap thickness on corneal biomechanical behavior: a finite element analysis. BMC Ophthalmol. 2020;20:67.
Slade SG. The use of the femtosecond laser in the customization of corneal flaps in laser in situ keratomileusis. Curr Opin Ophthalmol. 2007;18(4):314-319.
Randleman JB, Woodward M, Lynn MJ, Stulting RD. Risk assessment for ectasia after corneal refractive surgery. Ophthalmology. 2008;115:37-50.
Stulting RD, Randleman JB, Cowan LA, Thompson KP, Bradley EV, Lynn MJ. The epidemiology of diffuse lamellar keratitis. Cornea. 2004;23(7):680-688.
Santhiago MR, Smadja D, Gomes BF, et al. Association between the percent tissue altered and post-LASIK ectasia in eyes with normal preoperative topography. Am J Ophthalmol. 2014;158:87-95.e1.
Moshirfar M, Tukan AN, Bundogji N, et al. Ectasia after corneal refractive surgery: a systematic review. Ophthalmol Ther. 2021;10:753-776.
Hersh PS, Stulting RD, Muller D, et al. U.S. multicenter clinical trial of corneal collagen crosslinking for treatment of corneal ectasia after refractive surgery. Ophthalmology. 2017;124:1475-1484.
Linebarger EJ, Hardten DR, Lindstrom RL. Diffuse lamellar keratitis: diagnosis and management. J Cataract Refract Surg. 2000;26(7):1072-1077.
American Academy of Ophthalmology Corneal/External Disease Preferred Practice Pattern Panel. Corneal Ectasia Preferred Practice Pattern. San Francisco, CA: AAO; 2024.