角膜パラメータ

屈折矯正手術後のエクタジア(角膜拡張症)
1. 屈折矯正手術後のエクタジアとは
Section titled “1. 屈折矯正手術後のエクタジアとは”屈折矯正手術後のエクタジア(iatrogenic keratectasia / post-refractive surgery ectasia)は、LASIK・PRK・SMILEなどの屈折矯正手術後に角膜実質が進行性かつ偏心性に菲薄化し、前表面・後表面が急峻化する病態である。屈折矯正手術における最も重篤な合併症の一つとされ、屈折矯正手術のガイドライン(第8版)でもエキシマレーザー手術の術後合併症として明記されている1)。
不可逆的であり、裸眼視力・眼鏡矯正視力の双方を著しく低下させる。進行が確認された場合は早期介入が予後を左右する。
術後エクタジアの全体的な有病率は0.02〜0.6%と報告される。角膜拡張症は角膜厚不足、既存の潜伏型(subclinical)円錐角膜の悪化、および遺伝的に規定された拡張症の術後顕在化によって生じると考えられている9)。リスク因子が特定されている症例でも、既知の因子をいずれも持たない個人がエクタジアを発症した報告があり、特に若年層に多い。
屈折矯正手術希望者の最大6%に何らかの臨床下拡張性疾患が存在すると推定されており、術前スクリーニングの精度が発症率を左右する9)。
術式別の発症率
Section titled “術式別の発症率”術式によってエクタジア発症リスクは大きく異なる。
| 術式 | 有病率(10万眼あたり) | 主な特徴 |
|---|---|---|
| LASIK | 約90 | フラップ作製により角膜バイオメカニクスが低下。リスクが最も高い |
| PRK | 約20 | フラップなし。LASIKの約1/4のリスク |
| SMILE | 約11 | キャップが角膜強度に一定程度寄与する可能性2) |
LASIKの発症率はPRKの約4.5倍である3)。ただしSMILEは承認後の追跡期間が短く、過小評価の可能性がある3)。
2. リスク因子と術前スクリーニング
Section titled “2. リスク因子と術前スクリーニング”
エクタジアの最も重要な予防策は、術前の徹底したリスク評価である。
主要なリスク因子
Section titled “主要なリスク因子”Jin et al.7)によるリスク因子の包括的レビューでは、術後エクタジアの発症予測における角膜形状・断層撮影・バイオメカニクス評価の組み合わせの重要性が強調されており、単一指標では感度が不十分であることが示されている。Randleman et al.14)のリスクスコアリングシステムは5因子を組み合わせることで術前スクリーニングの精度を向上させる実践的なツールとして広く使用されている。
患者要因
若年: 34歳未満。18歳以下では77%に断層撮影上の進行が認められた10)
強度近視: 多量の切除が必要となり残余実質床が不足しやすい
円錐角膜の既往・家族歴
眼をこする習慣: 進行と関連する唯一の確認された生活習慣因子9)
アトピー性疾患の合併9)
安全閾値の基準
Section titled “安全閾値の基準”KLEx(小切開角膜片抽出術)のエビデンスに基づく国際ガイドラインでは、以下の安全閾値を推奨している2)。
| 指標 | 安全基準 | 禁止基準 |
|---|---|---|
| RST(残余角膜実質床) | ≧280μm | <250μm(測定誤差考慮後も不可) |
| LT index(LT/CCT比) | ≦28% | 28%超 |
| PTA(組織変化率)※LASIK | <40% | ≧40% |
SMILE(KLEx)ではPTA計算の解釈がLASIKと異なる。キャップはフラップと異なり角膜構造強度に寄与するため、LASIK基準のPTA閾値をそのまま適用することには議論がある2)。
Randleman拡張症リスクスコアリングシステム
Section titled “Randleman拡張症リスクスコアリングシステム”Randlemanらが提唱した拡張症リスクスコアリングシステムでは、以下の5因子に各0〜4点を割り当てて総合評価を行う14)。
| 因子 | 高リスク基準 |
|---|---|
| 角膜形状解析像 | 異常パターン(最重要予測因子) |
| RST厚 | 低値(<280μm) |
| 年齢 | 若年(34歳未満) |
| 角膜厚 | 低値(500μm未満) |
| 近視度数 | 強度(8D超) |
ロジスティック回帰分析では「異常な角膜形状解析像」が最も重要な予測因子であった9)。
角膜バイオメカニクス評価
Section titled “角膜バイオメカニクス評価”角膜形状解析やRST単独では術後エクタジア予測の感度は70%を超えない2)。マルチモーダルデータによる包括的評価が必要である。バイオメカニクス的な拡張症疑い基準として、CBI(Corvis Biomechanical Index)> 0.5 かつ TBI(Tomographic and Biomechanical Index)> 0.29 が提唱されており、TBI(SUCRA 96.2)、CBI(SUCRA 83.8)が早期円錐角膜検出に有用である2)。
3. 臨床所見と診断
Section titled “3. 臨床所見と診断”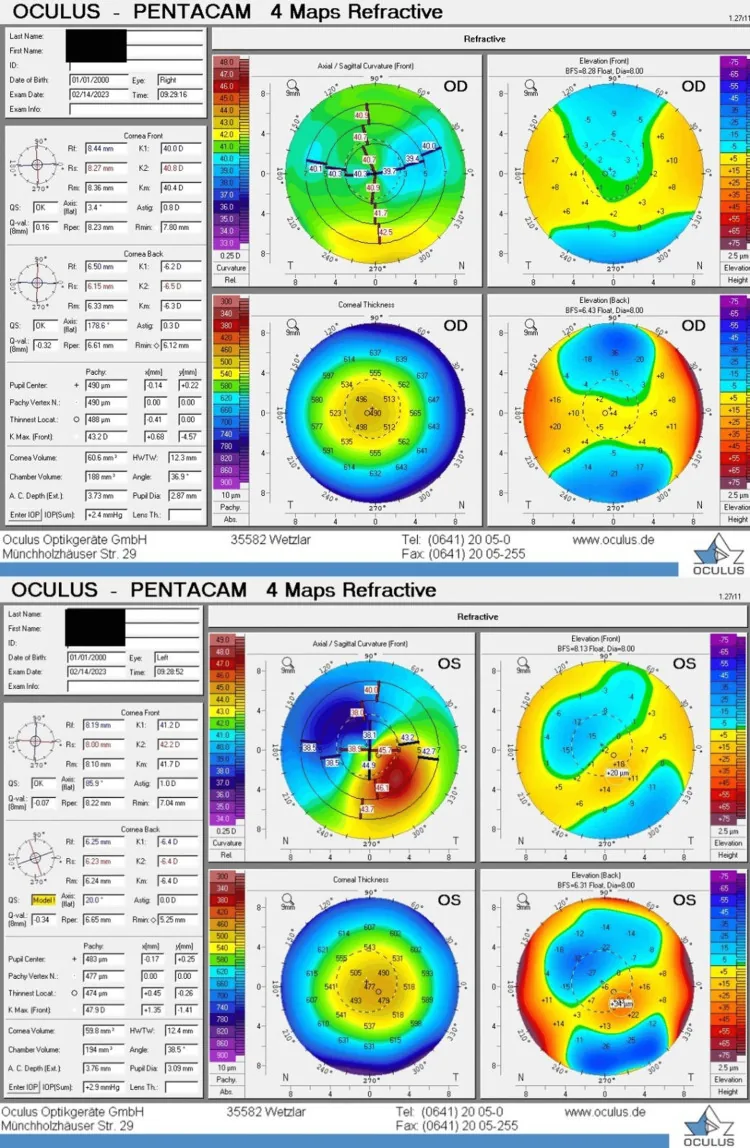
術後数か月〜数年を経て以下の症状が出現する。いずれも進行性であることが特徴である。
- 進行性の視力低下(眼鏡矯正でも不十分)
- 不正乱視による歪み・複視・多重視
- 眩しさ・光輪(ハロー)・光芒(グレア)の増悪
- コンタクトレンズの不快感増加(フィッティング不良・頻繁な脱落)
- 屈折値の急速な変化・眼鏡度数の頻繁な変更が必要となる
- 下方または鼻側の見え方の歪み(角膜前突部の方向に対応)
初期症状は軽微で、経過観察中の角膜形状解析で偶然発見されることも多い。特に術前のベースライン角膜形状解析との比較が早期発見に不可欠である。術後3〜6か月ごとの経時的なシェインプラグ断層撮影(Pentacam等)が推奨される5)。
角膜形状解析所見
下方急峻化(inferior steepening): I/S比≧1.2
角膜屈折力の急峻化: 46D超はエクタジアを示唆
非対称的パターン: スキュー(skewed radial axes)21°超
角膜断層撮影所見
後面エレベーション上昇: 角膜後面の前方突出が初期変化
最薄点の偏心: 角膜厚マップでの偏心
BAD-D値上昇: 1.65超で拡張症疑い2)
細隙灯顕微鏡所見
Fleischer ring: 円錐底部の上皮内鉄沈着
Vogt’s striae: デスメ膜の皺
角膜頂点の瘢痕: 進行例で出現
診断に用いる検査
Section titled “診断に用いる検査”角膜断層撮影(Tomography): シェインプラグカメラ(Pentacam等)により角膜の3次元評価(前後表面+全角膜厚マップ)が可能になる9)。角膜形状解析(Topography)はプラチドディスクに基づき角膜前表面のみを画像化するが、Tomographyでは前後両面を評価できるため、術後拡張症の早期診断に不可欠とされる。
Belin-Ambrósio Enhanced Ectasia Display(BAD): Pentacamで利用可能なソフトウェアで、9つのパラメータを解析して「D値(BAD-D)」を算出する9)。BAD-D > 1.65は拡張症疑いの閾値であり、前方隆起・後方隆起・パキメトリックデータを統合した多変量指標として有用である。
上皮厚マッピング: 中心部の上皮菲薄化と周囲の上皮肥厚からなる「ドーナツパターン」は角膜拡張症で特徴的に認められる9)。高解像度AS-OCTや高周波超音波で評価する。
波面収差解析: 高次収差増加(コマ収差優位)の確認に有用である。
前眼部OCT(AS-OCT): 角膜全層断面・フラップ深度確認・パキメトリーマッピングが可能である。
2015年の国際コンセンサスでは「拡張症の進行」を以下のパラメータのうち少なくとも2つにおいて測定ノイズを超える一貫した変化が認められることと定義した5)。
若年患者(18歳以下)では77%に断層撮影上の進行が認められたとの報告があり10)、同一機器での3〜6か月ごとの経時的評価が推奨される。
| 進行指標 | 閾値 |
|---|---|
| KMAX | +1.20D以上10) |
| 後方隆起 | +24.3μm以上10) |
| 最薄点角膜厚 | −30.5μm以上10) |
術後エクタジアと自然発症の円錐角膜は角膜形状・臨床所見が類似するが、屈折矯正手術の既往の有無が鑑別の鍵となる。円錐角膜疑いで施術を受け術後に拡張が顕在化したケースと、正常角膜での術後エクタジアは病態的に連続している部分もある6)。鑑別に際しては、手術記録(フラップ厚・切除深・術後RST)の確認が重要である。
角膜拡張症(エクタジア)は屈折矯正手術後の医原性病態、円錐角膜は自然発症の変性疾患という点で原因が異なります。しかし両者の臨床像(角膜菲薄化・急峻化・不正乱視)と発症機序(角膜バイオメカニクスの破綻)は本質的に類似しており、潜伏型円錐角膜が手術侵襲により顕在化したケースも多いとされています6)。鑑別は手術既往の有無と術前データの確認が基本です。
角膜形状解析(プラチドディスク)だけでは不十分です。シェインプラグ断層撮影(Pentacam等)による前後表面と角膜厚の3次元評価が必須です。BAD-D値の算出、AS-OCTによる上皮厚マッピング、角膜バイオメカニクス測定(Corvis ST等)を組み合わせた包括的評価が推奨されます2)。
4. 治療と管理
Section titled “4. 治療と管理”エクタジアの治療方針は、①進行阻止と②視機能の矯正・回復の二本柱である。進行が確認された時点での早期介入が視機能温存に重要である。
| 治療法 | 適応 | 目的 |
|---|---|---|
| 角膜クロスリンキング(CXL) | 進行確認時・第一選択 | 進行阻止(コラーゲン架橋強化) |
| ハードコンタクトレンズ(RGP) | 不正乱視が強い場合 | 視機能矯正 |
| 角膜内リング(ICRS) | 中等度エクタジア | 不正乱視軽減 |
| CXL + topography-guided PRK | 進行したエクタジア | 不正乱視矯正と進行阻止の同時達成 |
| CXL + ICRS | 中等度〜高度エクタジア | 複合的アプローチ |
| 全層角膜移植(PKP) | 高度進行例・角膜混濁 | 最終手段 |
| 深部層状角膜移植(DALK) | 内皮機能が保たれている例 | PKP代替(内皮温存) |
角膜クロスリンキング(CXL)
Section titled “角膜クロスリンキング(CXL)”進行が確認されたエクタジアに対する第一選択治療である1)9)。CXLの目的は角膜コラーゲン間の架橋結合を強化することで角膜の構造的安定化を図ることであり、以下のプロトコルがある。
標準法(Dresden protocol):角膜上皮を直径8〜9mmの範囲で除去したのち0.1%リボフラビン点眼を30分間(2分毎)施行し、紫外線A(UVA:370nm、3mW/cm²)を30分間照射する。総UVAエネルギーは5.4J/cm²。長期の安定化効果が確立されている9)。
加速法(accelerated CXL):より高強度のUVAを短時間照射する(例:9mW/cm²×10分、30mW/cm²×3分)。治療時間を短縮できるが、長期成績は標準法と比較して劣るとの報告もあり、エネルギー密度の最適化が研究されている11)。
経上皮(transepithelial)CXL:上皮を除去せずにリボフラビンを浸透させるプロトコル。侵襲が少ない一方、標準法より効果が劣るとの報告が多い9)。
CXL後は多くの症例で進行が停止し、若干の角膜急峻化の改善(1.0〜2.5D程度の平坦化)が得られることもある9)。米国FDAはCXLを14〜65歳の進行性円錐角膜・屈折矯正手術後エクタジアに承認しており、日本では2022年より保険適用されている。
Hersh et al.15)の米国多施設試験では、屈折矯正手術後エクタジアに対するCXLが有効性・安全性の基準を満たし、治療1年後の最大角膜屈折力(Kmax)の有意な低下と角膜形状の安定化が確認された。未治療対照群と比較して治療群では進行が有意に抑制されており、エクタジアへの早期CXL介入の有効性が実証されている15)。
CXLの禁忌:UVA照射時の角膜実質厚400μm未満は内皮障害のリスクがあるため禁忌である9)。
CXLの合併症:点状角膜炎・角膜混濁・光過敏・疼痛・感染性角膜炎・滅菌性浸潤・非治癒性上皮欠損・角膜浮腫等9)。
若年患者への早期CXL:若年患者(思春期前・若年者)では症状悪化を待たずに早期CXL介入が推奨される9)。KERALINK試験では18歳以下の進行性円錐角膜においてCXLが有効であることが示されており、CXLが長期的には角膜移植必要性を低下させることがシステマティックレビューで支持されている12)。
ハードコンタクトレンズ(RGP)
Section titled “ハードコンタクトレンズ(RGP)”角膜不正乱視による矯正視力低下に対する視機能矯正の主柱である。レンズ後面に涙液レンズを形成することで不正乱視を光学的に補正する。中等度までのエクタジアで有効であり、多くの患者で日常視機能の維持が可能となる。強膜レンズは進行例・不規則形状に有効である。センタリングと動きの良好なフィッティングが重要であり、球面レンズが不可能な場合は多段階カーブのレンズも選択できる9)。
トポグラフィーガイド下PRK + CXL
Section titled “トポグラフィーガイド下PRK + CXL”進行した拡張症に対して角膜不正乱視の軽減と構造安定化を同時に行うアプローチである。Athens protocol(Kanellopoulos)やLYRA/San Diego protocol(Motwani)などの計画手法が報告されている11)。RSB > 350μm・最大切除深50〜60μm以内・CXLとの同時施行が推奨されるが、エビデンスはまだ限定的である。
LYRA/San Diego protocolによる治療では、裸眼視力20/20・高次収差(HOA RMS)の有意な改善(1.642から0.920への低下)が報告されており11)、topography-guided PRK単独よりもCXL同時施行による角膜強化と組み合わせることで長期的な安定性が期待される。ただしこの術式は専門センターでのみ実施されており、術前の包括的な評価と患者の十分なインフォームドコンセントが必要である。
角膜内リングセグメント(ICRS)
Section titled “角膜内リングセグメント(ICRS)”ICRSはPMMAまたはポリカーボネート製の半円形インプラントを角膜実質内に埋植することで、角膜周辺部を機械的にサポートし、中央部の不正乱視を軽減する9)。FerraraリングやIntacsなど複数のデザインが存在し、角膜形状に応じた配置・厚さの選択が重要である。フェムトセカンドレーザーによるチャネル形成が現在の標準法であり、機械式より精度が高い。ICRSは視機能改善(UCVA・BCVA向上・高次収差減少)を目的とし、コンタクトレンズのフィッティング改善にも寄与する。CXLとの組み合わせ(通常CXL先行またはICRS後1〜6か月でCXL)が複合アプローチとして推奨される場合がある9)。
進行例で角膜混濁・瘢痕を伴い、コンタクトレンズによる矯正が不可能な場合に検討する。全層角膜移植(PKP)が従来の標準だが、内皮機能が正常な場合は深部層状角膜移植(DALK)が選択肢となる。DALKは内皮拒絶反応のリスクがなく、長期的な内皮細胞喪失がPKPより少ない可能性がある9)。
5. 白内障手術合併時のIOL度数計算
Section titled “5. 白内障手術合併時のIOL度数計算”エクタジアが進行すると近視と不正乱視を誘発し、白内障が合併した場合の眼内レンズ(IOL)度数計算が著しく困難となる。標準的な眼内レンズ計算式を用いた場合、術後遠視化(hyperopic surprise)を生じやすいため、専門的な対応が必要である13)。
IOL度数計算が困難な理由
Section titled “IOL度数計算が困難な理由”- 角膜後面急峻化による屈折力の過大評価:通常の角膜計測は固定換算係数(n=1.3375)を使用するが、エクタジアでは前後面比率が異なるため過大評価が生じる
- 不正乱視による計測不確実性:軸方向曲率マップの非対称性により、代表的な角膜曲率値の選択自体が困難
- 術式による影響の重複:屈折矯正手術既往(角膜形状変化)とエクタジアの影響が重複し、通常の算出式では補正が不十分
- ELP(有効レンズ位置)の予測誤差:角膜形状と前房深度の異常な組み合わせがELP予測を困難にする
推奨される対応
Section titled “推奨される対応”- Pentacam等のシェインプラグ断層撮影によるTK(True Keratometry)値を用いた度数計算(前後面の直接測定値を使用)13)
- Abulafia-Koch、Barrett True K(post-LASIK)、Potvin-Hill Pentacam等の術後屈折矯正眼専用計算式の使用
- 角膜移植後はレトロ反射法(Haigis-L等)や偏心測定値を利用した特殊計算を検討
- 術前の目標屈折値を正視〜軽度近視方向に設定し(conservative approach)、hyperopic surpriseを回避する
- IOL度数計算の不確実性を患者に十分説明し、必要に応じて術後の屈折矯正(眼鏡・コンタクトレンズ)計画を事前に立てておく
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”角膜バイオメカニクスの破綻
Section titled “角膜バイオメカニクスの破綻”屈折矯正手術後エクタジアの本態は、手術侵襲による角膜バイオメカニクスの破綻である。前実質の層板構造(Bowman膜直下の強固なコラーゲン)を損傷することで、眼圧に対する角膜の抵抗力が低下する。LASIKフラップの作製は前実質を完全に遊離させてしまうため、SMILEのキャップ設計よりもバイオメカニクス的に不利とされる。Reinstein et al.の数学モデルでは、PRK・LASIK・SMILEの相対的corneal tensile strengthが数値化されており、SMILEはLASIKと比較して前方実質を温存するため同等の矯正量においてより多くの角膜強度を保持する8)。
角膜バイオメカニクスの破綻は段階的に進行する。術直後は眼圧の正常な範囲内でも角膜が変形しやすい状態となり( biomechanical vulnerability)、術後数か月〜数年にわたって潜在的な角膜変形が顕在化することがある。このプロセスには、眼をこする習慣・アレルギーによる慢性的な機械的刺激・さらなる矯正手術(エンハンスメント)などの二次的侵襲が促進因子となる。バイオメカニクスの評価指標として、CH(角膜ヒステリシス)とCRF(角膜抵抗因子)は術前から術後を通じてモニタリングすることで進行リスクの変化を捉えることができる。術後にこれらの値が継続的に低下する場合は、エクタジア発症の前兆と解釈されることがある。術後にCorvis ST等によるバイオメカニクス測定を定期的に実施することが、エクタジアの早期発見に役立つ9)。
潜伏型円錐角膜の顕在化
Section titled “潜伏型円錐角膜の顕在化”術前に検出できなかった微細な角膜バイオメカニクスの脆弱性(潜伏型・subclinical円錐角膜)が、手術侵襲を契機に顕在化するケースが多い。forme fruste keratoconusへのLASIK施術後のエクタジア発症は1998年に最初に報告されている6)。
角膜後面エレベーションの意義
Section titled “角膜後面エレベーションの意義”角膜後面エレベーションの前方シフトがエクタジアの初期サインとして認識されている。前面の変化に先立って後面が変化する例もあり、後面評価を含む断層撮影が早期診断に不可欠である。
生化学的・遺伝的要因
Section titled “生化学的・遺伝的要因”角膜拡張症の病因には酵素活性異常と酸化ストレスが関与する9)。角膜ではマトリックスメタロプロテアーゼ(MMP)の増加とTIMP(組織メタロプロテアーゼ阻害物質)の減少が認められ、基質分解が進行する。遺伝的素因(Ehlers-Danlos症候群・骨形成不全症等のコラーゲン異常疾患)を有する患者では、眼をこするなどの環境的二次刺激や手術による医原性菲薄化を受けることで拡張症が顕在化しやすい9)。
術後エクタジアリスク因子の包括的評価
Section titled “術後エクタジアリスク因子の包括的評価”Jin et al.7)のレビューでは、術後エクタジアの主要なリスク因子として異常な角膜形状・薄い角膜・RST不足・高度近視・若年・眼をこする習慣が挙げられており、これらを組み合わせたリスクスコアリングが術前判断に有用であることが示されている。Randleman et al.14)のスコアリングシステムでは角膜形状異常が最も重要な予測因子であり、他の因子はそれを補完する役割を担う。Shetty et al.16)の研究では、SMILEとLASIKの術後バイオメカニクス変化を比較し、SMILEが術後12か月時点でより良好な角膜強度指標(CRF・CH)を維持することを示している。この優位性が術後エクタジア発症率の差に寄与していると考えられる16)。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”加速CXLの長期成績と最適化
Section titled “加速CXLの長期成績と最適化”加速法CXL(9mW/cm²×10分)によるLASIK術後エクタジアへの2年成績では、多くの症例で進行停止が達成され安全性が確認されている11)。ただし超加速法(45mW/cm²)では熱効果の影響が懸念されており、パルス照射(pulsed-light CXL)による最適化研究が進んでいる。
2021年のKERALINK試験12)では、16〜25歳の進行性円錐角膜患者を対象にCXLと経過観察を比較し、CXL群では3年時点でKmaxの有意な低下(−1.35D)と安定化が確認された。この試験結果はCXLの若年患者への積極的適応を支持するものであり、術後エクタジアにも同様の原則が適用される。
CXL術前には角膜実質厚が400μm以上であることが必要条件とされているが、薄い角膜(300〜400μm)に対してはhypotonic riboflavinやsub400プロトコル(少量のリボフラビンで角膜を膨張させてから照射)を用いることで、より薄い角膜でもCXLが施行可能な場合がある9)。
予防的CXLの可能性
Section titled “予防的CXLの可能性”ハイリスク患者(薄い角膜・若年・強度近視)を対象とした屈折矯正手術と同時のCXL(LASIK-CXL)が研究されており、一部の施設では実施されている。ただし現時点では標準治療ではなく、RCTによるエビデンス蓄積が必要である。
生体材料による角膜補強
Section titled “生体材料による角膜補強”新規コラーゲン架橋材料(例:グルコース含有リボフラビン、ルテイン含有製剤)やナノ粒子を用いた角膜補強材料の研究が進行中である。また、SMILEで摘出されたレンチクルを円錐角膜・術後エクタジアへの角膜インレイとして再利用する研究も注目されている。この「レンチクル再移植」アプローチは角膜バンク資源を活用しない自己または同種組織の利用という観点から将来的な可能性が期待されるが、現時点では研究段階であり一般臨床応用には至っていない9)。
ABCD分類とCXL効果判定
Section titled “ABCD分類とCXL効果判定”Pentacam等のABCD分類(A:前方半径曲率、B:後方半径曲率、C:最小角膜厚、D:最高矯正視力)を用いたCXL効果判定システムが普及しつつある。定量的な進行指標としての活用が期待される。ABCD分類は進行の判定基準として、同一機器での経時的な比較において感度が高く、術後エクタジアの管理においてもCXL前後の経過比較に有用である9)。
8. 参考文献
Section titled “8. 参考文献”-
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第8版). 日眼会誌. 2024;128(2):135-138.
-
Wang Y, Xie L, Yao K, et al. Evidence-Based Guidelines for Keratorefractive Lenticule Extraction Surgery. Ophthalmology. 2025;132:397-419.
-
Moshirfar M, Tukan AN, Bundogji N, et al. Ectasia after corneal refractive surgery: a systematic review. Ophthalmol Ther. 2021;10:753-776.
-
Santhiago MR, Smadja D, Gomes BF, et al. Association between the percent tissue altered and post-LASIK ectasia in eyes with normal preoperative topography. Am J Ophthalmol. 2014;158:87-95.e1.
-
Gomes JA, Tan D, Rapuano CJ, et al. Global consensus on keratoconus and ectatic diseases. Cornea. 2015;34:359-369.
-
Seiler T, Quurke AW. Iatrogenic keratectasia after LASIK in a case of forme fruste keratoconus. J Cataract Refract Surg. 1998;24:1007-1009.
-
Jin SX, Dackowski E, Chuck RS. Risk factors for postlaser refractive surgery corneal ectasia. Curr Opin Ophthalmol. 2020;31:288-292.
-
Reinstein DZ, Archer TJ, Randleman JB. Mathematical model to compare the relative tensile strength of the cornea after PRK, LASIK, and SMILE. J Refract Surg. 2013;29:454-460.
-
American Academy of Ophthalmology Corneal/External Disease Preferred Practice Pattern Panel. Corneal Ectasia Preferred Practice Pattern. San Francisco, CA: AAO; 2024.
-
Gore DM, et al. Tomographic progression of keratoconus in children and young adults. Br J Ophthalmol. 2024;108:176-182.
-
Motwani M, Agu E, Xu A, Yung M. Application of Surgical Protocols for the Treatment of Highly Irregular Astigmatism with Topographic Guided Ablation in a Case of Post-LASIK Ectasia. Int Med Case Rep J. 2025;18:91-98.
-
Larkin DFP, Chowdhury K, Burr JM, et al. Effect of corneal cross-linking versus standard care on keratoconus progression in young patients: The Keralink randomized controlled trial. Ophthalmology. 2021;128:1516-1526.
-
European Society of Cataract and Refractive Surgeons (ESCRS). ESCRS Clinical Guidelines for Cataract Surgery. ESCRS; 2024.
-
Randleman JB, Woodward M, Lynn MJ, Stulting RD. Risk assessment for ectasia after corneal refractive surgery. Ophthalmology. 2008;115:37-50.
-
Hersh PS, Stulting RD, Muller D, et al. U.S. multicenter clinical trial of corneal collagen crosslinking for treatment of corneal ectasia after refractive surgery. Ophthalmology. 2017;124:1475-1484.
-
Shetty R, Francis M, Shroff R, et al. Corneal biomechanical changes and tissue remodeling after SMILE and LASIK. Invest Ophthalmol Vis Sci. 2017;58:5703-5712.
