Intacs
形状:六角形断面、外径8.0mm・内径6.8mm。
厚さ:0.21〜0.45mm(0.05mm刻み)で屈折効果を調節する。
Intacs SK:内径6mm・楕円形断面の新型。急峻K値57D以上の重症例に対応する。
承認:米国FDAで唯一承認された合成ICRS製品である。

角膜内リングセグメント(ICRS:intrastromal corneal ring segments)は、角膜実質の約2/3深さ(中央光学帯の外側)に配置する合成弧状インプラントである。1987年に近視矯正用として導入された後、現在は円錐角膜やLASIK後拡張症などの角膜拡張性疾患に対する治療的介入として位置づけられる。
ICRSは角膜層板の間にスペーサーとして機能する。デバイスの厚さに比例して中央部の弧の長さを短縮させる(弧短縮効果:arc shortening effect)。この結果、角膜前面の中央部が平坦化し、リング挿入部に隣接する周辺領域は前方に押し出される。
Barraquerの法則に基づくと、角膜周辺部に組織を追加すれば中央部は平坦化する。ICRSはこの原理を利用した治療法である。デバイスが厚く直径が小さいほど、得られる屈折矯正効果は大きくなる。
ICRSは円錐角膜を根治する治療法ではなく、角膜移植の必要性を遅らせる外科的代替手段として位置づけられる。角膜クロスリンキング(CXL)の併用で進行停止効果が加わり、相乗効果が期待できる。
ICRS適応疾患である角膜拡張症では以下の症状を呈する。
症状は一般に思春期から20代で始まり、30歳頃に進行が緩徐化することが多い2)。
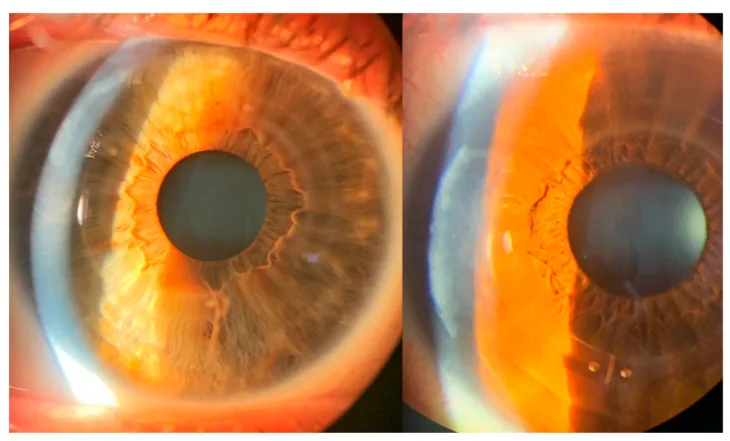
円錐角膜では角膜中央部〜傍中心部の突出と菲薄化を認める。角膜トポグラフィーで急峻化パターンを示す1)。角膜バイオメカニクスの変化は形態変化に先行して生じる1)。
特徴的な所見としてVogt線条(実質深層の縦走微細線条)、Fleischer環(円錐基底部の上皮内鉄沈着)、角膜瘢痕がある2)。細隙灯顕微鏡で中央からやや下方の角膜の前方突出・菲薄化を確認できる。
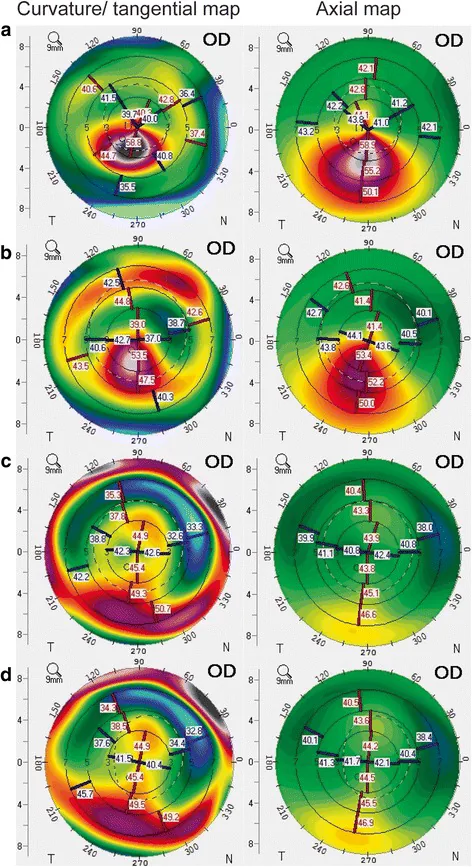
ICRS挿入後のトポグラフィーでは、角膜全体の平坦化・角膜頂点の中央への移動・角膜非球面性の維持・表面不正性の減少が示される。
ICRS適応疾患である角膜拡張症の病因は多因子性である。
角膜のコラーゲン分解が菲薄化の本態である1)。マトリックスメタロプロテアーゼ(MMP)の増加とTIMPの低下が認められる1)。涙液中のIL-6、TNF-α、MMP-9の増加がケラトサイトのアポトーシスを誘導する1)。
眼擦りは円錐角膜の主要なリスク因子である1)。アトピー性疾患(花粉症、喘息、湿疹、春季カタル)との関連が知られている1)。
円錐角膜は通常両眼性であるが重症度に左右差を認めることが多い。思春期に発症し30歳頃に進行が停止ないし緩徐になる傾向がある2)。治療介入なしでは約20%の症例が角膜移植を要する2)。
LASIK後拡張症は、術前に認識されなかった潜在的円錐角膜に対してレーザー屈折矯正手術を行った場合に生じうる1)。残存実質床の菲薄化や角膜構造の脆弱化が関与する。

角膜拡張症の診断には角膜トモグラフィー(Scheimpflug撮影やOCT)と角膜バイオメカニクス評価の併用が推奨される3)。
術前評価に必要な主要指数を以下に示す。
| 指標 | 特徴 |
|---|---|
| TBI(Tomographic Biomechanical Index) | 形態+バイオメカニクスの統合指標。診断性能が高い3) |
| CBI(Corvis Biomechanical Index) | 空気噴射による角膜変形応答の指標3) |
| SimK1/Ks | 強主経線の角膜曲率 |
| SAI / SRI | 角膜形状の対称性・均一性 |
| CRF(角膜抵抗係数) | 角膜の総合的な剛性を反映する3) |
単一の指標では偽陰性を生じうるため、角膜トモグラフィーとバイオメカニクス評価を組み合わせた包括的スクリーニングが推奨される3)。円錐角膜ではバイオメカニクスの変化が形態変化に先行するため、早期検出に有用である1)。
前眼部OCT(CASIA等)は断層像と角膜形状を高解像度(約10μm)で取得でき、混濁部の検出精度に優れる。ICRS植込み後の深度・位置評価にも有用である。
小児・若年者の円錐角膜では進行速度が速い場合がある4)。KERALINK試験では若年患者におけるクロスリンキングの進行抑制効果が検討された4)。
術前には角膜トモグラフィー(Pentacam等)で前後面曲率・角膜厚マップ・エレベーションマップを取得する。角膜バイオメカニクス評価(TBI・CBI・CRF)と組み合わせた包括的評価が推奨される。前眼部OCTでリング挿入部位の角膜厚を計測し、450μm以上を確認することが重要である。
主要なICRS製品の特徴を以下に示す。
Intacs
形状:六角形断面、外径8.0mm・内径6.8mm。
厚さ:0.21〜0.45mm(0.05mm刻み)で屈折効果を調節する。
Intacs SK:内径6mm・楕円形断面の新型。急峻K値57D以上の重症例に対応する。
承認:米国FDAで唯一承認された合成ICRS製品である。
Ferrara / KeraRings
断面:三角形(プリズム効果で羞明を軽減)。
光学帯:4.5〜6.0mmで、Intacsより小さいため平坦化効果が強い。
弧の長さ:90°〜355°の多様な選択肢がある。
適応:主に円錐角膜の屈折矯正に用いる。
CAIRS / CTAK
チャンネル作成法には機械的解離法とフェムトセカンドレーザー法がある1)。植込み深度は角膜厚の70〜80%が合成ICRSの一般的な基準である。フェムトセカンドレーザーでは厚み計測マップに基づき正確な深度・径でチャネルを作成する1)。
CAIRSはより浅い深度(35〜70%)でも挿入可能であり、より大きな平坦化効果が期待できる5)。
ICRS挿入後の平均角膜曲率変化は2.14〜9.60Dと幅がある。球面度数・乱視度数・等価球面屈折値の減少が報告されている。中等度円錐角膜(Kmax 58.0D未満)で最も有効とされる1)。ただし乱視変化は予測困難なことがある1)。
| 術式 | Kmax改善 | CDVA改善 | 特記事項 |
|---|---|---|---|
| 合成ICRS単独 | 2〜10D平坦化 | 1〜2段階改善 | 重症例では不十分なことがある |
| ICRS+CXL同時 | ICRS単独より優れる | 球面誤差でも改善 | メタアナリシスで推奨1) |
| CAIRS | Kmax 57.8→53.6D | CDVA 0.52→0.19 logMAR | 露出・融解リスクが低い5) |
ICRSとCXLの同時施行に関するメタアナリシス(12か月追跡・6研究)では、同時施行がCXL先行・ICRS先行のいずれよりも球面屈折誤差とsteep-Kで優れた結果を示した1)。
| 合併症 | 備考 |
|---|---|
| ICRS脱出 | 全抜去症例の48.2%を占める。平均発症時期は術後約10年 |
| セグメント移動 | 浅い植込み・幅の不適合で発生しやすい |
| 感染性角膜炎 | 両方式で報告あり。重症例は眼内炎に至る可能性がある |
| 角膜瘢痕・融解 | 稀だが視力に影響する |
| 層板内沈着物 | 最大74%に出現。視機能への影響は少ない1) |
| 術中穿孔 | 機械的:前方穿孔。レーザー:不完全チャネル |
ICRS単独では円錐角膜の進行を止められないことがある。CXLとの同時施行は、CXL先行やICRS先行よりも球面屈折誤差とsteep-Kにおいて優れた結果を示した1)。Chanらの報告ではIntacs+CXL併用がIntacs単独よりも円錐角膜改善に有効であった6)。HashemianらによるICRS+CXL+tPRK(角膜トポグラフィーガイドPRK)の3段階治療では、Kmax値の持続的改善が6か月追跡で確認されている8)。
Faria-Correiaら(2023年)は輪部切開(limbal incision)アプローチによるICRS植込みの成績を報告した9)。輪部からの進入は角膜の光学域を回避でき、術後角膜瘢痕リスクが低減する。AAO角膜拡張症PPP(2024年)では機械的解離法・フェムトセカンドレーザー法ともに同等の成績が示されているとされ、フェムトセカンドレーザー法がより精確なチャネル深度制御を提供する1)。
円錐角膜の有病率は一般集団の50〜230人/10万人(最新の大規模メタアナリシスでは138人/10万人)と報告されている15)。治療介入なしでは約20%が角膜移植を要するため、早期のCXL・ICRSによる介入が重要である2)。Pédrettiらのメタアナリシス(2022年)ではICRS挿入後の平均UDVAとCDVAの有意な改善が確認されている11)。Vega-Estradaらの5年間長期追跡では、ICRS挿入後の屈折・視力改善効果が5年間維持されることが示され、長期的な有効性と予測可能性が確認された12)。Rabinowitzeの1998年の総説では有病率を0.05%と報告していたが15)、最新のAAO角膜拡張症PPP(2024年)はこの値を大きく上回る可能性を示唆している1)。
Nuzziら(2025年)は合成ICRSの長期合併症後にCAIRSへ置換する手技を報告した7)。前眼部OCTで評価された耳側ポケット入口部の上皮下実質線維化を持つ症例において、合成ICRSを抜去し3か月後にCAIRSを挿入した。術後Kmaxは68.9→61.9D、UCVA 20/400→20/30に改善した。合成ICRSが失敗した症例でもCAIRSが有効な救済策となりうる。
角膜拡張症の治療において、ICRSはコンタクトレンズ不耐症・視力障害が進行しているが中央角膜が透明な症例に適応される。全層角膜移植(PKP)・深層前層角膜移植(DALK)の前段階として位置づけられる。AAO PPPではDALKの利点として内皮拒絶反応リスクがなく、眼球破裂リスクもPKPより低いことを挙げている1)。近年の角膜移植件数の減少傾向はCXL・ICRSによる早期介入の普及を反映していると考えられる。屈折矯正ガイドライン(第8版)では円錐角膜はエキシマレーザー手術の禁忌・SMILE手術の禁忌として明確に規定されており10)、適切な術前スクリーニングが重要である。
ICRS挿入術を受けた患者への術後指導の主要ポイント:
AAO角膜拡張症PPP(2024年)に基づく診断基準と評価指標1):
ABCD分類(Scheimpflugカメラ統合)では以下のパラメータを0〜4のスコアで評価する:
AAO角膜拡張症PPP(2024年)と臨床実践から一般的な治療アルゴリズムを以下に示す1)。
ICRS脱出(extrusion)は、進行性の角膜実質菲薄化と上皮破綻によりリングが角膜表面から突出する合併症である。全抜去症例の**48.2%**を占め、発症時期は平均約10年であるが術後1か月〜20年の間のどの時点でも起こりうる。
CAS-OCTによる術後早期のリスク層別化が有用である。植込み後第1週・第1か月に平均深度パーセンテージ60%未満またはトンネル深度70%未満の症例を高リスクと判定する。
| リスク要因 | 詳細 |
|---|---|
| リング移動 | 薄い角膜にICRS幅が広すぎる、トンネルが浅い・狭い |
| 角膜融解 | 切開創近くのリング配置、感染・外傷・実質分離による炎症 |
| CXL同時施行 | 偏心性コーン+グレード3円錐角膜で移動・融解リスク増加 |
抜去はICRS脱出の根本的治療である。適応は脱出のほか、視力の質の低下・変動、角膜融解、感染性角膜炎、コンタクトレンズ不耐症、角膜穿孔である。
切開法は状況に応じて2通りある。脱出が切開部位の近くであればシンスキーフックで以前の入口を開く。切開部位が治癒済みであれば、元の深さに設定したダイヤモンドナイフで脱出リング下に切開窓を作成する。いずれの場合も10-0ナイロン縫合糸で欠損部を閉鎖する。
感染性角膜炎合併時
培養検査:結膜・角膜擦過物による培養を全例で実施する。
治療:高濃度抗菌点眼薬と抜去を併用する。抜去なしの抗菌薬単独でも有効な場合がある。
重症例:眼内炎への進展があり全身抗菌薬を使用。早期の全層角膜移植が代替案となりうる。
術後管理
リング抜去後に矯正視力・乱視・近視の悪化は認めなかった。層状混濁の痕跡は時間経過とともに減少する。
主な予防策は3つある。「パキメトリーの法則」を遵守しリング厚を植込み部位の角膜厚の半分未満にする。フェムトセカンドレーザーでチャネル深度80%のトンネルを正確に作成する。リングの先端を切開創から離して配置する。術後はCAS-OCTで早期にリング位置の安定性を確認する。
角膜の弾性係数(elastic modulus)は、力が加わった際に弾性的に変形しようとする性質を定量化した指標である。円錐角膜では実質の病理的変化により弾性係数が低下している。
弾性係数の低下はコラーゲン線維の分解と変性に起因する3)。これによりバイオメカニカル破綻サイクルが始動する。応力レベルが上昇・再分布し、角膜の急峻化と菲薄化が進行する3)。菲薄化部位では局所的に応力がさらに増大し、突出が悪化する悪循環を形成する。
ICRSはこの悪循環に対し以下のメカニズムで介入する。
Andreassen らは円錐角膜実質の弾性係数が正常角膜の約60%に低下していることを報告している13)。この弾性低下が角膜拡張症の主要なバイオメカニクス的背景であり、ICRSはその構造的補強として機能する。
ICRSの効果は角膜実質のコラーゲン骨格の構造的特性と密接に関連する。実質は角膜厚の90%を占め、その機械的特性が角膜全体のバイオメカニクスを規定している。
ICRS脱出の病態はリング移動と角膜融解の2つの機序に大別される。
リング移動は浅い植込みに起因する。ICRSを浅く配置すると前方の引張歪みが増大し、実質圧縮が生じる。前方実質深度の圧縮が進行すると上皮・実質の破綻をきたし、角膜菲薄化を経て自然脱出に至る。
角膜融解は潜在的な炎症過程を反映する。切開およびトンネル作成時の手術侵襲が進行性のケラトサイトアポトーシスと組織変性を誘発する。MMPの関与が示唆されており、外因性刺激の導入が角膜マトリックスの分解と菲薄化をもたらす。
CAIRS(Corneal Allogenic Intrastromal Ring Segments)は、ドナー角膜組織由来の実質セグメントを実質内に挿入する。合成ICRSと同様のアーチ短縮効果で円錐部分の曲率を減少させる。
合成ICRSは角膜深層(70〜80%深度)への挿入が必要だが、CAIRSはより浅い深度(35〜70%)でも挿入可能であり、より大きな平坦化効果を生み出す可能性がある5)。
同種セグメントは無血管で細胞密度の低い角膜実質層に植え込まれる。この環境では線維性癒着が最小限に抑えられ、手術の可逆性が保たれる。合成ICRSで問題となる角膜融解・急性実質壊死・角膜新生血管のリスクも低減される5)。
角膜バイオメカニクス評価の進歩が注目されている。TBIやCBIなどの新しい指標は、従来の形態学的指標を補完し、早期円錐角膜の検出精度を向上させている3)。バイオメカニクス指標と角膜トモグラフィーの統合評価により、屈折矯正手術の予測精度が25%以上改善したとの報告がある3)。
CXLとICRSの併用に関するメタアナリシスでは、12か月追跡の6研究で同時施行がCXL先行よりも球面屈折誤差とflat-Kにおいて優れ、steep-KではCXL先行・ICRS先行の両方よりも優れた結果を示した。1)
系統的レビュー(AlQahtaniら、2025年)によると、CAIRS植え込み後の平均UDVAは0.83→0.40 logMAR、CDVAは0.52→0.19 logMARに改善した。等価球面度数は−7.09D→−2.34Dに減少し、Kmaxは57.8→53.6D、Kmeanは49.3→45.3Dに低下した5)。CXLの長期効果については、Caporossiらのシエナ眼クロス研究(平均追跡期間6年)でリボフラビン・UV-A角膜クロスリンキングが円錐角膜の進行を74%の症例で停止・改善させたことが報告されている14)。
CTAKでも同様の改善が報告されている。平均UDVAは1.21→0.61 logMAR、CDVAは0.63→0.34 logMARに改善した5)。
CAIRSの合併症は少なく軽微である。一過性ドライアイとチャネル内沈着が最も多いが臨床的に有意ではない。グレアやハローは合成ICRSと比較して著しく低い頻度であった5)。
合成ICRSの合併症発生率は最大30%と報告されている5)。ICRS露出・前房内迷入・角膜融解等の合併症に対し、CAIRSによるレスキューが成功例として複数報告されている5)。49歳女性のICRS不全例(UCVA 20/400)では合成ICRSを除去し3か月後にCAIRSを挿入、Kmax 68.9→61.9D、UCVA 20/30に改善した5)。
今後の主要な課題として以下が挙げられる。