โรคเส้นประสาทตา ที่เกี่ยวข้องกับอะมิโอดาโรน (AAO N) เป็นความผิดปกติของเส้นประสาทตา ที่เกิดขึ้นระหว่างการใช้ยาต้านจังหวะเต้นผิดปกติอะมิโอดาโรน โดยประมาณการอุบัติการณ์อยู่ที่ 0.3–2%ผลข้างเคียงทางตาที่พบบ่อยที่สุดคือ กระจกตา เสื่อมแบบเกลียว (70–100%) แต่โรคเส้นประสาทตา รุนแรงที่สุด
มีลักษณะเด่นคือเริ่มต้นแบบค่อยเป็นค่อยไปและมี papilledema ที่คงอยู่นาน (นานถึง 15 เดือนหลังจากหยุดยา) และการแยกความแตกต่างจากโรคเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่ใช่หลอดเลือดแดงอักเสบ (NAION ) เป็นความท้าทายทางคลินิกที่ใหญ่ที่สุด
ประมาณหนึ่งในสามของผู้ป่วยไม่มีอาการ ดังนั้นการตรวจติดตามดวงตาเป็นประจำจึงสำคัญ
หลักการรักษาคือการหยุดยาที่สงสัย แต่เนื่องจากเป็นยารักษาภาวะหัวใจเต้นผิดจังหวะที่ร้ายแรงถึงชีวิต จึงจำเป็นต้องประสานงานกับแพทย์โรคหัวใจ
หลังจากหยุดอะมิโอดาโรน การมองเห็น ดีขึ้นเพียง 58% ของผู้ป่วย แย่ลง 21% และถึงขั้นตาบอดตามกฎหมาย (น้อยกว่า 20/200) ใน 20%
อะมิโอดาโรนเป็นอนุพันธ์ของเบนโซฟูแรนที่มีไอโอดีนสองอะตอม ซึ่งพัฒนาขึ้นในทศวรรษ 1960 เพื่อเป็นยารักษาโรคหลอดเลือดหัวใจตีบ จัดเป็นยาต้านจังหวะเต้นผิดปกติคลาส III แต่ยังมีคุณสมบัติของคลาส I, II และ IV ร่วมด้วย 1) มีการจ่ายอย่างกว้างขวางสำหรับภาวะหัวใจห้องบนสั่นพลิ้ว หัวใจห้องล่างเต้นเร็ว และหัวใจห้องล่างสั่นพลิ้ว และเป็นที่รู้จักในญี่ปุ่นภายใต้ชื่อการค้า Ankaron (ต่างประเทศคือ Cordarone, Pacerone เป็นต้น)
อะมิโอดาโรนมีชีวประสิทธิผลทางปาก 30–80% ครึ่งชีวิตยาวมาก 20–100 วัน มีคุณสมบัติละลายในไขมันสูงและสะสมในเนื้อเยื่อไขมัน 1) ถูกเมแทบอลิซึมโดย CYP3A4/CYP2C8 ในตับเพื่อสร้างเมแทบอไลต์ที่ออกฤทธิ์ desethylamiodarone (DEA) 1)
อะมิโอดาโรนทำให้เกิดผลข้างเคียงทางตาหลายประการ
กระจกตา เสื่อมแบบเกลียวกระจกตา เกิดขึ้นในสองในสามของผู้ป่วยที่ใช้ยา สัมพันธ์กับขนาดยาและระยะเวลาการรักษา ปรากฏเกือบ 100% ที่ขนาดสูง (400 มก./วัน) ประเมินโดยการจำแนก Orlando เกรด I–IV หากมีเพียงกระจกตา เสื่อมแบบเกลียว โดยทั่วไปสามารถใช้อะมิโอดาโรนต่อไปได้โรคเส้นประสาทตา ที่เกี่ยวข้องกับอะมิโอดาโรน (AAO N)อื่นๆ : เลนส์ตาขุ่นใต้แคปซูลด้านหน้า กุ้งยิง หลายจุด ตาแห้ง เป็นต้น
นอกจากนี้ยังมีผลข้างเคียงทางระบบต่างๆ เช่น ความผิดปกติของต่อมไทรอยด์ พิษต่อปอด (ปอดอักเสบจากภูมิไวเกิน ซึ่งอาจถึงแก่ชีวิต) โรคเส้นประสาทส่วนปลาย และการไวต่อแสง
ในการศึกษาตามรุ่นของ Cheng และคณะ โดยใช้ฐานข้อมูลประกันสุขภาพแห่งชาติของไต้หวัน (กลุ่มที่ได้รับ amiodarone 6,175 คน เทียบกับกลุ่มควบคุม 24,700 คน) พบโรคเส้นประสาทตา ในกลุ่ม amiodarone ร้อยละ 0.3 โดยมี hazard ratio 2.09 (95% CI 1.13–3.85) เมื่อเทียบกับกลุ่มที่ไม่ได้รับ (0.1%)1) .
Q
เมื่อรับประทาน amiodarone มีโอกาสเป็นโรคเส้นประสาทตาเท่าใด?
A
ในการศึกษาตามรุ่นของไต้หวัน พบว่าผู้ใช้ amiodarone ร้อยละ 0.3 เป็นโรคเส้นประสาทตา โดยมี hazard ratio 2.09 เมื่อเทียบกับกลุ่มที่ไม่ใช้1) รายงานย้อนหลังแสดงอุบัติการณ์ร้อยละ 0.36–2 และอุบัติการณ์รายปีสูงสุดโดยประมาณในการศึกษาไปข้างหน้าแบบ double-blind (มากกว่า 1,600 คน) อยู่ที่ร้อยละ 0.23–0.741) .
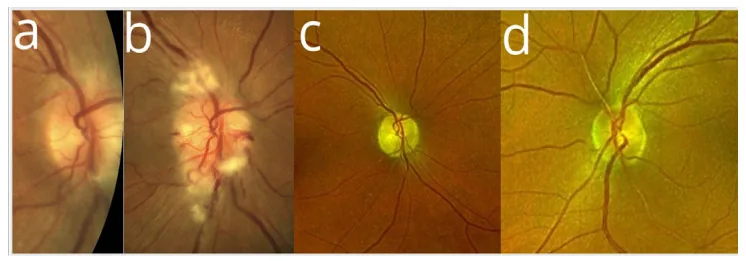
????????????????? Dina Lešin Gaćina et al. Is Semaglutide Linked to
NAION ? A Case Report on a Rare Ocular Complication. Reports. 2025 Aug 20; 8(3):149. Figure 1. PM
CI D: PMC12372079. License: CC BY.
???????????????????????????????????????????????????????????????????????????
การมองเห็น ลดลงไม่มีอาการ : ผู้ป่วย AAO N มากถึงหนึ่งในสามไม่มีอาการที่รับรู้ มักพบเพียงจากภาวะบวมของจานประสาทตา ความผิดปกติของการมองเห็นสี (dyschromatopsia)
ผลการตรวจทางคลินิกหลักของ AAO N แสดงดังต่อไปนี้
จานประสาทตา บวมจานประสาทตา บวมคงอยู่นานเฉลี่ย 3 เดือน (สูงสุด 15 เดือน) หลังจากหยุด amiodaroneจานประสาทตา บวมแบบต่อเนื่องจานประสาทตา บวมปรากฏในตาอีกข้าง 3–48 สัปดาห์หลังจากเริ่มในตาแรก1) .ร่วมกับการสะสมของกระจกตา แบบเกลียว : พบได้บ่อยร่วมกับพิษต่อเส้นประสาทตา
Patel และคณะได้เสนอการจำแนก 5 ประเภทดังต่อไปนี้2)
ชนิดเริ่มต้นแบบแอบแฝง
ประเภทที่พบบ่อยที่สุด : แสดงภาวะ papilledema ร่วมกันทั้งสองข้างและดำเนินไปอย่างช้าๆ มักมีอาการน้อย
ชนิดคล้ายโรคเส้นประสาทตาขาดเลือดส่วนหน้าชนิดไม่ใช่หลอดเลือดแดงอักเสบ
ประเภทที่พบบ่อยเป็นอันดับสอง : แสดงการสูญเสียการมองเห็น เฉียบพลันข้างเดียวหรือทั้งสองข้าง คล้ายคลึงทางคลินิกกับโรคเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่ใช่หลอดเลือดแดงอักเสบ
ชนิดหลังลูกตา
วินิจฉัยยากที่สุด : แสดงจอประสาทตา ปกติ ต้องใช้การตรวจภาพและการตรวจเลือดเพื่อวินิจฉัย
ชนิดอื่นๆ
ชนิดความดันในกะโหลกศีรษะสูง : ความดันน้ำไขสันหลังเกิน 200 มม. H₂O
ชนิดดำเนินไปช้า : papilledema ปรากฏขึ้นภายในไม่กี่วันถึงไม่กี่สัปดาห์หลังจากหยุด amiodarone
ระยะเวลาการใช้ amiodarone : ระยะเวลาเฉลี่ยจนกระทั่งเกิด AAO N คือ 9 เดือน (ช่วง 1–84 เดือน) มีรายงานค่ามัธยฐานประมาณ 4 เดือน2) หากระยะเวลาการรักษาเกินค่ามัธยฐาน 41 วัน ความเสี่ยงของโรคเส้นประสาทตา เพิ่มขึ้น 3.5 เท่า1) ขนาดสะสม : ขนาดสะสมและระยะเวลาการรักษามีความสำคัญในการประเมินความเสี่ยงมากกว่าขนาดรายวัน1) ค่ามัธยฐานของขนาดยาในผู้ป่วยที่มีอาการทางตาคือ 200 มก./วัน (ช่วง 57–1,200 มก./วัน)เพศ : จากการทบทวนผู้ป่วย 296 ราย อายุเฉลี่ย 66 ปี 74% เป็นเพศชาย เพศชายมีความเสี่ยงสูงกว่าเพศหญิงประมาณ 3 เท่า 1) ความดันโลหิตสูง : ในเพศชาย การใช้ยา amiodarone และความดันโลหิตสูงเป็นปัจจัยเสี่ยงที่สำคัญต่อโรคเส้นประสาทตา 1) การมีปัจจัยเสี่ยงโรคหัวใจและหลอดเลือดร่วม : ผู้ป่วยที่ใช้ยา amiodarone จำนวนมากมีปัจจัยเสี่ยงโรคหัวใจและหลอดเลือด ซึ่งเพิ่มความเสี่ยงต่อการเกิดโรคเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่ใช่หลอดเลือดแดงอักเสบ (NA-AION) ลักษณะของ NA-AION ที่เกี่ยวข้องกับ amiodarone ได้แก่: การเกิดทั้งสองข้าง, การเริ่มแบบค่อยเป็นค่อยไป, การสูญเสียลานสายตาแบบทั่วไป (ไม่ใช่ hemianopsia แนวนอน), และอาการบวมของจานประสาทตา ที่ยาวนานเป็นเดือน
แนะนำให้รับการประเมินทางจักษุวิทยาเป็นระยะในช่วงปีแรกหลังจากเริ่มใช้ยา amiodarone และหลังจากนั้นตรวจปีละครั้ง หากคุณรู้สึกว่าการมองเห็น เปลี่ยนไป (พร่ามัว, การรับรู้สีเปลี่ยนไป) ให้ไปพบจักษุแพทย์ทันที
Q
การลดขนาดยา amiodarone จะลดความเสี่ยงของโรคเส้นประสาทตาหรือไม่?
A
ขนาดยารายวันไม่ใช่ปัจจัยเสี่ยงที่มีนัยสำคัญ ในขณะที่ขนาดยาสะสมและระยะเวลาการรักษาถือว่าสำคัญกว่า 1) รายงานระบุว่าการเกินระยะเวลาการรักษาเฉลี่ย 41 วันจะเพิ่มความเสี่ยง 3.5 เท่า ดังนั้นจึงจำเป็นต้องติดตามแม้ในกรณีใช้ระยะสั้น
AAO N เป็นการวินิจฉัยทางคลินิก และไม่มีเกณฑ์การวินิจฉัยที่เป็นกลางที่ชัดเจน
สงสัย AAO N เมื่อมีอาการต่อไปนี้ร่วมกัน:
การเริ่มแบบค่อยเป็นค่อยไป
การดำเนินโรคช้า
อาการบวมของจานประสาทตา ที่ยาวนาน (คงอยู่นานหลายเดือนแม้หลังจากหยุดยา amiodarone)
หลุมขนาดใหญ่ในตาอีกข้าง (ลักษณะจานประสาทตา ที่ไม่มีความเสี่ยง)
ความผิดปกติของเส้นประสาทตา เล็กน้อย (การมองเห็น 20/40 หรือดีกว่า, RAPD ≤ 0.9 หน่วยล็อก)
ผู้ป่วย NA-AION ทุกรายควรสอบถามประวัติการใช้ยา amiodarone และหากมีประวัติควรแจ้งให้แพทย์โรคหัวใจทราบ โรคเส้นประสาทตา จากยาควรให้ความสำคัญโดยสอบถามประวัติการใช้ยาและสงสัยเป็นอันดับแรก
การแยกโรคระหว่าง AAO N และภาวะเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่ใช่อักเสบจากหลอดเลือดแดงเป็นความท้าทายทางคลินิกที่สำคัญที่สุด ตารางต่อไปนี้แสดงจุดแยกโรคหลัก
จุดแยกโรค ภาวะเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่ใช่อักเสบจากหลอดเลือดแดง AAO N ลักษณะการเริ่มต้น เฉียบพลัน – หลายวันถึงหลายสัปดาห์ ค่อยเป็นค่อยไปถึงเฉียบพลัน ลักษณะของจานประสาทตา จานประสาทตา ที่มีความเสี่ยง (จานเล็ก)ไม่มีลักษณะจำเพาะ ระยะเวลาของจานประสาทตา บวม หายไปใน 2–6 สัปดาห์ คงอยู่นาน 1–15 เดือน ข้าง มักเป็นข้างเดียว มักเป็นสองข้าง
ต้องระมัดระวังในการแยกจากหลอดเลือดแดงอักเสบชนิดเซลล์ยักษ์ด้วย มีรายงานผู้ป่วยชายอายุ 72 ปีที่ใช้ยา amiodarone และสงสัยว่าเป็น AAO N แต่ได้รับการยืนยันว่าเป็นหลอดเลือดแดงอักเสบชนิดเซลล์ยักษ์โดยการตัดชิ้นเนื้อหลอดเลือดแดงขมับ 3) ในหลอดเลือดแดงอักเสบชนิดเซลล์ยักษ์ การตัดชิ้นเนื้ออาจให้ผลบวกแม้ว่า ESR และ CRP จะปกติ 3) นอกจากนี้ ในหลอดเลือดแดงอักเสบชนิดเซลล์ยักษ์ MRI อาจแสดงการเพิ่มความเข้มของปลอกประสาทตา (optic perineuritis) ซึ่งเป็นลักษณะที่ไม่พบใน AAO N 3)
การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน ของจอตา : เพื่อยืนยันภาวะ papilledema สองข้างและเลือดออกที่ผิวของ papillaการตรวจลานสายตา Humphrey ความบกพร่องของลานสายตา แบบ hemianopia ถึง scotoma ส่วนกลางMRI : ปกติใน AAO N โดยไม่มีการเพิ่มความเข้มของเส้นประสาทตา ในกรณีที่สงสัยหลอดเลือดแดงอักเสบชนิดเซลล์ยักษ์ ให้ตรวจสอบว่ามีการเพิ่มความเข้มของปลอกประสาทตา (optic perineuritis) หรือไม่ 3)
หลักการรักษาโรคเส้นประสาทตา จากยาคือการหยุดยาที่สงสัย
เนื่องจาก amiodarone ใช้รักษาภาวะหัวใจเต้นผิดจังหวะที่คุกคามชีวิต จึงไม่สามารถหยุดยาได้โดยง่าย ให้ดำเนินการตามขั้นตอนต่อไปนี้
ปรึกษาแพทย์โรคหัวใจอย่างเร่งด่วน : หารือเกี่ยวกับการเปลี่ยนไปใช้ยาทางเลือกหรือการทำ catheter ablation กับแพทย์โรคหัวใจหากมีเพียง corneal verticillata : โดยทั่วไปสามารถใช้ amiodarone ต่อไปได้หากเกิด AAO N : ควรปรึกษาความเสี่ยงและประโยชน์ของการใช้ยาต่อไปอย่างรอบคอบระหว่างแพทย์โรคหัวใจ จักษุแพทย์ และผู้ป่วยหากมีโรคเส้นประสาทตา ที่มีอยู่ก่อน : ผู้เชี่ยวชาญบางท่านแนะนำให้หลีกเลี่ยงการใช้ amiodarone
ผลลัพธ์ทางสายตาหลังหยุดยามีดังนี้:
การมองเห็น ดีขึ้น: 58%ไม่เปลี่ยนแปลง: 21%
การมองเห็น แย่ลงอีก: 21%ตาบอดตามกฎหมาย (น้อยกว่า 20/200 ในตาข้างเดียวหรือทั้งสองข้าง): 20%
ปัจจุบันยังไม่มีการรักษาด้วยยาที่เป็นมาตรฐานสำหรับ AAO N
ประมาณ 21% ของผู้ป่วยมีการมองเห็น แย่ลงอีกแม้หลังจากหยุด amiodarone แล้ว อาการบวมของจานประสาทตา อาจคงอยู่นานถึง 15 เดือนหลังหยุดยา จึงจำเป็นต้องติดตามผลทางจักษุวิทยาในระยะยาว ครึ่งชีวิตของ amiodarone ยาวมาก (20-100 วัน) ทำให้ยายังคงอยู่ในร่างกายเป็นเวลานานหลังจากหยุดยา 1)
Q
หากหยุด amiodarone การมองเห็นจะดีขึ้นหรือไม่?
A
หลังจากหยุด amiodarone การมองเห็น ดีขึ้นเพียง 58% ของผู้ป่วย ไม่เปลี่ยนแปลง 21% แย่ลงอีก 21% และ 20% ถึงขั้นตาบอดตามกฎหมาย (น้อยกว่า 20/200) นอกจากนี้ ครึ่งชีวิตที่ยาว (20-100 วัน) หมายความว่ายายังคงอยู่ในร่างกายหลังจากหยุดยา 1)
กลไกหลักของ AAO N เชื่อว่าเกิดจากความเสียหายของแอกซอนที่เกี่ยวข้องกับ phospholipidosis (phospholipidosis)
ความผิดปกติของไลโซโซม : Amiodarone ยับยั้ง sphingomyelinase ในไลโซโซม ทำให้เกิด phospholipidosis 1) การสะสมของ lamellar inclusion : Lamellar inclusion ในไซโทพลาสซึมจะสะสมอย่างเฉพาะเจาะจงในแอกซอนขนาดใหญ่ของเส้นประสาทตา การเปลี่ยนแปลงที่คล้ายกันยังพบในแอกซอนและเซลล์ชวานน์ของเส้นประสาทส่วนปลายในโรคปลายประสาทอักเสบที่เกิดจาก amiodaroneการรบกวนการไหลของแอกโซพลาสซึม : Lamellar body จะลดการไหลของแอกโซพลาสซึมทั้งทางกลและทางชีวเคมี ซึ่งถือเป็นกลไกของการบาดเจ็บเส้นประสาทตา 1) การรบกวนนี้อาจทำให้เกิด papilledemaความเครียดออกซิเดชันและอะพอพโทซิส : Amiodarone กระตุ้นการสังเคราะห์ H₂O₂ ในไมโทคอนเดรียและการสร้างอนุมูลอิสระออกซิเจน ทำให้เกิดความเสียหายของเซลล์จากออกซิเดชัน 1) ผลต่อเซลล์ปมประสาทจอตา : ในการทดลองในหนู พบว่ามีอะพอพโทซิส ของเซลล์ปมประสาทจอตาและการลดลงของคลื่น a และ b ในคลื่นไฟฟ้าจอตา 1)
Q
Amiodarone ทำลายเส้นประสาทตาด้วยกลไกใด?
A
Amiodarone ยับยั้ง sphingomyelinase ในไลโซโซม ทำให้เกิด phospholipidosis และนำไปสู่การสะสมของ lamellar inclusion ในแอกซอนของเส้นประสาทตา 1) การสะสมนี้ขัดขวางการไหลของแอกโซพลาสซึม ทำให้เกิด papilledema ร่วมกับความเสียหายของเซลล์จากความเครียดออกซิเดชัน ส่งผลให้การทำงานของเส้นประสาทตา ลดลง
Liao และคณะ (2007) แสดงให้เห็นในแบบจำลองเซลล์ RPE ว่า IGF-1 ปกป้องเซลล์ RPE จากความเครียดออกซิเดชันและอะพอพโทซิส ที่เกิดจาก amiodarone ผ่านวิถี PI3K/Akt 1) ความมีชีวิตของเซลล์ RPE ลดลงตามความเข้มข้นของ amiodarone (LC50 = 50 μM) และ IGF-1 ยับยั้งผลนี้ การยับยั้งวิถี MAPK ไม่มีผลต่อฤทธิ์ป้องกัน 1)
การศึกษาในหนูปี 2017 แสดงให้เห็นว่า amiodarone ส่งผลต่อชั้นเซลล์ปมประสาทจอตา และ IGF-1 สามารถย้อนกลับผลนี้ได้ 1) การประยุกต์ใช้ IGF-1 ในอนาคตสำหรับการรักษา AAO N ยังคงต้องศึกษาเพิ่มเติม
ในการศึกษาไปข้างหน้าแบบอำพรางสองฝ่ายของ Mindel และคณะ (2007) (ผู้เข้าร่วมมากกว่า 1,600 คน ระยะเวลาการรักษามัธยฐาน 45.5 เดือน) ไม่มีรายงานการสูญเสียการมองเห็น ทั้งสองข้าง และอัตราการเกิดโรคต่อปีโดยประมาณสูงสุดคือ 0.23–0.74% 1) ซึ่งขัดแย้งกับรายงานย้อนหลังก่อนหน้านี้ (0.36–2%) และยังคงมีการถกเถียงกันว่า AAO N เป็นตัวตนของโรคที่แยกจากกันทางคลินิกจากภาวะเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่เกิดจากหลอดเลือดแดงอักเสบหรือไม่
ในกรณีหลอดเลือดแดงอักเสบชนิดเซลล์ยักษ์ ผล MRI ที่พบการเพิ่มความเข้มของปลอกประสาทตา (optic perineuritis) รายงานใน 57–78% ของกรณี ซึ่งเป็นผลที่ไม่พบใน AAO N 3) ในอนาคต การประเมินผล MRI อย่างเป็นระบบในกรณีที่สงสัย AAO N อาจช่วยเพิ่มความแม่นยำในการวินิจฉัยแยกโรค
Mitchell R, Chacko J. Clinical and Mechanistic Review of Amiodarone-Associated Optic Neuropathy . Biomolecules. 2022;12:1298.
Patel S, Mahmood R. Amiodarone-Associated Optic Neuropathy in a Patient With Associated Arrhythmia. Cureus. 2024;16(3):e55819.
Tseng AM, Bindiganavile SH, Bhat N, Divatia MK, Lee AG. Optic Perineuritis Distinguishing Arteritic Ischaemic from Amiodarone-Associated Optic Neuropathy . Neuro-Ophthalmology. 2021;45(5):329-333.
ถาม AI เกี่ยวกับบทความนี้
คัดลอกข้อความบทความแล้ววางในผู้ช่วย AI ที่คุณต้องการใช้
เปิดผู้ช่วย AI ด้านล่าง แล้ววางข้อความที่คัดลอกลงในช่องแชต