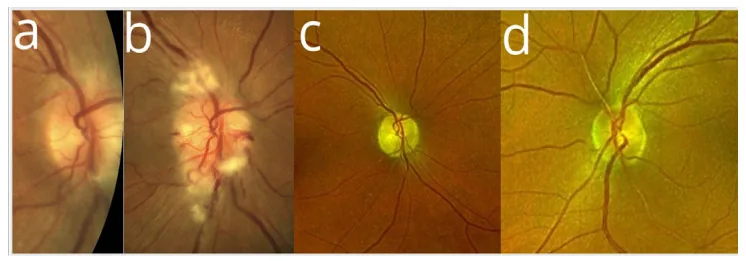
胺碘酮相關視神經病變(AAO N)是服用抗心律不整藥物胺碘酮期間發生的視神經 疾病,估計發生率為0.3–2%。
最常見的眼部副作用是渦狀角膜 變性(70–100%),但視神經病變 是最嚴重的眼部副作用。
其特徵為隱匿性發病和遷延性視乳頭水腫 (停藥後可持續長達15個月),與非動脈炎性前部缺血性視神經病變 (NAION )的鑑別是臨床上的最大挑戰。
約三分之一的患者無症狀,因此定期眼科監測很重要。
治療原則是停用可疑藥物,但由於該藥用於治療致命性心律不整,必須與心臟內科協作。
停用胺碘酮後,視力 改善僅見於58%的患者,21%進一步惡化,20%進展為法定盲(低於20/200)。
胺碘酮是一種二碘化苯並呋喃衍生物,於1960年代作為抗心絞痛藥物開發。它被歸類為III類抗心律不整藥,但也具有I、II、IV類特性1) 。廣泛用於心房顫動、心室心搏過速和心室顫動,在日本以商品名Ancaron(國外為Cordarone、Pacerone等)銷售。
胺碘酮的口服生物利用度為30–80%,半衰期極長,為20–100天。它親脂性高,蓄積於脂肪組織1) ,經肝臟CYP3A4/CYP2C8代謝,產生活性代謝物去乙基胺碘酮(DEA)1) 。
胺碘酮可引起多種眼部副作用。
渦狀角膜 變性(verticillate keratopathy) :最常見的眼部副作用。表現為角膜上皮 深層褐色渦狀色素沉著,發生於三分之二的治療患者。與劑量和用藥時間相關,高劑量(400 mg/天)時幾乎100%出現。採用Orlando分級(I–IV級)評估。僅有渦狀角膜 變性通常無需停用胺碘酮。胺碘酮相關視神經病變(AAO N) :最嚴重的眼部副作用。發生率報導為0.36–2%。其他 :前囊下水晶體 混濁、多發性霰粒腫 、乾眼症 等。
胺碘酮還具有多種全身副作用,包括甲狀腺功能障礙、肺毒性(過敏性肺炎,可能致命)、周邊神經病變和光敏感性。
Cheng等人利用台灣國民健康保險資料庫進行的世代研究(胺碘酮組6,175人 vs 對照組24,700人)顯示,胺碘酮組0.3%出現視神經病變 ,與非用藥組(0.1%)相比,風險比為2.09(95% CI 1.13~3.85)1) 。
Q
服用胺碘酮發生視神經病變的機率是多少?
A
台灣的世代研究報告胺碘酮服用者中0.3%出現視神經病變 ,與非服用組相比風險比為2.091) 。回顧性報告顯示發生率為0.362%,前瞻性雙盲試驗(超過1,600人)的最大估計年發生率為0.230.74%1) 。
????????????????? Dina Lešin Gaćina et al. Is Semaglutide Linked to
NAION ? A Case Report on a Rare Ocular Complication. Reports. 2025 Aug 20; 8(3):149. Figure 1. PM
CI D: PMC12372079. License: CC BY.
???????????????????????????????????????????????????????????????????????????
視力 下降無症狀 :多達三分之一的AAO N患者無自覺症狀。常僅透過視盤水腫 發現。色覺異常
AAO N的主要臨床所見如下。
視盤水腫 視盤水腫 持續中位數3個月(最長15個月)。序貫性視盤腫脹 :有報告稱一眼發病後3~48週對側眼出現視盤腫脹的「序貫」模式1) 。合併角膜 渦狀沉積 :常與視神經 毒性同時出現,發生率較高。
Patel等人提出了以下五種分類2) 。
隱匿發病型
最常見的分類 :表現為雙側同時性視乳頭水腫 ,緩慢進展。通常主觀症狀較少。
非動脈炎性前部缺血性視神經病變樣型
第二常見的分類 :表現為急性單側或雙側視力 喪失,臨床上與非動脈炎性前部缺血性視神經病變 非常相似。
球後視神經病變型
最難診斷的分類 :表現為眼底正常,需要影像學和血液檢查來確診。
其他類型
顱內壓增高型 :腦脊髓液壓力超過200 mmH₂O。
遲發進展型 :停用胺碘酮後數天至數週出現視乳頭水腫 。
胺碘酮使用時間 :AAO N發病的平均時間為9個月(範圍1-84個月)。有報告中位數約為4個月2) 。治療時間超過中位數41天時,視神經病變 風險增加3.5倍1) 。累積劑量 :累積劑量和用藥時間比日劑量對風險評估更重要1) 。出現視覺症狀的患者劑量中位數為200 mg/天(範圍57-1,200 mg/天)。性別 :一項對296例病例的回顧性研究顯示,平均年齡66歲,74%為男性。男性的風險約為女性的3倍1) 。高血壓 :在男性中,使用胺碘酮和高血壓是視神經病變 的顯著危險因子1) 。合併心血管危險因子 :許多服用胺碘酮的患者具有心血管危險因子,並且本身發生非動脈炎性前部缺血性視神經病變 的風險也很高。胺碘酮相關NA-AION的特徵包括雙側、潛行性發病、全身性(非水平半盲型)視野缺損 以及持續數月的視乳頭水腫 。
Q
減少胺碘酮的劑量是否能降低視神經病變的風險?
A
日劑量並非顯著的危險因子;累積劑量和用藥時間更為重要1) 。有報告稱,治療中位時間超過41天時風險增加3.5倍,因此即使短期使用也需要追蹤。
AAO N是一種臨床診斷,尚無確立的客觀診斷標準。
當出現以下表現時,懷疑AAO N:
潛行性發病
緩慢進展
持續性視乳頭水腫 (停藥後仍持續數月)
對側眼大杯(非危險視盤形態)
輕度視神經 功能障礙(視力 20/40以上,RAPD ≤ 0.9 log單位)
所有NA-AION患者應詢問胺碘酮使用史,若陽性應通知心臟科。藥物性視神經病變 需注意用藥史,首先懷疑至關重要。
AAO N與非動脈炎性前部缺血性視神經病變 的鑑別是臨床上的最大挑戰。下表列出主要鑑別點。
鑑別點 非動脈炎性前部缺血性視神經病變 AAO N 發病方式 急性,數天至數週 潛隱至急性 視盤形態 危險視盤(小視盤) 無特定形態 視盤水腫 持續時間2~6週消退 持續1~15個月 側別 多為單側 多為雙側
還需注意與巨細胞動脈炎 鑑別。有報告指出,一名使用胺碘酮的72歲男性被懷疑為AAO N,但顳動脈切片確診為巨細胞動脈炎 3) 。巨細胞動脈炎 即使ESR和CRP 正常,切片也可能呈陽性3) 。此外,巨細胞動脈炎 在MRI上可見視神經 鞘增強(視神經周圍炎 ),而AAO N未見此表現3) 。
藥物性視神經病變 的治療原則是停用可疑藥物。
由於胺碘酮用於治療致命性心律不整,不能輕易停藥。按以下步驟處理。
緊急諮詢心臟內科 :與心臟內科討論是否更換為替代藥物或進行導管 消融。如果僅有渦狀角膜 病變 :通常可以繼續使用胺碘酮。若發生AAO N :需由心臟科、眼科與患者三方仔細協商繼續用藥的風險與益處。若已有視神經 疾病 :部分專家建議避免使用胺碘酮。
停藥後的視力 預後如下:
視力 改善:58%不變:21%
進一步視力 下降:21%
法定盲(單眼或雙眼視力 低於20/200):20%
目前尚無針對AAO N的既定藥物治療。
Q
停用胺碘酮後視力會恢復嗎?
A
停用胺碘酮後,視力 改善僅佔58%,21%不變,21%進一步惡化,20%進展為法定盲(低於20/200)。此外,由於半衰期長達20-100天,停藥後藥物仍會殘留體內,需注意此點1) 。
AAO N的主要發病機制被認為與磷脂質沉積症相關的軸突損傷扮演核心角色。
溶酶體功能障礙 :胺碘酮抑制溶酶體鞘磷脂酶,誘導磷脂質沉積症1) 。板層狀包涵體蓄積 :板層狀包涵體選擇性蓄積在視神經 粗大軸突的細胞質內。在胺碘酮誘導的周邊神經病變中,周邊神經的軸突和許旺細胞也觀察到類似變化。軸漿流障礙 :板層小體機械性和生化性地減少軸漿流,這被認為是視神經 損傷的機制1) 。這種紊亂可能導致視乳頭水腫 。氧化壓力與細胞凋亡 :胺碘酮誘導粒線體H₂O₂合成和活性氧(ROS)形成,導致氧化性細胞損傷1) 。對視網膜神經節細胞 (RGC )的影響 :大鼠實驗證實RGC 凋亡以及視網膜電圖 a波和b波振幅降低1) 。
Q
胺碘酮透過什麼機制損傷視神經?
A
胺碘酮抑制溶酶體鞘磷脂酶,誘導磷脂質沉積症,導致視神經 軸突內板層狀包涵體蓄積1) 。這種蓄積損害軸漿流,引起視乳頭水腫 ,同時氧化壓力也導致細胞損傷,從而降低視神經 功能。
Liao等人(2007)在RPE 細胞模型中顯示,IGF-1透過PI3K/Akt路徑保護RPE 細胞免受胺碘酮誘導的氧化壓力和細胞凋亡 1) 。胺碘酮以濃度依賴性方式降低RPE 細胞活力(LC50 = 50 μM),而IGF-1抑制了這種降低。MAPK路徑的抑制不影響保護效果1) 。
2017年的一項大鼠研究表明,胺碘酮影響視網膜神經節細胞 層,而IGF-1逆轉了這種效應1) 。IGF-1未來在AAO N治療中的應用有待進一步研究。
Mindel等人(2007年)的前瞻性雙盲試驗(超過1600人,中位用藥45.5個月)未報告雙側視力 喪失病例,最大估計年發生率為0.23%–0.74% 1) 。這與既往回顧性報告(0.36%–2%)相矛盾,因此關於AAO N是否是一種臨床不同於非動脈炎性前部缺血性視神經病變 的獨立疾病實體的爭論仍在繼續。
巨細胞動脈炎 病例的MRI表現為視神經 鞘增強(optic perineuritis),報告率為57%–78%,而AAO N中未見此表現 3) 。未來,對疑似AAO N病例進行系統性MRI評估可能有助於提高鑑別診斷的準確性。
Mitchell R, Chacko J. Clinical and Mechanistic Review of Amiodarone-Associated Optic Neuropathy . Biomolecules. 2022;12:1298.
Patel S, Mahmood R. Amiodarone-Associated Optic Neuropathy in a Patient With Associated Arrhythmia. Cureus. 2024;16(3):e55819.
Tseng AM, Bindiganavile SH, Bhat N, Divatia MK, Lee AG. Optic Perineuritis Distinguishing Arteritic Ischaemic from Amiodarone-Associated Optic Neuropathy . Neuro-Ophthalmology. 2021;45(5):329-333.
開啟下方的 AI 助手,並將複製的內容貼到聊天欄。