النوع الخفي البداية
النوع الأكثر شيوعًا: يظهر بوذمة حليمة العصب البصري ثنائية متزامنة ويتقدم ببطء. غالبًا ما تكون الأعراض الذاتية قليلة.

الأميودارون هو مشتق بنزوفيوران ثنائي اليود تم تطويره في الستينيات كدواء لعلاج الذبحة الصدرية. يُصنف ضمن مضادات اضطراب النظم من الفئة الثالثة، لكنه يمتلك أيضًا خصائص الفئات I و II و IV 1). يُوصف على نطاق واسع للرجفان الأذيني، تسرع القلب البطيني، والرجفان البطيني، ويُعرف في اليابان باسم أنكارون (وفي الخارج باسم كوردارون، باسيرون، إلخ).
تبلغ التوافر الحيوي الفموي للأميودارون 30-80%، وعمر النصف طويل جدًا يتراوح بين 20-100 يوم. وهو شديد الذوبان في الدهون ويتراكم في الأنسجة الدهنية 1)، ويتم استقلابه بواسطة CYP3A4/CYP2C8 في الكبد لإنتاج المستقلب النشط ديسيثيل أميودارون (DEA) 1).
يسبب الأميودارون العديد من الآثار الجانبية العينية.
كما أن له آثارًا جانبية جهازية متنوعة مثل خلل الغدة الدرقية، السمية الرئوية (التهاب رئوي فرط الحساسية، قد يكون مميتًا)، الاعتلال العصبي المحيطي، والحساسية للضوء.
في دراسة أترابية أجراها Cheng وزملاؤه باستخدام قاعدة بيانات التأمين الصحي الوطني في تايوان (6,175 شخصًا في مجموعة الأميودارون مقابل 24,700 شخصًا في المجموعة الضابطة)، وُجد أن 0.3% من مجموعة الأميودارون أصيبوا باعتلال عصبي بصري، مع نسبة خطر 2.09 (فاصل ثقة 95%: 1.13–3.85) مقارنة بالمجموعة غير المعالجة (0.1%)1).
في الدراسة الأترابية التايوانية، وُجد أن 0.3% من متناولي الأميودارون أصيبوا باعتلال عصبي بصري، مع نسبة خطر 2.09 مقارنة بالمجموعة غير المتناولة1). أظهرت التقارير بأثر رجعي معدلات حدوث تتراوح بين 0.36% و2%، بينما بلغ الحد الأقصى المقدر للمعدل السنوي في تجربة مستقبلية مزدوجة التعمية (أكثر من 1,600 شخص) 0.23% إلى 0.74%1).
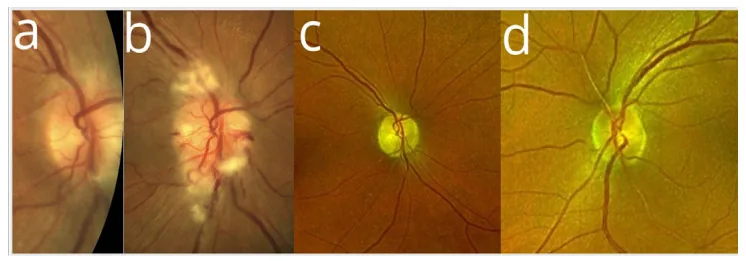
فيما يلي النتائج السريرية الرئيسية لـ AAON.
اقترح باتيل وزملاؤه التصنيفات الخمسة التالية2).
النوع الخفي البداية
النوع الأكثر شيوعًا: يظهر بوذمة حليمة العصب البصري ثنائية متزامنة ويتقدم ببطء. غالبًا ما تكون الأعراض الذاتية قليلة.
النوع الشبيه باعتلال العصب البصري الإقفاري الأمامي غير الشرياني
ثاني أكثر الأنواع شيوعًا: يظهر بفقدان حاد للرؤية في عين واحدة أو كلتا العينين، ويشبه سريريًا اعتلال العصب البصري الإقفاري الأمامي غير الشرياني.
النوع خلف المقلة
الأكثر صعوبة في التشخيص: يظهر بقاع عين طبيعي، ويتطلب التصوير والفحوصات الدموية للتشخيص.
أنواع أخرى
النوع الناتج عن ارتفاع الضغط داخل القحف: يتجاوز ضغط السائل النخاعي 200 مم H₂O.
النوع التقدمي المتأخر: تظهر وذمة حليمة العصب البصري بعد أيام إلى أسابيع من إيقاف الأميودارون.
الجرعة اليومية ليست عامل خطر ذا دلالة إحصائية، بينما تعتبر الجرعة التراكمية ومدة العلاج أكثر أهمية 1). تشير التقارير إلى أن تجاوز متوسط مدة العلاج 41 يومًا يزيد الخطر بمقدار 3.5 مرات، لذا فإن المراقبة ضرورية حتى مع الاستخدام قصير المدى.
AAON هو تشخيص سريري، ولا توجد معايير تشخيصية موضوعية محددة.
يُشتبه في AAON عند وجود العلامات التالية مجتمعة:
يجب الاستفسار عن تاريخ استخدام الأميودارون لدى جميع مرضى الاعتلال العصبي البصري الإقفاري الأمامي غير الشرياني، وفي حالة الإيجابية يجب إبلاغ طبيب القلب. من المهم الانتباه إلى تاريخ تناول الأدوية والاشتباه أولاً في الاعتلال العصبي البصري الدوائي.
التفريق بين الاعتلال العصبي البصري الإقفاري الأمامي المرتبط بالأميودارون والاعتلال العصبي البصري الإقفاري الأمامي غير الشرياني هو التحدي السريري الأكبر. يوضح الجدول التالي نقاط التمايز الرئيسية.
| نقطة التمايز | الاعتلال العصبي البصري الإقفاري الأمامي غير الشرياني | الاعتلال العصبي البصري الإقفاري الأمامي المرتبط بالأميودارون |
|---|---|---|
| نمط البداية | حاد – من أيام إلى أسابيع | خفي إلى حاد |
| شكل القرص البصري | قرص معرض للخطر (قرص صغير) | لا شكل محدد |
| مدة وذمة القرص | تختفي خلال 2-6 أسابيع | تستمر من 1 إلى 15 شهرًا |
| الجانب | غالبًا أحادي الجانب | غالبًا ثنائي الجانب |
يجب أيضًا توخي الحذر عند التفريق بين التهاب الشرايين ذو الخلايا العملاقة. تم الإبلاغ عن حالة لرجل يبلغ من العمر 72 عامًا يتناول الأميودارون ويُشتبه في إصابته بـ AAON، ولكن تم تأكيد التهاب الشرايين ذو الخلايا العملاقة بواسطة خزعة الشريان الصدغي 3). في التهاب الشرايين ذو الخلايا العملاقة، قد تكون خزعة الشريان الصدغي إيجابية حتى لو كانت قيم ESR و CRP طبيعية 3). أيضًا، في التهاب الشرايين ذو الخلايا العملاقة، قد يُظهر التصوير بالرنين المغناطيسي تعزيز تباين غمد العصب البصري (التهاب محيط العصب البصري)، وهي نتيجة لم تُبلغ عنها في AAON 3).
المبدأ الأساسي لعلاج الاعتلال العصبي البصري الدوائي هو إيقاف الدواء المشتبه به.
نظرًا لاستخدام الأميودارون لعلاج اضطرابات النظم القاتلة، لا يمكن إيقافه باستخفاف. يتم التعامل معه وفقًا للخطوات التالية.
نتائج الرؤية بعد التوقف هي كما يلي:
لا يوجد حالياً علاج دوائي مثبت لـ AAON.
بعد التوقف عن الأميودارون، تتحسن الرؤية في 58% فقط من الحالات، بينما تبقى دون تغيير في 21%، وتتدهور أكثر في 21%، ويصل 20% إلى العمى القانوني (أقل من 20/200). كما يجب ملاحظة أن عمر النصف الطويل (20-100 يوم) يعني بقاء الدواء في الجسم بعد التوقف 1).
يُعتقد أن الآلية الرئيسية لـ AAON هي تلف المحاور العصبية المرتبط بداء الفوسفوليبيد (phospholipidosis).
يثبط الأميودارون إنزيم سفينغومييليناز الليزوزومي مسببًا داء الفوسفوليبيدات، مما يؤدي إلى تراكم الادراج الصفائحية داخل محاور العصب البصري 1). يُعتقد أن هذا التراكم يعيق التدفق المحوري مسببًا وذمة حليمة العصب البصري، بالإضافة إلى التلف الخلوي الناتج عن الإجهاد التأكسدي، مما يؤدي إلى تدهور وظيفة العصب البصري.
أظهر Liao وآخرون (2007) في نموذج خلايا RPE أن IGF-1 يحمي خلايا RPE من الإجهاد التأكسدي والاستماتة الناجمين عن الأميودارون عبر مسار PI3K/Akt 1). انخفضت قابلية بقاء خلايا RPE بشكل يعتمد على التركيز بسبب الأميودارون (LC50 = 50 ميكرومولار)، وثبط IGF-1 هذا التأثير. لم يؤثر تثبيط مسار MAPK على التأثير الوقائي 1).
أظهرت دراسة على الفئران عام 2017 أن الأميودارون يؤثر على طبقة الخلايا العقدية الشبكية، وأن IGF-1 يعكس هذا التأثير 1). التطبيق المستقبلي لـ IGF-1 في علاج الاعتلال العصبي البصري الناجم عن الأميودارون هو موضوع للبحث المستقبلي.
في دراسة Mindel وآخرين (2007) المستقبلية مزدوجة التعمية (أكثر من 1600 شخص، متوسط مدة العلاج 45.5 شهرًا)، لم يُبلغ عن أي حالة فقدان رؤية ثنائي، وكان الحد الأقصى المقدر للمعدل السنوي للإصابة 0.23-0.74% 1). يتعارض هذا مع التقارير الاستعادية السابقة (0.36-2%)، ولا يزال الجدل قائمًا حول ما إذا كان اعتلال العصب البصري الإقفاري الأمامي المرتبط بالأدوية كيانًا مرضياً مستقلاً يختلف سريريًا عن اعتلال العصب البصري الإقفاري الأمامي غير الشرياني.
في حالات التهاب الشرايين ذو الخلايا العملاقة، تم الإبلاغ عن تعزيز غمد العصب البصري (التهاب محيط العصب البصري) في 57-78% من الحالات بواسطة التصوير بالرنين المغناطيسي، وهي نتيجة غير مبلغ عنها في اعتلال العصب البصري الإقفاري الأمامي المرتبط بالأدوية 3). في المستقبل، يمكن أن يساهم التقييم المنهجي لنتائج التصوير بالرنين المغناطيسي في الحالات المشتبه فيها باعتلال العصب البصري الإقفاري الأمامي المرتبط بالأدوية في تحسين دقة التشخيص التفريقي.