VEP
الجهد المستثار البصري (VEP): الكشف عن إطالة زمن كمون P100. ورد أن 34.8% من المرضى الذين يتناولون الإيثامبوتول لديهم P100 يزيد عن 107 مللي ثانية2). مفيد للكشف عن تلف العصب البصري الكامن، لكنه ليس خاصًا بـ EON.

الإيثامبوتول (EMB) هو دواء من الخط الأول يستخدم ضد المتفطرات، وخاصة المتفطرة السلية (Mycobacterium tuberculosis) والمتفطرة الطيرية المعقدة (MAC) وغيرها من المتفطرات غير السلية. أخطر الآثار الجانبية للإيثامبوتول هو اعتلال العصب البصري الناتج عن الإيثامبوتول (EON)، والذي يحتل دائمًا مرتبة عالية بين اعتلالات الأعصاب البصرية الدوائية.
يقدر معدل انتشار EON بين مرضى علاج السل بنسبة 1-2%. وفقًا لمنظمة الصحة العالمية (WHO)، يتم الإبلاغ عن حوالي 9.2 مليون حالة سل جديدة سنويًا، مما قد يؤدي إلى ما يصل إلى 100,000 حالة جديدة من EON سنويًا.
خطر EON يعتمد بشكل كبير على الجرعة. فيما يلي معدلات الانتشار المقدرة حسب جرعة EMB:
| جرعة EMB | معدل الانتشار المقدر |
|---|---|
| <15 ملغ/كغ/يوم | أقل من 1% |
| 25 ملغ/كغ/يوم | 5-6% |
| >35 ملغم/كغم/يوم | 18–33% |
ومع ذلك، تم الإبلاغ عن حدوث EON حتى مع الجرعات المنخفضة (<15 ملغم/كغم). في المسح الوطني الياباني، حدث 52.2% من حالات EON بجرعات منخفضة، ولا توجد جرعة “آمنة” حقًا3).
في عام 2009، قامت منظمة الصحة العالمية (WHO) بمراجعة إرشاداتها لتشمل EMB في مرحلة الصيانة من علاج السل، مما أدى إلى إطالة مدة العلاج. مع هذا التغيير، هناك قلق من زيادة خطر الإصابة بـ EON1).
يحدث في حوالي 1–2% من مرضى علاج السل. يزداد الخطر مع الجرعات الأعلى، حيث يصل إلى 5–6% عند 25 ملغم/كغم/يوم و18–33% عند أكثر من 35 ملغم/كغم/يوم. يمكن أن يحدث حتى مع الجرعات المنخفضة، لذلك لا توجد جرعة آمنة حقًا. راجع قسم “ما هو الاعتلال العصبي البصري الناتج عن الإيثامبوتول” للحصول على التفاصيل.
على عكس الاعتلالات العصبية البصرية السامة الأخرى، يمكن أن يحدث EON في فترة قصيرة نسبيًا بعد بدء العلاج. تتراوح فترة البداية من شهر واحد إلى 36 شهرًا بعد بدء الدواء، ولكن من النادر حدوثه خلال شهرين، ومتوسط الفترة هو 7 أشهر.
الأعراض الذاتية الرئيسية هي كما يلي:
قد يكون خلل رؤية الألوان أول علامة. الإحساس بأن اللون الأحمر لم يعد يبدو نابضًا بالحياة كما كان سابقًا يمكن أن يكون دليلاً. نظرًا لأن انخفاض حدة البصر في كلتا العينين يتقدم بشكل خفي، فإن الفحص الدوري لحدة البصر ورؤية الألوان مهم للكشف المبكر.
الآلية الدقيقة للسمية العصبية للإيثامبوتول غير معروفة، لكن يُعتقد أن تأثيرها المخلبى للمعادن هو السبب الرئيسي. يُعتقد أن الإيثامبوتول ومستقلبه حمض 2,2-إيثيلين ثنائي أمينو ثنائي البوتيريك (EDBA) كلاهما مواد مخلبية، ويسببان تلف العصب البصري عبر المسارات التالية 2).
أظهرت التجارب على الحيوانات أن نقص الزنك يرتبط بتدمير غمد الميالين وتكاثر الخلايا الدبقية. عند البشر أيضًا، قد يؤدي نقص فيتامين E و B1 الناتج عن الاستخدام طويل الأمد للإيثامبوتول إلى تفاقم اعتلال العصب البصري.
يُعتقد أن اعتلالات العصب البصري الناتجة عن الأدوية مثل الإيثامبوتول واللينيزوليد والميسالازين ناتجة عن خلل وظيفي مكتسب في الميتوكوندريا، وتتشابه في الفيزيولوجيا المرضية مع اعتلال ليبر الوراثي للعصب البصري.
من عوامل الخطر المعروفة: الجرعات العالية والاستخدام طويل الأمد، العمر فوق 65 عامًا، القصور الكلوي، ارتفاع ضغط الدم، السكري، التدخين، والاستخدام المتزامن مع أيزونيازيد. راجع قسم “الأسباب وعوامل الخطر” للتفاصيل.
يتم تشخيص EON سريريًا. الفحوصات الأساسية قبل العلاج ضرورية، ويُوصى بإجراء فحوصات الرؤية، مجال الرؤية، قيمة الوميض المركزي، وفحص رؤية الألوان قبل البدء بالإيثامبوتول، ثم متابعتها كل 1-2 شهر أثناء العلاج.
VEP
الجهد المستثار البصري (VEP): الكشف عن إطالة زمن كمون P100. ورد أن 34.8% من المرضى الذين يتناولون الإيثامبوتول لديهم P100 يزيد عن 107 مللي ثانية2). مفيد للكشف عن تلف العصب البصري الكامن، لكنه ليس خاصًا بـ EON.
OCT
التصوير المقطعي التوافقي البصري (OCT): الكشف عن ترقق طبقة الألياف العصبية الشبكية المحيطة بالحليمة (pRNFL) وتغيرات طبقة الخلايا العقدية-الطبقة الضفيرية الداخلية (GCIPL). التغيرات في الجانب الصدغي مميزة، مع انخفاض بنسبة 20-79%2). مفيد أيضًا لتقييم تشخيص حدة البصر.
إذا استمر تدهور الرؤية بعد إيقاف EMB، يجب النظر في اعتلالات العصب البصري الأخرى.
لا يوجد علاج مثبت لـ EON. لا يوجد علاج أفضل من إيقاف الدواء المسبب، وإذا اشتبه في EON، فإن إيقاف EMB فورًا هو أهم إجراء. يجب على طبيب العيون الاتصال بالطبيب الموصي قبل إيقاف EMB.
بعد إيقاف EMB، قد يستمر تدهور الرؤية والمجال البصري لمدة 2-3 أشهر. ثم يبدأ التعافي تدريجيًا، لكنه قد يكون بطيئًا، من نصف عام إلى عامين.
يجب إيقاف التدخين لأنه يسبب تأثيرات ضارة إضافية في تسمم المذيبات واعتلال العصب البصري الناتج عن الإيثامبوتول. إذا كانت هناك أمراض أساسية تؤثر على تدفق الدم مثل ارتفاع ضغط الدم أو السكري، فيجب العلاج بالتنسيق مع الطب الباطني.
| عامل الإنذار | التأثير |
|---|---|
| الكشف المبكر والإيقاف المبكر | تحسن الرؤية بنسبة 30-64% |
| أقل من 60 عامًا | معدل التعافي حوالي 80% |
| 60 عامًا فأكثر | معدل التعافي حوالي 20% |
في المرضى الذين تتحسن رؤيتهم، يحدث تحسن بمتوسط سطرين في جدول سنيلن 2). بينما يتعافى بعض المرضى تمامًا، يعاني آخرون من ضعف بصري دائم. يرتبط وجود شحوب القرص البصري عند البداية بسوء التشخيص.
هناك تقارير تفيد بأن انخفاض سمك طبقة الألياف العصبية الشبكية (RNFL) يستمر حتى بعد إيقاف EMB، وقد يحدث فقدان بصري لا رجعة فيه على الرغم من المراقبة الدقيقة والإيقاف الفوري للدواء 2).
إذا تم إيقاف EMB قبل حدوث ضمور العصب البصري غير القابل للرجوع، تتحسن الوظيفة البصرية لدى 30-64% من المرضى. لكن التعافي الكامل نادر، ومتوسط التحسن هو سطرين في جدول سنيلن. قد تستمر الأعراض في التفاقم لمدة 2-3 أشهر بعد الإيقاف، لذا فإن المتابعة المستمرة ضرورية. راجع قسم «العلاج القياسي» لمزيد من التفاصيل.
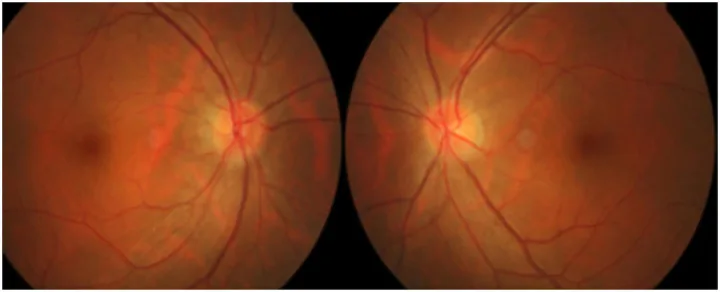
الاعتلال العصبي البصري الخلفي هو الشكل الأكثر شيوعًا لـ EON، ويبدو القرص البصري طبيعيًا عند البداية.
يعمل كل من EMB ومستقلبه EDBA كعوامل مخلبية للمعادن. EDBA لديه تصفية داخل العين أقل من الإيثامبوتول نفسه، مما يؤدي إلى تركيز موضعي أعلى، ويُعتقد أنه يساهم بشكل أكبر في السمية 2).
المسارات الرئيسية للضرر هي كما يلي:
المحاور العصبية من النوع parvo-cellular التي تشكل الحزمة الحليمية البقعية (papillomacular bundle) لديها طلب مرتفع بشكل خاص على الطاقة من الميتوكوندريا. ولهذا السبب، في الاعتلال العصبي البصري السام أو التغذوي، تتضرر هذه المحاور بشكل تفضيلي 2).
من بين الخلايا العقدية الشبكية، يُفترض أن الخلايا p التي تستهلك ATP بشكل كبير تتضرر بشكل رئيسي، وهو ما يتوافق مع آلية تكوين العتمة المركزية. من ناحية أخرى، يتم الحفاظ على الخلايا γ المشاركة في رد فعل الحدقة، وبالتالي يبقى رد فعل الحدقة محفوظًا نسبيًا.
في التجارب الحيوانية، يُقال إن الاعتلال العصبي المحوري الناجم عن EMB يحدث بشكل متكرر في التصالب البصري، وهو ما يتوافق مع وجود حالات سريرية تظهر عمى نصفي صدغي ثنائي.
أجرى Sabhapandit وآخرون (2023) مراجعة منهجية لـ 12 دراسة نُشرت بين 2010 و2021 (5818 شخصًا، منهم 309 مصابًا بـ EON) ووجدوا أن الاستخدام المطول لـ EMB لأكثر من شهرين يؤدي إلى سمية عصبية بصرية كبيرة 1). كان تحسن الرؤية بعد إيقاف EMB ذا دلالة إحصائية (P = 0.035). لم يصل تحسن تشوهات رؤية الألوان والمجال البصري إلى مستوى الدلالة.
أبلغ Matsumoto وآخرون (2021) عن حالة رجل يبلغ من العمر 85 عامًا تدهورت رؤيته بشكل حاد بعد إيقاف EMB وأدى إلى فقدان رؤية لا رجعة فيه، على الرغم من الجرعة المنخفضة (12 مغ/كغ) والمدة القصيرة (2.5 شهرًا) 3). انخفضت حدة الرؤية المصححة من 20/17 قبل الإيقاف إلى 20/330 (العين اليمنى) و20/1000 (العين اليسرى) في غضون 3 أسابيع. توضح هذه الحالة أن فقدان الرؤية الكارثي يمكن أن يحدث حتى مع الجرعات المنخفضة.
أبلغ Peterson & Hawy (2022) عن حالة رجل يبلغ من العمر 82 عامًا أصيب بـ EON متأخر بعد تناول EMB بجرعة <15 مغ/كغ/يوم لمدة 3 سنوات أثناء علاج MAC 4). تحسنت الرؤية بعد إيقاف EMB واستمر التحسن لمدة 10 أشهر. متوسط وقت الظهور هو 9 أشهر، ولكن تم إثبات إمكانية الظهور بعد أكثر من 3 سنوات.
أبلغ كونانا وآخرون (2024) عن 3 حالات من خلل المخاريط الناتج عن سمية الإيثامبوتول 5). تمثلت الأعراض الرئيسية في حساسية الضوء وانخفاض حدة البصر، وأظهر تخطيط كهربية الشبكية تأخرًا في زمن استجابة الوميض. تشير هذه التقارير إلى أن سمية الإيثامبوتول تؤثر ليس فقط على العصب البصري بل أيضًا على طبقات خلايا الشبكية.
من المتوقع أن يؤدي إدخال الأقراص المركبة بجرعات ثابتة (FDC: تحتوي كل قرص على أيزونيازيد وريفامبيسين وبيرازيناميد وإيثامبوتول) وتمديد فترة العلاج إلى زيادة حدوث اعتلال العصب البصري الناتج عن الإيثامبوتول 2). تشمل موضوعات البحث الهامة المستقبلية تطوير أنظمة الفحص، والتحقق من فائدة التصوير المقطعي التوافقي البصري (OCT) والجهد المستثار البصري (VEP) في الكشف عن اعتلال العصب البصري الكامن، وتوضيح آلية حدوثه، وتحديد عوامل الخطر.