VEP
پتانسیل برانگیخته بینایی (VEP): تشخیص افزایش زمان نهفتگی P100. گزارش شده است که در 34.8% از بیماران مصرفکننده اتامبوتول، P100 به بیش از 107 میلیثانیه افزایش یافته است2). برای تشخیص آسیب بالقوه عصب بینایی مفید است اما اختصاصی برای EON نیست.

اتامبوتول (EMB) یک داروی خط اول برای درمان عفونتهای مایکوباکتریومی، به ویژه سل (Mycobacterium tuberculosis) و مایکوباکتریوم آویوم کمپلکس (MAC) است. مهمترین عارضه جانبی EMB، نوروپاتی بینایی اتامبوتول (EON) است که از شایعترین نوروپاتیهای بینایی ناشی از دارو محسوب میشود.
شیوع EON در بیماران تحت درمان سل ۱ تا ۲٪ تخمین زده میشود. بر اساس گزارش سازمان جهانی بهداشت (WHO)، سالانه حدود ۹.۲ میلیون مورد جدید سل گزارش میشود که میتواند منجر به ۱۰۰ هزار مورد جدید EON در سال شود.
خطر EON به شدت وابسته به دوز است. شیوع تخمینی بر اساس دوز EMB در زیر آورده شده است:
| دوز EMB | شیوع تخمینی |
|---|---|
| <15 mg/kg/روز | کمتر از ۱٪ |
| 25 mg/kg/روز | ۵ تا ۶٪ |
| بیشتر از 35 میلیگرم/کیلوگرم/روز | 18 تا 33٪ |
با این حال، بروز EON حتی با دوزهای پایین (کمتر از 15 میلیگرم/کیلوگرم) نیز گزارش شده است. در یک بررسی ملی در ژاپن، 52.2٪ از موارد EON با دوز پایین رخ داده است و هیچ دوز واقعاً «ایمنی» وجود ندارد3).
در سال 2009، WHO دستورالعمل خود را اصلاح کرد تا EMB را در مرحله نگهدارنده درمان سل نیز شامل شود و دوره مصرف طولانیتر شد. با این تغییر، نگرانیهایی در مورد افزایش خطر بروز EON وجود دارد1).
حدود 1 تا 2٪ از بیماران تحت درمان سل به آن مبتلا میشوند. با افزایش دوز، خطر افزایش مییابد: با 25 میلیگرم/کیلوگرم/روز 5 تا 6٪ و با بیش از 35 میلیگرم/کیلوگرم/روز 18 تا 33٪. حتی با دوز پایین نیز ممکن است رخ دهد، بنابراین هیچ دوز واقعاً ایمنی وجود ندارد. برای جزئیات به بخش «نوروپاتی بینایی اتامبوتول چیست» مراجعه کنید.
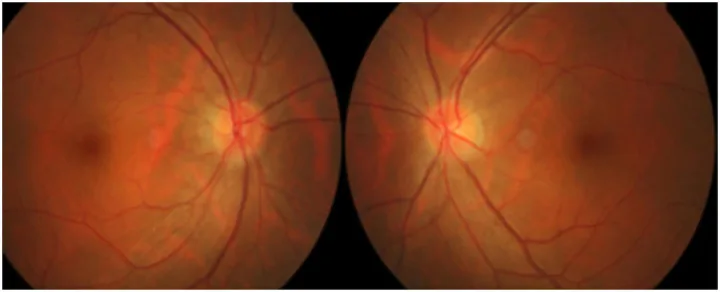
برخلاف سایر نوروپاتیهای بینایی سمی، EON میتواند نسبتاً زود پس از شروع درمان رخ دهد. زمان شروع از 1 ماه تا 36 ماه پس از شروع مصرف متغیر است، اما در 2 ماه اول نادر است و میانگین آن 7 ماه است.
علائم ذهنی اصلی به شرح زیر است:
اختلال بینایی رنگ ممکن است اولین علامت باشد. احساس اینکه رنگ قرمز به وضوح قبل دیده نمیشود، میتواند سرنخی باشد. کاهش بینایی دوطرفه به صورت مخفیانه پیشرفت میکند، بنابراین بررسی منظم بینایی و دید رنگی برای تشخیص زودهنگام مهم است.
مکانیسم دقیق نوروتوکسیسیتی EMB ناشناخته است، اما تصور میشود که خاصیت کلاته کردن فلزات عامل اصلی باشد. EMB و متابولیت آن، 2،2-اتیلن دی آمینو دی بوتیریک اسید (EDBA)، هر دو مواد کلاته کننده هستند و تصور میشود از طریق مسیرهای زیر باعث آسیب عصب بینایی میشوند 2).
مطالعات حیوانی نشان دادهاند که کمبود روی با تخریب غلاف میلین و تکثیر سلولهای گلیال مرتبط است. در انسان نیز، کمبود ویتامین E و B1 ناشی از مصرف طولانیمدت EMB ممکن است نوروپاتی بینایی را تشدید کند.
نوروپاتیهای بینایی ناشی از داروهایی مانند اتامبوتول، لینزولید و مسالازین احتمالاً به دلیل اختلال عملکرد میتوکندری اکتسابی ایجاد میشوند و پاتوفیزیولوژی مشابهی با نوروپاتی بینایی ارثی لبر دارند.
عوامل خطر شامل مصرف دوز بالا و طولانی مدت، سن بالای 65 سال، نارسایی کلیوی، فشار خون بالا، دیابت، سیگار کشیدن و مصرف همزمان ایزونیازید است. برای جزئیات به بخش «علل و عوامل خطر» مراجعه کنید.
تشخیص EON به صورت بالینی انجام میشود. آزمایش پایه قبل از مصرف دارو ضروری است و توصیه میشود قبل از تجویز EMB، آزمایشهای بینایی، میدان بینایی، فرکانس فلیکر مرکزی و دید رنگی انجام شود و در طول درمان هر 1 تا 2 ماه یکبار بررسی شود.
VEP
پتانسیل برانگیخته بینایی (VEP): تشخیص افزایش زمان نهفتگی P100. گزارش شده است که در 34.8% از بیماران مصرفکننده اتامبوتول، P100 به بیش از 107 میلیثانیه افزایش یافته است2). برای تشخیص آسیب بالقوه عصب بینایی مفید است اما اختصاصی برای EON نیست.
OCT
توموگرافی انسجام نوری (OCT): تشخیص نازک شدن لایه فیبرهای عصبی شبکیه اطراف پاپی (pRNFL) و تغییرات لایه سلولهای گانگلیونی-شبکه داخلی (GCIPL). تغییرات غالب در بخش تمپورال مشخصه است و کاهش 20-79% گزارش شده است2). همچنین برای ارزیابی پیشآگهی بینایی مفید است.
اگر پس از قطع EMB کاهش بینایی ادامه یابد، باید سایر نوروپاتیهای بینایی را در نظر گرفت.
هیچ درمان اثباتشدهای برای EON وجود ندارد. هیچ درمانی بهتر از قطع داروی مسبب نیست و در صورت مشکوک شدن به EON، قطع سریع EMB مهمترین اقدام است. چشمپزشک باید قبل از قطع EMB مستقیماً با پزشک تجویزکننده تماس بگیرد.
پس از قطع EMB، ممکن است اختلال بینایی و میدان بینایی تا ۲-۳ ماه دیگر پیشرفت کند. سپس به تدریج بهبود مییابد، اما بهبودی آهسته است و ۶ ماه تا ۲ سال طول میکشد.
سیگار کشیدن باید قطع شود زیرا اثرات منفی افزایشی در مسمومیت با رقیقکنندهها و نوروپاتی اپتیک اتیلن گلیکول دارد. در صورت وجود بیماریهای زمینهای مانند فشار خون بالا یا دیابت که بر جریان خون تأثیر میگذارند، درمان باید با همکاری پزشک داخلی انجام شود.
| عامل پیشآگهی | تأثیر |
|---|---|
| تشخیص زودهنگام و قطع زودهنگام | بهبود بینایی در ۳۰ تا ۶۴٪ موارد |
| زیر ۶۰ سال | نرخ بهبود حدود ۸۰٪ |
| ۶۰ سال و بالاتر | نرخ بهبود حدود ۲۰٪ |
در بیمارانی که بینایی بهبود مییابد، به طور متوسط ۲ خط بهبود در نمودار اسنلن مشاهده میشود2). با این حال، برخی بیماران بهبودی کامل بینایی دارند و برخی دیگر دچار اختلال دائمی عملکرد بینایی میشوند. وجود رنگپریدگی دیسک بینایی در زمان شروع بیماری با پیشآگهی ضعیف مرتبط است.
گزارش شده است که کاهش ضخامت RNFL حتی پس از قطع EMB ادامه مییابد و از دست دادن غیرقابل برگشت بینایی میتواند علیرغم نظارت دقیق و قطع سریع دارو رخ دهد2).
اگر EMB قبل از ایجاد آتروفی غیرقابل برگشت عصب بینایی قطع شود، عملکرد بینایی در ۳۰-۶۴٪ بیماران بهبود مییابد. با این حال، بهبودی کامل نادر است و میانگین بهبود ۲ خط اسنلن است. علائم ممکن است تا ۲-۳ ماه پس از قطع ادامه یابد، بنابراین پیگیری مداوم لازم است. برای جزئیات به بخش «روشهای درمانی استاندارد» مراجعه کنید.
نوروپاتی رتروبولبار شایعترین شکل EON است و در زمان شروع، دیسک بینایی طبیعی به نظر میرسد.
EMB و متابولیت آن EDBA هر دو به عنوان مواد کلاته کننده فلزات عمل میکنند. EDBA کلیرانس داخل چشمی کمتری نسبت به خود اتامبوتول دارد و غلظت موضعی بالاتری دارد، بنابراین تصور میشود که سهم بیشتری در سمیت داشته باشد2).
مسیرهای اصلی آسیب به شرح زیر است:
آکسونهای پارو-سلولی (parvo-cellular) که دسته عصبی پاپیلوماکولار (papillomacular bundle) را تشکیل میدهند، نیاز انرژی میتوکندریایی بالایی دارند. به همین دلیل، در نوروپاتیهای بینایی سمی و تغذیهای، این آکسونها در اولویت آسیب قرار میگیرند 2).
تصور میشود که در میان سلولهای گانگلیونی شبکیه، سلولهای p که مصرف ATP بالایی دارند، به طور غالب آسیب میبینند که با مکانیسم تشکیل اسکوتوم مرکزی مطابقت دارد. از سوی دیگر، سلولهای γ که در پاسخ به نور نقش دارند، حفظ میشوند، بنابراین پاسخ به نور نسبتاً باقی میماند.
در آزمایشات حیوانی، نوروپاتی آکسونی ناشی از EMB بیشتر در کیاسمای بینایی رخ میدهد که با وجود موارد بالینی با همیانوپسی دوطرفه گیجگاهی مطابقت دارد.
Sabhapandit و همکاران (2023) یک مرور سیستماتیک از 12 مطالعه منتشر شده بین سالهای 2010 تا 2021 (5818 نفر، که 309 نفر مبتلا به EON بودند) انجام دادند و گزارش کردند که استفاده طولانیمدت از EMB بیش از 2 ماه منجر به سمیت عصبی بینایی قابل توجهی میشود 1). بهبود بینایی پس از قطع EMB از نظر آماری معنیدار بود (P = 0.035). بهبود در اختلال رنگ بینایی و نقص میدان بینایی به سطح معنیداری نرسید.
Matsumoto و همکاران (2021) مورد یک مرد 85 ساله را گزارش کردند که با وجود مصرف EMB با دوز پایین (12 میلیگرم/کیلوگرم) و مدت کوتاه (2.5 ماه)، پس از قطع EMB بینایی وی به شدت کاهش یافت و به از دست دادن غیرقابل برگشت بینایی منجر شد 3). قبل از قطع، حدت بینایی اصلاح شده 20/17 بود که در عرض 3 هفته به 20/330 (چشم راست) و 20/1000 (چشم چپ) کاهش یافت. این مورد نشان میدهد که حتی با دوز پایین نیز ممکن است از دست دادن فاجعهبار بینایی رخ دهد.
Peterson و Hawy (2022) مورد یک مرد 82 ساله را گزارش کردند که در طول درمان MAC به مدت 3 سال EMB با دوز <15 میلیگرم/کیلوگرم/روز مصرف کرده بود و به EON دیررس مبتلا شد 4). پس از قطع EMB، بینایی بهبود یافت و این بهبود تا 10 ماه ادامه داشت. اگرچه میانه زمان بروز 9 ماه گزارش شده است، اما نشان داده شده است که بروز پس از بیش از 3 سال نیز ممکن است.
Konana و همکاران (2024) سه مورد از اختلال عملکرد مخروطی ناشی از سمیت اتامبوتول را گزارش کردند5). علائم اصلی شامل حساسیت به نور و کاهش بینایی بود و در الکترورتینوگرافی تأخیر در زمان نهفته پاسخ فلیکر مشاهده شد. این گزارش نشان میدهد که سمیت اتامبوتول نه تنها بر عصب بینایی بلکه بر لایههای سلولی شبکیه نیز تأثیر میگذارد.
با معرفی قرصهای ترکیبی با دوز ثابت (FDC: حاوی ایزونیازید، ریفامپیسین، پیرازینامید و اتامبوتول در یک قرص) و افزایش مدت درمان، انتظار میرود بروز نوروپاتی بینایی اتامبوتولی (EON) افزایش یابد2). توسعه سیستمهای غربالگری، بررسی سودمندی OCT و VEP در تشخیص EON تحت بالینی، و کشف مکانیسم بیماری و عوامل خطر از موضوعات مهم تحقیقاتی آینده هستند.