VEP
दृश्य उत्पन्न विभव (VEP) : P100 विलंबता के बढ़ने का पता लगाएं। एक रिपोर्ट के अनुसार, एथमब्यूटोल लेने वाले 34.8% रोगियों में P100 107 ms से अधिक बढ़ गया था2)। संभावित ऑप्टिक तंत्रिका क्षति का पता लगाने में उपयोगी, लेकिन EON के लिए विशिष्ट नहीं।

एथमब्यूटोल (EMB) माइकोबैक्टीरियम, विशेष रूप से तपेदिक बैसिलस (Mycobacterium tuberculosis) और गैर-तपेदिक माइकोबैक्टीरियल रोगों जैसे माइकोबैक्टीरियम एवियम कॉम्प्लेक्स (MAC) के खिलाफ उपयोग की जाने वाली पहली पंक्ति की दवा है। EMB का सबसे गंभीर दुष्प्रभाव एथमब्यूटोल ऑप्टिक न्यूरोपैथी (EON) है, जो दवा-प्रेरित ऑप्टिक न्यूरोपैथियों में हमेशा शीर्ष पर रहता है।
तपेदिक उपचार प्राप्त करने वाले रोगियों में EON का प्रसार 1-2% अनुमानित है। विश्व स्वास्थ्य संगठन (WHO) के अनुसार, प्रतिवर्ष लगभग 9.2 मिलियन नए तपेदिक मामले सामने आते हैं, जिससे प्रति वर्ष 100,000 तक नए EON मामले हो सकते हैं।
EON का जोखिम अत्यधिक खुराक-निर्भर है। EMB खुराक के अनुसार अनुमानित प्रसार नीचे दिया गया है।
| EMB खुराक | अनुमानित प्रसार |
|---|---|
| <15 मिलीग्राम/किग्रा/दिन | 1% से कम |
| 25 मिलीग्राम/किग्रा/दिन | 5-6% |
| >35 mg/kg/दिन | 18-33% |
हालांकि, कम खुराक (<15 mg/kg) पर भी EON के मामले सामने आए हैं। जापान के एक राष्ट्रीय सर्वेक्षण में, 52.2% EON मामले कम खुराक पर हुए, जिससे पता चलता है कि कोई वास्तव में ‘सुरक्षित’ खुराक मौजूद नहीं है3)।
2009 में, WHO ने तपेदिक उपचार के रखरखाव चरण में EMB को शामिल करने के लिए दिशानिर्देशों में संशोधन किया, जिससे प्रशासन की अवधि बढ़ गई। इस बदलाव के साथ EON के जोखिम में वृद्धि की आशंका है1)।
यह तपेदिक के इलाज करा रहे लगभग 1-2% रोगियों में होती है। खुराक जितनी अधिक होगी, जोखिम उतना ही बढ़ता है: 25 mg/kg/दिन पर 5-6%, और 35 mg/kg/दिन से अधिक पर 18-33%। कम खुराक पर भी हो सकती है, इसलिए कोई वास्तव में सुरक्षित खुराक नहीं है। अधिक जानकारी के लिए, “एथमब्यूटोल ऑप्टिक न्यूरोपैथी क्या है” अनुभाग देखें।
EON, अन्य विषाक्त ऑप्टिक न्यूरोपैथियों के विपरीत, उपचार शुरू होने के बाद अपेक्षाकृत कम समय में हो सकता है। शुरुआत का समय उपचार शुरू होने के 1 महीने से 36 महीने तक भिन्न होता है, लेकिन पहले 2 महीनों में दुर्लभ है, औसत 7 महीने है।
मुख्य व्यक्तिपरक लक्षण इस प्रकार हैं:
रंग दृष्टि असामान्यताएं पहला संकेत हो सकती हैं। लाल रंग पहले जितना चमकीला नहीं दिखने की अनुभूति एक सुराग हो सकती है। द्विपक्षीय दृश्य तीक्ष्णता में कमी धीरे-धीरे बढ़ती है, इसलिए शीघ्र पहचान के लिए नियमित दृश्य तीक्ष्णता और रंग दृष्टि जांच महत्वपूर्ण है।
EMB की न्यूरोटॉक्सिसिटी का सटीक तंत्र अज्ञात है, लेकिन इसका धातु केलेशन प्रभाव मुख्य कारण माना जाता है। EMB और इसका मेटाबोलाइट 2,2-एथिलीनडायमिनोडाइब्यूटिरिक एसिड (EDBA) दोनों ही केलेटिंग एजेंट हैं और निम्नलिखित मार्गों से ऑप्टिक न्यूरोपैथी उत्पन्न करते हैं 2)।
पशु प्रयोगों से पता चला है कि जिंक की कमी माइलिन आवरण के विनाश और ग्लियाल कोशिकाओं के प्रसार से जुड़ी है। मनुष्यों में भी, EMB के दीर्घकालिक उपयोग से विटामिन E और B1 की कमी ऑप्टिक न्यूरोपैथी को बढ़ा सकती है।
एथमब्यूटोल, लाइनज़ोलिड और मेसालजीन जैसी दवाओं से होने वाली ऑप्टिक न्यूरोपैथी को अधिग्रहित माइटोकॉन्ड्रियल डिसफंक्शन के कारण माना जाता है, और इसकी रोगविज्ञान वंशानुगत लेबर ऑप्टिक न्यूरोपैथी के समान है।
उच्च खुराक और लंबे समय तक उपयोग, 65 वर्ष से अधिक आयु, गुर्दे की शिथिलता, उच्च रक्तचाप, मधुमेह, धूम्रपान करने वाले, और आइसोनियाज़िड के साथ सह-उपयोग जोखिम कारक के रूप में जाने जाते हैं। विवरण के लिए “कारण और जोखिम कारक” अनुभाग देखें।
EON का निदान नैदानिक रूप से किया जाता है। उपचार से पहले आधारभूत जांच आवश्यक है। EMB देने से पहले दृश्य तीक्ष्णता, दृश्य क्षेत्र, केंद्रीय फ्लिकर मान और रंग दृष्टि परीक्षण करने की सलाह दी जाती है, और उपचार के दौरान हर 1-2 महीने में जांच करना वांछनीय है।
VEP
दृश्य उत्पन्न विभव (VEP) : P100 विलंबता के बढ़ने का पता लगाएं। एक रिपोर्ट के अनुसार, एथमब्यूटोल लेने वाले 34.8% रोगियों में P100 107 ms से अधिक बढ़ गया था2)। संभावित ऑप्टिक तंत्रिका क्षति का पता लगाने में उपयोगी, लेकिन EON के लिए विशिष्ट नहीं।
OCT
ऑप्टिकल कोहेरेंस टोमोग्राफी (OCT) : पेरिपैपिलरी रेटिनल नर्व फाइबर लेयर (pRNFL) के पतले होने या गैंग्लियन सेल लेयर-इनर प्लेक्सिफॉर्म लेयर (GCIPL) में परिवर्तन का पता लगाएं। टेम्पोरल-प्रमुख परिवर्तन विशिष्ट हैं, और 20-79% की कमी बताई गई है2)। दृश्य पूर्वानुमान के मूल्यांकन में भी उपयोगी।
यदि EMB बंद करने के बाद भी दृष्टि हानि बढ़ती है, तो अन्य ऑप्टिक न्यूरोपैथी पर विचार किया जाना चाहिए।
EON के लिए कोई स्थापित उपचार मौजूद नहीं है। कारण दवा को बंद करने से बेहतर कोई उपचार नहीं है। यदि EON का संदेह हो, तो EMB को तुरंत बंद करना सबसे महत्वपूर्ण कदम है। नेत्र रोग विशेषज्ञ को EMB बंद करने से पहले निर्धारित चिकित्सक से सीधे संपर्क करना चाहिए।
EMB बंद करने के बाद भी दृष्टि और दृश्य क्षेत्र दोष लगभग 2-3 महीने तक बढ़ सकते हैं। फिर धीरे-धीरे सुधार शुरू होता है, लेकिन सुधार धीमा होता है, 6 महीने से 2 साल तक।
धूम्रपान बंद कर देना चाहिए क्योंकि इसका विलायक विषाक्तता और इथेनॉल ऑप्टिक न्यूरोपैथी में अतिरिक्त हानिकारक प्रभाव होता है। उच्च रक्तचाप या मधुमेह जैसी रक्त प्रवाह को प्रभावित करने वाली अंतर्निहित बीमारियों के मामले में, आंतरिक चिकित्सा के सहयोग से उपचार किया जाना चाहिए।
| पूर्वानुमान कारक | प्रभाव |
|---|---|
| शीघ्र पहचान और शीघ्र बंद करना | 30-64% मामलों में दृष्टि में सुधार |
| 60 वर्ष से कम आयु | लगभग 80% रिकवरी दर |
| 60 वर्ष और अधिक | लगभग 20% रिकवरी दर |
जिन रोगियों की दृष्टि ठीक होती है, उनमें स्नेलन चार्ट पर औसतन 2 पंक्तियों का सुधार देखा जाता है 2)। हालांकि, कुछ रोगियों की दृष्टि पूरी तरह से ठीक हो जाती है, जबकि कुछ में स्थायी दृश्य हानि बनी रहती है। शुरुआत में ऑप्टिक डिस्क पैलर की उपस्थिति खराब पूर्वानुमान से जुड़ी होती है।
EMB बंद करने के बाद भी RNFL मोटाई में कमी जारी रहने की रिपोर्ट है, और करीबी निगरानी और तत्काल दवा बंद करने के बावजूद अपरिवर्तनीय दृष्टि हानि हो सकती है 2)।
यदि अपरिवर्तनीय ऑप्टिक शोष होने से पहले EMB बंद कर दिया जाए, तो 30-64% रोगियों में दृश्य कार्य में सुधार होता है। हालांकि पूर्ण सुधार दुर्लभ है, और औसत सुधार स्नेलन की 2 पंक्तियाँ है। बंद करने के बाद 2-3 महीने तक लक्षण बढ़ सकते हैं, इसलिए निरंतर अनुवर्ती आवश्यक है। विवरण के लिए «मानक उपचार» अनुभाग देखें।
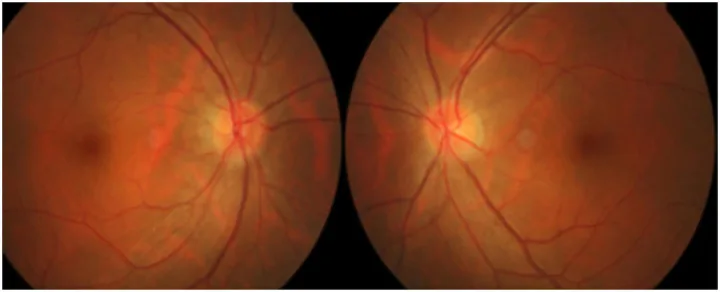
रेट्रोबुलबार ऑप्टिक न्यूरोपैथी EON का सबसे सामान्य रूप है, और शुरुआत में ऑप्टिक डिस्क सामान्य दिखाई देती है।
EMB और इसका मेटाबोलाइट EDBA दोनों धातु केलेटर के रूप में कार्य करते हैं। EDBA की अंतःनेत्र निकासी एथमब्युटोल की तुलना में कम होती है, जिससे स्थानीय सांद्रता अधिक होती है, और अनुमान है कि यह विषाक्तता में अधिक योगदान देता है 2)।
क्षति के मुख्य मार्ग इस प्रकार हैं:
पैपिलोमैक्यूलर बंडल (papillomacular bundle) बनाने वाले पार्वो-सेल्युलर अक्षतंतु (parvo-cellular axons) में माइटोकॉन्ड्रिया की ऊर्जा की मांग विशेष रूप से अधिक होती है। इस कारण विषाक्त और पोषण संबंधी ऑप्टिक न्यूरोपैथी में ये अक्षतंतु प्राथमिक रूप से क्षतिग्रस्त होते हैं 2)।
रेटिनल गैंग्लियन कोशिकाओं में से, अत्यधिक ATP खपत करने वाली P कोशिकाओं के प्रमुख रूप से क्षतिग्रस्त होने का अनुमान है, जो केंद्रीय स्कोटोमा (central scotoma) के निर्माण की प्रक्रिया से मेल खाता है। दूसरी ओर, प्रकाश प्रतिक्रिया में शामिल γ कोशिकाएं संरक्षित रहती हैं, इसलिए प्रकाश प्रतिक्रिया अपेक्षाकृत बनी रहती है।
पशु प्रयोगों में, EMB द्वारा प्रेरित एक्सोनल न्यूरोपैथी ऑप्टिक काइआज़्म (optic chiasm) पर अधिक होती है, जो चिकित्सकीय रूप से द्विपार्श्विक हेमियानोप्सिया (bitemporal hemianopia) वाले रोगियों के अस्तित्व से मेल खाती है।
Sabhapandit et al. (2023) ने 2010-2021 में प्रकाशित 12 अध्ययनों (5818 लोग, जिनमें से 309 EON से पीड़ित) की एक व्यवस्थित समीक्षा की और बताया कि 2 महीने से अधिक समय तक EMB का लंबे समय तक उपयोग महत्वपूर्ण ऑप्टिक न्यूरोटॉक्सिसिटी का कारण बनता है 1)। EMB बंद करने के बाद दृश्य तीक्ष्णता में सुधार सांख्यिकीय रूप से महत्वपूर्ण था (P = 0.035)। रंग दृष्टि और दृश्य क्षेत्र की असामान्यताओं में सुधार महत्व स्तर तक नहीं पहुंचा।
Matsumoto et al. (2021) ने एक 85 वर्षीय पुरुष का मामला रिपोर्ट किया, जिसमें कम खुराक वाले EMB (12 mg/kg) और छोटी अवधि (2.5 महीने) के बावजूद, EMB बंद करने के बाद दृश्य तीक्ष्णता तेजी से बिगड़ गई और अपरिवर्तनीय दृष्टि हानि हुई 3)। बंद करने से पहले 20/17 की सुधारित दृश्य तीक्ष्णता 3 सप्ताह में 20/330 (दाहिनी आंख) और 20/1000 (बाईं आंख) तक गिर गई। यह मामला दर्शाता है कि कम खुराक पर भी विनाशकारी दृष्टि हानि हो सकती है।
Peterson & Hawy (2022) ने MAC उपचार के दौरान 3 वर्षों तक <15 mg/kg/दिन EMB लेने वाले 82 वर्षीय पुरुष में विलंबित EON के विकास का मामला रिपोर्ट किया 4)। EMB बंद करने के बाद दृश्य तीक्ष्णता में सुधार हुआ, और 10 महीने बाद भी सुधार बना रहा। शुरुआत का माध्य समय 9 महीने माना जाता है, लेकिन 3 वर्ष से अधिक समय बाद भी शुरुआत संभव दिखाई गई।
कोनाना एट अल. (2024) ने एथमब्यूटोल विषाक्तता के कारण शंकु कोशिका शिथिलता (cone dysfunction) के तीन मामलों की रिपोर्ट दी 5)। मुख्य शिकायतें प्रकाश संवेदनशीलता और दृष्टि में कमी थीं, और इलेक्ट्रोरेटिनोग्राम में फ्लिकर प्रतिक्रिया में विलंबता देरी पाई गई। यह रिपोर्ट बताती है कि एथमब्यूटोल विषाक्तता न केवल ऑप्टिक तंत्रिका बल्कि रेटिना की कोशिका परतों को भी प्रभावित करती है।
फिक्स्ड-डोज़ कॉम्बिनेशन (FDC: एक गोली में आइसोनियाज़िड, रिफैम्पिसिन, पायराज़िनामाइड और एथमब्यूटोल) की शुरुआत और उपचार अवधि बढ़ने से EON (एथमब्यूटोल-प्रेरित ऑप्टिक न्यूरोपैथी) के मामलों में वृद्धि की आशंका है 2)। स्क्रीनिंग प्रणाली स्थापित करना, OCT और VEP की उप-नैदानिक EON का पता लगाने में उपयोगिता का सत्यापन, EON के रोगजनन तंत्र को स्पष्ट करना और जोखिम कारकों की पहचान करना भविष्य के महत्वपूर्ण शोध विषय हैं।