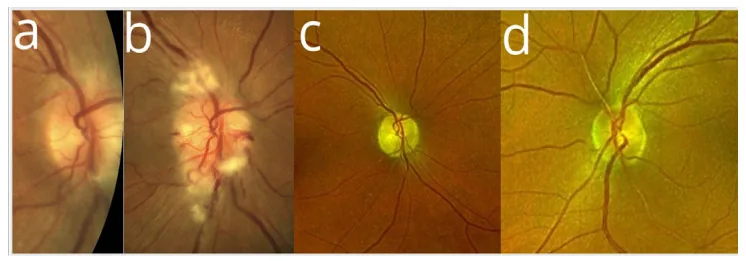
胺碘酮相关性视神经病变(AAO N)是服用抗心律失常药物胺碘酮期间发生的视神经 疾病,估计发生率为0.3–2%。
最常见的眼部副作用是涡状角膜 变性(70–100%),但视神经病变 是最严重的眼部副作用。
其特征为隐匿性发病和迁延性视乳头水肿 (停药后可持续长达15个月),与非动脉炎性前部缺血性视神经病变 (NAION )的鉴别是临床上的最大挑战。
约三分之一的患者无症状,因此定期眼科监测很重要。
治疗原则是停用可疑药物,但由于该药用于治疗致命性心律失常,必须与心内科协作。
停用胺碘酮后,视力 改善仅见于58%的患者,21%进一步恶化,20%进展为法定盲(低于20/200)。
胺碘酮是一种二碘化苯并呋喃衍生物,于20世纪60年代作为抗心绞痛药物开发。它被归类为III类抗心律失常药,但也具有I、II、IV类特性1) 。广泛用于房颤、室性心动过速和室颤,在日本以商品名Ancaron(国外为Cordarone、Pacerone等)销售。
胺碘酮的口服生物利用度为30–80%,半衰期极长,为20–100天。它亲脂性高,蓄积于脂肪组织1) ,经肝脏CYP3A4/CYP2C8代谢,产生活性代谢物去乙基胺碘酮(DEA)1) 。
胺碘酮可引起多种眼部副作用。
涡状角膜 变性(verticillate keratopathy) :最常见的眼部副作用。表现为角膜上皮 深层褐色涡状色素沉着,发生于三分之二的治疗患者。与剂量和用药时间相关,高剂量(400 mg/天)时几乎100%出现。采用Orlando分级(I–IV级)评估。仅有涡状角膜 变性通常无需停用胺碘酮。胺碘酮相关性视神经病变(AAO N) :最严重的眼部副作用。发生率报道为0.36–2%。其他 :前囊下晶状体 混浊、多发性霰粒肿 、干眼症 等。
胺碘酮还具有多种全身副作用,包括甲状腺功能障碍、肺毒性(过敏性肺炎,可能致命)、周围神经病变和光敏性。
Cheng等人利用台湾国民健康保险数据库进行的队列研究(胺碘酮组6,175人 vs 对照组24,700人)显示,胺碘酮组0.3%出现视神经病变 ,与非用药组(0.1%)相比,风险比为2.09(95% CI 1.13~3.85)1) 。
Q
服用胺碘酮发生视神经病变的概率是多少?
A
台湾的队列研究报告胺碘酮服用者中0.3%出现视神经病变 ,与非服用组相比风险比为2.091) 。回顾性报告显示发生率为0.362%,前瞻性双盲试验(超过1,600人)的最大估计年发生率为0.230.74%1) 。
????????????????? Dina Lešin Gaćina et al. Is Semaglutide Linked to
NAION ? A Case Report on a Rare Ocular Complication. Reports. 2025 Aug 20; 8(3):149. Figure 1. PM
CI D: PMC12372079. License: CC BY.
???????????????????????????????????????????????????????????????????????????
视力 下降无症状 :多达三分之一的AAO N患者无自觉症状。常仅通过视盘水肿 发现。色觉异常
AAO N的主要临床所见如下。
视盘水肿 视盘水肿 持续中位时间3个月(最长15个月)。序贯性视盘肿胀 :有报告称一眼发病后3~48周对侧眼出现视盘肿胀的“序贯”模式1) 。合并角膜 涡状沉积 :常与视神经 毒性同时出现,发生率较高。
Patel等人提出了以下五种分类2) 。
隐匿起病型
最常见的类型 :表现为双侧同时性视乳头水肿 ,缓慢进展。通常主观症状较少。
非动脉炎性前部缺血性视神经病变样型
第二常见的类型 :表现为急性单侧或双侧视力 丧失,临床上与非动脉炎性前部缺血性视神经病变 非常相似。
球后视神经病变型
最难诊断的类型 :表现为眼底正常,需要影像学和血液检查来确诊。
其他类型
颅内压增高型 :脑脊液压力超过200 mmH₂O。
迟发进展型 :停用胺碘酮后数天至数周出现视乳头水肿 。
胺碘酮使用时间 :AAO N发病的平均时间为9个月(范围1-84个月)。有报道中位数约为4个月2) 。治疗时间超过中位数41天时,视神经病变 风险增加3.5倍1) 。累积剂量 :累积剂量和用药时间比日剂量对风险评估更重要1) 。出现视觉症状的患者剂量中位数为200 mg/天(范围57-1,200 mg/天)。性别 :一项对296例病例的回顾性研究显示,平均年龄66岁,74%为男性。男性的风险约为女性的3倍1) 。高血压 :在男性中,使用胺碘酮和高血压是视神经病变 的显著危险因素1) 。合并心血管危险因素 :许多服用胺碘酮的患者具有心血管危险因素,并且本身发生非动脉炎性前部缺血性视神经病变 的风险也很高。胺碘酮相关NA-AION的特征包括双侧、隐匿性发病、全身性(非水平半盲型)视野缺损 以及持续数月的视盘水肿 。
Q
减少胺碘酮的剂量是否能降低视神经病变的风险?
A
日剂量并非显著的危险因素;累积剂量和用药时间更为重要1) 。有报告称,治疗中位时间超过41天时风险增加3.5倍,因此即使短期使用也需要随访。
AAO N是一种临床诊断,尚无确立的客观诊断标准。
当出现以下表现时,怀疑AAO N:
隐匿性发病
缓慢进展
持续性视盘水肿 (停药后仍持续数月)
对侧眼大杯(非危险视盘形态)
轻度视神经 功能障碍(视力 20/40以上,RAPD ≤ 0.9 log单位)
所有NA-AION患者应询问胺碘酮使用史,若阳性应通知心内科。药物性视神经病变 需注意用药史,首先怀疑至关重要。
AAO N与非动脉炎性前部缺血性视神经病变 的鉴别是临床上的最大挑战。下表列出主要鉴别点。
鉴别点 非动脉炎性前部缺血性视神经病变 AAO N 发病方式 急性,数天至数周 隐匿至急性 视盘形态 危险视盘(小视盘) 无特定形态 视盘水肿 持续时间2~6周消退 持续1~15个月 侧别 多为单侧 多为双侧
还需注意与巨细胞动脉炎 鉴别。有报道称,一名使用胺碘酮的72岁男性被怀疑为AAO N,但颞动脉活检确诊为巨细胞动脉炎 3) 。巨细胞动脉炎 即使ESR和CRP 正常,活检也可能呈阳性3) 。此外,巨细胞动脉炎 在MRI上可见视神经 鞘增强(视神经周围炎 ),而AAO N未见此表现3) 。
药物性视神经病变 的治疗原则是停用可疑药物。
由于胺碘酮用于治疗致命性心律失常,不能轻易停药。按以下步骤处理。
紧急咨询心内科 :与心内科讨论是否更换为替代药物或进行导管消融。如果仅有涡状角膜 病变 :通常可以继续使用胺碘酮。如果发生AAO N :需由心内科、眼科和患者三方仔细协商继续用药的风险和获益。如果存在已有的视神经 疾病 :一些专家建议避免使用胺碘酮。
停药后的视力 结局如下:
视力 改善:58%无变化:21%
进一步视力 下降:21%
法定盲(单眼或双眼视力 低于20/200):20%
目前尚无针对AAO N的既定药物治疗。
Q
停用胺碘酮后视力会恢复吗?
A
停用胺碘酮后,视力 改善仅占58%,21%无变化,21%进一步恶化,20%进展为法定盲(低于20/200)。此外,由于半衰期长达20-100天,停药后药物仍会在体内残留,这一点需要注意1) 。
AAO N的主要发病机制被认为与磷脂质沉积症相关的轴突损伤起核心作用。
溶酶体功能障碍 :胺碘酮抑制溶酶体鞘磷脂酶,诱导磷脂质沉积症1) 。板层状包涵体蓄积 :板层状包涵体选择性蓄积在视神经 粗大轴突的细胞质内。在胺碘酮诱导的周围神经病变中,周围神经的轴突和施万细胞也观察到类似变化。轴浆流障碍 :板层小体机械性和生化性地减少轴浆流,这被认为是视神经 损伤的机制1) 。这种紊乱可能导致视乳头水肿 。氧化应激 与凋亡1) 。对视网膜神经节细胞 (RGC )的影响 :大鼠实验证实RGC 凋亡以及视网膜电图 a波和b波振幅降低1) 。
Q
胺碘酮通过什么机制损伤视神经?
A
胺碘酮抑制溶酶体鞘磷脂酶,诱导磷脂质沉积症,导致视神经 轴突内板层状包涵体蓄积1) 。这种蓄积损害轴浆流,引起视乳头水肿 ,同时氧化应激 也导致细胞损伤,从而降低视神经 功能。
Liao等人(2007)在RPE 细胞模型中显示,IGF-1通过PI3K/Akt通路保护RPE 细胞免受胺碘酮诱导的氧化应激 和凋亡1) 。胺碘酮以浓度依赖性方式降低RPE 细胞活力(LC50 = 50 μM),而IGF-1抑制了这种降低。MAPK通路的抑制不影响保护效果1) 。
2017年的一项大鼠研究表明,胺碘酮影响视网膜神经节细胞 层,而IGF-1逆转了这种效应1) 。IGF-1未来在AAO N治疗中的应用有待进一步研究。
Mindel等人(2007年)的前瞻性双盲试验(超过1600人,中位用药45.5个月)未报告双侧视力 丧失病例,最大估计年发生率为0.23%–0.74% 1) 。这与既往回顾性报告(0.36%–2%)相矛盾,因此关于AAO N是否是一种临床不同于非动脉炎性前部缺血性视神经病变 的独立疾病实体的争论仍在继续。
巨细胞动脉炎 病例的MRI表现为视神经 鞘增强(optic perineuritis),报告率为57%–78%,而AAO N中未见此表现 3) 。未来,对疑似AAO N病例进行系统性MRI评估可能有助于提高鉴别诊断的准确性。
Mitchell R, Chacko J. Clinical and Mechanistic Review of Amiodarone-Associated Optic Neuropathy . Biomolecules. 2022;12:1298.
Patel S, Mahmood R. Amiodarone-Associated Optic Neuropathy in a Patient With Associated Arrhythmia. Cureus. 2024;16(3):e55819.
Tseng AM, Bindiganavile SH, Bhat N, Divatia MK, Lee AG. Optic Perineuritis Distinguishing Arteritic Ischaemic from Amiodarone-Associated Optic Neuropathy . Neuro-Ophthalmology. 2021;45(5):329-333.
复制全文后,可以粘贴到你常用的 AI 助手中提问。
打开下面的 AI 助手,并把复制的内容粘贴到聊天框。