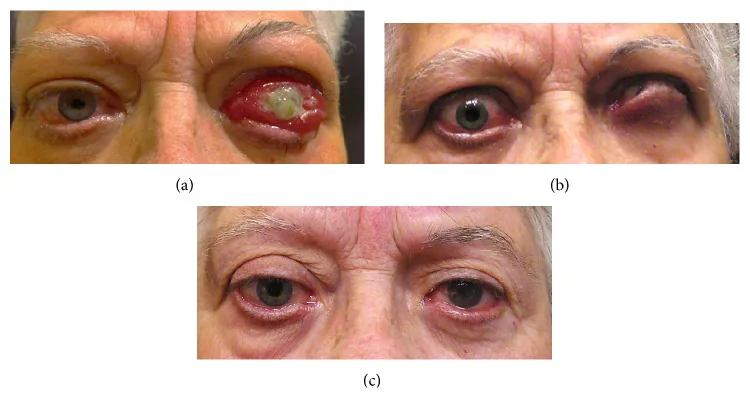
是甲状腺眼病(TED)最严重的并发症,发生于所有TED病例的3%至8%。
主要发病机制是眼外肌 肿大导致眶尖部视神经 受压。
主要症状包括视力 下降、色觉异常 和视野缺损 ,但半数以上患者矫正视力 保持在0.5以上。
约70%为双侧发病。
首选治疗为类固醇冲击疗法 ;若2周内无改善,应考虑眼眶 减压手术。
通过适当治疗,约70%以上的患者可恢复视 功能。
甲状腺视神经病变(dysthyroid optic neuropathy: DON)是甲状腺眼病(thyroid eye disease: TED)相关的视神经 功能障碍。TED又称格雷夫斯眼病 (Graves orbitopathy: GO),是一种自身免疫性疾病,由于眼外肌 和眶内脂肪肿大导致眶内压升高,压迫视神经 而引起。它是TED最严重的并发症之一,若不治疗,可能导致永久性视力 丧失。
DON发生于所有TED病例的0.9%至8.6%1) ,约70%为双眼发病。半数以上患者矫正视力 保持在0.5以上,但最严重时可导致失明。通过适当治疗,视功能有望恢复,因此早期诊断极为重要。
Q
患有甲状腺眼病就一定会得DON吗?
A
只有约3%至8%的TED病例会发展为DON,因此大多数TED患者不会进展为DON。但若存在肌病型表型、吸烟、高龄等风险因素,则需注意。详情请参见“病因与风险因素”一节 。
???????????????????? Jesús Barrio-Barrio, Alfonso L Sabater, Elvira Bonet-Farriol et al. Graves’ Ophthalmopathy: VISA versus EUGOGO Classification, Assessment, and Management. Journal of Ophthalmology. 2015 Aug 17; 2015:249125. Figure 4. PM
CI D: PMC4553342. License: CC BY.
???????????????????????????????????????????????????????????????????????????
DON的首发症状是中心视力 模糊和颜色鲜艳度下降(饱和度降低)。视力 下降程度从轻微到无光感不等,但半数以上患者保持视力 0.5以上。
主要自觉症状如下所示。
视力 下降视力 雾视 。呈急性至亚急性病程。饱和度降低 :以红色为主,颜色不如以前鲜艳。复视 复视 。眼眶 不适
DON的主要临床所见及其出现频率如下所示。
临床所见 出现频率 视力 下降约80% 色觉减退 约77% 视野缺损 约71% 眼球运动受限 约70% 视乳头水肿 约20%
其他重要的临床发现列举如下。
相对性传入性瞳孔 障碍(RAPD ) :当视神经病变 程度不对称时呈阳性。双眼同等程度受损时无法检测到。闪烁值降低 :反映视神经 功能障碍。充血 性软组织征象结膜 充血 和水肿变得明显。上视时眼压 升高 :可能观察到超过9 mmHg的升高。眼球突出 眼眶 压力弥漫性升高。
76%的DON病例为双侧,约半数无视乳头肿胀。即使视乳头无异常,DON也可能发生,因此视功能检查与影像学检查的结合至关重要。
TED是一种自身免疫性疾病,由针对眼眶 成纤维细胞表面TSH受体和IGF-1受体的自身抗体引起。抗体结合导致脂肪分化、T淋巴细胞活化和细胞因子释放,导致糖胺聚糖(GAG)在眼眶 脂肪和肌肉中沉积。
TED大致分为两种表型。
脂肪增生型
别名 :I型、脂肪生成型
特征 :主要表现为脂肪扩大和上睑提肌瘢痕化。约占TED患者的三分之二。
与DON的关系 :除非严重眼球突出 导致视神经 牵拉,否则很少导致DON。
肌病型
别名 :II型、肌病型
特征 :伴有眼外肌 肥大,表现为充血 性软组织体征和眼球运动障碍 。约占TED患者的三分之一。
与DON的关系 :容易在眼眶 尖部发生视神经 压迫,是DON的主要原因。
TED本身在女性中更常见(男女比例1:4),而DON倾向于发生在老年男性中。主要风险因素如下所示。
吸烟 :TED进展和DON发生的最大风险因素。高龄 :60岁以上人群中重度TED的频率更高。糖尿病 :作为合并症,增加DON的风险。放射性碘治疗(RAI) :使TED进展风险增加高达40%。免疫应答刺激因子 :包括间歇性感染、局部手术和其他诱发因素。
甲状腺功能异常与TED的严重程度相关,但与DON的发生或严重程度无明确相关性。此外,即使所有甲状腺自身抗体均为阴性,也可能发生DON。
Q
吸烟会使DON风险增加多少?
A
吸烟被认为是TED进展和DON发生的最重要风险因素。放射性碘治疗后TED恶化的风险在吸烟者中也更高。已知戒烟可降低TED的治疗抵抗性。
DON的诊断基于TED患者视神经 功能障碍的确认以及影像学上眶尖部压迫的表现。
自动视野计 :最常用的检查。常见中心暗点 和旁中心暗点 。约70%的病例可检测到下方弓形暗点、水平缺损 、弥漫性敏感度下降和生理盲点扩大。色觉检查 视神经病变 中,受累较重的眼可检测到色饱和度下降。对称且缓慢发病的病例可能不明显。RAPD 检查视神经病变 的简单有效方法。对称性受累时为阴性。闪烁值检查 :作为视神经 功能下降的早期指标有用。VEP (视觉诱发电位 )OCT (光学相干断层扫描 )视网膜神经纤维层 (RNFL )和黄斑 神经节细胞复合体(GCL)的变薄。
影像学检查对于DON的确诊和手术计划是必需的。
检查 主要优点 CT 骨骼显示清晰。最适合手术计划。 MRI(STIR) 有助于评估炎症活动性。
CT :常显示眶尖部的拥挤状态(apical crowding)。重度眶尖部拥挤是预测因子,敏感性62%,特异性91%。当视神经 尖部消失超过50%时,敏感性80%,特异性70.6%。也用于手术计划和术中导航。MRI :特别是STIR(短tau反转恢复)序列可评估炎症活动性。内直肌和上直肌-提肌复合体的肥大会增加DON的发生率。仅冠状切面可能遗漏总腱环附近的视神经 压迫,因此联合使用水平切面成像很重要。
有报告称,近期发生DON的患者中96%具有高滴度的甲状腺刺激免疫球蛋白(TSI)。然而,即使所有自身抗体均为阴性,也可能发生DON,因此仅凭血清学检查不能排除诊断。
Q
CT和MRI哪个应优先选择?
A
CT因骨骼显示清晰、快速、廉价且适合手术计划,常作为首选。另一方面,MRI的STIR序列在评估炎症活动性方面更优。两者互补,应根据情况选择使用。
DON的一线治疗是类固醇冲击疗法 (或半冲击疗法)。
类固醇冲击疗法 1) 。后续治疗 :冲击治疗后改为口服泼尼松龙。应避免快速减量,否则可能导致视神经病变 复发。累积剂量限制 :泼尼松龙等效累积剂量超过8克时,急性肝损伤导致的死亡风险增加1) 。日本指南建议在冲击治疗前进行肝功能检查、肝炎病毒检查和T-SPOT检查等预处理检查1) 。
EUGOGO指南(2021年)推荐每日最多1克,连续3天,如有改善趋势则每周重复的高剂量给药方案。
外部放射治疗(EB RT)靶向淋巴细胞和成纤维细胞以抑制炎症。由于起效不快,不单独用于急性期治疗,而是作为类固醇 治疗的辅助手段。与类固醇 联合使用,已报道可预防DON的发生。
如果类固醇 冲击治疗开始后2周内视神经 功能未见改善,则考虑紧急眼眶减压术 。在日本,22%至38%的DON患者接受了眼眶减压术 1) 。
手术入路包括以下:
经皮入路 :通过上眼睑皱褶切口到达深部外侧壁。经结膜 入路 :到达包括内侧壁和后支柱在内的眼眶 底。经鼻内镜入路 :用于经内侧壁的入路。
通过扩大眶尖部的容积来减压视神经 ,目标部位包括内侧壁、眶底和深外侧壁。术前CT计划和术中导航是有用的。
放射性碘(RAI)治疗可能使多达20%的现有TED患者症状恶化。建议在RAI前口服泼尼松进行预防性给药。RAI后TED恶化的相关因素包括吸烟、治疗前T3水平高、治疗后甲状腺功能减退症和巨大甲状腺肿。
通过适当治疗,约70%以上的患者可获得视功能恢复。进行外科减压术时,完全视力 恢复的概率更高。
Q
如果类固醇冲击疗法没有改善怎么办?
A
如果冲击疗法开始后两周内视神经 功能没有改善,则考虑紧急眶减压术。在日本,22-38%的DON患者接受了眶减压术1) 。
DON的发生涉及多种机制。
压迫机制(最重要) :在眶尖部,肥大的眼外肌 压迫视神经 ,阻碍轴浆流。眶减压术后立即获得视力 和视野恢复,这强烈支持该机制。内直肌和上直肌/提肌复合体在通过Zinn腱环时靠近视 神经,因此这些肌肉的肥大尤其会增加DON的发生率。牵拉机制(罕见) :严重的眼球突出 牵拉视神经 ,损害轴突功能和血流。这比压迫机制罕见得多。炎症机制 :眶内炎症引起视神经炎 。肾上腺皮质激素 的有效性支持该机制。
作为TED的根本病理,自身抗体与具有多能性的眶成纤维细胞上的TSH受体和IGF-1受体结合,导致以下级联反应。
成纤维细胞分化为脂肪细胞或肌成纤维细胞
T淋巴细胞的活化产生TNF -α和IL-6等炎性细胞因子
糖胺聚糖(GAG)和透明质酸的沉积导致眼眶 水肿和肌肉肿大
这些过程的结果是眼眶 内体积增加,在骨性眼眶 的限制下导致视神经 受压或牵拉。
替普罗妥木单抗是一种单克隆抗体,特异性结合IGF-1受体(IGF-1R)的细胞外结构域,抑制TED中的免疫反应。
Cong等人(2024)对5项RCT(共411例)进行的荟萃分析报告,与安慰剂相比,替普罗妥木单抗显著减少眼球突出 、改善临床活动评分(CAS)和复视 。不良事件和严重不良事件的风险与安慰剂组无显著差异2) 。
对于DON,多项观察性研究报告替普罗妥木单抗对类固醇 、放射治疗和手术抵抗的病例有效。替普罗妥木单抗在日本患者中的疗效有待未来研究1) 。
利妥昔单抗 (抗CD20抗体)眼眶 病。托珠单抗 (抗IL-6抗体)
这两种药物对DON的有效性证据均有限,需要进一步研究。
Mizuochi等人(2025年)报告了一例55岁女性患者,她从甲状腺功能减退症转变为格雷夫斯病并发展为DON。经过3个疗程的1 g脉冲治疗后,病情进展为DON,但追加脉冲治疗后视力 恢复。然而,疾病活动持续超过4年,共经历5次加重。她反复接受门诊0.5 g每周一次脉冲治疗,甲泼尼龙累积剂量达到59.5 g,但未观察到严重不良反应1) 。
该报告提示,在DON的长期管理中,仔细监测(CAS、TSAb、眼眶 MRI)非常重要。
Q
替普罗妥木单抗可以用于DON吗?
A
目前,替普罗妥木单抗尚未被确立为DON的标准治疗方法。然而,多项观察性研究报告了其对类固醇 或放射治疗抵抗的DON病例有效,未来研究值得期待。
Mizuochi K, Hiromatsu Y, Nakamura Y, et al. Transition from hypothyroidism to Graves’ disease, development of thyroid eye disease, progression to optic neuropathy after inpatient pulse therapy, and long-term administration of outpatient pulse therapy: a case report with review of literature. Endocr J. 2025;72(1):115-122.
Cong X, Pei L, Hu H. Teprotumumab for treating active thyroid eye disease: a meta-analysis. Medicine. 2024;104:e42966.
Potvin ARGG, Pakdel F, Saeed P. Dysthyroid Optic Neuropathy . Ophthalmic Plast Reconstr Surg. 2023;39(6S):S65-S80. PMID: 38054987.
复制全文后,可以粘贴到你常用的 AI 助手中提问。
打开下面的 AI 助手,并把复制的内容粘贴到聊天框。