정형 ON

특발성 시신경염
1. 특발성 시신경염이란
섹션 제목: “1. 특발성 시신경염이란”시신경염은 어떤 원인으로 시신경에 염증이 생겨 시기능이 저하되는 질환입니다. 감염성·비감염성(중독성·유전성·압박성) 시신경병증을 배제한 후, 자가면역 기전이 원인으로 생각되는 특발성이 대부분을 차지합니다.
호발 연령은 15~45세로 여성에 많고, 단안성 급성 시신경병증으로 발병합니다. 수일에서 2주 정도까지 시기능 장애가 진행되고, 이후 5주 이내에 회복 경향을 보입니다.
해부학적 분류
섹션 제목: “해부학적 분류”- 전부 시신경염(시신경 유두염): 유두 부종을 동반합니다. 일본에서는 약 50%에서 나타납니다(서양 35%보다 높음).
- 구후 시신경염: 급성기에는 안저가 정상으로 보입니다. 4~6주 후부터 유두 창백이 나타납니다.
병형과 원인별 분류
섹션 제목: “병형과 원인별 분류”| 병형 | 특징 |
|---|---|
| 특발성 (자가면역 기전) | 가장 흔함. 기본적으로 단상 경과 |
| 항AQP4 항체 양성 (NMOSD 관련) | 특발성의 약 10%. 스테로이드 저항성, 여성:남성 비율 9:1 |
| 항MOG 항체 양성 (MOGAD) | 양측성, 시신경유두부종, 긴 구간 병변. 스테로이드 반응성이나 재발 경향 |
| MS 관련 | MS 환자의 최대 75%가 일생 동안 한 번 이상 ON 경험 |
| CRION | 스테로이드 의존성, 재발성. 2003년 Kidd 등이 제안5) |
| 감염성 | 매독, 바이러스 등. 스테로이드 전에 반드시 배제 |
초진 시 항AQP4 항체를 측정하고, 음성인 경우 특발성으로 취급합니다.
일본의 연간 발병률은 성인 10만 명당 1.6명입니다. 호발 연령은 1545세이며 여성이 약 70%를 차지합니다. 전 세계 유병률은 약 10만 명당 15명으로 추정됩니다.
MS와의 연관성은 매우 깊으며, 특발성 시신경염 발병 후 15년간 MS로의 전환 누적 확률은 50%입니다. 첫 발병 시 뇌 MRI에서 탈수초 병변이 없으면 전환율은 25%에 그치지만, 병변이 1개 이상 있으면 78%에 이릅니다.
소아에서는 호발 연령이 9~10세이며, 어릴수록 양안성 및 중증 시력 장애를 보이며, 특히 5세 이하에서 두드러집니다. 소아 MS로의 전환율은 Adachi 등이 약 30%, Mizota 등이 16%로 보고했습니다.
MOGAD의 연간 발병률은 100만 명당 1.6~4.8명으로 추정됩니다. 1)
특발성 시신경염의 약 50%가 15년 이내에 MS로 전환됩니다. 단, 첫 발병 시 뇌 MRI에서 탈수초 병변이 없으면 전환율은 25%에 그칩니다. 발병 후에는 뇌 MRI를 통한 위험 평가와 신경과와의 협력을 통한 경과 관찰이 중요합니다.
2. 주요 증상 및 임상 소견
섹션 제목: “2. 주요 증상 및 임상 소견”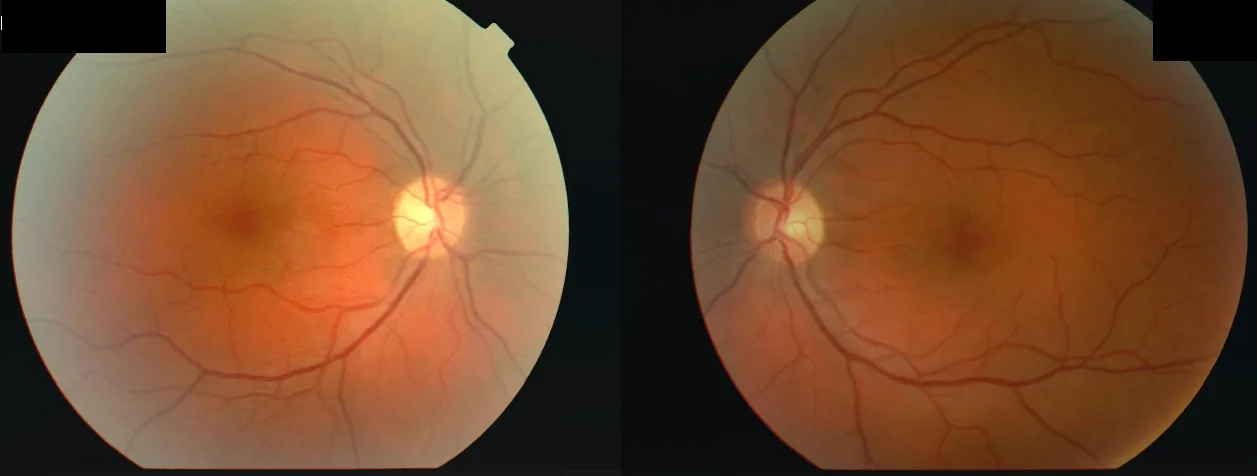
자각 증상
섹션 제목: “자각 증상”급성 발병 양상을 보이며, 다음 증상이 특징적입니다.
- 급성 한쪽 눈 시력 저하: 수일에서 2주 정도까지 진행됩니다. 발병 후 약 1주일 경에 시기능이 가장 악화됩니다.
- 안통/안구 운동통: 일본에서는 약 50~60%에서 나타납니다. 시력 저하 수일 전부터 나타날 수 있습니다.
- 시야 장애: 중심 암점 또는 맹점 중심 암점이 많지만 수평 반맹인 경우도 있습니다. 미만성 장애도 많습니다.
- 색각 이상: 적색 채도 저하가 특징적입니다.
- Uhthoff 징후: 체온 상승(목욕, 운동 후)으로 일과성 시력 저하 또는 흐림을 자각합니다. 수분 내에 나타나 1시간 이내에 소실됩니다.
- 광시증(phosphenes): 빛의 섬광을 자각함
- Pulfrich 현상: 움직이는 물체의 깊이 지각 변화
임상 소견
섹션 제목: “임상 소견”- 상대적 구심성 동공 장애(RAPD): 가장 중요한 소견. 단안성 또는 좌우 차이가 있을 때 양성. 시신경염에서는 기능 장애가 경미해도 이상을 보임. 산동 전에 전치렌즈와 세극등으로 확인
- 시력 장애 정도: ONTT에서 시력 1.0 이상이 10%, 0.5
1.0이 25%, 0.10.5가 29%, 그 이하가 36%로 보고됨 - 안저 소견: 전부 시신경염에서는 유두의 발적과 종창이 보이며, 형광 안저 촬영에서 과형광. 구후 시신경염에서는 초기에는 정상이고 4~6주 후에 창백화
- 핵간 안근 마비: 다발성 경화증(MS) 합병 예에서 내측 세로 다발의 탈수초 병변으로 나타남
- 망막 혈관초 형성 및 주변부 포도막염: MS 환자의 5~10%
비정형 ON을 시사하는 소견
섹션 제목: “비정형 ON을 시사하는 소견”다음 징후가 있는 경우 비정형 시신경염을 의심하고 상세한 원인 검사를 시행한다.
- 연령 15~45세 이외(18세 미만 또는 50세 이상)
- 양안 동시 발병
- 발병 후 2주 이후에도 증상 진행
- 스테로이드 의존성 경과
- 전신 증상 동반
병형별 임상 특징
섹션 제목: “병형별 임상 특징”| 특징 | MOG-ON | AQP4-ON | MS-ON | CRION |
|---|---|---|---|---|
| 성비 (남:여) | 1:1 | 1:7~9 | 1:3 | 1:1.7~2.3 |
| 양안성 | 31~84% | 13~82% | 매우 드물음 | 있음 |
| 유두부종 | 45~92% | 7~52% | 11~14% | 경증 |
| 안통 | 73~92% | 28~50% | 10~46% | 있음 |
| 최저 시력 | 중등도~중증 | 중등도~중증 | 경증~중등도 | 다양함 |
| 회복 | 양호 | 불량할 수 있음 | 양호 | 스테로이드 의존 |
출처: Jeyakumar N, et al. Eye. 20241)
소아 특이 소견
섹션 제목: “소아 특이 소견”소아 시신경염에서는 성인에서 보이는 구후시신경염보다 시신경유두의 발적·종창을 동반한 전형적인 유두염이 흔합니다. 염증 부위는 유두뿐만 아니라 시신경 전체에 걸쳐 있습니다. 양안성은 5075%, 전방시신경염형은 5075%를 차지합니다.
항AQP4 항체 양성 시신경염은 특발성 시신경염의 약 10%를 차지하는 난치성 병형입니다. 일반 시신경염에 비해 발병 시 시력이 더 나쁘고, 스테로이드 치료에 대한 반응이 좋지 않으며, 재발이 많습니다. 양안성으로 이행하기 쉬운 점도 다릅니다. 진단에는 혈청 항AQP4 항체 측정이 필수입니다.
3. 원인과 위험 요인
섹션 제목: “3. 원인과 위험 요인”자가면역 기전이 의심되는 특발성에서는 미세아교세포 등의 염증 관련 세포가 시신경 내로 침윤하여 염증을 일으킵니다. 반복적인 염증은 신경 섬유에 손상을 축적시키고 시신경 위축으로 이행합니다.
바이러스 감염이 자가면역 반응의 방아쇠가 된다는 가설이 제기되어 있으며, 일부 환자의 뇌척수액에서 홍역·수두·인플루엔자 등의 바이러스 항체가 검출됩니다. 소아에서는 발열·두통을 동반한 급성 파종성 뇌척수염(ADEM)과의 연관성이 알려져 있습니다.
위험 요인
섹션 제목: “위험 요인”- 성별: 여성에 많음 (남녀 비율 약 1:2 ~ 1:3)
- 연령: 20~45세에 호발
- 전구 증상: 인플루엔자 유사 질환이 선행할 수 있음
- MS 환자: 평생 적어도 한 번의 ON을 경험하는 비율이 최대 75%. 부검 시 최대 90%에서 시신경 병변 확인
MOGAD 발병 계기로 백신 접종·감염이 보고되었으며, bystander 활성화 등 면역 관용 파괴 기전이 추정됩니다. 1)
COVID-19 감염 후·백신 접종 후 ON 발병 보고가 있습니다. 백신 접종부터 ON 발병 중앙값은 18일이며, 55예 중 14예에서 MOG-IgG 양성이었습니다. 11)
4. 진단과 검사 방법
섹션 제목: “4. 진단과 검사 방법”시신경염은 임상 진단입니다. 급성 단안 시력 저하, 안구 운동통, RAPD 양성, 시야 결손의 조합으로 진단합니다.
기본 검사
섹션 제목: “기본 검사”- 시력 검사: 원거리·근거리 교정 시력을 평가합니다
- 대광 반사 검사(swinging flashlight test): RAPD 검출에 필수
- 시야 검사: 자동 시야계로 중심 암점이나 신경 섬유층 결손을 검출합니다
- 색각 및 대비감도 검사
- 중심 깜빡임 값(CFF): 감소
- 안저 검사: 유두 부종 유무 확인
영상 검사
섹션 제목: “영상 검사”- 안와 MRI: 관상면 지방억제 STIR 및 조영증강 T1 강조 영상. 시신경의 비대, 고신호, 조영증강 확인.
- 뇌 MRI FLAIR: 뇌의 탈수초 병변 유무 평가. MS 동반 평가 및 향후 MS 발병 위험 평가에 필수.
전형적 ON과 비전형적 ON의 MRI 소견은 다음과 같이 다릅니다.
| 특징 | 전형적 ON (MS 관련) | 비전형적 ON |
|---|---|---|
| 조영 패턴 | 짧은 분절 조영증강 | 긴 분절 조영증강 (1/2 이상) |
| 병변 위치 | 전방 (구후 시신경) | 후방 (시교차 및 시삭)까지 확장 |
| 시신경초 | 조영증강 없음 | 시신경초 및 안와 지방의 조영증강 |
NMOSD-ON, MOG-ON, MS-ON의 영상 특징 비교:
| 특징 | NMOSD-ON | MOG-ON | MS-ON |
|---|---|---|---|
| 침범 패턴 | 양측성 | 양측성 | 단안성 |
| 호발 부위 | 두개내 및 시교차 | 구후 (전방) | 구후 및 관내 |
| 병변 길이 | 긴 범위 | 긴 범위 | 짧은 분절 |
| 시신경초 조영증강 | 드물다 | 50%에서 양성 | 보고 없음 |
출처: Jeyakumar 20241); Cacciaguerra & Flanagan4)
OCT (광간섭단층촬영)
섹션 제목: “OCT (광간섭단층촬영)”시신경유두주위 망막신경섬유층(pRNFL) 두께를 측정한다. 급성기에는 pRNFL 비후(MOG-ON 중앙값 164μm 대 MS-ON 103μm)가 관찰된다. 만성기에는 pRNFL 얇아짐이 발생하며, 재발 횟수와 pRNFL 감소가 상관관계를 보인다. pRNFL 50μm 역치 이하에서는 시야 평균편차가 유의하게 악화된다. 1)
시각유발전위(VEP)
섹션 제목: “시각유발전위(VEP)”P100 잠복기 연장이 관찰된다. 이는 탈수초를 반영하는 소견이다.
항체 검사
섹션 제목: “항체 검사”비전형적인 경과를 보이는 경우 다음을 측정한다.
- 항AQP4 항체: 2013년 건강보험 적용. 스테로이드 저항성 또는 재발이 반복되는 경우 조기 평가가 중요합니다.
- 항MOG 항체 (MOG-IgG): 살아있는 세포 기반 분석(live cell-based assay)을 통한 혈청 검사가 권장됩니다. 고정 CBA는 민감도와 특이도가 낮습니다.
- 2023년 MOGAD 국제 진단 기준에서는 양성 CBA + 핵심 임상 표현형 + 대체 진단 배제로 확진합니다. 낮은 역가인 경우 하나 이상의 지지적 임상/MRI 특징이 필요합니다 2).
- 해당 기준의 검증: 민감도 96.5%, 특이도 98.9%, 정확도 98.5% 3).
McDonald 기준에 의한 MS 진단
섹션 제목: “McDonald 기준에 의한 MS 진단”시신경염이 MS의 초기 증상일 가능성을 평가합니다. 중추신경계의 염증성 탈수초 병변의 시간적 및 공간적 다발성을 증명하고 다른 질환을 배제하여 진단합니다. 뇌실주위, 피질/피질하, 천막하, 척수의 4개 영역 중 2개 이상에서 T2 고신호 병변이 있으면 공간적 다발성을 증명할 수 있습니다.
감별 진단
섹션 제목: “감별 진단”| 분류 | 주요 감별 질환 | 감별 포인트 |
|---|---|---|
| 탈수초성 | MS 관련 시신경염, NMO | 항체 검사, MRI |
| 면역 매개성 | CRION, 유육종증, SLE | 스테로이드 의존성, 전신 소견 |
| 감염성 | 매독, 헤르페스, 결핵 | 스테로이드 전에 반드시 배제 |
| 유전성 | 레버 유전성 시신경병증 | 젊은 남성, 양안, 무통 → 유전자 검사 |
| 약물성 | 에탐부톨, 리네졸리드 | MRI에서 조영 증강 없음 |
| 혈관성 | 비동맥염성 전방 허혈성 시신경병증 | 고령, 보통 무통, 유두 부분 창백 부종 |
| 소아 | 급성 파종성 뇌척수염 | 발열, 두통, 의식 장애 동반 |
구후시신경염으로 진단된 증례가 안와 림프종에 의한 압박성 시신경병증이었다는 보고가 있으며, 비정형 특징이 있는 경우 쉽게 스테로이드를 투여하지 말고 정밀 검사를 시행해야 합니다. 9)
소아 검사
섹션 제목: “소아 검사”일반적으로 성인에서 시행되는 FA(형광안저조영술), CFF, 동적 시야 검사는 소아에게 적합하지 않으며, 안저 소견과 두부 MRI로 진단합니다.
정형 ON에서는 시신경의 짧은 분절에만 조영 증강이 나타납니다. 반면, 비정형 ON에서는 시신경의 긴 조영 증강(길이의 1/2 이상), 후방 진행(시교차, 시삭), 시신경초의 조영 증강 등의 소견을 보입니다. 이러한 MRI 소견은 원인 질환의 감별에 직접 연결됩니다.
5. 표준 치료법
섹션 제목: “5. 표준 치료법”자연 경과와 치료 목표
섹션 제목: “자연 경과와 치료 목표”특발성 시신경염의 시기능 예후는 양호합니다. 90% 이상의 시신경염에서 경과 관찰 또는 스테로이드 전신 투여로 시력이 개선됩니다. ONTT의 장기 성적에 따르면, 발병 1년 후 시력이 0.5 이상인 경우가 93%, 1.0 이상인 경우가 70% 이상입니다.
경증/경과 관찰
섹션 제목: “경증/경과 관찰”교정 시력이 비교적 좋은 특발성 시신경염에서는 메코발라민 1,500μg/일 경구 투여(보험 적용 외)로 경과를 관찰할 수 있습니다.
항AQP4 항체 양성 ON
급성기: 스테로이드 펄스 요법 (일차 선택).
무효 시: 3~4일 간격으로 재펄스 → 여전히 무효 → 혈장교환술 고려.
혈장교환: 단순 혈장교환 > 이중막 여과 혈장교환 > 면역흡착 요법 (효과 순). 1쿠르 5~6회.
유지 요법: 프레드니솔론 510mg/일 + 아자티오프린 50100mg/일.
주의: 특발성 ON과 달리 경구 스테로이드에 의한 재발 예방이 중요.
항MOG 항체 양성 ON (MOGAD)
급성기: 스테로이드 펄스 요법이 매우 효과적. 완전 회복 50%, 부분 회복 44%. 13)
재발 경향: 스테로이드 의존성이 강하며, 경구 프레드니솔론 감량 중 (특히 10mg/일 미만 또는 중단 후 2개월 이내) 70%가 재발. 14)
유지 요법: IVIg (≥1g/kg/4주로 유의하게 재발 감소). 15) 리툭시맙은 AQP4-ON보다 효과가 떨어질 수 있음.
치료 시작 시기: 보통 두 번째 발작 후 시작 (단상성인 경우가 50% 이상이므로).
CRION (만성 재발성 염증성 시신경병증)
급성기: 메틸프레드니솔론 정맥주사 1mg/kg × 3~5일.
중간기: 경구 프레드니손 1mg/kg에서 최소 유효량까지 점감.
장기 유지: 아자티오프린, 메토트렉세이트, 시클로포스파미드, 마이코페놀레이트 모페틸이 후보입니다. IVIG도 선택지입니다.
주의: 치료 중단 시 재발하므로 장기간 지속이 필요합니다.
경구 스테로이드 단독 요법의 금기
섹션 제목: “경구 스테로이드 단독 요법의 금기”표준 용량(1mg/kg/일)의 경구 프레드니솔론 단독 요법은 ONTT에서 위약이나 정맥 스테로이드와 비교하여 재발률이 높았으므로 권장되지 않습니다.
소아의 스테로이드 펄스 요법
섹션 제목: “소아의 스테로이드 펄스 요법”메틸프레드니솔론 30mg/kg/일×3일을 시행합니다. 시력 예후는 일반적으로 양호합니다.
ADEM 동반 시신경염
섹션 제목: “ADEM 동반 시신경염”적극적으로 스테로이드 요법을 시행합니다. 스테로이드 펄스에 반응이 부족한 경우 면역글로불린 대량 정맥 주사나 혈장 교환 요법이 선택지가 됩니다.
MS 재발 예방
섹션 제목: “MS 재발 예방”MS 동반 예에서는 시력 개선 후 재발 예방을 위한 치료를 고려합니다. 신경과와 협력하여 질병 조절 약물(인터페론 베타, 글라티라머 아세테이트, 핑골리모드, 나탈리주맙 등)을 검토합니다.
ONTT 결과에 따르면, 스테로이드 펄스 요법은 회복 속도를 단축시키지만 발병 1년 후 최종 시력에는 유의한 차이가 없었습니다. 특발성 시신경염에서는 치료 없이도 93%가 0.5 이상의 시력으로 회복됩니다. 그러나 항AQP4 항체 양성인 경우는 스테로이드 저항성이므로 조기 혈장교환술을 포함한 적극적인 치료가 필요합니다.
CRION은 치료 중단 시 재발하는 질환이므로 증상 관해 후에도 장기적인 면역억제 치료의 지속이 필요한 경우가 많습니다. 스테로이드의 최소 유효 용량을 확인한 후 비스테로이드성 면역억제제를 병용하여 치료 요법을 개별적으로 설계합니다.
6. 병태생리학 및 상세한 발병 기전
섹션 제목: “6. 병태생리학 및 상세한 발병 기전”특발성(자가면역성) 시신경염의 병태
섹션 제목: “특발성(자가면역성) 시신경염의 병태”자가면역 기전이 의심되는 특발성에서는 미세아교세포 등의 염증 관련 세포가 시신경 내에 침윤하여 염증을 유발합니다.
- 면역 매개성 수초 파괴: 자가면역 기전에 의해 시신경의 수초가 공격받습니다. 도약 전도가 불가능해져 축삭의 충격 전달 장애가 발생합니다.
- 축삭 변성: 수초 파괴 후 망막 신경절 세포의 축삭이 변성을 시작합니다.
- 대식세포에 의한 탐식: 대식세포가 잔여 수초를 제거합니다.
- 신경아교증: 별아교세포가 증식하여 신경아교 흉터를 형성합니다. 다발성 경화증의 ‘경화’는 이에서 유래합니다.
반복적인 시신경 염증을 경험하면 신경 섬유에 누적 손상이 발생하여 시신경 위축으로 이행됩니다.
항AQP4 항체 양성 시신경염의 기전
섹션 제목: “항AQP4 항체 양성 시신경염의 기전”항AQP4 항체가 보체와 결합하여 시신경 내의 신경아교세포인 별아교세포를 공격함으로써 발병합니다. 시신경 및 시교차의 별아교세포는 AQP4를 많이 발현하고 있어 표적이 되기 쉽습니다.
항MOG 항체 양성 ON의 기전
섹션 제목: “항MOG 항체 양성 ON의 기전”MOG-IgG(주로 IgG1 아류)는 CNS 수초 표면의 MOG를 표적으로 합니다. 보체 경로 활성화와 항체 의존성 세포 포식이 탈수초에 관여합니다. 그러나 보체 활성화는 AQP4-IgG에 비해 약합니다. MOGAD에서는 CD4 양성 T 세포와 대식세포가 주를 이루는 반면, MS에서는 CD8 양성 T 세포가 우세합니다. 1)4)
MOG는 망막에서 발현되지 않음에도 불구하고 MOG-ON에서는 망막 신경절 세포 손상이 발생합니다. 이 기전으로 글루타메이트 독성과 시신경 유두의 혈액뇌장벽 취약성이 제시되고 있습니다. 1)
IL-6가 혈액뇌장벽 투과성을 증가시키고 형질아세포 분화를 촉진하는 기전도 주목받고 있습니다.
CRION의 병태적 위치
섹션 제목: “CRION의 병태적 위치”CRION은 원래 스테로이드 반응성이고 재발 경향이 있는 시신경염을 포괄하는 증후군으로 제안되었습니다. 5) 이후 CRION 코호트의 항체 검사에서 최대 22%가 AQP4-IgG 양성, 최대 25%가 MOG-IgG 양성인 것으로 밝혀졌습니다. 6)7)8) 이로부터 CRION은 MOG 항체 관련 시신경염 및 AQP4 항체 관련 시신경염을 포함하는 이질적인 병인군을 포괄하는 증후군적 진단으로 간주됩니다.
발병 트리거
섹션 제목: “발병 트리거”바이러스 감염이 자가면역 반응의 방아쇠가 된다는 가설이 제시되었습니다. 일부 ON 환자의 뇌척수액에서 수두대상포진 바이러스 및 단순포진 바이러스 DNA가 검출되었다는 보고가 있습니다. MOGAD에서는 백신 접종이나 감염에 의한 면역 관용 파괴(방관자 활성화, 분자 모방)가 가정됩니다. 1)
7. 최신 연구와 향후 전망
섹션 제목: “7. 최신 연구와 향후 전망”AQP4 양성 NMOSD에 대한 새로운 생물학적 제제
섹션 제목: “AQP4 양성 NMOSD에 대한 새로운 생물학적 제제”AQP4 양성 NMOSD에 대해 Level 1 근거를 가진 생물학적 제제가 등장했습니다. 4)
- 에쿨리주맙: C5 억제제. 3상 시험에서 재발 위험 94% 감소
- 라불리주맙: C5 억제제(에쿨리주맙의 개량형). 3상 시험에서 재발 위험 98.6% 감소
- 이네빌리주맙: CD19 표적 B세포 제거 약물. AQP4 양성 NMOSD에서 재발 위험을 77% 감소시킵니다.
- 사트랄리주맙: IL-6 수용체 억제제. AQP4 양성 NMOSD에서 재발 위험을 74~79% 감소시킵니다. 피하 주사로 가정에서 투여 가능합니다.
이 두 약물은 모두 AQP4 양성 NMOSD에 대한 근거가 확립되어 있지만, MOGAD에 대한 적응증은 아직 확립되지 않았습니다.
MOGAD에 대한 임상시험
섹션 제목: “MOGAD에 대한 임상시험”사트랄리주맙(NCT05271409)과 로자놀릭시주맙(NCT05063162)의 3상 무작위 대조 시험이 진행 중입니다. 토실리주맙(IL-6 수용체 항체)의 허가 외 사용에서 최대 29개월간 재발 예방 효과가 보고되었습니다. 1)
COVID-19 관련 시신경염
섹션 제목: “COVID-19 관련 시신경염”COVID-19 감염 후 탈수초성 시신경염이 발생한 사례가 보고되었습니다. Jossy 등(2022)은 감염 회복기에 시신경염이 발생한 사례를 보고했으며, 모든 환자가 스테로이드 펄스 요법으로 시력을 회복했습니다. 10)
COVID-19 백신 접종 후 시신경염 발생 보고가 축적되었으며, 접종 후 시신경염 발생까지의 중앙값은 18일입니다. 55예 중 14예에서 MOG-IgG 양성이었고, AQP4-IgG 양성 예는 없었습니다. 11) SARS-CoV-2 감염 후 MOG 항체 관련 시신경염이 발생한 사례도 보고되었습니다. 12)
CRION의 질환 개념 재정의
섹션 제목: “CRION의 질환 개념 재정의”MOG-IgG 및 AQP4-IgG 항체 검사의 보급에 따라, 기존에 CRION으로 진단되었던 사례 중 일부가 MOGAD나 NMOSD로 재분류되는 추세입니다. 향후 항체 프로파일에 기반한 질환 개념의 재정의가 진행될 것으로 생각됩니다.
8. 참고문헌
섹션 제목: “8. 참고문헌”- Jeyakumar N, Lerch M, Dale RC, Ramanathan S. MOG antibody-associated optic neuritis. Eye. 2024;38:2289-2301.
- Banwell B, Bennett JL, Marignier R, et al. Diagnosis of myelin oligodendrocyte glycoprotein antibody-associated disease: International MOGAD Panel proposed criteria. Lancet Neurol. 2023;22:268-82.
- Varley JA, Champsas D, Prossor T, et al. Validation of the 2023 International Diagnostic Criteria for MOGAD in a Selected Cohort of Adults and Children. Neurology. 2024.
- Cacciaguerra L, Flanagan EP. Updates in NMOSD and MOGAD Diagnosis and Treatment. Neurol Clin. 2024.
- Kidd D, Burton B, Plant GT, Graham EM. Chronic relapsing inflammatory optic neuropathy (CRION). Brain. 2003;126:276-84.
- Petzold A, Woodhall M, Khaleeli Z, et al. Aquaporin-4 and myelin oligodendrocyte glycoprotein antibodies in immune-mediated optic neuritis at long-term follow-up. J Neurol Neurosurg Psychiatry. 2019;90:1021-6.
- Lee H-J, Kim B, Waters P, et al. Chronic relapsing inflammatory optic neuropathy (CRION): a manifestation of myelin oligodendrocyte glycoprotein antibodies. J Neuroinflammation. 2018;15:302.
- Petzold A, Pittock S, Lennon V, et al. Neuromyelitis optica-IgG (aquaporin-4) autoantibodies in immune mediated optic neuritis. J Neurol Neurosurg Psychiatry. 2010;81:109-11.
- McElhinney K, Rhatigan M, Tsvetanova Z, et al. Beware the retrobulbar optic neuritis diagnosis. Case Rep Ophthalmol. 2022;13:453-458.
- Jossy A, Jacob N, Sarkar S, et al. COVID-19-associated optic neuritis - A case series and review of literature. Indian J Ophthalmol. 2022;70:310-6.
- Bhatti MT, Gilbert AL, Watson G, et al. Shot in the dark. Surv Ophthalmol. 2023;68:821-829.
- Bosello F, Marastoni D, Pizzini FB, et al. Atypical MOG antibody-associated optic neuritis and acute demyelinating polyneuropathy after SARS-CoV-2 infection. J Neuroimmunol. 2023;375:578011.
- Jarius S, Ruprecht K, Kleiter I, et al. MOG-IgG in NMO and related disorders: a multicenter study of 50 patients. Part 2: Epidemiology, clinical presentation, radiological and laboratory features, treatment responses, and long-term outcome. J Neuroinflammation. 2016;13:280.
- Ramanathan S, Mohammad S, Tantsis E, et al. Clinical course, therapeutic responses and outcomes in relapsing MOG antibody-associated demyelination. J Neurol Neurosurg Psychiatry. 2018;89:127-37.
- Chen JJ, Flanagan EP, Jitprapaikulsan J, et al. MOG antibody-positive optic neuritis: clinical characteristics, radiologic clues, and outcome. Am J Ophthalmol. 2018;195:8-15.
