혈액 검사

동맥염성 전방 허혈성 시신경병증 (AAION)
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 동맥염성 전방 허혈성 시신경병증(AAION)이란?
섹션 제목: “1. 동맥염성 전방 허혈성 시신경병증(AAION)이란?”동맥염성 전방 허혈성 시신경병증(AAION)은 영양 혈관의 혈관염으로 인한 시신경 허혈이 원인입니다. 혈관염에서는 혈관벽 비후로 인한 혈관 내강 협소화·혈전 형성으로 허혈성 괴사가 발생합니다. 시신경 유두에 영양을 공급하는 짧은 뒤섬모체동맥(SPCAs)의 혈관염이 그 본태로 간주됩니다. 전방 허혈성 시신경병증 전체의 5~10%를 차지하며, 대다수는 비동맥염성 전방 허혈성 시신경병증(NAION)입니다.
원발 질환으로 거대세포동맥염(GCA, 구 측두동맥염)이 가장 많으며, 그 외에도 대상포진·재발성 다발연골염·타카야수동맥염·류마티스 관절염·결절성 동맥주위염·SLE·알레르기성 육아종성 혈관염(Churg-Strauss 증후군) 등이 원발 질환이 됩니다.
거대세포동맥염(GCA)의 개요와 역사
섹션 제목: “거대세포동맥염(GCA)의 개요와 역사”GCA는 중~대형 혈관을 침범하는 전신성 육아종성 혈관염입니다. 10세기 바그다드의 Ali Ibn Isa al-Kahhal에 의한 기술이 가장 오래된 것으로 간주됩니다. 1890년 Hutchinson이 두부 통증을 동반한 붉은 줄을 기술했고, 1932년 Bayard Horton이 최초의 측두동맥 생검을 시행하여 육아종성 혈관염으로 기술했습니다. 1941년 Gilmour가 거대세포를 처음 기술하여 현재의 병명이 정착되었습니다.
50세 이상 여성에서 많고(남녀 비율 1:3), 70세 이상에서 급격히 발병률이 증가합니다. GCA 발병 중앙 연령은 75세입니다. AAION의 추정 연간 발병률은 50세 이상에서 10만 명당 0.36명입니다.
GCA의 시각 합병증은 1030%(최대 70% 보고도 있음)에서 발생하며, AAION은 GCA 관련 시력 상실의 6090%를 차지합니다 3). GCA 발병률은 연령과 함께 증가하여 60대에서 10만 명당 2.3명, 90대에서 44.7명에 이릅니다.
북유럽 백인에서 가장 흔하며(노르웨이에서는 10만 명당 약 30명), 흑인과 동양인에서는 드뭅니다. 일본에서의 발병률은 10만 명당 1.47명으로 서양에 비해 매우 드뭅니다. 유럽에서는 50세 이상 원발성 전신 혈관염 중 가장 흔하며, 매년 100만 명당 32~290명의 발병이 보고됩니다 6).
AAION은 전체 전방 허혈성 시신경병증의 5~10%를 차지하며, 거대 세포 동맥염 등의 혈관염이 원인입니다. 시력 예후는 NAION보다 현저히 나빠서 60% 이상이 시력 20/200 미만이 됩니다. NAION에서는 반대안 유두에 ‘disc at risk’(작은 유두, 작은 함몰)가 보이지만, AAION에서는 반대안 유두 직경과 생리적 함몰이 정상입니다. 감별에는 ESR, CRP 등의 염증 표지자가 유용하며, NAION에서는 이러한 수치가 상승하지 않습니다.
2. 주요 증상과 임상 소견
섹션 제목: “2. 주요 증상과 임상 소견”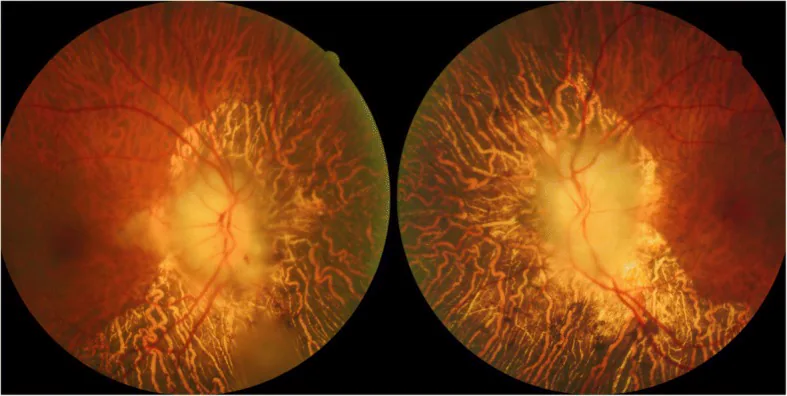
자각 증상
섹션 제목: “자각 증상”GCA에서는 고령자에서 급격한 한쪽 또는 양쪽 눈의 시력 저하로 발병합니다. 전구 증상으로 일과성 흑암시를 자각하는 경우가 많습니다. 치료하지 않으면 단기간 내에 높은 빈도로 반대안에도 발병합니다.
- 급격한 시력 저하: 60% 이상에서 시력 20/200 미만의 중증 장애를 초래합니다. 20% 이상에서 광각 없음이라는 중증 시기능 장애에 이릅니다.
- 일과성 흑암시: 영구적 시력 상실의 약 30%에서 전구 증상으로 나타나며, 평균 8.5일 전에 관찰됩니다. 발병률은 2~19%로 보고됩니다. NAION에서는 매우 드물며 중요한 감별점입니다.
- 두통: 가장 흔한 전신 증상이며, 65~90%에서 나타납니다. 새로 발생한 측두부 또는 후두부 두통이 특징적입니다 1).
- 턱 파행: 저작 시 턱의 통증이나 피로감. GCA에 가장 특이적인 증상입니다. 빈도는 11~45%입니다 1).
- 두피 압통: 측두동맥이나 두피 영역의 압통. 머리를 빗거나 베개에 머리를 댈 때 불편감이 발생합니다.
- 전신 증상: 발열, 체중 감소, 권태감, 식욕 부진, 근육통, 관절통 등.
- PMR(류마티스성 다발근육통) 증상: 최대 50%에서 동반됨. 양측성 목, 어깨, 골반의 통증과 뻣뻣함을 나타냄.
- 복시: 제3, 4, 6 뇌신경 마비로 인함. 10~15%에서 발생3).
- 안구 운동 제한: 뇌신경 마비로 인해 발생할 수 있음.
- 잠복성 GCA(occult GCA): AAION 환자의 최대 20%에서 명백한 전신 증상이 없음.
있다. 잠복성 거대세포동맥염(occult GCA)이라는 병태가 AAION 환자의 최대 20%에 존재하며, 두통, 턱 파행 등의 전형적인 전신 증상이 없다. 전신 증상이 없다고 해서 거대세포동맥염을 배제할 수 없으며, 혈액 검사(ESR, CRP) 및 측두동맥 생검을 통한 평가가 필수적이다.
임상 소견(의사가 진찰로 확인하는 소견)
섹션 제목: “임상 소견(의사가 진찰로 확인하는 소견)”- 창백 유두 부종(pallid swelling): AAION의 전형적 소견. 백악색 창백 부종(chalky-white pallor)으로 나타나며, NAION의 충혈성 부종과 대조적이다.
- 화염상 출혈: 유두 주위에서 관찰될 수 있음.
- 연성 백반(cotton wool spots): 후극부에서 관찰될 수 있음.
- 유두 주위 망막 세동맥 협소화.
- 모양체망막동맥 폐쇄: AAION에 비교적 특이적인 소견.
- 중심망막동맥 폐쇄(CRAO): 동반될 수도 있음.
- RAPD 양성: 단안성 또는 비대칭성 시신경병증에서 상대구심성동공운동장애(RAPD)가 양성으로 나타남.
- 시야 결손: 수평 반맹(altitudinal field defect)이 가장 흔합니다.
- 반대안 시신경 유두: 정상(NAION의 disc at risk와 차이점).
- 시신경 위축과 유두 함몰: 발병 후 6~8주에 시신경 위축이 진행되며 유두 함몰을 동반합니다. AAION의 90% 이상에서 관찰됩니다3).
- 측두동맥 이상: 팽창, 결절, 압통, 박동 감소 또는 소실.
- 호르너 증후군: 드물게 동반되며, 부분적 안검하수와 축동을 나타냅니다5).
- 형광 안저 조영술: 시신경 유두의 충만 지연, 유두 주변 맥락막의 충만 지연 및 결손(분절상 허혈)이 특징적입니다.
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”발병 기전 개요
섹션 제목: “발병 기전 개요”혈관염에서는 혈관벽 비후로 인한 혈관 내강 협소화 및 혈전 형성으로 허혈성 괴사가 발생합니다. 짧은 뒤섬모체동맥(SPCAs)의 혈관염이 앞시신경 허혈을 유발하며, 맥락막의 분절상 허혈도 동반됩니다.
눈에 대한 직접적인 기전은 다음과 같습니다.
- 짧은 뒤섬모체동맥의 염증 → 혈관벽 비후 → 내강 협소화 → 혈전 형성 → 시신경 유두 허혈.
- 안쪽 SPCA의 폐쇄가 가장 흔합니다(증례의 20%에서 특히 침범됨).
- SPCA는 앞사상판부와 사상판부에 영양을 공급하고, 유두 주변 맥락막 순환도 담당합니다.
GCA를 유발하는 혈관염의 메커니즘
섹션 제목: “GCA를 유발하는 혈관염의 메커니즘”혈관벽의 수지상 세포가 질병의 주요 기여 인자로 작용합니다. 외막의 영양혈관(vasa vasorum)을 통해 대식세포와 T세포가 침입하여 병원성 캐스케이드를 시작하고 중형~대형 동맥을 침범하는 육아종성 혈관염을 유발합니다.
주요 위험 요인
섹션 제목: “주요 위험 요인”- 노화: 가장 큰 위험 인자. 중앙값 75세. 50세 이하 발병은 극히 드뭅니다.
- 성별: 여성의 위험이 2~6배 높습니다.
- 인종: 북유럽 백인에서 가장 흔합니다. 흑인과 동양인에서는 드뭅니다.
- 유전적 요인: HLA-DRB1*04, DRW6, DR3가 감수성 증가와 관련됩니다. TNF-α 유전자좌 및 IL-10 프로모터의 다형성도 위험 증가와 상관관계가 있습니다. 비백인에서 가족성 GCA 보고도 있습니다7).
- 환경 및 감염 인자: 수두대상포진바이러스(VZV), 클라미디아 뉴모니에, 파르보바이러스 B19의 관여가 시사됩니다.
- 노화 관련 메커니즘: 내탄력판, 엘라스틴, 세포외기질의 석회화가 연령 특이적 발현을 설명할 수 있습니다.
- 흡연, 낮은 BMI, 조기 폐경: 모두 위험 인자로 보고되었습니다.
- PMR 동반: GCA와 PMR은 강한 연관성을 보입니다.
- COVID-19: 팬데믹 기간 동안 GCA 발병률이 70% 증가했다는 보고가 있습니다2). SARS-CoV-2가 혈관 내피에 대한 친화성을 가지며, 혈관염과의 유사성이 병태적 연관성으로 시사됩니다.
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”AAION의 진단은 거대세포동맥염 확진과 병행하여 진행합니다. AAION과 NAION의 감별이 치료 방침에 직접 연결되므로 신속하고 체계적인 평가가 중요합니다.
AAION과 NAION의 감별
섹션 제목: “AAION과 NAION의 감별”| 항목 | AAION | NAION |
|---|---|---|
| 연령 | 50세 이상 (대부분 75세 이상) | 40세 이상 |
| 시력 저하 정도 | 중증 (대부분 20/200 미만) | 비교적 경증 |
| 시신경 유두 소견 | 창백 부종 | 충혈 부종 (발적 및 부종) |
| 건안 유두 | 정상 (위험 유두 아님) | 위험 유두 (작은 유두, 작은 함몰) |
| 전신 증상 | 있음 (발열, 두통, 턱 파행) | 없음 |
| 염증 표지자 | ESR/CRP 상승 | 정상 |
| 일과성 흑암시 | 자주 선행 | 매우 드묾 |
| 맥락막 충만 지연 | 있음 (분절성) | 특징적이지 않음 |
| 치료 | 고용량 스테로이드 필수 | 확립된 치료 없음 |
측두동맥 생검 (TAB)
위치: 거대세포동맥염 확진의 금본위. 적절히 시행될 경우 민감도와 특이도 모두 95% 이상.
양성 소견: 내막 비후, 내탄력판 파열, 거대세포를 동반한 만성 염증성 침윤. 병리 확진에는 내탄력판 파괴와 염증 세포 침윤(급성기) 또는 섬유화(만성기)가 필요함. 거대세포는 확진에 필수적이지 않음.
위음성: 건너뛰기 병변(skip lesion)으로 인한 위음성률 3–5%. 최대 61%라는 보고도 있음 6). TAB 음성이어도 GCA를 배제할 수 없음.
시행 시기: 스테로이드 치료 시작 후에도 수일 내에 생검을 시행해야 함.
영상 진단
측두동맥 초음파 (CDUS): 비침습적이고 반복 가능한 검사. 민감도 77%, 특이도 96% 4). 특징적 소견으로는 후광 징후(혈관벽 비후로 인한 저에코 환), 압박 징후, 협착, 폐쇄가 있음. 건너뛰기 병변 때문에 양측 및 다영역의 포괄적 검사가 중요함 4). 양측에서 후광 징후가 양성인 경우 특이도가 100%로 상승함 4).
PET-CT: 대혈관형 GCA (LV-GCA)에서 대동맥 및 분지의 이상 섭취를 검출 가능. GAPS 연구에서 민감도 92%, 특이도 85% 6).
MRI: AAION과 NAION의 감별에 유용. 시신경초와 안와 지방의 조영 증강(중앙 밝은 점)을 확인함.
안과 검사
형광안저혈관조영술(FA) : 시신경유두의 충만 지연, 유두주위 맥락막의 충만 지연 또는 결손(분절성 허혈)은 AAION의 특징입니다. 유두부종이 나타나기 전에도 관찰될 수 있습니다. NAION과의 중요한 감별점입니다.
OCT/OCTA : 분절성 유두부종, 망막신경섬유층(RNFL) 두께 평가, 시신경유두의 허혈 상태 평가에 유용합니다.
ACR 분류 기준(1990년) 및 2022년 ACR/EULAR 분류 기준
섹션 제목: “ACR 분류 기준(1990년) 및 2022년 ACR/EULAR 분류 기준”1990년 ACR 분류 기준은 다음 5개 항목 중 3개 이상을 충족해야 합니다.
| 항목 | 기준 |
|---|---|
| 발병 연령 | 50세 이상 |
| 새로운 두통 | 새로 발생한 국소 두통 |
| 측두동맥 이상 | 압통 또는 맥박 감소 |
| 적혈구 침강 속도 | ≥50 mm/h |
| 동맥 생검 | 단핵세포 침윤 또는 육아종성 염증 |
2022년 ACR/EULAR 분류 기준은 CRP ≥10 mg/L를 추가하여 보다 포괄적인 진단을 가능하게 했습니다 4).
감별 진단
섹션 제목: “감별 진단”결절성 다발동맥염, 다발혈관염성 육아종증(베게너 육아종증), SLE 등 다른 혈관염과 감별해야 합니다. GCA는 폐와 신장을 침범하지 않는 것이 중요한 감별점입니다. 안매독이 GCA 유사 증상을 나타낼 수 있습니다 10). 전신 증상이 없는 잠재성 GCA(약 20%)에도 주의해야 합니다.
배제할 수 없습니다. 건너뛰기 병변(염증이 혈관의 일부에만 존재)으로 인한 위음성률은 3~5%(최대 61%라는 보고도 있음 6))입니다. TAB이 음성이더라도 ESR, CRP 상승을 동반한 임상적 GCA 의심이 있으면 치료를 지속해야 합니다. 임상 소견, 혈액 검사, 초음파 소견을 종합적으로 판단하는 것이 중요합니다.
5. 표준 치료법
섹션 제목: “5. 표준 치료법”시력 장애가 의심되면 생검에 의한 확진을 기다리지 않고 즉시 치료를 시작합니다. 치료의 주목적은 반대편 눈의 발병 예방이며, 환측 눈의 시력 개선은 거의 기대할 수 없습니다. 치료로 시력이 개선되는 경우는 15~20%에 불과합니다. 입원하여 스테로이드 대량 점적 정맥 주사 요법이 바람직합니다.
스테로이드 치료(급성기, 유지기, 감량)
섹션 제목: “스테로이드 치료(급성기, 유지기, 감량)”- 급성기: 즉시 메틸프레드니솔론 1g/일을 3~5일간 정맥 주사합니다.
- 유지기: 프레드니솔론 1mg/kg/일 경구 투여로 전환합니다.
- 감량: 전신 상태와 적혈구 침강 속도를 보면서 최소 4~6개월에 걸쳐 서서히 감량합니다. 경우에 따라 1년 이상이 필요할 수 있습니다.
- 주의: 스테로이드 격일 투여는 권장되지 않습니다.
눈 및 중추신경계 증상이 없는 경우 프레드니솔론 30~40mg/일부터 시작하기도 합니다.
감량 프로토콜(참고)
섹션 제목: “감량 프로토콜(참고)”| 투여량 | 기간 |
|---|---|
| 프레드니손 60 mg | 2주 |
| 프레드니손 50 mg | 2주 |
| 프레드니손 40 mg | 2주 |
| 프레드니손 30 mg | 1주 |
| 프레드니손 20 mg | 1주 |
| 프레드니손 10 mg | 1주 |
전신 상태, ESR, CRP를 지표로 하여 감량 속도를 개별적으로 조정합니다.
스테로이드 절약 약물 (토실리주맙, 메토트렉세이트)
섹션 제목: “스테로이드 절약 약물 (토실리주맙, 메토트렉세이트)”장기 스테로이드 투여에 따른 부작용(쿠싱양 증후군, 고혈당, 골다공증, 소화기 증상 등, 약 60%에서 발생)이 문제가 되는 경우 고려합니다.
- 토실리주맙(tocilizumab; IL-6 수용체 억제제): 2017년 GCA 치료제로 FDA 승인. 무작위 대조 시험(RCT)에서 글루코코르티코이드 절약 효과와 12개월에 걸친 관해 달성의 유효성이 입증됨4). 스테로이드 저항성 AAION에 효과적이라는 보고가 있음. COVID-19 백신 후 GCA 사례에서도 TCZ 162mg 피하 주사 사용이 보고됨8)9).
- 메토트렉세이트: 스테로이드 지속 중단 달성률을 높이고 재발 위험을 낮춤. 증례 보고에서는 15mg/주 병용이 사용됨1). 재발 시 스테로이드 증량 + MTX 병용이 권장되는 경우가 있음.
- 저용량 아스피린: 심장 질환 및 뇌혈관 허혈성 합병증 예방을 위해 병용을 고려할 수 있음.
환안의 시력 개선은 거의 기대할 수 없음. 시력이 개선되는 경우는 15~20% 정도이며, 많은 증례에서 시력 저하가 잔존함. 스테로이드 치료의 주목적은 반대쪽 눈의 발병을 예방하는 것임.
6. 병태생리학 및 상세 발병 기전
섹션 제목: “6. 병태생리학 및 상세 발병 기전”거대세포 동맥염의 병태는 두 가지 주요 면역 반응 기전으로 구성됨. 혈관벽의 수지상 세포가 활성화되는 것을 시작으로 하는 T 세포 매개 육아종성 혈관염이며, 중형~대형 동맥을 선택적으로 침범함.
면역 및 염증 캐스케이드 (2축 모델)
섹션 제목: “면역 및 염증 캐스케이드 (2축 모델)”전신 염증 반응
항원 특이적 반응
동맥벽 침투: 대식세포와 T세포가 외막의 영양혈관(vasa vasorum)을 이용하여 침투합니다.
면역 캐스케이드: 활성화된 T세포 → CD4+ T세포 동원 → Th1/Th17 분극 → IFN-γ/IL-17 생성 → 단핵구 동원 → 대식세포 분화 → 거대세포 형성.
혈관벽 파괴: 메탈로프로테아제와 활성산소 중간체에 의한 내탄력판 파괴가 발생합니다.
B세포 비관여: B세포의 관여는 확인되지 않았으며, 이는 ANCA 관련 혈관염과의 중요한 감별점입니다.
시신경으로의 혈액 공급과 허혈
섹션 제목: “시신경으로의 혈액 공급과 허혈”- 시신경으로의 혈액 공급은 주로 SPCA와 망막중심동맥의 가지에 의해 이루어집니다.
- SPCA는 전사상판부와 사상판부에 영양을 공급하고 유두주위 맥락막 순환도 담당합니다.
- GCA에서 SPCA(20%의 증례에서 특히 침범됨)의 혈전성 폐쇄가 시신경유두 허혈을 유발합니다.
- 급성 AAION 사후 조사에서는 사상판전부, 사상판, 사상판후부의 괴사를 동반한 시신경유두 부종과 만성 염증세포 침윤이 확인되었습니다.
- 형광안저혈관조영 데이터는 SPCA 관여의 조직병리학적 증거를 뒷받침합니다.
병리 소견
섹션 제목: “병리 소견”내탄력판의 파열이 특징적이며, 거대세포는 파열된 내탄력판 근처에 위치합니다. 급성기에는 림프구 침윤이 주를 이루고, 만성기에는 섬유화가 발생합니다. 염증에 대한 치유 반응으로 내막 비후, 근섬유아세포 증식, 세포외 기질 침착이 발생하여 혈관 협착 및 폐색을 초래합니다.
7. 최신 연구와 향후 전망 (연구 단계 보고)
섹션 제목: “7. 최신 연구와 향후 전망 (연구 단계 보고)”우파다시티닙 (JAK1 억제제)
섹션 제목: “우파다시티닙 (JAK1 억제제)”경구 JAK1 선택적 억제제인 우파다시티닙이 2025년에 GCA 치료제로 FDA 승인을 받았습니다. IL-6–JAK–STAT 경로를 표적으로 하는 새로운 치료 옵션으로 주목받고 있습니다.
토실리주맙의 RCT 증거
섹션 제목: “토실리주맙의 RCT 증거”토실리주맙은 RCT에서 글루코코르티코이드 절약 효과와 12개월에 걸친 관해 달성의 유효성이 입증되었으며4), 장기 글루코코르티코이드 사용에 따른 독성을 줄이는 대체 요법으로 자리잡고 있습니다.
Fast-track 경로 (초음파 신속 진단 경로)
섹션 제목: “Fast-track 경로 (초음파 신속 진단 경로)”초음파를 활용한 거대세포동맥염 신속 진단 경로가 유럽에서 보급되고 있습니다. fast-track 경로 도입으로 시력 상실 감소, 과잉 치료 억제, 비용 효율성 개선이 나타나는 것으로 보고되었습니다4). 초음파는 비침습적이고 반복 가능하며 여러 동맥 영역을 동시에 평가할 수 있어 조기 진단의 주요 도구로 자리매김하고 있습니다.
GCA-MDS 아형과 저메틸화 약물
섹션 제목: “GCA-MDS 아형과 저메틸화 약물”골수이형성증후군(MDS)을 배경으로 발생하는 GCA 아형(GCA-MDS)이 인식되고 있습니다. MDS 환자의 10~20%에서 자가면역 질환이 발생하는 것으로 알려져 있습니다. GCA-MDS는 전형적인 GCA보다 고전적 증상(두통, 턱 파행, AAION 등)의 유병률이 낮을 수 있으며, 스테로이드 의존성이 되기 쉽고 무스테로이드 생존율 및 무재발 생존율이 낮아지는 경향이 있습니다. 저메틸화 약물(아자시티딘/데시타빈) 추가가 유익할 수 있으며, 전향적 연구(NCT02985190)가 진행 중입니다. 가장 큰 규모의 보고는 2019년 프랑스 다기관 21례입니다.
COVID-19와 GCA의 연관성
섹션 제목: “COVID-19와 GCA의 연관성”COVID-19 팬데믹 기간 동안 GCA 발생률이 70% 증가했다는 보고가 있습니다2). 여러 보고에 따르면 2020년에 GCA 사례가 증가하고 안구 합병증 비율이 상승했으며, 내피 손상, Th1 면역, 단핵구-대식세포 계열의 관여가 추정됩니다2). SARS-CoV-2가 GCA를 유발했을 가능성을 시사하는 증례 보고도 존재합니다.
COVID-19 백신 접종 후 GCA 발병 사례가 여러 건 보고되었습니다. Yoshimoto 등(2023)은 14건의 사례를 검토하여 발병부터 진단까지의 기간이 2주에서 4개월(평균 약 6주)임을 보고했습니다8). 14건 중 2건에서 실명이 발생했습니다.
GCA와 Horner 증후군
섹션 제목: “GCA와 Horner 증후군”Sverdlichenko 등(2022)은 53명의 GCA 환자 중 2명에서 Horner 증후군(부분 안검하수와 축동)이 동반되었음을 보고했습니다5). 추정 기전은 척추동맥과 그 분지의 혈관염으로 인한 뇌간 내 첫 번째 교감신경세포의 허혈입니다. 50세 이상의 새로운 Horner 증후군에서는 GCA 증상 확인과 염증 표지자 검사를 권장합니다.
GCA의 드문 허혈성 합병증
섹션 제목: “GCA의 드문 허혈성 합병증”GCA는 시각 외에도 다양한 허혈성 합병증을 유발할 수 있습니다3).
- 뇌혈관 장애: 2~7%에서 발생.
- 혀 괴사 및 두피 괴사: 드물지만 심각한 합병증.
- 말초동맥 합병증.
- Charles Bonnet 증후군: 영구적 시력 상실 후 발생하는 만성 시각 환각. 시각 장애 환자의 0.4~30%에서 보고됨3).
가족성 GCA 보고
섹션 제목: “가족성 GCA 보고”Hayreh 등(2021)은 인도계 5형제 중 3명이 거대세포동맥염을 발병한 사례를 보고하며 상염색체 열성 유전 패턴을 시사했습니다7). 비백인에서 첫 가족성 GCA 보고로 주목받고 있습니다.
8. 참고문헌
섹션 제목: “8. 참고문헌”- Mandura RA. Giant cell arteritis presenting as unilateral arteritic anterior ischemic optic neuropathy. Cureus. 2021;13(7):e16653.
- Szydelko-Pako U, Przedziecka-Dolyk J, Krcicka J, et al. Arteritic anterior ischemic optic neuropathy in the course of giant cell arteritis after COVID-19. Am J Case Rep. 2022;23:e933471.
- Jalaledin DS, Ross C, Makhzoum JP. Rare ischemic complications of giant cell arteritis: case series and literature review. Am J Case Rep. 2022;23:e937565.
- Piccus R, Hansen MS, Hamann S, Mollan SP. An update on the clinical approach to giant cell arteritis. Clin Med (Lond). 2022;22(2):108-112.
- Sverdlichenko I, Lam C, Donaldson L, Margolin E. Horner Syndrome in Giant Cell Arteritis: Case Series and Review of the Literature. J Neuro-Ophthalmol. 2022;42(4):e573-e580.
- Stewart C, Asif RH, Dakkak T, et al. Diagnostic Dilemmas in Giant Cell Arteritis: Overcoming Anchoring Bias. Case Reports in Rheumatology. 2025.
- Hayreh SS. Familial giant cell arteritis. BMJ Case Rep. 2021;14(8):e244865.
- Yoshimoto K, Kaneda S, Asada M, et al. Giant Cell Arteritis after COVID-19 Vaccination with Long-Term Follow-Up. Medicina. 2023;59(5):932.
- Wakabayashi H, Iwayanagi M, Sakai D, et al. Development of giant cell arteritis after vaccination against SARS-CoV2. Medicine. 2023;102(21):e33814.
- Qadir A, Khakwani AS, Khan MR, et al. Ocular Syphilis Mimicking Giant Cell Arteritis. Cureus. 2022;14(9):e29286.
