โรคเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดหลอดเลือดแดงอักเสบ (AAION) เป็นภาวะฉุกเฉินทางจักษุวิทยา ที่เกิดจากหลอดเลือดแดงใหญ่เซลล์ยักษ์อักเสบ (GCA)เกิดในผู้สูงอายุอายุมากกว่า 50 ปี (โดยเฉพาะมากกว่า 75 ปี) ทำให้สูญเสียการมองเห็น อย่างรุนแรงเฉียบพลัน (มากกว่า 20% ไม่มีการรับรู้แสง)
หากไม่รักษา 65% จะเกิดที่ตาอีกข้างภายใน 10 วัน
การฟื้นคืนการมองเห็น ในตาที่เป็นนั้นแทบเป็นไปไม่ได้ แต่การรักษาด้วยสเตียรอยด์ มีประสิทธิภาพในการป้องกันการเกิดที่ตาอีกข้าง
การวินิจฉัยอาศัยการตรวจเลือด ESR และ CRP ร่วมกับการตัดชิ้นเนื้อหลอดเลือดแดงขมับ (TAB) การใช้ ESR+CRP ร่วมกันให้ความไว 99.2%
คิดเป็น 5-10% ของโรคเส้นประสาทตา ขาดเลือดส่วนหน้าทั้งหมด ส่วนที่เหลือคือ NAION การแยกโรคมีความสำคัญโดยตรงต่อแนวทางการรักษา
อุบัติการณ์ของหลอดเลือดแดงใหญ่เซลล์ยักษ์อักเสบในญี่ปุ่นพบน้อย (1.47 ต่อ 100,000 คน) แต่การพลาดการวินิจฉัยอาจเป็นอันตรายถึงชีวิต
โรคเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดหลอดเลือดแดงอักเสบ (Arteritic Anterior Ischemic Optic Neuropathy ; AAION) เป็นภาวะขาดเลือดของเส้นประสาทตา ที่เกิดจากหลอดเลือดที่เลี้ยงเกิดการอักเสบ การอักเสบของหลอดเลือดทำให้ผนังหลอดเลือดหนาตัว รูหลอดเลือดตีบ และเกิดลิ่มเลือด ส่งผลให้เนื้อเยื่อตายจากการขาดเลือด การอักเสบของหลอดเลือดปรับเลนส์สั้นด้านหลัง (SPCAs) ที่เลี้ยงหัวประสาทตาถือเป็นสาเหตุหลัก AAION คิดเป็น 5-10% ของโรคเส้นประสาทตา ขาดเลือดส่วนหน้าทั้งหมด ส่วนใหญ่เป็น NAION
โรคต้นเหตุที่พบบ่อยที่สุดคือหลอดเลือดแดงใหญ่เซลล์ยักษ์อักเสบ (Giant Cell Arteritis; GCA หรือเดิมเรียกว่าหลอดเลือดแดงขมับอักเสบ ) สาเหตุอื่นๆ ได้แก่ งูสวัด กระดูกอ่อนอักเสบเรื้อรัง หลอดเลือดแดงทาคายาสุอักเสบ โรคข้ออักเสบรูมาตอยด์ หลอดเลือดแดงอักเสบชนิดก้อนกลม โรคเอสแอลอี และหลอดเลือดอักเสบชนิดแกรนูโลมาภูมิแพ้ (กลุ่มอาการเชิร์ก-สเตราส์)
GCA เป็นหลอดเลือดอักเสบชนิดแกรนูโลมาทั่วร่างกายที่ส่งผลต่อหลอดเลือดขนาดกลางถึงใหญ่ คำอธิบายที่เก่าแก่ที่สุดเชื่อว่าเป็นของ Ali Ibn Isa al-Kahhal แห่งแบกแดดในศตวรรษที่ 10 ในปี 1890 ฮัทชินสันบรรยายถึงเส้นสีแดงเจ็บปวดบนศีรษะ และในปี 1932 เบยาร์ด ฮอร์ตันได้ตัดชิ้นเนื้อหลอดเลือดแดงขมับเป็นครั้งแรกและบรรยายว่าเป็นหลอดเลือดอักเสบชนิดแกรนูโลมา ในปี 1941 กิลมัวร์บรรยายถึงเซลล์ยักษ์เป็นครั้งแรก ทำให้ชื่อโรคปัจจุบันเป็นที่ยอมรับ
พบได้บ่อยในผู้หญิงอายุมากกว่า 50 ปี (อัตราส่วนชาย:หญิง 1:3) และอัตราการเกิดเพิ่มขึ้นอย่างรวดเร็วหลังจากอายุ 70 ปี อายุมัธยฐานของการเกิด GCA คือ 75 ปี อัตราการเกิด AAION โดยประมาณต่อปีในผู้ที่มีอายุมากกว่า 50 ปีคือ 0.36 ต่อ 100,000 คน
ภาวะแทรกซ้อนทางตาของ GCA เกิดขึ้นใน 10-30% (บางรายงานสูงถึง 70%) และ AAION คิดเป็น 60-90% ของการสูญเสียการมองเห็น ที่เกี่ยวข้องกับ GCA3) อัตราการเกิด GCA เพิ่มขึ้นตามอายุ โดยสูงถึง 2.3 รายต่อ 100,000 คนในช่วงอายุ 60 ปี และ 44.7 รายในช่วงอายุ 90 ปี
พบบ่อยที่สุดในชาวคอเคเชียนยุโรปเหนือ (ประมาณ 30 ต่อ 100,000 คนในนอร์เวย์) และพบได้ยากในคนผิวดำและชาวเอเชีย อัตราการเกิดในญี่ปุ่นคือ 1.47 ต่อ 100,000 คน ซึ่งพบได้น้อยมากเมื่อเทียบกับยุโรปและอเมริกา ในยุโรป เป็นโรคหลอดเลือดอักเสบทั่วร่างกายปฐมภูมิที่พบบ่อยที่สุดในผู้ที่มีอายุมากกว่า 50 ปี โดยมีรายงาน 32-290 รายต่อล้านคนต่อปี6)
Q
AAION กับภาวะเส้นประสาทตาขาดเลือดส่วนหน้าชนิดไม่มีการอักเสบของหลอดเลือดแดง (NAION) แตกต่างกันอย่างไร?
A
AAION คิดเป็น 5-10% ของภาวะเส้นประสาทตา ขาดเลือดส่วนหน้าทั้งหมด และเกิดจากหลอดเลือดอักเสบ เช่น หลอดเลือดแดงอักเสบชนิดเซลล์ยักษ์ การพยากรณ์โรคทางสายตาแย่กว่า NAION อย่างมีนัยสำคัญ โดยมากกว่า 60% มีค่าสายตาน้อยกว่า 20/200 ใน NAION จะพบ “จานประสาทตา เสี่ยง” (หัวประสาทตาเล็ก/รอยบุ๋มเล็ก) ที่จานประสาทตา ของตาอีกข้าง ในขณะที่ AAION เส้นผ่านศูนย์กลางจานประสาทตา และรอยบุ๋มทางสรีรวิทยาของตาอีกข้างเป็นปกติ ตัวบ่งชี้การอักเสบ เช่น ESR และ CRP มีประโยชน์ในการแยกโรค และใน NAION จะไม่พบการเพิ่มขึ้นของค่าเหล่านี้
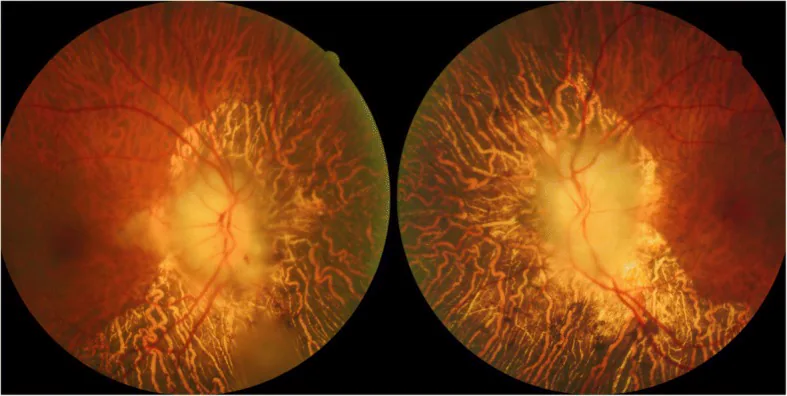
ภาพถ่ายจอประสาทตาของภาวะเส้นประสาทตาขาดเลือดส่วนหน้าชนิดมีการอักเสบของหลอดเลือดแดง พบหัวประสาทตาซีดและบวมในตาทั้งสองข้าง Tian G, et al. Giant cell arteritis presenting as bilateral anterior ischemic optic neuropathy: a biopsy-proven case report in Chinese patient. BMC Ophthalmol. 2018. Figure 1. PM
CI D: PMC6208180. License: CC BY.
ภาพถ่ายจอประสาทตา เมื่อมาพบครั้งแรก แสดงให้เห็นภาวะบวมของจานประสาทตา ทั้งสองข้างอย่างรุนแรงที่มีลักษณะซีดคล้ายชอล์ก มีเลือดออกเป็นเส้นและจุดขาวนิ่มในตาข้างขวา และการฝ่อของคอรอยด์ แบบกระจายรอบจานประสาทตา ซึ่งสอดคล้องกับ “อาการบวมซีดคล้ายชอล์ก” ที่กล่าวถึงในหัวข้อ “2. อาการหลักและผลการตรวจทางคลินิก”
ใน GCA การเริ่มต้นคือการมองเห็น ลดลงอย่างเฉียบพลันในตาข้างเดียวหรือทั้งสองข้างในผู้สูงอายุ มักมีอาการนำคือตามัวชั่วคราว หากไม่รักษา ตาอีกข้างมักจะเกิดตามมาด้วยความถี่สูงในระยะเวลาสั้น
การมองเห็น ลดลงอย่างเฉียบพลันตามัวชั่วคราว การมองเห็น ถาวร โดยเฉลี่ยก่อน 8.5 วัน อุบัติการณ์รายงานอยู่ที่ 2-19% พบได้น้อยมากใน NAION จึงเป็นจุดแยกโรคที่สำคัญปวดศีรษะ : อาการทั่วร่างกายที่พบบ่อยที่สุด เกิดขึ้นใน 65-90% มีลักษณะเฉพาะคือปวดศีรษะใหม่บริเวณขมับหรือท้ายทอย1) ขากรรไกรล้าเมื่อเคี้ยว (jaw claudication): ปวดหรือเมื่อยล้าที่ขากรรไกรขณะเคี้ยว อาการที่จำเพาะที่สุดต่อ GCA ความถี่ 11-45%1) กดเจ็บหนังศีรษะ : กดเจ็บบริเวณหลอดเลือดแดงขมับและหนังศีรษะ ทำให้รู้สึกไม่สบายเมื่อหวีผมหรือวางศีรษะบนหมอนอาการทั่วร่างกาย : มีไข้ น้ำหนักลด อ่อนเพลีย เบื่ออาหาร ปวดกล้ามเนื้อ ปวดข้อ ฯลฯอาการ PMR (Polymyalgia Rheumatica) : เกิดขึ้นในผู้ป่วยสูงถึง 50% มีอาการปวดและตึงสองข้างที่คอ ไหล่ และเชิงกรานภาพซ้อน (Diplopia)3) ข้อจำกัดในการเคลื่อนไหวลูกตา : อาจเกิดขึ้นเนื่องจากอัมพาตของเส้นประสาทสมองGCA แฝง (occult GCA) : ผู้ป่วย AAION สูงถึง 20% ไม่มีอาการทั่วร่างกายที่ชัดเจน
Q
เป็นไปได้หรือไม่ที่จะเป็น AAION โดยไม่มีอาการทั่วร่างกาย?
A
ได้ ภาวะที่เรียกว่า หลอดเลือดแดงอักเสบชนิดเซลล์ยักษ์แฝง (occult GCA) พบในผู้ป่วย AAION สูงถึง 20% โดยไม่มีอาการทั่วร่างกายทั่วไป เช่น ปวดศีรษะและขากรรไกรขัดขณะเคี้ยว การไม่มีอาการทั่วร่างกายไม่สามารถตัดหลอดเลือดแดงอักเสบชนิดเซลล์ยักษ์ออกได้ จำเป็นต้องประเมินด้วยการตรวจเลือด (ESR/CRP ) และการตัดชิ้นเนื้อหลอดเลือดแดงขมับ
ปุ่มประสาทตาบวม ซีด (pallid swelling)NAION เลือดออกเป็นรูปเปลวไฟ : อาจพบรอบขั้วประสาทตาจุดปุยฝ้าย (cotton wool spots) : อาจพบที่ขั้วหลังลูกตาหลอดเลือดแดงจอประสาทตา ส่วนรอบขั้วประสาทตาตีบแคบ การอุดตันของหลอดเลือดแดงซิลิโอเรตินัล : ลักษณะที่ค่อนข้างจำเพาะต่อ AAIONการอุดตันของหลอดเลือดแดงจอประสาทตา ส่วนกลาง (CRAO ) : อาจเกิดร่วมเป็นภาวะแทรกซ้อนRAPD บวกโรคเส้นประสาทตา ข้างเดียวหรือไม่สมมาตร การตรวจรูม่านตา ผิดปกติแบบสัมพัทธ์ (RAPD ) จะให้ผลบวกความบกพร่องของลานสายตา จานประสาทตา ของตาอีกข้างNAION )ฝ่อของเส้นประสาทตา และบุ๋มของจานประสาทตา เส้นประสาทตา ฝ่อดำเนินไปภายใน 6-8 สัปดาห์และมีบุ๋มของจานประสาทตา ร่วมด้วย พบในมากกว่า 90% ของผู้ป่วย AAION3) ความผิดปกติของหลอดเลือดแดงขมับ : โป่งพอง, เป็นก้อน, กดเจ็บ, ชีพจรลดลงหรือหายไปกลุ่มอาการฮอร์เนอร์ หนังตาตก บางส่วนและม่านตา หด5) การตรวจหลอดเลือดด้วยฟลูออเรสซีน : การเติมสีของจานประสาทตา ล่าช้า, การเติมสีของคอรอยด์ รอบจานประสาทตา ล่าช้าหรือขาด (ischemia แบบแบ่งส่วน) เป็นลักษณะเฉพาะ
ภาวะตามัวชั่วคราว (การสูญเสียการมองเห็น ชั่วคราว) อาจเป็นอาการนำของ AAION หากมีอาการทางสายตาชั่วคราวหรือปวดศีรษะ/ปวดกรามร่วมด้วย ควรรีบพบจักษุแพทย์หรืออายุรแพทย์ระบบประสาท หากไม่ได้รับการรักษา 65% ของผู้ป่วย AAION จะเกิดที่ตาอีกข้างภายใน 10 วัน1)
ในหลอดเลือดอักเสบ ผนังหลอดเลือดหนาตัวทำให้รูหลอดเลือดตีบแคบและเกิดลิ่มเลือด นำไปสู่เนื้อตายจากการขาดเลือด การอักเสบของหลอดเลือดแดงซิลิอารีส่วนหลังสั้น (SPCAs) ทำให้เกิดการขาดเลือดของเส้นประสาทตา ส่วนหน้า และยังมีการขาดเลือดแบบแบ่งส่วนของคอรอยด์ ร่วมด้วย
กลไกโดยตรงต่อตาดังนี้:
การอักเสบของหลอดเลือดแดงซิลิอารีส่วนหลังสั้น → ผนังหลอดเลือดหนาตัว → รูหลอดเลือดตีบแคบ → เกิดลิ่มเลือด → จานประสาทตา ขาดเลือด
การอุดตันของหลอดเลือดแดงซิลิอารีส่วนหลังสั้นด้านในพบได้บ่อยที่สุด (พบเฉพาะใน 20% ของผู้ป่วย)
SPCAs เลี้ยง lamina cribrosa ส่วนหน้าและ lamina cribrosa และยังมีส่วนร่วมในการไหลเวียนของคอรอยด์ รอบจานประสาทตา
เซลล์เดนไดรต์ในผนังหลอดเลือดทำหน้าที่เป็นปัจจัยหลักของโรค แมคโครฟาจและทีเซลล์บุกรุกผ่าน vasa vasorum ในชั้นแอดเวนทิเชีย เริ่มต้นกระบวนการก่อโรคที่นำไปสู่การอักเสบของหลอดเลือดแบบแกรนูโลมาซึ่งส่งผลต่อหลอดเลือดแดงขนาดกลางถึงใหญ่
อายุ : ปัจจัยเสี่ยงที่ใหญ่ที่สุด อายุมัธยฐาน 75 ปี พบน้อยมากก่อนอายุ 50 ปีเพศ : ความเสี่ยงสูงกว่า 2–6 เท่าในเพศหญิงเชื้อชาติ : พบบ่อยที่สุดในคนผิวขาวเชื้อสายยุโรปเหนือ พบน้อยในคนผิวดำและชาวเอเชียปัจจัยทางพันธุกรรม : HLA-DRB1*04, DRW6 และ DR3 สัมพันธ์กับความไวที่เพิ่มขึ้น ความหลากหลายทางพันธุกรรมที่ตำแหน่ง TNF -α และโปรโมเตอร์ IL-10 ก็สัมพันธ์กับความเสี่ยงที่เพิ่มขึ้นเช่นกัน มีรายงาน GCA ในครอบครัวในคนที่ไม่ใช่ผิวขาว 7) ปัจจัยสิ่งแวดล้อมและการติดเชื้อ : สงสัยว่ามีการเกี่ยวข้องของไวรัส varicella-zoster (VZV), Chlamydia pneumoniae และ parvovirus B19กลไกที่เกี่ยวข้องกับอายุ : การกลายเป็นปูนของแผ่นยืดหยุ่นชั้นใน อีลาสติน และเมทริกซ์นอกเซลล์อาจอธิบายการแสดงออกเฉพาะตามอายุการสูบบุหรี่ ค่าดัชนีมวลกายต่ำ วัยหมดประจำเดือนเร็ว : ทั้งหมดรายงานว่าเป็นปัจจัยเสี่ยงโรคร่วม PMR : GCA และ PMR มีความสัมพันธ์ที่แน่นแฟ้นCOVID-19 : มีรายงานว่าอุบัติการณ์ของ GCA เพิ่มขึ้น 70% ในช่วงการระบาดใหญ่ 2) SARS-CoV-2 มีความสัมพันธ์กับเยื่อบุผนังหลอดเลือด และความคล้ายคลึงกับหลอดเลือดอักเสบถูกเสนอว่าเป็นความสัมพันธ์ทางพยาธิวิทยา
การวินิจฉัย AAION ดำเนินการควบคู่ไปกับการยืนยันการวินิจฉัยหลอดเลือดแดงเซลล์ยักษ์ เนื่องจากการแยกความแตกต่างระหว่าง AAION และ NAION ส่งผลโดยตรงต่อแผนการรักษา การประเมินที่รวดเร็วและเป็นระบบจึงมีความสำคัญ
รายการ AAION NAION อายุ ≥50 ปี (ส่วนใหญ่ ≥75 ปี) ≥40 ปี ระดับการมองเห็น ลดลง รุนแรง (ส่วนใหญ่ <20/200) ค่อนข้างน้อย ลักษณะของจานประสาทตา บวมซีด บวมแดง (แดงและบวม) จานประสาทตา ข้างปกติปกติ (ไม่ใช่ disc at risk) Disc at risk (จานประสาทตา เล็ก, รอยบุ๋มเล็ก) อาการทั่วร่างกาย มี (ไข้ ปวดศีรษะ ปวดขากรรไกรเวลาเคี้ยว) ไม่มี เครื่องหมายการอักเสบ ESR/CRP สูงขึ้น ปกติ ตามัวชั่วคราว มักเกิดก่อน พบน้อยมาก การเติมเลือดคอรอยด์ ล่าช้า มี (เป็นปล้อง) ไม่จำเพาะ การรักษา จำเป็นต้องใช้สเตียรอยด์ ขนาดสูง ไม่มีการรักษาที่ชัดเจน
การตรวจเลือด
ESR : ความไว 86% อาจสูงถึง 70–120 มม./ชม. ค่าปกติ: ผู้ชาย = อายุ/2, ผู้หญิง = (อายุ+10)/2 อย่างไรก็ตาม สูงสุด 10% อาจมีค่าปกติ
CRP : ความไว 97.5% มีความจำเพาะมากกว่า ESR ในเกณฑ์การจำแนก ACR/EULAR ปี 2022 ได้เพิ่ม CRP ≥10 มก./ล. เป็นรายการเพิ่มเติม 4)
ESR+CRP ร่วมกัน : ความไว 99.2% ความจำเพาะ 97% โปรตีนระยะเฉียบพลันสูงขึ้นในมากกว่า 80% ของกรณี
อื่นๆ : ภาวะเกล็ดเลือดสูง – การรวมกันของ CRP และเกล็ดเลือดมีประโยชน์ในการวินิจฉัยมากที่สุด (p<0.001) 4)
การตัดชิ้นเนื้อหลอดเลือดแดงขมับ (TAB)
ตำแหน่ง : มาตรฐานทองคำสำหรับการวินิจฉัยที่แน่นอนของหลอดเลือดแดงเซลล์ยักษ์ หากทำอย่างเหมาะสม ความไวและความจำเพาะ >95%
ผลบวก : ผนังชั้นในหนา, การฉีกขาดของเยื่อยืดหยุ่นชั้นใน, การแทรกซึมของเซลล์อักเสบเรื้อรังร่วมกับเซลล์ยักษ์ การยืนยันทางพยาธิวิทยาต้องมีการทำลายเยื่อยืดหยุ่นชั้นในและการแทรกซึมของเซลล์อักเสบ (ระยะเฉียบพลัน) หรือพังผืด (ระยะเรื้อรัง) เซลล์ยักษ์ไม่จำเป็นสำหรับการวินิจฉัยที่แน่นอน
ผลลบเท็จ : อัตราผลลบเท็จเนื่องจากรอยโรคข้าม (skip lesion) 3–5% มีรายงานสูงถึง 61% 6) ไม่สามารถตัด GCA ออกได้แม้ TAB จะเป็นลบ
ระยะเวลาดำเนินการ : ควรตัดชิ้นเนื้อภายในไม่กี่วันแม้หลังจากเริ่มการรักษาด้วยสเตียรอยด์
การวินิจฉัยด้วยภาพ
อัลตราซาวนด์หลอดเลือดแดงขมับ (CDUS) : การตรวจที่ไม่รุกรานและทำซ้ำได้ ความไว 77% ความจำเพาะ 96% 4) สัญญาณรัศมี (วงแหวนสะท้อนต่ำเนื่องจากผนังหลอดเลือดหนา), สัญญาณกด, การตีบ และการอุดตันเป็นลักษณะเฉพาะ เนื่องจากรอยโรคข้าม การค้นหาทั้งสองข้างและหลายบริเวณอย่างครอบคลุมจึงสำคัญ 4) หากสัญญาณรัศมีเป็นบวกทั้งสองข้าง ความจำเพาะจะเพิ่มขึ้นเป็น 100% 4)
PET-CT : สามารถตรวจพบการสะสมที่ผิดปกติในเอออร์ตาและกิ่งก้านใน GCA ชนิดหลอดเลือดใหญ่ (LV-GCA) การศึกษา GAPS พบความไว 92% ความจำเพาะ 85% 6)
MRI : มีประโยชน์ในการแยก AAION และ NAION ตรวจสอบการเพิ่มความเข้มของปลอกประสาทตาและไขมันในเบ้าตา (จุดสว่างกลาง)
การตรวจตา
การตรวจหลอดเลือดด้วยฟลูออเรสซีน (FA ) : การเติมของจานประสาทตา ล่าช้า การเติมของคอรอยด์ รอบจานประสาทตา ล่าช้าหรือบกพร่อง (ischemia แบบแบ่งส่วน) เป็นลักษณะเฉพาะของ AAION อาจพบได้ก่อนที่จานประสาทตา จะบวม จุดสำคัญในการแยกจาก NAION
OCT /OCTA จานประสาทตา บวมแบบแบ่งส่วนและความหนาของชั้นใยประสาทจอตา (RNFL ) รวมถึงประเมินภาวะขาดเลือดของจานประสาทตา
ในเกณฑ์การจำแนก ACR ปี 1990 จำแนกโดยมี 3 ใน 5 ข้อต่อไปนี้:
ข้อ เกณฑ์ อายุที่เริ่มมีอาการ ≥50 ปี ปวดศีรษะใหม่ ปวดศีรษะเฉพาะที่ใหม่ ความผิดปกติของหลอดเลือดแดงขมับ กดเจ็บหรือชีพจรลดลง อัตราการตกตะกอนของเม็ดเลือดแดง ≥50 มม./ชม. การตัดชิ้นเนื้อหลอดเลือดแดง การแทรกซึมของเซลล์โมโนนิวเคลียร์หรือการอักเสบแบบแกรนูโลมา
เกณฑ์ ACR/EULAR ปี 2022 ได้เพิ่ม CRP ≥10 มก./ล. ทำให้สามารถวินิจฉัยได้ครอบคลุมมากขึ้น4)
โรคหลอดเลือดแดงอักเสบชนิดเซลล์ยักษ์ต้องแยกจากหลอดเลือดอักเสบชนิดอื่น เช่น โพลีอาร์เทอริติส โนโดซา, แกรนูโลมาโทซิสกับโพลีแองจิไอติส (เวเกเนอร์) และเอสแอลอี จุดสำคัญคือ GCA ไม่ส่งผลต่อปอดหรือไต ซิฟิลิสที่ตาอาจมีอาการคล้าย GCA10) ควรระวัง GCA แบบแฝง (ประมาณ 20%) ที่ไม่มีอาการทั่วร่างกาย
Q
สามารถตัดโรคหลอดเลือดแดงอักเสบชนิดเซลล์ยักษ์ออกได้หรือไม่แม้การตัดชิ้นเนื้อหลอดเลือดแดงขมับจะให้ผลลบ?
A
ไม่สามารถตัดออกได้ อัตราผลลบลวงเนื่องจากรอยโรคแบบข้าม (การอักเสบเฉพาะบางส่วนของหลอดเลือด) อยู่ที่ 3-5% (มีรายงานสูงถึง 61%6) ) แม้ TAB จะให้ผลลบ หากสงสัยทางคลินิกว่าเป็น GCA ร่วมกับ ESR และ CRP ที่สูงขึ้น ควรให้การรักษาต่อเนื่อง สิ่งสำคัญคือการประเมินผลทางคลินิก การตรวจเลือด และอัลตราซาวนด์อย่างครอบคลุม
เมื่อสงสัยว่ามีความบกพร่องทางการมองเห็น ควรเริ่มการรักษาทันทีโดยไม่รอการวินิจฉัยที่แน่ชัดจากการตัดชิ้นเนื้อ เป้าหมายหลักของการรักษาคือ การป้องกันการเกิดโรคในตาอีกข้าง เนื่องจากการมองเห็น ที่ดีขึ้นในตาที่เป็นนั้นแทบจะไม่เกิดขึ้น มีเพียง 15-20% ของผู้ป่วยที่การมองเห็น ดีขึ้นด้วยการรักษา ควรให้สเตียรอยด์ ขนาดสูงทางหลอดเลือดดำในโรงพยาบาล
ระยะเฉียบพลัน : ให้เมทิลเพรดนิโซโลน 1 กรัม/วัน ทางหลอดเลือดดำทันทีเป็นเวลา 3-5 วันระยะคงสภาพ : เปลี่ยนเป็นเพรดนิโซโลนชนิดรับประทาน 1 มก./กก./วันการลดขนาดยา : ค่อยๆ ลดขนาดยาอย่างน้อย 4-6 เดือน โดยพิจารณาจากสภาพทั่วไปและอัตราการตกตะกอนของเม็ดเลือดแดง บางรายอาจต้องใช้เวลามากกว่าหนึ่งปีข้อควรระวัง : ไม่แนะนำให้ให้สเตียรอยด์ วันเว้นวัน
หากไม่มีอาการทางตาหรือระบบประสาทส่วนกลาง อาจเริ่มด้วยเพรดนิโซโลน 30-40 มก./วัน
ขนาดยา ระยะเวลา เพรดนิโซน 60 มก. 2 สัปดาห์ เพรดนิโซน 50 มก. 2 สัปดาห์ เพรดนิโซน 40 มก. 2 สัปดาห์ เพรดนิโซน 30 มก. 1 สัปดาห์ เพรดนิโซน 20 มก. 1 สัปดาห์ เพรดนิโซน 10 มก. 1 สัปดาห์
ปรับอัตราการลดขนาดยารายบุคคลโดยใช้สภาพทั่วไป ESR และ CRP เป็นตัวชี้วัด
พิจารณาเมื่อผลข้างเคียงที่เกี่ยวข้องกับการใช้สเตียรอยด์ ระยะยาว (กลุ่มอาการคุชชิง, น้ำตาลในเลือดสูง, กระดูกพรุน, อาการทางเดินอาหาร ฯลฯ ซึ่งเกิดขึ้นประมาณ 60% ของกรณี) กลายเป็นปัญหา
โทซิลิซูแมบ 4) มีรายงานประสิทธิภาพใน AAION ที่ดื้อต่อสเตียรอยด์ นอกจากนี้ยังมีรายงานการใช้โทซิลิซูแมบ 162 มก. ฉีดใต้ผิวหนังในผู้ป่วย GCA หลังวัคซีน COVID-19 8) 9) เมโธเทรกเซท สเตียรอยด์ อย่างต่อเนื่องและลดความเสี่ยงของการกลับเป็นซ้ำ ในรายงานผู้ป่วย ใช้ขนาด 15 มก./สัปดาห์ร่วมกับสเตียรอยด์ 1) เมื่อกลับเป็นซ้ำ อาจแนะนำให้เพิ่มขนาดสเตียรอยด์ ร่วมกับเมโธเทรกเซท แอสไพรินขนาดต่ำ : อาจพิจารณาใช้เพื่อป้องกันภาวะแทรกซ้อนจากการขาดเลือดของหัวใจและสมอง
ใน AAION ที่ไม่ได้รับการรักษา 65% จะเกิดที่ตาอีกข้างภายใน 10 วัน 1) หากสงสัย ให้เริ่มการรักษาทันที
แม้จะได้รับการรักษา 1-4% ยังเกิดเหตุการณ์ขาดเลือดใหม่ 3)
การใช้สเตียรอยด์ ระยะยาวทำให้เกิดผลข้างเคียงรุนแรงในประมาณ 60% ของผู้ป่วย ควรประเมินระดับน้ำตาลในเลือดสูงและความดันโลหิตสูงภายใน 2 สัปดาห์แรกของการรักษา หากผลข้างเคียงเป็นปัญหา ให้พิจารณาเพิ่มการรักษาด้วยยากดภูมิคุ้มกัน
หากไม่รักษา 15-40% จะสูญเสียการมองเห็น ทั้งสองข้าง
Q
การรักษาด้วยสเตียรอยด์ช่วยให้การมองเห็นดีขึ้นหรือไม่?
A
การมองเห็น ที่ดีขึ้นในตาที่ได้รับผลกระทบแทบจะไม่เกิดขึ้น การมองเห็น ดีขึ้นเพียง 15-20% ของผู้ป่วย และในกรณีส่วนใหญ่ การมองเห็น ที่ลดลงยังคงอยู่ เป้าหมายหลักของการรักษาด้วยสเตียรอยด์ คือการป้องกันการเกิดที่ตาอีกข้าง
พยาธิสรีรวิทยาของหลอดเลือดแดงอักเสบชนิดเซลล์ยักษ์ประกอบด้วยกลไกการตอบสนองทางภูมิคุ้มกันหลักสองประการ เป็นหลอดเลือดอักเสบชนิดแกรนูโลมาที่อาศัยทีเซลล์เป็นสื่อกลาง ซึ่งเริ่มต้นจากการกระตุ้นเซลล์เดนไดรต์ในผนังหลอดเลือด และเลือกทำลายหลอดเลือดแดงขนาดกลางถึงใหญ่
การตอบสนองการอักเสบทั่วร่างกาย
การตอบสนองภูมิคุ้มกันโดยกำเนิดที่อาศัย IL-6 : แมคโครฟาจ นิวโทรฟิล และโมโนไซต์ที่ไหลเวียนผลิต IL-6
การกระตุ้นการตอบสนองระยะเฉียบพลันมากเกินไป : สัมพันธ์กับการเพิ่มขึ้นของ CRP , haptoglobin, fibrinogen และ complement
สาเหตุของอาการทั่วร่างกาย : ทำให้เกิดไข้ อ่อนเพลีย และน้ำหนักลด
การรักษาแบบมุ่งเป้า : แกน IL-6–Th17–IL-17/IL-21 สามารถถูกยับยั้งได้โดย glucocorticoid และ tocilizumab (ยาที่ยับยั้ง IL-6)
การตอบสนองจำเพาะต่อแอนติเจน
การบุกรุกผนังหลอดเลือดแดง : แมคโครฟาจและทีเซลล์บุกรุกโดยใช้ vasa vasorum ของชั้นแอดเวนทิเทีย
การทำงานต่อเนื่องของระบบภูมิคุ้มกัน : การกระตุ้นทีเซลล์ → การโพลาไรซ์ Th1/Th17 → การผลิต IFN-γ/IL-17 → การเรียกโมโนไซต์ → การเปลี่ยนแปลงเป็นแมคโครฟาจ → การเกิดเซลล์ยักษ์
การทำลายผนังหลอดเลือด : เกิดการทำลาย lamina elastica interna โดย metalloproteinase และ reactive oxygen species
การไม่มีส่วนร่วมของบีเซลล์ : ยังไม่ได้รับการยืนยันการมีส่วนร่วมของบีเซลล์ ซึ่งเป็นจุดแยกสำคัญจาก vasculitis ที่เกี่ยวข้องกับ ANCA
การส่งเลือดไปยังเส้นประสาทตา ส่วนใหญ่มาจากหลอดเลือดแดงซิลิอารีส่วนหลังสั้น (SPCAs) และแขนงของหลอดเลือดแดงจอประสาทตา ส่วนกลาง
SPCAs หล่อเลี้ยงส่วนก่อนแผ่นกรองและส่วนแผ่นกรอง และยังมีส่วนร่วมในการไหลเวียนของคอรอยด์ รอบหัวประสาทตา
ในภาวะหลอดเลือดแดงอักเสบจากเซลล์ยักษ์ (GCA) การอุดตันของ SPCAs (ซึ่งถูกกระทบเป็นพิเศษใน 20% ของผู้ป่วย) ทำให้เกิดภาวะขาดเลือดที่หัวประสาทตา
การตรวจหลังเสียชีวิตใน AAION เฉียบพลันยืนยันว่ามีอาการบวมของหัวประสาทตาร่วมกับเนื้อตายในส่วนก่อนแผ่นกรอง ส่วนแผ่นกรอง และส่วนหลังแผ่นกรอง รวมถึงการแทรกซึมของเซลล์อักเสบเรื้อรัง
ข้อมูลการถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน สนับสนุนหลักฐานทางจุลพยาธิวิทยาของการมีส่วนร่วมของ SPCAs
การฉีกขาดของเยื่อยืดหยุ่นชั้นในเป็นลักษณะเด่น และเซลล์ยักษ์จะอยู่ใกล้กับเยื่อยืดหยุ่นชั้นในที่ฉีกขาด ในระยะเฉียบพลัน การแทรกซึมของลิมโฟไซต์เป็นหลัก และในระยะเรื้อรังจะเกิดพังผืด เพื่อตอบสนองต่อการรักษาอาการอักเสบ จะเกิดการหนาตัวของชั้นอินติมา การเพิ่มจำนวนของไมโอไฟโบรบลาสต์ และการสะสมของสารเมทริกซ์นอกเซลล์ ซึ่งนำไปสู่การตีบและอุดตันของหลอดเลือด
เนื้อหาต่อไปนี้อยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิกในปัจจุบัน และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับการพัฒนาทางการแพทย์ในอนาคต
อูปาดาซิทินิบ ซึ่งเป็นยายับยั้ง JAK1 แบบเลือกสรรชนิดรับประทาน ได้รับการอนุมัติจาก FDA ในปี 2025 ให้เป็นยารักษา GCA ถือเป็นทางเลือกการรักษาใหม่ที่มุ่งเป้าไปที่วิถี IL-6–JAK–STAT
โทซิลิซูแมบ ได้รับการพิสูจน์ในการทดลองแบบสุ่มที่มีกลุ่มควบคุมว่ามีฤทธิ์ประหยัดกลูโคคอร์ติคอยด์และประสิทธิภาพในการบรรลุการทุเลาเป็นเวลา 12 เดือน 4) และกำลังถูกกำหนดให้เป็นทางเลือกในการรักษาเพื่อลดพิษที่เกี่ยวข้องกับการใช้กลูโคคอร์ติคอยด์ในระยะยาว
เส้นทางการวินิจฉัยเร็วสำหรับหลอดเลือดแดงอักเสบชนิดเซลล์ยักษ์โดยใช้อัลตราซาวนด์กำลังแพร่หลายในยุโรป การนำเส้นทางด่วนมาใช้แสดงให้เห็นว่าช่วยลดการสูญเสียการมองเห็น ลดการรักษาที่มากเกินไป และปรับปรุงความคุ้มค่า 4) อัลตราซาวนด์ไม่รุกราน ทำซ้ำได้ และสามารถประเมินบริเวณหลอดเลือดแดงหลายแห่งพร้อมกัน จึงเป็นเครื่องมือหลักในการวินิจฉัยตั้งแต่เนิ่นๆ
ชนิดย่อยของ GCA ที่เกิดขึ้นบนพื้นฐานของกลุ่มอาการไมอีโลดิสพลาสติก (GCA-MDS) ได้รับการยอมรับ คาดว่าผู้ป่วย MDS 10-20% จะเกิดโรคภูมิต้านตนเอง GCA-MDS อาจมีความชุกของอาการคลาสสิก (ปวดศีรษะ, ขากรรไกรขัดขณะเคี้ยว, AAION ฯลฯ) ต่ำกว่า GCA ทั่วไป และมีแนวโน้มที่จะพึ่งพาสเตียรอยด์ โดยมีอัตราการรอดชีวิตโดยไม่ใช้สเตียรอยด์ และไม่กลับเป็นซ้ำต่ำกว่า การเพิ่มยาลดเมทิลเลชัน (อะซาซิทิดีน/เดซิทาบีน) อาจมีประโยชน์ และกำลังมีการศึกษาระยะยาว (NCT 02985190) รายงานที่ใหญ่ที่สุดคือ 21 รายจากหลายศูนย์ในฝรั่งเศสปี 2019
มีรายงานว่าอุบัติการณ์ของ GCA เพิ่มขึ้น 70% ในระหว่างการระบาดของ COVID-19 2) รายงานหลายฉบับระบุว่ามีผู้ป่วย GCA เพิ่มขึ้นในปี 2020 โดยมีอัตราภาวะแทรกซ้อนทางตาเพิ่มขึ้น และสันนิษฐานว่ามีการเกี่ยวข้องของความเสียหายของเยื่อบุผนังหลอดเลือด ภูมิคุ้มกัน Th1 และระบบโมโนไซต์/มาโครฟาจ 2) นอกจากนี้ยังมีรายงานผู้ป่วยที่ชี้ว่า SARS-CoV-2 อาจเป็นตัวกระตุ้น GCA
มีรายงานผู้ป่วย GCA หลายรายหลังการฉีดวัคซีน COVID-19 Yoshimoto และคณะ (2023) ได้ทบทวนผู้ป่วย 14 ราย และรายงานว่าระยะเวลาตั้งแต่เริ่มมีอาการจนถึงการวินิจฉัยอยู่ระหว่าง 2 สัปดาห์ถึง 4 เดือน (เฉลี่ยประมาณ 6 สัปดาห์) 8) การสูญเสียการมองเห็น เกิดขึ้นใน 2 ใน 14 ราย
Sverdlichenko และคณะ (2022) รายงานกลุ่มอาการฮอร์เนอร์ (หนังตาตก บางส่วนและม่านตา หด) ในผู้ป่วย GCA 2 ใน 53 ราย 5) กลไกที่สันนิษฐานคือภาวะขาดเลือดของเซลล์ประสาทซิมพาเทติกลำดับที่หนึ่งในก้านสมองเนื่องจากหลอดเลือดแดง vertebral และกิ่งก้านอักเสบ ในผู้ป่วยอายุมากกว่า 50 ปีที่มีกลุ่มอาการฮอร์เนอร์ ใหม่ แนะนำให้ตรวจสอบอาการของ GCA และตรวจเครื่องหมายการอักเสบ
GCA สามารถทำให้เกิดภาวะแทรกซ้อนจากการขาดเลือดได้หลายอย่างนอกเหนือจากการมองเห็น 3)
โรคหลอดเลือดสมอง : เกิดขึ้นใน 2-7% ของผู้ป่วยเนื้อตายของลิ้นและหนังศีรษะ : ภาวะแทรกซ้อนที่พบได้น้อยแต่รุนแรงภาวะแทรกซ้อนของหลอดเลือดแดงส่วนปลาย กลุ่มอาการชาร์ลส์ บอนเนต์ : ภาพหลอนทางตาที่เรื้อรังเกิดขึ้นหลังสูญเสียการมองเห็น ถาวร พบรายงานในผู้ป่วยที่มีความบกพร่องทางการมองเห็น 0.4-30% 3)
Hayreh และคณะ (2021) รายงานผู้ป่วย 3 ใน 5 พี่น้องเชื้อสายอินเดียที่เป็นโรคหลอดเลือดแดงเซลล์ยักษ์ ซึ่งบ่งชี้รูปแบบการถ่ายทอดทางพันธุกรรมแบบ autosomal recessive 7) นี่เป็นรายงานแรกของ GCA ในครอบครัวในผู้ที่ไม่ใช่คนผิวขาว
Mandura RA. Giant cell arteritis presenting as unilateral arteritic anterior ischemic optic neuropathy. Cureus. 2021;13(7):e16653.
Szydelko-Pako U, Przedziecka-Dolyk J, Krcicka J, et al. Arteritic anterior ischemic optic neuropathy in the course of giant cell arteritis after COVID-19. Am J Case Rep. 2022;23:e933471.
Jalaledin DS, Ross C, Makhzoum JP. Rare ischemic complications of giant cell arteritis: case series and literature review. Am J Case Rep. 2022;23:e937565.
Piccus R, Hansen MS , Hamann S, Mollan SP. An update on the clinical approach to giant cell arteritis. Clin Med (Lond). 2022;22(2):108-112.
Sverdlichenko I, Lam C, Donaldson L, Margolin E. Horner Syndrome in Giant Cell Arteritis: Case Series and Review of the Literature. J Neuro-Ophthalmol. 2022;42(4):e573-e580.
Stewart C, Asif RH, Dakkak T, et al. Diagnostic Dilemmas in Giant Cell Arteritis: Overcoming Anchoring Bias. Case Reports in Rheumatology. 2025.
Hayreh SS. Familial giant cell arteritis. BMJ Case Rep. 2021;14(8):e244865.
Yoshimoto K, Kaneda S, Asada M, et al. Giant Cell Arteritis after COVID-19 Vaccination with Long-Term Follow-Up. Medicina. 2023;59(5):932.
Wakabayashi H, Iwayanagi M, Sakai D, et al. Development of giant cell arteritis after vaccination against SARS-CoV2. Medicine. 2023;102(21):e33814.
Qadir A, Khakwani AS, Khan MR, et al. Ocular Syphilis Mimicking Giant Cell Arteritis. Cureus. 2022;14(9):e29286.