前駆病変
日光角化症: 40代以降の色白の人に多い過角化病変。円形〜楕円形で紅斑性基部を伴う。有棘細胞原位癌とみなされる。
Bowen病(原位癌): 持続的な褐色〜赤色斑として現れる。乾癬や湿疹と誤診されやすい。HPV16型との関連が強い。
皮角: 丘疹〜結節状の基部に角質キャップを持つ。基部に有棘細胞原位癌や浸潤性有棘細胞癌を伴うことがあり常に切除が必要。
角化棘細胞腫: 中央に角質クレーターを持つカップ状結節。有棘細胞癌の亜型として分類されることもある。
眼瞼有棘細胞癌は、皮膚上皮の有棘層から発生する浸潤性悪性腫瘍である。眼瞼悪性腫瘍の中で基底細胞癌に次いで2番目に多く、眼瞼悪性新生物全体の5%未満を占める。
発生率は人口10万人あたり0.09〜2.42人と報告されており、米国・カナダでは年齢調整した有棘細胞癌発症率が過去数十年で50〜200%増加している。診断時の平均年齢は一般に60歳前後である。
地域差: 欧米では眼瞼悪性腫瘍の大部分を基底細胞癌(80〜95%)が占め、有棘細胞癌は5〜10%にとどまる。インド536例の研究では、有棘細胞癌は18%を占め脂腺癌(53%)・基底細胞癌(24%)に次ぐ3位であった1)。日本の1研究では有棘細胞癌が眼瞼悪性腫瘍の48%を占めるとの報告もあり、アジアでは欧米と比較して有棘細胞癌の比率が高い1)。
インドの536例を対象とした後方視的研究(Kaliki 2019)では、有棘細胞癌の診断時平均年齢は55歳(範囲8〜90歳)、男女比は1:1.1でわずかに女性優位であった1)。好発部位は上眼瞼40%・下眼瞼41%で大きな差はなかった1)。
転移率は1〜21%と報告に幅があり、基底細胞癌より侵襲的な生物学的挙動を示す。
人口10万人あたり0.09〜2.42人と推定される。欧米では眼瞼悪性腫瘍の5〜10%を占めるが、アジアでは比率が高く、日本では眼瞼悪性腫瘍の約半数を占めるとの報告もある。
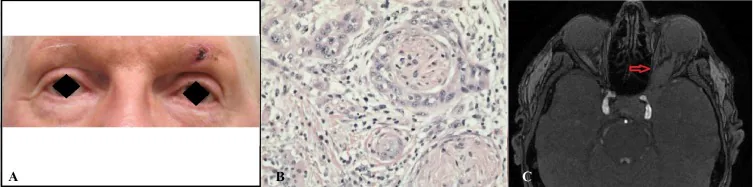
前駆病変と浸潤性有棘細胞癌で臨床像が大きく異なる。
前駆病変
日光角化症: 40代以降の色白の人に多い過角化病変。円形〜楕円形で紅斑性基部を伴う。有棘細胞原位癌とみなされる。
Bowen病(原位癌): 持続的な褐色〜赤色斑として現れる。乾癬や湿疹と誤診されやすい。HPV16型との関連が強い。
皮角: 丘疹〜結節状の基部に角質キャップを持つ。基部に有棘細胞原位癌や浸潤性有棘細胞癌を伴うことがあり常に切除が必要。
角化棘細胞腫: 中央に角質クレーターを持つカップ状結節。有棘細胞癌の亜型として分類されることもある。
浸潤性有棘細胞癌
瞼結膜面からの発症は非常にまれである。角化が強いと白色調、腫瘍血管を伴う場合は扁平な赤色調を呈する。
有棘細胞癌の発生は複数のリスク因子が重なることで促進される。
大きく高まる。皮膚の有棘細胞癌は固形臓器移植後に最も一般的な悪性腫瘍の一つであり、5年以内の発症率は肺移植で30%、心臓移植で最大26%に達する。移植後は定期的な皮膚・眼科的検査が重要である。
臨床診断と病理診断の一致率は有棘細胞癌で46%と低く(基底細胞癌の86%・脂腺癌の91%と比較)、生検による確定診断が不可欠である1)。診察では以下を評価する。
臨床的に基底細胞癌との区別が困難な場合、免疫組織化学染色が補助診断として有用である。
| マーカー | 有棘細胞癌 | 基底細胞癌 |
|---|---|---|
| Ber-EP4 | 陰性 | ほぼ常に陽性 |
| 上皮膜抗原(EMA) | 高陽性率 | 低陽性率 |
組織学的に腫瘍消失縁を確認した完全外科切除が最強のエビデンスを持つ標準治療である。有棘細胞癌は基底細胞癌と比較して境界が不明瞭な場合があり、臨床的な腫瘍縁の決定が困難なことがある。
Kaliki 2019では、広範切除生検が眼瞼悪性腫瘍全体の82%(有棘細胞癌では76%)に施行された1)。
液体窒素による組織破壊。日光角化症および有棘細胞原位癌にのみ適応される。浸潤癌には不適。表在性早期の有棘細胞原位癌の5年生存率は95%と報告されている。
手術リスクが高すぎる患者への単独療法、あるいは神経・リンパ節進展や境界不明瞭な癌に対する術後補助療法として使用される。週3〜5回、約1〜2ヶ月間の照射が行われる。
日光角化症および有棘細胞原位癌に適応される。外科的切除と比較して再発率が高い可能性がある。
遠隔転移を伴う進行の有棘細胞癌に適応される。
インド99例の有棘細胞癌患者における治療成績を以下に示す1)。
| 指標 | 割合 |
|---|---|
| 腫瘍再発 | 8% |
| 局所リンパ節転移 | 8% |
| 遠隔転移 | 4% |
| 疾患による死亡 | 4% |
| 眼球温存 | 79% |
5年Kaplan-Meier推定では、局所リンパ節転移22%・遠隔転移11%・転移関連死亡11%であった1)。
Kaliki 2019の研究では術後腫瘍再発が8%に認められた。5年Kaplan-Meier推定では局所リンパ節転移が22%に達することが示されており、手術後も定期的な経過観察が重要である。
紫外線はDNAを直接的(塩基転位)または間接的(活性酸素種を介した酸化的損傷)に損傷する2)。サンバーンによるアポトーシス誘導が防御機構として働くが、DNA修復が追いつかない場合に変異が蓄積する。
増殖・過角化 → 軽度〜中等度異形成 → 重度異形成・原位癌 → 浸潤性有棘細胞癌 → 転移性有棘細胞癌
マルジョリン潰瘍: 慢性難治性創傷や長期火傷跡の瘢痕組織からSCCが発生する病態。
ステージ0〜IB
ステージ0(Tis N0 M0): 原位癌。基底膜を越えない。
ステージIA(T1 N0 M0): 腫瘍径5mm以下、瞼板非浸潤。
ステージIB(T2a N0 M0): 腫瘍径5mm超〜10mm以下、または瞼板浸潤。
ステージIC〜IV
ステージIC(T2b N0 M0): 腫瘍径10mm超〜20mm以下、または眼瞼全層進展。
ステージII(T3a N0 M0): 腫瘍径20mm超、または眼近接部位進展。
ステージIIIB(any T N1 M0): 所属リンパ節転移あり。
ステージIV(any T any N M1): 遠隔転移。
Kaliki 2019の病期分布は T1: 26%、T2: 37%、T3: 7%、T4: 29%であった1)。組織学的グレードはG1(高分化)〜G4(未分化)で、グレードが低いほど予後良好とされる。
Yeら(NEJM 2025)は、ZAP70の生殖細胞系列変異によるT細胞受容体シグナル障害を持つ34歳女性において、β-HPV19のゲノム統合を伴う治療抵抗性の浸潤性皮膚の有棘細胞癌が発生した症例を報告した3)。この症例では典型的な有棘細胞癌ドライバー変異(TP53・NOTCH1/2・CDKN2A)は検出されず、紫外線変異シグネチャーも26%と低値(通常の皮膚の有棘細胞癌平均77%と比較)であった。同種造血幹細胞移植によりT細胞受容体シグナルを修復したところ、HPV特異的T細胞応答が回復し、35か月の追跡で皮膚の有棘細胞癌を含む全HPV関連疾患が安定消退した。
この報告は、適応免疫T細胞応答が有棘細胞癌の発症・進行の制御に関与することを示唆している3)。
セミプリマブ(抗PD-1抗体)は手術不能・転移性の皮膚有棘細胞癌に対してFDA承認されており、眼窩・リンパ節への進展例において今後の適応拡大が期待されている。免疫監視機構の関与が明らかになりつつあり、免疫抑制状態(臓器移植後・血液腫瘍など)での有棘細胞癌リスク増大もT細胞応答の制御異常と関連すると考えられている2)3)。
抗PD-1抗体セミプリマブが手術不能・転移性の皮膚有棘細胞癌に対してFDA承認されている。さらに、HPV駆動型有棘細胞癌では造血幹細胞移植による免疫再建で腫瘍が消退した症例報告がある。ただし後者は研究段階の知見であり、一般的な標準治療ではない。
早期発見・完全除去で予後は良好である。一方、基底細胞癌より侵襲的な生物学的挙動を示し、眼窩・リンパ節・遠隔臓器への転移リスクを持つ。悪性眼窩浸潤例は腫瘍内科・放射線腫瘍科等との多職種連携で管理する。
フォローアップの要点は以下の通りである。
5年Kaplan-Meier推定では局所リンパ節転移22%・遠隔転移11%・転移関連死亡11%が示されており1)、長期的なサーベイランスが求められる。