视网膜 分支动脉阻塞(BRAO )是由于视网膜 中央动脉的分支阻塞,导致其供血区域发生缺血性视网膜 损伤的疾病。动脉阻塞后约100分钟视网膜 开始发生不可逆变化,因此需要尽可能早期处理。
表现为无痛性急性单眼视野缺损 ,突然发病。鼻侧分支或颞侧周边阻塞可能无症状。
大多数病因是来自颈动脉或心脏的栓塞,常伴有高血压、动脉硬化、糖尿病等全身性疾病。
约25%的BRAO 患者在发病1周内合并脑梗死,需要紧急进行全身栓塞源检查和脑卒中评估。
急性期可进行亚硝酸异戊酯吸入、乙酰唑胺 静脉注射、尿激酶给药等治疗。
80%的BRAO 最终能维持0.5以上的视力 ,但如果黄斑部 受损,视力 预后不良。
视网膜动脉阻塞 是由于视网膜动脉阻塞 导致视网膜 缺血坏死,引起严重视功能障碍的疾病。根据阻塞部位分为以下三型:
视网膜中央动脉阻塞 (CRAO )视网膜中央动脉阻塞 。最严重类型,视力 预后差,常降至指数以下。视网膜 分支动脉阻塞(BRAO )视力 预后因阻塞部位而异。约占所有视网膜动脉阻塞 的38%5) 。睫状视网膜动脉阻塞 :睫状动脉阻塞。
BRAO 中,黄斑部 受损程度对视力 影响很大。如果黄斑 未受损,视力 不会下降,但阻塞区域对应的视野会缺损 。当阻塞发生在鼻侧动脉或颞侧周边时,常无自觉症状。另一方面,即使只有棉絮状白斑的细动脉阻塞,如果靠近黄斑 ,也会感觉到暗点。
BRAO 根据阻塞的持续性分为两个亚型。
永久性BRAO :闭塞持续存在,视网膜 缺血性改变固定化。一过性BRAO :闭塞自然解除,视网膜 表现消退。可能表现为一过性黑蒙 (amaurosis fugax)。
视网膜 动脉闭塞是一种紧急疾病,极早期的处理决定视力 预后。CRAO 的年发病率估计约为每10万人1例,或每1万门诊患者1例。CRAO 的平均发病年龄为60岁出头,男性多见,常单眼发病。1-2%可能双眼发病,双眼发病需怀疑巨细胞动脉炎 (GCA)5) 。日本的发病率略低于欧美。
无症状性视网膜 栓塞在49岁及以上一般人群中约占1.4%(Blue Mountains Eye Study)5) 。
在2013年AHA/ASA(美国心脏协会/美国卒中协会)修订的脑卒中定义中,视网膜 缺血被明确归类为CNS(中枢神经系统)梗死的一种类型5) 。约30%的CRAO 患者和约25%的BRAO 患者在发病1周内合并脑梗死。症状性RAO 患者的脑卒中风险在发病前2周至发病后1个月最高5) 。
Q
视网膜分支动脉闭塞与脑卒中有关吗?
A
BRAO 可能作为脑卒中的眼部表现出现,约25%的BRAO 患者在发病1周内合并脑梗死。AHA/ASA将视网膜 缺血纳入CNS梗死,发病后必须与神经科和心血管科协作进行全身评估。需要迅速进行颈动脉超声和超声心动图等栓塞源检查。
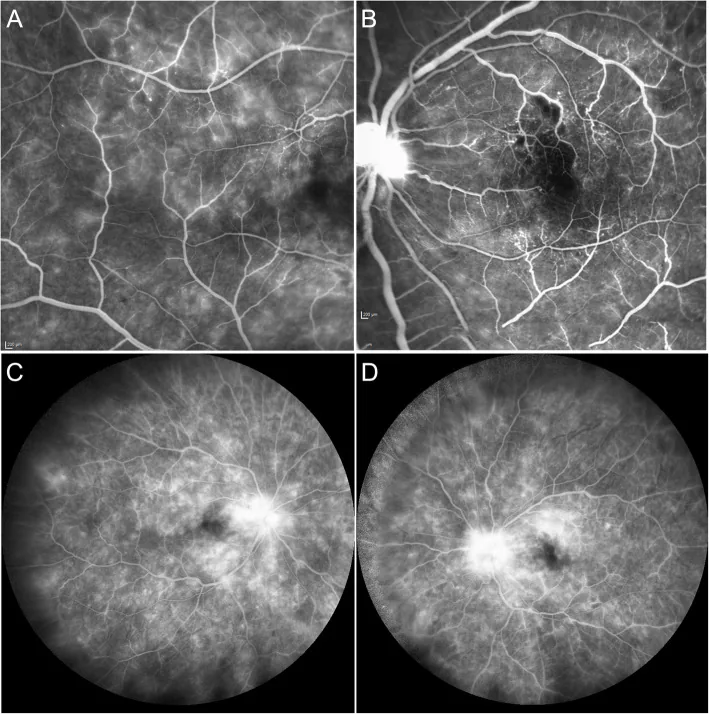
视网膜分支动脉闭塞的荧光眼底造影 González DP, et al. Occlusive retinal vasculopathy with macular branch retinal artery occlusion as a leading sign of atypical hemolytic uremic syndrome - a case report. BMC Ophthalmol. 2021. Figure 2. PM
CI D: PMC7847162. License: CC BY.
荧光眼底造影显示右眼黄斑 颞侧毛细血管渗漏和毛细血管扩张(a),左眼黄斑 上方视网膜 分支动脉闭塞导致的缺血性低荧光(b),以及晚期毛细血管渗漏和视盘染色(c-d)。这些对应于“2. 主要症状和临床所见”部分讨论的低荧光区域。
BRAO 典型表现为无痛性急性视野缺损 。
无痛性急性视野缺损 :突发无痛性视野缺损 是最特征性的表现。单眼视野缺损 :对应于闭塞分支支配区域的视野缺损 。视力 下降黄斑部 分支闭塞时尤为显著。鼻侧分支或颞侧周边分支闭塞时视力 可保持,许多病例无症状。自觉暗点 :即使仅有棉絮状白斑的小动脉闭塞,若靠近黄斑 ,患者也会感觉到暗点。前驱症状 :部分病例在反复出现一过性黑矇(amaurosis fugax)后发病。
例如,一名49岁女性在服用芬特明期间出现急性无痛性视野缺损 ,但矫正视力 保持在20/201) 。一名22岁男性在激光笔照射后出现幕状上方视野缺损 3) 。一名61岁男性在经皮冠状动脉成形术(PTCA)期间出现上方视野缺损 ,视力 降至6/362) 。
视网膜 白浊视网膜 混浊,由缺血性细胞肿胀引起。棉絮状白斑(cotton wool spot) :反映神经纤维层微梗死的白色病变。视网膜 栓子5) 。胆固醇栓子(Hollenhorst plaque)最常见5) 。混浊消退 :与CRAO 类似,视网膜 混浊在4-6周后消失,视网膜 厚度从增厚变为变薄。眼底镜下看似正常,但闭塞区域的视野缺损 仍然存在。这种“外观正常、功能残留”是向患者解释的重要要点。串珠状血流(beading)和节段状血流(fragmentation) :闭塞动脉中可见微小血柱缓慢流动的特征性表现。
OCT 所见(随时间变化)视网膜 内层(从神经纤维层到内颗粒层)增厚且呈高反射(由于细胞内水肿)。发病数天后视网膜 混浊减轻,但OCT 常显示内层高反射持续存在。数月后,闭塞区域的视网膜 内层变薄,但外层结构保留。慢性期OCT 可能显示内层甚至外层出现逆行性萎缩,层结构难以辨认。p-MLM(旁中心中层黄斑 病变)征反映双极细胞突触的快速肿胀2) 。OCTA 所见视网膜 毛细血管的灌注缺失。在永久性BRAO 中,据报道闭塞后9年表层视网膜 仍持续无灌注1) 。荧光素眼底血管造影 (FA )视网膜 循环时间通常约为12秒,但闭塞时常超过30秒3) 。还观察到血管壁不规则和荧光素 渗漏。视网膜电图 (ERG )脉络膜 营养存活,a波正常;但双极细胞和Müller细胞受损导致b波减弱或消失,呈负波型ERG 。a波正常提示光感受器存活,b波减弱提示内核层(双极细胞和Müller细胞)功能障碍,用于评估视网膜 缺血深度。
BRAO 的视力 预后如下表所示5) 。
分类 初诊时20/40或以上 随访时20/40或以上 永久性BRAO 74% 89% 一过性BRAO 94% 100%
Q
BRAO视力能恢复吗?
A
80%的BRAO 最终能维持矫正视力 0.5以上。永久性BRAO 在随访时89%保持20/40或以上5) 。一过性BRAO 则100%达到20/40或以上。但若黄斑部 分支闭塞,视力 预后可能不良。需向患者说明,混浊消退后视野缺损 仍常持续存在。
BRAO 的大多数原因是栓塞性的。好发于患有高血压、动脉硬化、糖尿病等全身性疾病的老年人。颈内动脉粥样硬化或心脏疾病形成的心腔内血栓成为栓子。血管炎、感染、外伤、血管痉挛等也可能成为原因。在年轻患者中,常可见血液凝固系统异常、心脏疾病、先天异常、视网膜血管炎 。
主要栓子的种类和来源如下所示。
栓子种类 主要来源 胆固醇/纤维蛋白 颈动脉、主动脉弓 钙化栓子 钙化心脏瓣膜 医源性栓子 PTCA、血管内治疗 美容填充剂 透明质酸注射(面部注射后)
已有报告因 PTCA 导致血栓栓塞症2) ,以及因神经血管内治疗导致斑块脱落4) 的病例。因美容目的的皮肤填充剂注射(如透明质酸)引起的视网膜 动脉闭塞正在增加,备受关注5) 。
血管痉挛 :偏头痛 、可卡因、西地那非使用等可引起血管痉挛,导致BRAO 。血管炎 :白塞病 、巨细胞动脉炎 (GCA)等。50岁以上患者应积极鉴别GCA 5) 。动脉炎性CRAO 约占CRAO 患者的4%,预后最差。怀疑GCA时,应检查头痛、头皮压痛、下颌跛行等症状,并迅速测量红细胞沉降率和CRP 。凝血异常 :抗磷脂抗体综合征、血栓形成倾向等。年轻患者尤其需要详细检查凝血系统。Susac综合征 :以脑病、感音神经性耳聋和BRAO 三联征为特征的自身免疫性疾病 5) 。药物性 :有报道与拟交感神经药芬特明(37.5 mg/日)相关 1) 。激光笔损伤 :全球首例因暴露于波长450–495 nm蓝色激光3秒导致BRAO 的病例被报道 3) 。
全身性风险因素包括以下内容:
高血压 :最重要的可改变风险因素 5) 血脂异常 :约60%的患者至少有一个未诊断的血管风险因素,其中血脂异常最常见低HDL胆固醇 :独立风险因素 5) 糖尿病 吸烟 心房颤动 5) 高BMI 阻塞性睡眠呼吸暂停综合征
Q
服药期间也会发生BRAO吗?
A
有报道称芬特明(食欲抑制剂)通过抑制去甲肾上腺素再摄取引起血管收缩和血管痉挛,诱发BRAO 1) 。可卡因、西地那非、填充剂注射等也可能成为原因5) 。务必告知眼科医生和内科医生您的既往病史和用药情况。
BRAO 的诊断以眼底所见为基础,结合多种影像检查和全身评估。该病紧急程度高,应尽量缩短诊断时间。
各项检查的主要发现如下所示。
检查方法 主要发现 OCT 急性期:内层高反射、增厚 → 慢性期:内层变薄(外层保留) FA 闭塞动脉充盈延迟,臂-视网膜 循环时间≥30秒(正常12秒) ERG a波正常(感光细胞 存活)·b波减弱(内层损伤)→负波型ERG OCTA 表层视网膜 毛细血管无灌注区 (无创)
眼底镜检查 :确认分支动脉分布区域的视网膜 混浊、闭塞动脉变细及白线化、棉絮状白斑、栓子可视化。血管内可能看不到血液。OCT 黄斑 病变(PAMM )5) 。数周内出现视网膜 和脉络膜 变薄。外层保留是感光细胞 存活的重要征象。OCTA 视网膜 毛细血管无灌注区 1, 4) 。慢性期灌注缺损 可能持续存在1) 。荧光素眼底血管造影 (FA )缺损 、血管壁不规则、荧光素 渗漏及视网膜 循环时间延长3) 。臂-视网膜 循环时间通常约为12秒,但常延长至30秒以上。视野检查 视野缺损 。视网膜电图 (ERG )ERG 模式评估内层视网膜 缺血。a波正常表明感光细胞 存活,b波减弱表明双极细胞和Müller细胞损伤。
急性症状性RAO 建议立即转诊至卒中中心5) 。CRAO 、BRAO 和一过性黑蒙 与脑梗死共享危险因素(动脉粥样硬化、颈动脉病变、心房颤动、瓣膜病等),遇到时应迅速评估脑梗死及其发病风险。
颈动脉超声 :评估狭窄和斑块。对于症状性颈动脉狭窄(50-99%),颈动脉内膜剥脱术优于内科治疗5) 。超声心动图和心电图 :寻找心脏栓塞来源,检测心房颤动。血液检查 :红细胞沉降率和C反应蛋白(排除巨细胞动脉炎 ),全血细胞计数和凝血功能(排除血液疾病)。50岁以上患者应积极鉴别GCA5) 。若高度怀疑GCA,应紧急考虑全身性类固醇 治疗5) 。MRI/CT :评估无症状性脑梗死。
另一方面,对于无症状的BRAO 或偶然发现的视网膜 栓塞,目前没有证据支持紧急卒中评估5) 。
动脉闭塞后约100分钟,视网膜 开始发生不可逆变化。CRAO 最好在发病后立即治疗,但发病后1天内的病例也应积极治疗。BRAO 在发病早期伴有视力 障碍时,采用与CRAO 相同的治疗。
血管扩张药
亚硝酸异戊酯 :将0.25 mL/瓶的安瓿压碎,吸附于覆盖物上,经鼻孔吸入(注意血压下降,医保外用药)。
硝酸异山梨酯舌下含服 :促进血管扩张。
卡波金吸入 :吸入95%氧气和5%二氧化碳的混合气体。
药物治疗
尿激酶 :初始每日剂量6万~24万单位,之后逐渐减量,约给药7天。注意脑出血和全身出血倾向。
Diamox注射液 :500 mg每日一次静脉注射(医保外用药)。通过降低眼压 促进视网膜 动脉扩张。
Ovalmon片 :5 μg×6片,分3次饭后服用(改善血流)。
全身评估与管理
寻找栓塞来源 :紧急进行颈动脉超声、超声心动图和凝血功能检查。
转诊至卒中中心 :急性症状性RAO 与卒中高度相关,建议立即转诊5) 。
抗血小板治疗 :如无禁忌,根据AHA卒中指南推荐。
急性期根据症状进行以下治疗。
眼球按摩/前房穿刺 :间歇性压迫眼球以降低眼压 ,促进栓子向周边移动。前房穿刺 (用27G针头抽取0.1-0.4 mL)也用于降低眼压 。但需注意,保守治疗(眼球按摩、前房穿刺 、卡波金)尚未被证明有显著效果5) 。星状神经节阻滞 :可能用于改善眼部血流。亚硝酸异戊酯吸入 :碾碎0.25 mL/瓶后吸入。通过血管扩张作用改善视网膜 血流(超说明书使用)。乙酰唑胺 (Diamox)静脉注射碳酸酐酶抑制剂 ,降低眼压 并促进视网膜 动脉扩张(超说明书使用)。尿激酶静脉注射 :初始日剂量6万-24万单位,之后逐渐减量,约持续7天。需注意脑出血和全身出血倾向。Opalmon片(利马前列素α-环糊精) :5 μg×6片,分3次饭后服用。前列腺素E₁衍生物,旨在改善末梢血流。
如果原因是血管痉挛,钙通道阻滞剂可能有效2) 。
t-PA制剂特异性吸附于血栓并发挥作用,因此在疗效和副作用方面均更优。目前,t-PA疗法被认为是急性CRAO 的最佳治疗方法之一。阿替普酶(Activacin®)已获批用于脑梗死和心肌梗死,但未获批用于CRAO 。多家机构在获得超说明书使用批准后进行了静脉注射治疗。
CRAO 的自然视力 恢复率为10-20%,但早期进行溶栓治疗可将其提高至约40%。荟萃分析表明,发病4.5小时内静脉注射tPA可能与改善预后相关5) 。
另一方面,EAGLE研究(RCT)显示,动脉内tPA与保守治疗相比,视力 改善无显著差异,并指出了颅内出血的安全性问题4) 。目前,对于BRAO /CRAO 的动脉内和静脉内溶栓治疗,证据尚不充分5) 。
高压氧治疗在一些小型回顾性研究中显示出轻微效果,但Cochrane综述认为证据不确定5) 。
新生血管 监测虹膜新生血管 和视网膜 新生血管 。CRAO 中高达20%的患者出现虹膜新生血管 ,通常在发病后30-60天出现5) 。注意新生血管性青光眼 的发生,全视网膜光凝 是适应症5) 。发病后约4个月内定期眼科检查很重要。全身管理 :控制全身动脉粥样硬化的危险因素(高血压、血脂异常、肥胖、阻塞性睡眠呼吸暂停综合征)很重要。建议饮食疗法、定期运动和戒烟。
80%的BRAO 患者最终维持矫正视力 0.5以上。永久性BRAO 中,89%在随访时保持20/40以上5) 。一过性BRAO 中,100%达到20/40以上。
CRAO 的视力 预后较差,仅约18%的CRAO 患者能自然恢复视 力。视网膜 混浊在4-6周后消失,但除非早期治疗有效,否则视功能无法恢复。在BRAO 中,即使闭塞血管再通,视野缺损 通常仍存在,但如果黄斑 未受累,视力 本身可保留。
动脉闭塞后约100分钟开始发生不可逆变化。需要尽可能早期处理。
亚硝酸异戊酯吸入有低血压风险,需在血压监测下使用。不在医保范围内。
尿激酶有脑出血和全身出血风险,需谨慎给药管理。
眼球按摩和前房穿刺 仅在发病超早期有意义,没有确凿证据表明其能改善预后优于自然病程5) 。
t-PA疗法目前尚未确立为BRAO 的标准治疗方法,且伴有ICH等严重并发症的风险。
新生血管 并发症好发于发病后30至60天,因此需要定期进行眼底和眼压 检查以持续随访。
Q
发病后应多快就医?
A
动脉闭塞后约100分钟,视网膜 的缺血性变化开始变得不可逆。发病1天内积极尝试治疗是一般标准,但治疗开始越早,预后越好。对于CRAO ,发病100分钟内治疗视力 改善率高。此外,由于BRAO 患者中风风险高达约25%,症状出现后应立即就诊眼科或急诊,并与神经科协作。
视网膜 动脉供应视网膜 内层2/3(从神经纤维层到内颗粒层)。视网膜 外层的感光细胞 接受脉络膜 血管的营养而存活。在BRAO 中,仅闭塞分支支配区域的内层视网膜 缺血,外层通过脉络膜 获得氧气和营养而得以保存。ERG 中a波保留(感光细胞 存活)而b波减弱(双极细胞和Müller细胞功能障碍)直接反映了这一解剖特性。
睫状视网膜 动脉是短后睫状动脉的分支,存在于约32%的眼睛中,供应视乳头黄斑 束附近的视网膜 。即使发生CRAO ,如果睫状视网膜 动脉得以保留,视乳头黄斑 束附近的视网膜 功能可能得以维持,中心视力 可能得以保留。
RAO 最常见的原因是血栓栓塞,通常发生在视网膜 中央动脉管腔最狭窄的部分,即穿过视神经 硬膜鞘的部位。栓子来源于颈动脉或心脏的斑块。
Hollenhorst斑块由胆固醇结晶组成,从颈动脉或主动脉弓的动脉粥样硬化斑块脱落,嵌顿于视网膜 动脉分叉处5) 。闭塞的动脉可能显著变细、白线化,血管内可能看不到血液。
动脉闭塞后约100分钟发生严重的视网膜 损伤。超急性期(~2小时)眼底可能看起来几乎正常,但OCT 显示内层高反射开始。急性期(2小时至数天)视网膜 混浊明显,动脉变细,OCT 内层增厚和高反射显著。亚急性期(1至6周)混浊消退,可能出现虹膜 或视网膜 新生血管 。慢性期(6周后)内层变薄,逆行性萎缩延伸至外层,视盘苍白。在慢性高血压状态下,不可逆变化发生的时间可能延长至240分钟,据某些报道4, 2) 。
芬特明 :抑制去甲肾上腺素再摄取,激活交感神经系统,引起血管收缩和血管痉挛1) 。激光笔 :热损伤、光化学损伤和光机械损伤导致血管壁损伤3) 。巨细胞动脉炎 (GCA)CRAO 约占CRAO 患者的4%,预后最差。
Sano等人(2025年)在德岛红十字医院对发病24小时内的CRAO 患者进行了PGE₁早期给药效果的回顾性研究6) 。PGE₁组(n=4)将阿普司他阿尔法地斯40 μg溶于250 mL生理盐水中,以125 mL/h的速度每日两次静脉注射(80 μg/天),持续5天,随后口服利马前列素阿尔法地斯10 μg每日三次(30 μg/天),持续至少1个月。与传统治疗组(n=6)相比,PGE₁组在1个月时的最佳矫正视力 (BCVA)显著更好。基线最大视网膜 厚度(MRT)与1个月BCVA呈负相关,提示其可能成为预后预测因子。两组均未观察到不良事件6) 。
PGE₁除了具有血管扩张作用外,还通过减轻氧化应激 和炎症发挥神经保护作用。尽管样本量较小且需要前瞻性随机对照试验,但在现有治疗缺乏确切疗效的情况下,这一发现值得关注。
自2013年AHA/ASA修订定义将视网膜 缺血认定为中枢神经系统梗死以来5) ,支持对急性RAO 应用卒中方案的趋势加速。正在推进立即转诊至卒中中心以及建立类似于脑梗死的全身管理系统。
荟萃分析报告称,发病4.5小时内静脉注射tPA可能与视力 恢复率提高相关,但EAGLE研究未显示动脉内tPA的疗效,并提出了安全性担忧4) ,而静脉注射tPA也缺乏足够的随机对照试验证据5) 。
OCTA 技术的进步使得发病后9年以上追踪表层视网膜 灌注缺损 成为可能1) 。目前正在研究急性期灌注缺损 模式是否可作为长期预后的预测因子。
眼眶 超声检测钙化栓子的“斑点征”据报道敏感性为83%,特异性为100%4) ,作为一种非侵入性急性期诊断辅助手段备受关注。
虽然一些小规模回顾性研究提示有效,但Cochrane综述得出结论,非动脉炎性CRAO 干预措施的整体证据不确定5) 。
PGE₁疗法
日本报告 :CRAO 患者使用PGE₁(前列地尔80 μg/天×5天)后1个月BCVA显著改善6) 。
预后预测 :基线MRT(最大视网膜 厚度)与1个月视力 呈负相关。无不良事件。
tPA的现状
EAGLE试验 :IA tPA与保守治疗相比无视力 改善效果,且存在ICH风险4) 。
IV tPA :荟萃分析提示发病4.5小时内可能提高视力 恢复率,但RCT证据不足5) 。
Liu J, Rosenfeld PJ, Dubovy SR. Branch retinal artery occlusion in a 49-year-old woman taking phentermine. Am J Ophthalmol Case Rep. 2024;35:102013.
Zokri MF, Othman O. A case series of retinal artery occlusion: when time is of the essence. Cureus. 2024;16(5):e60520.
Gebara A, Nguedia Vofo B, Jaouni T. Branch retinal artery occlusion from laser pointer misuse. Am J Ophthalmol Case Rep. 2024;36:102118.
Dalzotto K, Richards P, Boulter TD, Kay M, Mititelu M. Complications of intra-arterial tPA for iatrogenic branch retinal artery occlusion: a case report through multimodal imaging and literature review. Medicina. 2021;57(9):963.
American Academy of Ophthalmology Retina/Vitreous Panel. Retinal and Ophthalmic Artery Occlusions Preferred Practice Pattern. San Francisco, CA: American Academy of Ophthalmology; 2024.
Sano H, Yanai R, Kondo H, Mitamura Y. Early prostaglandin E₁ treatment improves visual outcomes in central retinal artery occlusion: a retrospective study. Front Med (Lausanne). 2025.
复制全文后,可以粘贴到你常用的 AI 助手中提问。
打开下面的 AI 助手,并把复制的内容粘贴到聊天框。