視網膜 分支動脈阻塞(BRAO )是視網膜 中央動脈的分支阻塞,導致其支配區域發生缺血性視網膜 病變的疾病。動脈阻塞後約100分鐘視網膜 開始發生不可逆變化,因此需要盡早處理。
表現為無痛性急性單眼視野缺損 ,突然發作。鼻側分支或顳側周邊阻塞可能無症狀。
大多數病因是來自頸動脈或心臟的栓塞,常伴有高血壓、動脈硬化、糖尿病等全身性疾病。
約25%的BRAO 患者在發病1週內合併腦梗塞,需要緊急進行全身栓塞源檢查和腦中風評估。
急性期可進行亞硝酸異戊酯吸入、乙醯唑胺 靜脈注射、尿激酶給藥等治療。
80%的BRAO 最終能維持0.5以上的視力 ,但如果黃斑部 受損,視力 預後不良。
視網膜動脈阻塞 是由於視網膜動脈阻塞 導致視網膜 缺血壞死,引起嚴重視功能障礙的疾病。根據阻塞部位分為以下三型:
視網膜中央動脈阻塞 (CRAO )視網膜中央動脈阻塞 。最嚴重類型,視力 預後差,常降至指數以下。視網膜 分支動脈阻塞(BRAO )視力 預後因阻塞部位而異。約佔所有視網膜動脈阻塞 的38%5) 。睫狀視網膜動脈阻塞 :睫狀動脈阻塞。
BRAO 中,黃斑部 受損程度對視力 影響很大。如果黃斑 未受損,視力 不會下降,但阻塞區域對應的視野會缺損 。當阻塞發生在鼻側動脈或顳側周邊時,常無自覺症狀。另一方面,即使只有棉絮狀白斑的細動脈阻塞,如果靠近黃斑 ,也會感覺到暗點。
BRAO 根據阻塞的持續性分為兩個亞型。
永久性BRAO :阻塞持續存在,視網膜 缺血性變化固定化。一過性BRAO :阻塞自然解除,視網膜 表現消退。可能表現為一過性黑矇 (amaurosis fugax)。
視網膜動脈阻塞 是一種緊急疾病,極早期的處理決定視力 預後。CRAO 的年發生率估計約為每10萬人1例,或每1萬門診患者1例。CRAO 的平均發病年齡為60歲出頭,男性多見,常單眼發病。1-2%可能雙眼發病,雙眼發病需懷疑巨細胞動脈炎 (GCA)5) 。日本的發生率略低於歐美。
無症狀性視網膜 栓塞在49歲及以上一般人群中約佔1.4%(Blue Mountains Eye Study)5) 。
在2013年AHA/ASA(美國心臟協會/美國中風協會)修訂的腦中風定義中,視網膜 缺血被明確歸類為CNS(中樞神經系統)梗塞的一種類型5) 。約30%的CRAO 患者和約25%的BRAO 患者在發病1週內合併腦梗塞。症狀性RAO 患者的腦中風風險在發病前2週至發病後1個月最高5) 。
Q
視網膜分支動脈阻塞與腦中風有關嗎?
A
BRAO 可能作為腦中風的眼部表現出現,約25%的BRAO 患者在發病1週內合併腦梗塞。AHA/ASA將視網膜 缺血納入CNS梗塞,發病後必須與神經科和心臟科協作進行全身評估。需要迅速進行頸動脈超音波和心臟超音波等栓塞源檢查。
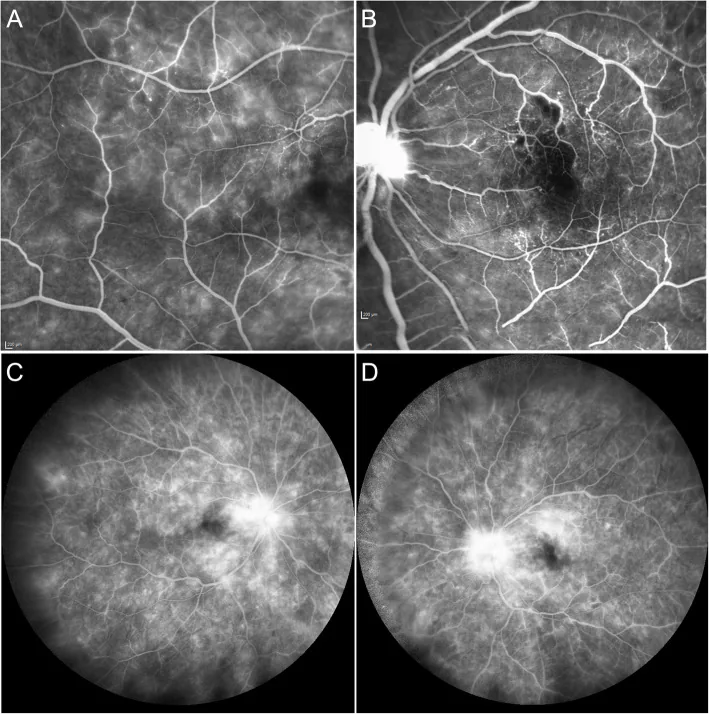
視網膜分支動脈阻塞的螢光眼底造影 González DP, et al. Occlusive retinal vasculopathy with macular branch retinal artery occlusion as a leading sign of atypical hemolytic uremic syndrome - a case report. BMC Ophthalmol. 2021. Figure 2. PM
CI D: PMC7847162. License: CC BY.
螢光眼底造影顯示右眼黃斑 顳側微血管滲漏和微血管擴張(a),左眼黃斑 上方視網膜 分支動脈阻塞導致的缺血性低螢光(b),以及晚期微血管滲漏和視神經 盤染色(c-d)。這些對應於「2. 主要症狀與臨床所見」部分討論的低螢光區域。
BRAO 典型表現為無痛性急性視野缺損 。
無痛性急性視野缺損 :突發無痛性視野缺損 是最特徵性的表現。單眼視野缺損 :對應於阻塞分支支配區域的視野缺損 。視力 下降黃斑部 分支阻塞時尤為顯著。鼻側分支或顳側周邊分支阻塞時視力 可保持,許多病例無症狀。自覺暗點 :即使僅有棉絮狀白斑的小動脈阻塞,若靠近黃斑 ,患者也會感覺到暗點。前驅症狀 :部分病例在反覆出現一過性黑矇 (amaurosis fugax)後發病。
例如,一名49歲女性在服用芬特明期間出現急性無痛性視野缺損 ,但矯正視力 保持在20/201) 。一名22歲男性在雷射筆照射後出現幕狀上方視野缺損 3) 。一名61歲男性在經皮冠狀動脈成形術(PTCA)期間出現上方視野缺損 ,視力 降至6/362) 。
視網膜 白濁視網膜 混濁,由缺血性細胞腫脹引起。棉絮狀白斑(cotton wool spot) :反映神經纖維層微梗塞的白色病變。視網膜 栓子5) 。膽固醇栓子(Hollenhorst plaque)最常見5) 。混濁消退 :與CRAO 類似,視網膜 混濁在4-6週後消失,視網膜 厚度從增厚變為變薄。眼底鏡下看似正常,但阻塞區域的視野缺損 仍然存在。這種「外觀正常、功能殘留」是向患者解釋的重要要點。串珠狀血流(beading)和節段狀血流(fragmentation) :阻塞動脈中可見微小血柱緩慢流動的特徵性表現。
OCT 所見(隨時間變化)視網膜 內層(從神經纖維層到內顆粒層)增厚且呈高反射(由於細胞內水腫)。發病數天後視網膜 混濁減輕,但OCT 常顯示內層高反射持續存在。數月後,阻塞區域的視網膜 內層變薄,但外層結構保留。慢性期OCT 可能顯示內層甚至外層出現逆行性萎縮,層結構難以辨認。p-MLM(旁中心中層黃斑 病變)徵反映雙極細胞突觸的快速腫脹2) 。OCTA 所見視網膜 毛細血管的灌注缺失。在永久性BRAO 中,據報導阻塞後9年表層視網膜 仍持續無灌注1) 。螢光眼底血管攝影 (FA )視網膜 循環時間通常約12秒,但阻塞時常超過30秒3) 。也可觀察到血管壁不規則和螢光素 滲漏。視網膜電圖 (ERG )感光細胞 依賴脈絡膜 營養存活,a波正常;但雙極細胞和Müller細胞受損導致b波減弱或消失,呈現負波型ERG 。a波正常表示感光細胞 存活,b波減弱表示內核層(雙極細胞和Müller細胞)功能障礙,用於評估視網膜 缺血深度。
BRAO 的視力 預後如下表所示5) 。
分類 初診時20/40或以上 追蹤時20/40或以上 永久性BRAO 74% 89% 暫時性BRAO 94% 100%
Q
BRAO視力會恢復嗎?
A
80%的BRAO 最終能維持矯正視力 0.5以上。永久性BRAO 在追蹤時89%保持20/40或以上5) 。暫時性BRAO 則100%達到20/40或以上。但若黃斑部 分支阻塞,視力 預後可能不良。需向患者說明,混濁消退後視野缺損 仍常持續存在。
BRAO 的大多數原因是栓塞性。好發於患有高血壓、動脈硬化、糖尿病等全身性疾病的老年人。頸內動脈粥樣硬化或心臟疾病形成的心腔內血栓成為栓子。血管炎、感染、外傷、血管痙攣等也可能成為原因。在年輕患者中,常可見血液凝固系統異常、心臟疾病、先天異常、視網膜血管炎 。
主要栓子的種類和來源如下所示。
栓子種類 主要來源 膽固醇/纖維蛋白 頸動脈、主動脈弓 鈣化栓子 鈣化心臟瓣膜 醫源性栓子 PTCA、血管內治療 美容填充劑 玻尿酸注射(臉部注射後)
已有報告因 PTCA 導致血栓栓塞症2) ,以及因神經血管內治療導致斑塊脫落4) 的病例。因美容目的的皮膚填充劑注射(如玻尿酸)引起的視網膜 動脈閉塞正在增加,備受關注5) 。
血管痙攣 :偏頭痛 、古柯鹼、西地那非使用等可引起血管痙攣,導致BRAO 。血管炎 :貝賽特氏症、巨細胞動脈炎 (GCA)等。50歲以上患者應積極鑑別GCA 5) 。動脈炎性CRAO 約佔CRAO 患者的4%,預後最差。懷疑GCA時,應檢查頭痛、頭皮壓痛、下頷跛行等症狀,並迅速測量紅血球沉降速率和CRP 。凝血異常 :抗磷脂抗體症候群、血栓形成傾向等。年輕患者尤其需要詳細檢查凝血系統。Susac症候群 :以腦病、感音神經性聽力損失 和BRAO 三聯徵為特徵的自體免疫疾病 5) 。藥物性 :有報導與擬交感神經藥芬特明(37.5 mg/日)相關 1) 。雷射筆傷害 :全球首例因暴露於波長450–495 nm藍色雷射3秒導致BRAO 的病例被報導 3) 。
全身性風險因素包括以下內容:
高血壓 :最重要的可改變風險因素 5) 血脂異常 :約60%的患者至少有一個未診斷的血管風險因素,其中血脂異常最常見低HDL膽固醇 :獨立風險因素 5) 糖尿病 吸菸 心房顫動 5) 高BMI 阻塞性睡眠呼吸中止症候群
Q
服藥期間也會發生BRAO嗎?
A
有報告指出芬特明(食慾抑制劑)透過抑制正腎上腺素再回收引起血管收縮和血管痙攣,誘發BRAO 1) 。古柯鹼、西地那非、填充劑注射等也可能成為原因5) 。務必告知眼科醫師和內科醫師您的既往病史和用藥情況。
BRAO 的診斷以眼底所見為基礎,結合多種影像檢查和全身評估。該疾病緊急程度高,應盡量縮短診斷時間。
各項檢查的主要發現如下所示。
檢查方法 主要發現 OCT 急性期:內層高反射、增厚 → 慢性期:內層變薄(外層保留) FA 閉塞動脈充盈延遲,臂-視網膜 循環時間≥30秒(正常12秒) ERG a波正常(感光細胞 存活)·b波減弱(內層損傷)→陰性型ERG OCTA 表層視網膜 毛細血管無灌流區域(非侵入性)
眼底鏡檢查 :確認分支動脈支配區域的視網膜 混濁、阻塞動脈變細及白線化、棉絮狀白斑、栓子可視化。血管內可能看不到血液。OCT 黃斑 病變(PAMM )5) 。數週內出現視網膜 和脈絡膜 變薄。外層保留是感光細胞 存活的重要徵象。OCTA 視網膜 毛細血管無灌流區域1, 4) 。慢性期灌流缺損 可能持續存在1) 。螢光眼底血管攝影 (FA )缺損 、血管壁不規則、螢光素 滲漏及視網膜 循環時間延長3) 。臂-視網膜 循環時間通常約12秒,但常延長至30秒以上。視野檢查 視野缺損 。視網膜電圖 (ERG )ERG 模式評估內層視網膜 缺血。a波正常表示感光細胞 存活,b波減弱表示雙極細胞和Müller細胞損傷。
急性症狀性RAO 建議立即轉診至腦中風中心5) 。CRAO 、BRAO 和一過性黑矇 與腦梗塞共享危險因子(動脈粥狀硬化、頸動脈病變、心房顫動、瓣膜病等),遇到時應迅速評估腦梗塞及其發病風險。
頸動脈超音波 :評估狹窄和斑塊。對於症狀性頸動脈狹窄(50-99%),頸動脈內膜剝除術優於內科治療5) 。心臟超音波和心電圖 :尋找心臟栓塞來源,檢測心房顫動。血液檢查 :紅血球沉降速率和C反應蛋白(排除巨細胞動脈炎 ),全血計數和凝血功能(排除血液疾病)。50歲以上患者應積極鑑別GCA5) 。若高度懷疑GCA,應緊急考慮全身性類固醇 治療5) 。MRI/CT :評估無症狀性腦梗塞。
另一方面,對於無症狀的BRAO 或偶然發現的視網膜 栓塞,目前沒有證據支持緊急腦中風評估5) 。
動脈阻塞後約100分鐘,視網膜 開始發生不可逆變化。CRAO 最好在發病後立即治療,但發病後1天內的病例也應積極治療。BRAO 在發病早期伴有視力 障礙時,採用與CRAO 相同的治療。
血管擴張藥
亞硝酸異戊酯 :將0.25 mL/瓶的安瓿壓碎,吸附於覆蓋物上,經鼻孔吸入(注意血壓下降,健保外用藥)。
硝酸異山梨酯舌下含服 :促進血管擴張。
卡波金吸入 :吸入95%氧氣和5%二氧化碳的混合氣體。
藥物治療
尿激酶 :初始每日劑量6萬~24萬單位,之後逐漸減量,約給藥7天。注意腦出血和全身出血傾向。
Diamox注射液 :500 mg每日一次靜脈注射(健保外用藥)。通過降低眼壓 促進視網膜 動脈擴張。
Ovalmon錠 :5 μg×6錠,分3次飯後服用(改善血流)。
全身評估與管理
尋找栓塞來源 :緊急進行頸動脈超音波、心臟超音波及凝血功能檢查。
轉診至中風中心 :急性症狀性RAO 與中風高度相關,建議立即轉診5) 。
抗血小板治療 :如無禁忌,根據AHA中風指南推薦。
急性期根據症狀進行以下治療。
眼球按摩/前房穿刺 :間歇性壓迫眼球以降低眼壓 ,促進栓子向周邊移動。前房穿刺 (用27G針頭抽取0.1-0.4 mL)也用於降低眼壓 。但需注意,保守治療(眼球按摩、前房穿刺 、卡波金)尚未被證明有顯著效果5) 。星狀神經節阻斷 :可能用於改善眼部血流。亞硝酸異戊酯吸入 :碾碎0.25 mL/瓶後吸入。通過血管擴張作用改善視網膜 血流(仿單外使用)。乙醯唑胺 (Diamox)靜脈注射碳酸酐酶抑制劑 ,降低眼壓 並促進視網膜 動脈擴張(仿單外使用)。尿激酶靜脈注射 :初始日劑量6萬-24萬單位,之後逐漸減量,約持續7天。需注意腦出血和全身出血傾向。Opalmon錠(利馬前列素α-環糊精) :5 μg×6錠,分3次飯後服用。前列腺素E₁衍生物,旨在改善末梢血流。
如果原因是血管痙攣,鈣離子通道阻斷劑可能有效2) 。
t-PA製劑特異性吸附於血栓並發揮作用,因此在療效和副作用方面均更優。目前,t-PA療法被認為是急性CRAO 的最佳治療方法之一。阿替普酶(Activacin®)已核准用於腦梗塞和心肌梗塞,但未核准用於CRAO 。多家機構在獲得仿單外使用批准後進行了靜脈注射治療。
CRAO 的自然視力 恢復率為10-20%,但早期進行血栓溶解治療可提升至約40%。統合分析顯示,發病4.5小時內靜脈注射tPA可能與改善預後相關5) 。
另一方面,EAGLE研究(RCT)顯示,動脈內tPA與保守治療相比,視力 改善無顯著差異,並指出顱內出血的安全顧慮4) 。目前,對於BRAO /CRAO 的動脈內及靜脈內溶栓治療,證據尚不充分5) 。
高壓氧治療 在一些小型回顧性研究中顯示輕微效果,但Cochrane回顧認為證據不確定5) 。
新生血管 監測虹膜新生血管 及視網膜 新生血管 。CRAO 中高達20%的患者出現虹膜新生血管 ,通常在發病後30-60天出現5) 。注意新生血管性青光眼 的發生,全視網膜 光凝是適應症5) 。發病後約4個月內定期眼科檢查很重要。全身管理 :控制全身動脈粥樣硬化的危險因子(高血壓、血脂異常、肥胖、阻塞性睡眠呼吸暫停症候群)很重要。建議飲食療法、定期運動及戒菸。
80%的BRAO 患者最終維持矯正視力 0.5以上。永久性BRAO 中,89%在追蹤時保持20/40以上5) 。一過性BRAO 中,100%達到20/40以上。
CRAO 的視力 預後較差,僅約18%的CRAO 患者能自然恢復視力 。視網膜 混濁在4-6週後消失,但除非早期治療有效,否則視功能無法恢復。在BRAO 中,即使阻塞血管再通,視野缺損 通常仍存在,但如果黃斑 未受影響,視力 本身可保留。
動脈阻塞後約100分鐘開始發生不可逆變化。需要盡可能早期處理。
亞硝酸異戊酯吸入有低血壓風險,需在血壓監測下使用。不在健保給付範圍。
尿激酶有腦出血及全身出血風險,需謹慎給藥管理。
眼球按摩及前房穿刺 僅在發病超早期有意義,沒有確鑿證據顯示其能改善預後優於自然病程5) 。
t-PA療法目前尚未確立為BRAO 的標準治療方法,且伴有ICH等嚴重併發症的風險。
新生血管 併發症好發於發病後30至60天,因此需要定期進行眼底和眼壓 檢查以持續追蹤。
Q
發病後應多快就醫?
A
動脈閉塞後約100分鐘,視網膜 的缺血性變化開始變得不可逆。發病1天內積極嘗試治療是一般標準,但治療開始越早,預後越好。對於CRAO ,發病100分鐘內治療視力 改善率高。此外,由於BRAO 患者中風風險高達約25%,症狀出現後應立即就診眼科或急診,並與神經科協作。
視網膜 動脈供應視網膜 內層2/3(從神經纖維層到內顆粒層)。視網膜 外層的感光細胞 接受脈絡膜 血管的營養而存活。在BRAO 中,僅閉塞分支支配區域的內層視網膜 缺血,外層通過脈絡膜 獲得氧氣和營養而得以保存。ERG 中a波保留(感光細胞 存活)而b波減弱(雙極細胞和Müller細胞功能障礙)直接反映了這一解剖特性。
睫狀視網膜 動脈是短後睫狀動脈的分支,存在於約32%的眼睛中,供應視乳頭黃斑 束附近的視網膜 。即使發生CRAO ,如果睫狀視網膜 動脈得以保留,視乳頭黃斑 束附近的視網膜 功能可能得以維持,中心視力 可能得以保留。
RAO 最常見的原因是血栓栓塞,通常發生在視網膜 中央動脈管腔最狹窄的部分,即穿過視神經 硬膜鞘的部位。栓子來源於頸動脈或心臟的斑塊。
Hollenhorst斑塊由膽固醇結晶組成,從頸動脈或主動脈弓的動脈粥樣硬化斑塊脫落,嵌頓於視網膜 動脈分叉處5) 。閉塞的動脈可能顯著變細、白線化,血管內可能看不到血液。
動脈閉塞後約100分鐘發生嚴重的視網膜 損傷。超急性期(~2小時)眼底可能看起來幾乎正常,但OCT 顯示內層高反射開始。急性期(2小時至數天)視網膜 混濁明顯,動脈變細,OCT 內層增厚和高反射顯著。亞急性期(1至6週)混濁消退,可能出現虹膜 或視網膜 新生血管 。慢性期(6週後)內層變薄,逆行性萎縮延伸至外層,視盤蒼白。在慢性高血壓狀態下,不可逆變化發生的時間可能延長至240分鐘,據某些報導4, 2) 。
芬特明 :抑制正腎上腺素再回收,活化交感神經系統,引起血管收縮和血管痙攣1) 。雷射筆 :熱損傷、光化學損傷和光機械損傷導致血管壁損傷3) 。巨細胞動脈炎 (GCA)CRAO 約佔CRAO 患者的4%,預後最差。
Sano等人(2025年)在德島紅十字醫院對發病24小時內的CRAO 患者進行了PGE₁早期給藥效果的回顧性研究6) 。PGE₁組(n=4)將阿普司他阿爾法地斯40 μg溶於250 mL生理鹽水中,以125 mL/h的速度每日兩次靜脈注射(80 μg/天),持續5天,隨後口服利馬前列素阿爾法地斯10 μg每日三次(30 μg/天),持續至少1個月。與傳統治療組(n=6)相比,PGE₁組在1個月時的最佳矯正視力 (BCVA)顯著較好。基線最大視網膜 厚度(MRT)與1個月BCVA呈負相關,提示其可能成為預後預測因子。兩組均未觀察到不良事件6) 。
PGE₁除了具有血管擴張作用外,還通過減輕氧化壓力和炎症發揮神經保護作用。儘管樣本量較小且需要前瞻性隨機對照試驗,但在現有治療缺乏確切療效的情況下,這一發現值得關注。
自2013年AHA/ASA修訂定義將視網膜 缺血認定為中樞神經系統梗塞以來5) ,支持對急性RAO 應用腦中風方案的趨勢加速。正在推動立即轉診至腦中風中心以及建立類似於腦梗塞的全身管理系統。
統合分析報告稱,發病4.5小時內靜脈注射tPA可能與視力 恢復率提高相關,但EAGLE研究未顯示動脈內tPA的療效,並提出了安全性擔憂4) ,而靜脈注射tPA也缺乏足夠的隨機對照試驗證據5) 。
OCTA 技術的進步使得發病後9年以上追蹤表層視網膜 灌流缺損 成為可能1) 。目前正在研究急性期灌流缺損 模式是否可作為長期預後的預測因子。
眼眶 超音波檢測鈣化栓子的「斑點徵」據報導敏感性為83%,特異性為100%4) ,作為非侵入性急性期診斷輔助備受關注。
雖然一些小規模回顧性研究顯示有效,但Cochrane回顧結論指出,非動脈炎性CRAO 的介入措施整體證據不確定5) 。
PGE₁療法
日本報告 :CRAO 患者使用PGE₁(前列地爾80 μg/天×5天)後1個月BCVA顯著改善6) 。
預後預測 :基線MRT(最大視網膜 厚度)與1個月視力 呈負相關。無不良事件。
tPA的現狀
EAGLE試驗 :IA tPA與保守治療相比無視力 改善效果,且存在ICH風險4) 。
IV tPA :統合分析提示發病4.5小時內可能提高視力 恢復率,但RCT證據不足5) 。
Liu J, Rosenfeld PJ, Dubovy SR. Branch retinal artery occlusion in a 49-year-old woman taking phentermine. Am J Ophthalmol Case Rep. 2024;35:102013.
Zokri MF, Othman O. A case series of retinal artery occlusion: when time is of the essence. Cureus. 2024;16(5):e60520.
Gebara A, Nguedia Vofo B, Jaouni T. Branch retinal artery occlusion from laser pointer misuse. Am J Ophthalmol Case Rep. 2024;36:102118.
Dalzotto K, Richards P, Boulter TD, Kay M, Mititelu M. Complications of intra-arterial tPA for iatrogenic branch retinal artery occlusion: a case report through multimodal imaging and literature review. Medicina. 2021;57(9):963.
American Academy of Ophthalmology Retina/Vitreous Panel. Retinal and Ophthalmic Artery Occlusions Preferred Practice Pattern. San Francisco, CA: American Academy of Ophthalmology; 2024.
Sano H, Yanai R, Kondo H, Mitamura Y. Early prostaglandin E₁ treatment improves visual outcomes in central retinal artery occlusion: a retrospective study. Front Med (Lausanne). 2025.