المرحلة 0-1
المرحلة 0 (طبيعي): حدود غير واضحة في الجانب الأنفي والعلوي والسفلي. طبقة ألياف عصبية نصف قطرية.
المرحلة 1 (مبكرة جدًا): عدم وضوح الحدود الأنفية للحليمة. لا ارتفاع في الحدود. هالة رمادية خفيفة. طيات مشيمية دائرية ونصف قطرية.

الوذمة الحليمية هي تورم القرص البصري الثنائي الناتج عن ارتفاع الضغط داخل الجمجمة (ICP). يُستخدم مصطلح “papilledema” فقط لارتفاع ICP، ويميز عن “وذمة القرص البصري” الناتجة عن أسباب أخرى. يؤدي ارتفاع الضغط في الحيز تحت العنكبوتي المحيط بالعصب البصري إلى انضغاط العصب وركود التدفق المحوري، مما يسبب تورم القرص.
معدل الإصابة السنوي لـ IIH هو 1.15/100,000 (بيانات الولايات المتحدة 1997-2016، النساء 1.97 مقابل الرجال 0.36) 2)، وهو الأعلى بين 18-44 سنة (2.47/100,000). انتشاره بين النساء 18-55 سنة في الولايات المتحدة هو 3.44/10,000 (95% CI 2.61-5.39) 3). حسب العرق: السود 2.05 > البيض 1.04 > الهسبان 0.67 > سكان جزر آسيا والمحيط الهادئ 0.16 (لكل 100,000) 2)، ويتوافق جغرافيًا مع انتشار السمنة (Moran I=0.20, P=0.03) 3).
الضغط الطبيعي داخل الجمجمة للبالغين <250 mmH2O، وللأطفال <280 mmH2O. IIH الخاطف (FIH) يحدث في 2-3% من جميع مرضى IIH، ويتميز بفقدان بصري سريع خلال 4 أسابيع من ظهور الأعراض، وهو حالة طارئة. 1)
وذمة حليمة العصب البصري (papilledema) هو مصطلح يقتصر على ارتفاع الضغط داخل الجمجمة (ICP)، بينما يُسمى التورم الناتج عن أسباب أخرى (مثل التهاب العصب البصري، نقص التروية، الآفات الارتشاحية) بوذمة القرص البصري (optic disc edema). هذا التمييز مهم لأنه يساعد في تحديد السبب واختيار العلاج المناسب.
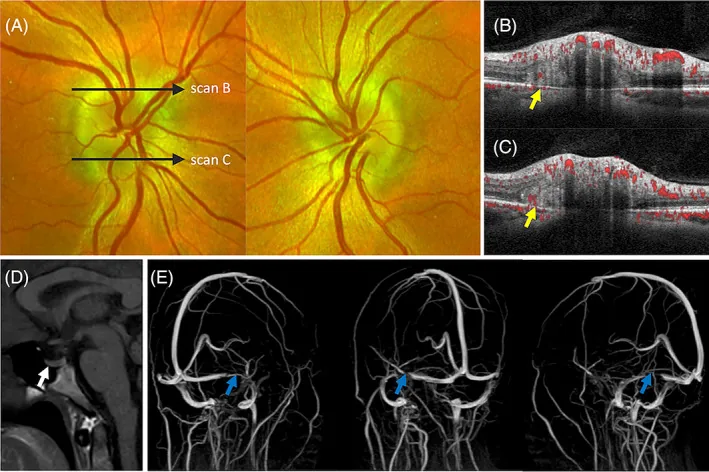
في المرحلة الحادة، تكون وذمة حليمة العصب البصري قليلة الأعراض في البداية، وعادةً ما تبقى الوظائف البصرية المركزية (أفضل حدة بصرية مصححة، رؤية الألوان) محفوظة.
عند الأطفال، غالبًا ما يُكتشف ارتفاع الضغط داخل الجمجمة من خلال الحول الداخلي المصاحب لشلل العصب المبعد الثنائي.
نتائج تنظير قاع العين في الوذمة الحليمية الحادة:
نتائج إضافية للوذمة الحليمية المزمنة: شحوب القرص البصري، دبق، وعاء تحويلة بصرية هدبية، جسم انكساري. في المرحلة المزمنة، لا تتورم الألياف العصبية الميتة، لذلك قد تختفي الوذمة حتى مع استمرار ارتفاع الضغط داخل الجمجمة (مرحلة نهاية ضامرة).
في حالة احمرار القرص البصري الثنائي مع رؤية جيدة، يجب دائمًا تضمين احتقان الحليمة في التشخيص التفريقي. في احتقان الحليمة، تكون الرؤية طبيعية تقريبًا ما لم تصل إلى المرحلة النهائية.
يتم تقييم شدة الوذمة الحليمية باستخدام مقياس Frisén (المراحل 0-5) ويستخدم كمؤشر للتنبؤ بالوظيفة البصرية.
المرحلة 0-1
المرحلة 0 (طبيعي): حدود غير واضحة في الجانب الأنفي والعلوي والسفلي. طبقة ألياف عصبية نصف قطرية.
المرحلة 1 (مبكرة جدًا): عدم وضوح الحدود الأنفية للحليمة. لا ارتفاع في الحدود. هالة رمادية خفيفة. طيات مشيمية دائرية ونصف قطرية.
المرحلة 2-3
المرحلة 2 (مبكرة): عدم وضوح جميع الحدود. ارتفاع الحد الأنفي. هالة كاملة حول القرص.
المرحلة 3 (متوسطة): زيادة قطر القرص. عدم وضوح أجزاء من الأوعية الرئيسية. امتدادات تشبه الأصابع على الحافة الخارجية للهالة.
المرحلة 4-5
المرحلة 4 (شديدة): ارتفاع القرص بأكمله. عدم وضوح كامل لأجزاء الأوعية الرئيسية فوق القرص.
المرحلة 5 (حرجة): بروز على شكل قبة. هالة ضيقة ذات حدود ناعمة. اختفاء الحفرة الفسيولوجية.
TVO هو عرض مميز لوذمة القرص، لكنه في حد ذاته ليس مؤشرًا مباشرًا لفقدان البصر. ومع ذلك، إذا استمر ارتفاع الضغط داخل الجمجمة لفترة طويلة، فقد يتطور إلى فقدان شديد في المجال البصري المحيطي ثم إلى تدهور الرؤية المركزية. إذا ظهر TVO بشكل متكرر، فمن المهم مراجعة أخصائي على الفور لتحديد السبب.
تعتمد سرعة تشكل وذمة القرص على سرعة ارتفاع الضغط داخل الجمجمة. في حالة الارتفاع البطيء للضغط داخل الجمجمة، قد تظهر خلال أسابيع، بينما في حالة الارتفاع الحاد، قد تظهر خلال ساعات إلى يوم واحد.
في حالة IIH، يؤدي فقدان الوزن بنسبة 5-10% إلى تحسن أعراض الضغط داخل الجمجمة ووذمة حليمة العصب البصري. لتطبيع الضغط داخل الجمجمة (الشفاء)، يلزم فقدان 24% من الوزن (تحليل per protocol لـ IIHWT) 15). إذا كان تحقيق ذلك صعبًا من خلال تعديل نمط الحياة فقط، فإن جراحة السمنة تعد خيارًا أيضًا. إدارة الوزن هي جزء من العلاج التحفظي فقط، وقد يلزم الجمع مع العلاج الدوائي أو الجراحي حسب درجة وذمة حليمة العصب البصري ووجود خلل وظيفي بصري.
يتم التقييم بالتسلسل التالي: تأكيد وذمة حليمة العصب البصري في كلتا العينين بمنظار العين → تصوير الأوعية بالفلوريسين → OCT → CT/MRI + MRV مع التباين → البزل القطني (LP). أولاً، يتم قياس ضغط الدم لاستبعاد ارتفاع ضغط الدم الخبيث، ثم يتم إجراء التصوير الطارئ (CT → MRI + MRV مع التباين) لتقييم الآفات الحيزة وتجلط الجيوب الوريدية. يتم إجراء LP بعد التأكد من عدم وجود خطر الانفتاق الدماغي.
MRI + MRV مع التباين هو الأمثل، وتقييم تضيق أو انسداد الجيوب الوريدية ضروري في IIH. يتم تقييم العلامات التالية لارتفاع الضغط داخل الجمجمة:
| المعيار | المحتوى |
|---|---|
| 1. وذمة حليمة العصب البصري | وجود وذمة حليمة العصب البصري في كلتا العينين |
| 2. الفحص العصبي | طبيعي باستثناء أي شذوذ في الأعصاب القحفية |
| 3. التصوير العصبي | طبيعي: لا توجد آفات في النسيج الدماغي، لا توسع بطيني، لا أورام، لا تعزيز شاذ |
| 4. تركيب السائل الدماغي الشوكي | طبيعي |
| 5. الضغط الافتتاحي للسائل الدماغي الشوكي | البالغون ≥250 مم H2O، الأطفال ≥280 مم H2O |
تشخيص مشتبه به: وجود وذمة حليمة العصب البصري الثنائية + استيفاء المعايير 1-4 ولكن ضغط السائل الدماغي الشوكي أقل من المعيار. يُوصى بإعادة التقييم في حالة 25-30 سم H2O كمنطقة رمادية.
تم الإبلاغ عن أن 17.8% من تشخيصات IIH غير دقيقة أو متسرعة، و13.0% تشخيص خاطئ 18). السبب الأكثر شيوعًا للتشخيص الخاطئ هو عدم إجراء تصوير الوريد بالرنين المغناطيسي (42.4%) في المرضى غير النمطيين (الذكور، مؤشر كتلة الجسم الطبيعي، الأطفال)، مما يؤدي إلى إغفال تخثر الجيب الوريدي المخي.
تحدث الوذمة الحليمية الكاذبة بسبب طول النظر الشديد، والدرزن، والقرص المائل، والألياف العصبية الميالينية، والورم العابي، وغيرها. تشير النتائج التالية إلى وذمة حليمية كاذبة.
قائمة التشخيص التفريقي: الدرزن المدفون، القرص المائل، الاعتلال الحليمي السكري، الاعتلال الحليمي الناتج عن ارتفاع ضغط الدم، التهاب الصلبة الخلفي، التهاب محيط العصب البصري، التهاب العنبية (الساركويد، VKH)، التهاب العصب البصري، اعتلال العين الدرقي، انسداد الوريد الشبكي المركزي، الاعتلال العصبي الإقفاري الأمامي الحاد للعصب البصري، الاعتلال العصبي البصري الارتشاحي، ورم سحائي في غمد العصب البصري.
يُذكر أن 10% من مرضى الوذمة الحليمية يعانون من فقر الدم الناجم عن نقص الحديد القابل للعلاج، ويوصى بإجراء فحص.
في الوذمة الحليمية الاحتقانية (وذمة حليمية ناتجة عن ارتفاع الضغط داخل الجمجمة)، قد تبقى الرؤية طبيعية في المراحل المبكرة. وذلك لأنه على الرغم من أن ارتفاع الضغط داخل الجمجمة يسبب ركود التدفق المحوري في القرص البصري، إلا أن التأثير على الوظيفة البصرية الواردة يكون خفيفًا في هذه المرحلة. من ناحية أخرى، في التهاب العصب البصري، يحدث انخفاض حاد في الرؤية بسهولة، وهذا الاختلاف يساعد في التفريق.
الأهداف الثلاثة للعلاج هي: ① علاج السبب الأساسي، ② الحفاظ على الوظيفة البصرية، ③ تخفيف الأعراض (مثل الصداع).
إذا انخفض الضغط داخل الجمجمة مبكرًا، فإن الوذمة الحليمية تتراجع بسرعة دون ترك خلل في الوظيفة البصرية. إذا تأخر العلاج وظهر خلل في الوظيفة البصرية، يصبح غير قابل للعكس.
| الدواء | الجرعة | ملاحظات |
|---|---|---|
| أسيتازولاميد (الخيار الأول) | 250-500 مجم مرتين/يوم → حتى 2-4 جم/يوم | أثبتت فعالية IIHTT (2014) في IIH مع عيوب بصرية خفيفة16). لا تأثير ثابت على الصداع. غير مشمول بالتأمين في اليابان |
| توبيرامات (الخيار الثاني) | تعديل فردي | يخفض الضغط داخل الجمجمة ويساعد في إنقاص الوزن. مفيد أيضًا للصداع الشبيه بالصداع النصفي. له تأثير ماسخ → ممنوع للحوامل |
| فوروسيميد | استخدام مساعد | بديل عند عدم تحمل الأسيتازولاميد |
| ميثيل بريدنيزولون وريدي | 1 جم/يوم × 3 أيام | إجراء مؤقت فقط في IIH الخاطف. ممارسة شائعة في أمريكا الشمالية |
الآثار الجانبية الرئيسية للأسيتازولاميد: تنميل (خدر في الأطراف)، اضطراب التذوق (طعم معدني)، أعراض هضمية (غثيان، قيء، إسهال)، إرهاق، حصوات كلوية. حماض استقلابي مزمن معوض، نقص بوتاسيوم خفيف.
| الإجراء الجراحي | معدل تحسن البصر | معدل تحسن الصداع | المضاعفات الرئيسية |
|---|---|---|---|
| شق غمد العصب البصري (ONSF) | 59% | 44% | مضاعفات 10-15% (بما في ذلك فقدان البصر 1-2% CRAO/CRVO). معدل التدهور 34% في سنة و45% في 3 سنوات1) |
| تحويلة السائل الدماغي الشوكي (LPS/VPS) | 54% | 80% | فشل التحويلة 43-50%، عدوى، إزاحة1) |
| دعامة الجيب الوريدي الجافوي (VSS) | 78% | 82-83% | العلاج المضاد للصفيحات إلزامي لمدة 6 أشهر بعد الجراحة. معدل إعادة الجراحة 10-18%1) |
| جراحة السمنة | — | — | في تجربة IIHWT RCT، استمر انخفاض الضغط داخل الجمجمة وفقدان الوزن لمدة عامين15) |
مؤشرات VSS (دعامة الجيب الوريدي الجافوي): عند تأكيد تضيق الجيب المستعرض مع تدرج ضغط >8 مم زئبقي. لا يخفض ONSF الضغط داخل القحف. قد لا يكون ONSF أحادي الجانب كافياً للتأثير على الجانب المقابل. غالباً ما يتم اختيار تحويلة قطنية صفاقية (LP) كتدخل جراحي أولي لـ IIH.
2-3% من مرضى IIH. يتميز بفقدان سريع للبصر خلال 4 أسابيع من ظهور الأعراض. يتطلب الإقامة في المستشفى وعلاجاً طبياً وجراحياً مكثفاً.
متوسط ضغط فتح السائل الدماغي الشوكي مرتفع جداً (54.1 سم H2O، النطاق 29-70) 6). في سلسلة Thambisetty المكونة من 16 حالة 6)، على الرغم من العلاج المكثف، وصل 50% إلى العمى القانوني، وبقي لدى جميع المرضى عيوب في المجال البصري وضمور العصب البصري. إذا كان خط الأساس MD لـ HVF أقل من -7 ديسيبل، فمن الصعب استعادة البصر. 1) كلما ارتفعت قيمة pRNFL الأولية، كان التشخيص البصري طويل المدى أسوأ. 1)
هناك تقارير عن تعافي FIH باستخدام الأسيتازولاميد وحده بجرعة قصوى 4 غرام/يوم (رجل يبلغ من العمر 36 عاماً، مؤشر كتلة الجسم 47.3، ضغط فتح السائل الدماغي الشوكي 45 سم H2O → اختفاء وذمة حليمة العصب البصري بعد 4 أشهر، واستعادة حدة البصر 20/20 في كلتا العينين بعد 6 أشهر) 8). إذا ترافق FIH مع ارتفاع ضغط الدم الخبيث، فإن متوسط تأخير التشخيص يصل إلى 3.2 أشهر، وقد يكون التشخيص النهائي سيئاً للغاية (حدة البصر النهائية 20/400 إلى إدراك الضوء) 7).
معدل انتشار IIH أثناء الحمل هو 16/100,000. تحدث 61% من الحالات في الثلث الأول من الحمل 9). لا يعتبر الحمل بحد ذاته عاملاً مسبباً لـ IIH. التشخيص البصري مشابه للحالات غير الحامل، ولا يعتبر عادةً حملاً عالي الخطورة.
الإنذار: معدل تكرار IIH يتراوح بين 9-28%2). عوامل سوء الإنذار: زيادة الوزن، شدة الوذمة الحليمية، وشدة الصداع الأساسي2).
الأسيتازولاميد هو الدواء الخط الأول الفعال لـ IIH، لكنه ممنوع في حالات تجلط الأوردة الدماغية لأنه قد يؤدي إلى تفاقم الحالة. كما يُمنع استخدامه في التهاب السحايا بالمكورات العقدية. من الضروري تحديد السبب أولاً واختيار العلاج بناءً على السبب الأساسي. تجدر الإشارة إلى أنه غير مشمول بالتأمين الصحي في اليابان.
يصنف ضمن الفئة C من إدارة الغذاء والدواء الأمريكية، لكن المراجعات المنهجية لم تجد علاقة سببية مع التشوهات الخلقية9). حتى الاستخدام بجرعات عالية (≥1 غرام/يوم) في الثلث الأول من الحمل لم يظهر زيادة في خطر التشوهات. يجب استخدامه بالتنسيق مع طبيب التوليد، وغالبًا ما يقتصر على ما بعد الأسبوع العشرين من الحمل.
IIH الخاطف هو نوع فرعي من IIH، ويتميز بفقدان بصري سريع وشديد خلال 4 أسابيع من ظهور الأعراض. يحدث في 2-3% من مرضى IIH. بينما يتطور IIH العادي ببطء نسبيًا، يتدهور البصر في IIH الخاطف في غضون أيام، ويمكن أن يؤدي إلى عمى لا رجعة فيه دون تدخل سريع6).
يؤدي ارتفاع الضغط في الفضاء تحت العنكبوتية حول العصب البصري إلى انضغاط العصب البصري وركود التدفق المحوري، مما يسبب الوذمة الحليمية. يحدث ذلك عبر المسار التالي.
ارتفاع الضغط داخل الجمجمة → ارتفاع الضغط في الحيز تحت العنكبوتية حول العصب البصري → انضغاط العصب البصري → توقف النقل المحوري الأمامي → وذمة عصبية (وذمة حليمة العصب البصري). استمرار الضغط → نقص تروية داخل العصب → فقدان المحاور → ضمور العصب البصري → ضعف البصر. في مرحلة الضمور، لا تتورم الألياف العصبية الميتة، لذلك قد تختفي وذمة الحليمة حتى مع استمرار ارتفاع الضغط داخل الجمجمة (المرحلة النهائية الضمورية).
فرضية ضعف تصريف السائل الدماغي الشوكي
تأخر تصريف السائل الدماغي الشوكي عبر حبيبات العنكبوتية والمسارات اللمفاوية يؤدي إلى ارتفاع الضغط داخل الجمجمة. المينوسيكلين يعطل إشارات cAMP في حبيبات العنكبوتية ويقلل امتصاص السائل الدماغي الشوكي 13).
فرضية ارتفاع ضغط الجيب الوريدي
أكثر من 90% من مرضى IIH يعانون من تضيق في الجيوب المستعرضة الثنائية 2). السلسلة: السمنة → ارتفاع الضغط داخل البطن → ارتفاع الضغط داخل الصدر → ضعف التصريف الوريدي الدماغي → ارتفاع الضغط داخل الجمجمة. فعالية دعامة الجيب الوريدي تدعم هذه الفرضية.
فرضية الاضطراب الأيضي والهرموني
يُقترح تورط خلل تنظيم الأندروجين 2). زيادة اللبتين → فرط نشاط الضفيرة المشيمية → فرط إنتاج السائل الدماغي الشوكي. مستقبلات GLP-1 موجودة في الضفيرة المشيمية، وقد ثبت أن ناهضات GLP-1 تقلل إنتاج السائل الدماغي الشوكي في نموذج الفئران.
في تجربة عشوائية محكومة تقارن جراحة السمنة مقابل تدخل إدارة الوزن المجتمعي، أظهرت مجموعة جراحة السمنة انخفاضًا مستدامًا في الضغط داخل الجمجمة (ICP) وفقدان الوزن على مدى عامين 15). كما كانت فعالية التكلفة بعد 5 سنوات أفضل من العلاج الغذائي. يرتبط مقدار انخفاض ICP بدرجة فقدان الوزن.
تُعتبر ناهضات مستقبلات GLP-1 مثل إكسيناتيد مرشحة جديدة لعلاج IIH. تقلل إفراز السائل الدماغي الشوكي (CSF) في الضفيرة المشيمية عبر تقليل نشاط Na⁺/K⁺-ATPase. هناك تقارير عن انخفاض ICP بمقدار 5.7 ± 2.9 سم H₂O بعد 2.5 ساعة من الإعطاء لدى البشر (P=0.048). يُتوقع آلية مزدوجة: تعزيز فقدان الوزن وخفض ICP المباشر. ومع ذلك، يجب الانتباه إلى خطر انتكاس الوزن بعد التوقف مما قد يؤدي إلى ظهور IIH.
تتراكم التقارير حول سلامة وفعالية وضع دعامة في الجيب المستعرض 4, 5). تجري حاليًا تجربة عشوائية محكومة في المملكة المتحدة تقارن VSS مقابل تحويلة بطينية صفاقية (VPS). معدل تحسن الرؤية في VSS هو 78% وتحسن الصداع 82-83% (تحليل تلوي). يتراوح معدل إعادة الجراحة بين 10-18%.
تُدرس مثبطات إنزيم 11β-HSD1 (11β-هيدروكسي ستيرويد ديهيدروجيناز النوع 1) كهدف علاجي جديد لـ IIH 1).
هناك نقاشات لاقتراح تعريف يعتمد على “تهديد البصر” بدلاً من المعيار الزمني “خلال 4 أسابيع” 1). قد يؤدي المعيار الزمني إلى تفويت حالات ذات تقدم سريع.
تم الإبلاغ عن وذمة حليمة العصب البصري في مرضى لا يتوافقون مع ملف المخاطر التقليدي 1). مثل IIH غير المرتبط بالسمنة أو الجنس الأنثوي، المرتبط بـ MIS-C (متلازمة الالتهاب متعدد الأجهزة لدى الأطفال)، وVITT بعد لقاح أسترازينيكا.
تم تأكيد وجود اختلافات كبيرة بين الولايات داخل الولايات المتحدة (Moran I=0.20، P=0.03) 3). في تكساس وأوكلاهوما وغيرها، لوحظ عدم تطابق بين ارتفاع معدل السمنة وانخفاض IIH، ولا يزال السبب غير معروف.
Bonelli L, Menon V, Arnold AC, Mollan SP. Managing idiopathic intracranial hypertension in the eye clinic. Eye. 2024;38:2472-2481.
Toshniwal SS, Kinkar J, Chadha Y, et al. Navigating the enigma: a comprehensive review of idiopathic intracranial hypertension. Cureus. 2024;16(3):e56256.
Fraz MA, Kim BM, Chen JJ, et al. Nationwide prevalence and geographic variation of idiopathic intracranial hypertension among women in the United States. Ophthalmology. 2025;132:476-483.
Ghorbani M, Griessenauer CJ, Wipplinger C, et al. Intracranial hypertension and papilledema secondary to an unruptured arteriovenous malformation: review of the literature. Neuroradiol J. 2025;38(4):387-393.
Waser B, Wood HM, Mews P, Lalloo S. Transverse sinus stenting for treatment of papilloedema secondary to a large brain herniation into a dural venous sinus with associated tectal plate lesion: case report and literature review. Interv Neuroradiol. 2021;27(6):756-762.
Thambisetty M, Lavin PJ, Newman NJ, Biousse V. Fulminant idiopathic intracranial hypertension. Neurology. 2007;68(3):229-232.
Aldhahwani B, Shah SM, Jiang H, Lam BL. Severe visual loss from concurrent fulminant idiopathic intracranial hypertension and malignant arterial hypertension: prompt suspicion matters. Am J Ophthalmol Case Reports. 2024;36:102201.
Srivastava O, Micieli JA. Resolution of fulminant idiopathic intracranial hypertension treated with acetazolamide. Case Rep Neurol. 2022;14:432-436.
Palermo M, Trevisi G, D’Arrigo S, Sturiale CL. Idiopathic intracranial hypertension in pregnancy: a systematic review on clinical course, treatments, delivery and maternal-fetal outcome. Eur J Neurol. 2025;32:e70186.
Alves S, Sousa N, Cardoso L, Alves J. Multidisciplinary management of idiopathic intracranial hypertension in pregnancy: case series and narrative review. Braz J Anesthesiol. 2022;72(6):790-794.
Regev T, Fried-Regev N, Leeman S, et al. Transverse venous sinus stenting for fulminant idiopathic intracranial hypertension during pregnancy: a report of two cases and literature review. Quant Imaging Med Surg. 2025;15(5):4796-4815.
Selvaraj J, Veeranki V, Kommaraju SY, et al. Abortion and fulminant idiopathic intracranial hypertension. Cureus. 2021;13(2):e13501.
Paramo R, Leishangthem L. Optic atrophy secondary to minocycline-induced idiopathic intracranial hypertension. BMJ Case Rep. 2023;16:e252731.
Mollan SP, Davies B, Silver NC, et al. Idiopathic intracranial hypertension: consensus guidelines on management. J Neurol Neurosurg Psychiatry. 2018;89(10):1088-1100.
Mollan SP, Mitchell JL, Ottridge RS, et al. Effectiveness of bariatric surgery vs community weight management intervention for the treatment of idiopathic intracranial hypertension: a randomized clinical trial. JAMA Neurol. 2021;78:678-686.
Wall M, McDermott MP, Kieburtz KD, et al. Effect of acetazolamide on visual function in patients with idiopathic intracranial hypertension and mild visual loss: the idiopathic intracranial hypertension treatment trial. JAMA. 2014;311:1641-1651.
Pasricha SV, Bhayana R, Wu PE. Supine headache and papilledema: a case and review of cerebral venous sinus thrombosis. Clin Case Rep. 2023;11:e07329.
Fisayo A, Bruce BB, Newman NJ, Biousse V. Overdiagnosis of idiopathic intracranial hypertension. Neurology. 2016;86:341-350.