變性與萎縮性疾病

眼底自體螢光(FAF)
一目瞭然的要點
Section titled “一目瞭然的要點”1. 眼底自發螢光
Section titled “1. 眼底自發螢光”眼底自發螢光(Fundus Autofluorescence; FAF)是一種非侵入性影像診斷方法,透過光激發眼底存在的天然螢光物質並繪製其發光圖7)。與螢光素眼底血管攝影(FA)不同,它不需要靜脈注射顯影劑7)。
1995年,人類視網膜的固有螢光特性首次被報導7)。隨後,隨著共焦掃描雷射檢眼鏡(cSLO)的普及,臨床應用迅速擴大。
主要螢光物質
Section titled “主要螢光物質”FAF的主要螢光團是積聚在RPE細胞內的脂褐素(LF)7)6)。LF是感光細胞外節盤膜不完全溶酶體降解的副產物,包含至少20種雙視黃醛化合物7)。
主要成分A2E(N-視黃亞基-N-視黃基乙醇胺)吸收藍光(峰值約470 nm),發射黃綠光(600–610 nm)6)7)。A2E通過光氧化產生活性氧(ROS),導致膜不穩定和細胞凋亡7)。
各雙視黃醛化合物的吸收峰值如下7):
| 螢光物質 | 吸收峰值 |
|---|---|
| A2E | 439 nm |
| A2PE | 449奈米 |
| isoA2E | 426奈米 |
| A2-DHP-PE | 490奈米 |
RPE細胞在一生中吞噬約30億個感光細胞外節盤膜6)。70歲以後,LF和黑色素脂褐素累積至約佔RPE細胞質體積的25%6)。
近紅外自發螢光(NIR-AF)使用約787 nm的光激發黑色素作為主要螢光物質7)6)。這可以評估RPE和脈絡膜中的黑色素分佈。
FA需要靜脈注射造影劑,評估血管結構和血-視網膜屏障狀態。FAF無需造影劑,利用RPE內脂褐素的固有螢光評估RPE代謝狀態。FAF的信號強度約為FA的百分之一,但通過直接反映RPE損傷提供補充信息7)。
2. 適應症與臨床意義
Section titled “2. 適應症與臨床意義”FAF用於多種視網膜和脈絡膜疾病的診斷和追蹤。
血管與代謝性疾病
發炎性與腫瘤性疾病
GA周圍FAF模式與進展速度
Section titled “GA周圍FAF模式與進展速度”GA進展預測採用IFAG(國際FAF分類組)分類,分為8種模式(正常、微小變化、局部增強、斑片狀、線狀、花邊狀、網狀、斑點狀)6)。
各模式的進展速度如下所示3)6):
| 模式 | 特徵 | 進展速度(mm²/年) |
|---|---|---|
| 無/輕微 | 邊界無變化 | 最慢 |
| 瀰漫性滴流 | 廣泛點狀高螢光 | 約2.61 |
| 斑片狀/帶狀 | 斑片狀/帶狀 | 中等 |
GA區域的低螢光表示RPE喪失,周圍的高螢光反映RPE肥大、脫落RPE的遷移和巨噬細胞聚集3)。
網狀假性玻璃膜疣在FAF上表現為50–400 μm的低螢光斑點,比彩色眼底照片更敏感6)。
地圖狀萎縮(GA)的進展監測、Stargardt病的螢光定量(qAF)、視網膜色素變性(RP)的高螢光環收縮評估特別有用。這些可能比OCT或FA更早檢測到結構變化。詳見「4. 正常所見與異常所見的解讀」。
3. 檢查步驟與拍攝方法
Section titled “3. 檢查步驟與拍攝方法”FAF攝影主要使用三種設備。
cSLO型
共焦掃描雷射檢眼鏡:透過共焦針孔阻擋離焦光線,減少水晶體螢光的影響7)6)。
Spectralis(Heidelberg):488 nm藍色雷射,>500 nm屏障濾光片,15–55度。支援OCT同步攝影和NIR-AF7)。
Nidek Mirante:490 nm激發,40–60度7)。
眼底相機型
白色閃光+帶通濾光片:可進行廣角拍攝。
Topcon TRC-50DX:500610 nm / 535585 nm(Spaide濾光片)激發7)。
Zeiss Clarus:藍光FAF(BLFI),435585 nm激發,支援133200度7)。
超廣角型
Optos(Natus):532 nm綠色雷射,200度超廣角拍攝。可在無散瞳(最小瞳孔直徑2 mm)下使用7)6)。
周邊病變檢測:有助於評估常規眼底相機無法捕捉的周邊視網膜病變。
主要設備規格比較
Section titled “主要設備規格比較”各設備的規格如下所示7):
| 設備 | 激發波長 | 視角 |
|---|---|---|
| Spectralis | 488 nm | 15~55度 |
| Optos | 532 nm | 200度 |
| Zeiss Clarus | 435~585 nm | 133~200度 |
實際拍攝操作
Section titled “實際拍攝操作”標準B-FAF(藍光FAF)拍攝時,在散大患者瞳孔後(或無需散瞳),將患者固定在設備上,在觀察即時影像的同時以最佳焦點進行拍攝。cSLO型透過多幀平均疊加處理提高訊噪比。
光漂白處理:拍攝前進行約20秒的強光照射,使視色素漂白,可將FAF訊號增強約30%2)1)。用於評估MEWDS等急性期病變。
綠光FAF(G-FAF):採用504/532 nm激發光拍攝,黃斑色素吸收較少,對中心凹評估效果優異4)6)。患者舒適度也較高。
門診標準檢查廣泛使用cSLO型(如Spectralis)。超廣角拍攝選擇Optos,中心凹評估選擇G-FAF相容設備。可同時拍攝OCT的cSLO型在追蹤中定位精度高,適用於GA面積測量等定量評估4)7)。
4. 正常所見與異常所見的解讀
Section titled “4. 正常所見與異常所見的解讀”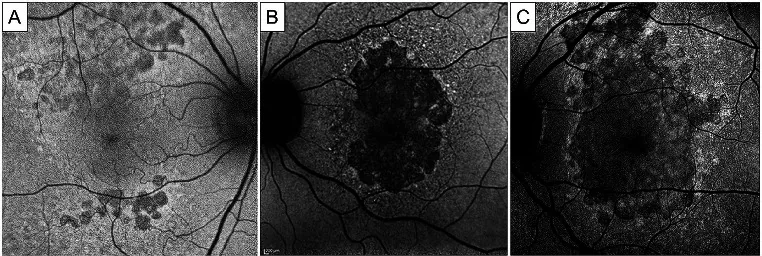
SW-AF(短波長FAF、B-FAF)的正常所見:
- 中心凹低螢光: 由於葉黃素色素(黃斑色素)吸收藍光,中心凹呈現低螢光6)7)。
- 視神經盤低螢光:因缺乏RPE,呈現低螢光7)。
- 視網膜血管低螢光:血液吸收光線,呈現低螢光7)。
- 最強螢光區域:距中心凹5–15度的旁中心凹區域顯示最強螢光6)。
NIR-AF(近紅外自發螢光)的正常表現:
由於中心凹黑色素密度高,在NIR-AF上反而表現為高螢光6)7)。這是與SW-AF的重要區別。
異常表現的判讀
Section titled “異常表現的判讀”強螢光與弱螢光的原因及代表性疾病如下所示7)1)2):
| 模式 | 主要原因 | 代表性疾病 |
|---|---|---|
| 強螢光 | 脂褐素積聚、黃斑色素消失、視網膜下螢光物質 | Stargardt病、MEWDS、GA周圍 |
| 低螢光 | RPE萎縮、出血遮蔽、纖維化 | GA、出血、疤痕 |
過螢光機制分類:
過螢光的產生機製分為原發性上升和繼發性上升2)。
- 原發性上升:ABCA4、RDH12功能異常導致雙視黃醛過度生成。對應Stargardt病、RDH12相關視網膜營養不良。
- 繼發性上升:光感受器細胞損傷後,下游雙視黃醛積累。繼發於RP或其他原因導致的光感受器細胞死亡。
與光漂白的鑑別:如果光漂白處理後高螢光消失,則可能是由於視色素(視紫紅質)螢光引起的假性高螢光1)。
黃斑色素減少(老化、陽光暴露)或光漂白也可能出現高螢光。結合OCT檢查結構變化,與真正的病理性高螢光進行鑑別。由於不同設備之間表現可能不同,縱向比較時應使用同一設備4)7)。
5. 注意事項與限制
Section titled “5. 注意事項與限制”6. 技術原理(脂褐素、黑色素、螢光團)
Section titled “6. 技術原理(脂褐素、黑色素、螢光團)”螢光的物理學基礎
Section titled “螢光的物理學基礎”螢光是指吸收光子的分子從激發態回到基態時發射出較低能量光子的現象7)。發射光波長總是長於吸收光波長(斯托克斯位移)。
脂褐素的生化形成過程
Section titled “脂褐素的生化形成過程”LF的主要成分A2E的形成途徑如下7)2):
- 11-順式視黃醛的光異構化:光感受產生全反式視黃醛。
- 與磷脂醯乙醇胺(PE)的反應:全反式視黃醛與PE縮合形成N-亞視黃基-PE(NRPE)。
- NRPE→A2-GPE:在盤膜內,NRPE與第二個全反式視黃醛分子反應,形成A2-GPE(A2E前體)。
- A2-GPE水解→A2E:RPE吞噬盤膜後,A2-GPE在溶酶體中水解生成A2E。
ABCA4的角色:ABC轉運蛋白ABCA4將NRPE運送至盤膜的細胞質側,並促進其還原為全反式視黃醇2)。ABCA4功能缺陷(Stargardt病的病因)導致NRPE滯留於盤膜內,引起雙視黃醛類化合物的過度累積。
黑色素與近紅外自體螢光
Section titled “黑色素與近紅外自體螢光”黑色素是NIR-AF(787 nm激發)的主要螢光物質,分佈於RPE和脈絡膜7)6)。與年齡相關的黑色素減少表現為NIR-AF信號減弱。黑色素脂褐素(黑色素與LF的複合物)也對NIR-AF信號有貢獻。
螢光定量(qAF)
Section titled “螢光定量(qAF)”qAF是在488 nm激發下,使用內部螢光參考(比色皿中的標準螢光物質)校正後的定量螢光值2)7)。qAF值隨年齡、偏心度、性別和種族而變化,標準化仍是一個挑戰。
螢光壽命成像(FLIO)
Section titled “螢光壽命成像(FLIO)”FLIO是一種測量每種螢光物質特有螢光衰減曲線(壽命)的技術,除了螢光強度外,還能識別螢光物質的類型6)7)。目前主要用於研究目的。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”qAF在臨床試驗終點的應用
Section titled “qAF在臨床試驗終點的應用”qAF正逐漸被用作Stargardt病、視網膜色素變性等遺傳性視網膜疾病進展的客觀指標,並被納入臨床試驗終點2)。校準設備和標準化測量方案是當前的挑戰。
FAH在地圖狀萎縮治療藥物試驗中的角色
Section titled “FAH在地圖狀萎縮治療藥物試驗中的角色”在使用pegcetacoplan(APL-2)和avacincaptad pegol(Zimura)治療地圖狀萎縮的臨床試驗中,基於FAF影像的GA面積測量已被採用為主要終點4)。有報告指出,B-FAF傾向於高估GA面積,而G-FAF在評估中心病變方面更優4)。
AI與深度學習自動分析
Section titled “AI與深度學習自動分析”已有研究報告將Optos超廣角FAF影像與深度學習演算法結合,用於檢測年齡相關性黃斑部病變,可實現高敏感度的早期病變偵測6)。
在遺傳性視網膜疾病的自動分類中,據報導神經網路識別Stargardt病、Best病和RP的準確率約為95%5)。
G-FAF臨床應用的擴展
Section titled “G-FAF臨床應用的擴展”G-FAF受中心凹黃斑色素影響較小,在檢測SW-AF難以觀察的中心凹病變方面具有優勢4)。患者眩光感也較輕,在舒適性方面更有利。未來有望獲得更廣泛的應用。
FLIO的臨床應用
Section titled “FLIO的臨床應用”螢光壽命成像(FLIO)在年齡相關性黃斑部病變、Stargardt病和糖尿病黃斑病變中顯示出疾病特異性螢光壽命模式,並可能在基於強度的FAF之前檢測到代謝變化7)。
多模態影像整合
Section titled “多模態影像整合”透過整合FAF、OCT、OCT-A和FA的多模態影像,正在建立一種彌補各檢查方法侷限性的診斷體系4)。
主要前景包括透過qAF標準化進行定量疾病監測、利用AI和深度學習進行自動診斷(遺傳性視網膜疾病準確率約95%)、FLIO的臨床應用以及G-FAF的普及5)6)。FAF已被用作地理萎縮治療藥物臨床試驗的主要終點,預計其在未來視網膜診療中的重要性將進一步增加4)。
8. 參考文獻
Section titled “8. 參考文獻”- Mantovani A, Corbelli E, Sacconi R, et al. Blue-light fundus autofluorescence in inflammatory photoreceptor diseases. Diagnostics. 2023;13(14):2466.
- Parmann R, Bhatt M, Sarraf D, et al. Primary versus secondary autofluorescence elevations in inherited retinal dystrophies. Int J Mol Sci. 2023;24(15):12327.
- Curcio CA, Meleth AD, Gelman R, et al. FAF variation in geographic atrophy: clinicopathologic correlation. Invest Ophthalmol Vis Sci. 2025;66(1):49.
- Ranetti AE, Ranetti MO, Pop A, et al. Blue-light and green-light fundus autofluorescence in age-related macular degeneration. Diagnostics. 2025;15(13):1688.
- Oh J, Lee CS, Kim JM, et al. Fundus autofluorescence in inherited retinal disease. J Clin Med. 2025;14(7):2293.
- Sahinoglu Kekek E, Sermet F. Fundus autofluorescence in dry age-related macular degeneration. Turk J Ophthalmol. 2021;51(3):169-176.
- Pole C, Ameri H. Fundus autofluorescence and clinical applications. J Ophthalmic Vis Res. 2021;16(3):432-461.
