การถ่ายภาพเรืองแสงเองของจอตา (FAF ) เป็นวิธีการถ่ายภาพจอประสาทตา แบบไม่รุกล้ำโดยไม่ต้องใช้สารทึบรังสี ซึ่งแสดงแผนที่สถานะเมแทบอลิซึมของ RPE
สารเรืองแสงหลักคือลิโพฟัสซิน (LF) ภายใน RPE ซึ่งเป็นผลผลิตจากการสลายที่ไม่สมบูรณ์ของส่วนนอกของเซลล์รับแสง
การเรืองแสงมากเกินไปบ่งชี้ถึงความผิดปกติของเมแทบอลิซึมของ RPE และการสะสมของ LF ในขณะที่การเรืองแสงน้อยเกินไปบ่งชี้ถึงการฝ่อของ RPE หรือการบดบัง
รูปแบบการเรืองแสงมากเกินไปรอบๆ จอประสาทตา ฝ่อแบบภูมิศาสตร์ (GA) ใช้ในการทำนายอัตราการดำเนินโรค โดยแบบ diffuse trickling แสดงถึงการดำเนินโรคที่เร็วที่สุด
อุปกรณ์ประกอบด้วยชนิด cSLO ชนิดกล้องถ่ายภาพจอตา และชนิดมุมกว้างพิเศษ ซึ่งแต่ละชนิดมีข้อบ่งชี้ที่แตกต่างกัน
การวิเคราะห์อัตโนมัติด้วย AI และการเรียนรู้เชิงลึกกำลังก้าวหน้า และ qAF กำลังได้รับความสนใจในฐานะจุดสิ้นสุดของการทดลองทางคลินิก
การเรืองแสงอัตโนมัติของจอตา (FAF ) เป็นวิธีการถ่ายภาพวินิจฉัยแบบไม่รุกรานที่กระตุ้นสารเรืองแสงธรรมชาติในจอตาด้วยแสงและบันทึกการเปล่งแสง7) ต่างจากการถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน (FA ) ซึ่งไม่จำเป็นต้องฉีดสารทึบรังสีทางหลอดเลือดดำ7) .
ในปี ค.ศ. 1995 มีรายงานครั้งแรกเกี่ยวกับคุณสมบัติการเรืองแสงอัตโนมัติของจอตามนุษย์7) หลังจากนั้น การประยุกต์ใช้ทางคลินิกก็แพร่หลายอย่างรวดเร็วตามการแพร่กระจายของกล้องตรวจจอตาชนิดเลเซอร์สแกนแบบคอนโฟคอล (cSLO).
ฟลูออโรฟอร์หลักในการถ่ายภาพเรืองแสงอัตโนมัติของจอประสาทตา คือลิโปฟัสซินที่สะสมภายในเซลล์อาร์พีอี7) 6) ลิโปฟัสซินเป็นผลพลอยได้จากการย่อยสลายของเยื่อแผ่นดิสก์ส่วนนอกของเซลล์รับแสง ที่ไม่สมบูรณ์ในไลโซโซม และประกอบด้วยสารประกอบบิสเรตินอยด์อย่างน้อย 20 ชนิด7)
A2E (N-เรตินิลิดีน-N-เรตินิลเอทานอลเอมีน) ซึ่งเป็นองค์ประกอบหลัก ดูดซับแสงสีน้ำเงิน (พีคประมาณ 470 นาโนเมตร) และปล่อยแสงสีเหลือง-เขียว (600–610 นาโนเมตร)6) 7) A2E ก่อให้เกิดอนุมูลอิสระออกซิเจนผ่านกระบวนการออกซิเดชันจากแสง ซึ่งเหนี่ยวนำให้เกิดความไม่เสถียรของเยื่อหุ้มเซลล์และการตายของเซลล์แบบอะพอพโทซิส 7)
ค่าการดูดกลืนแสงสูงสุดของบิสเรตินอยด์แต่ละชนิดมีดังนี้7) :
ฟลูออโรฟอร์ ค่าการดูดกลืนแสงสูงสุด A2E 439 นาโนเมตร A2PE 449 นาโนเมตร isoA2E 426 นาโนเมตร A2-DHP-PE 490 นาโนเมตร
เซลล์ RPE จะกินจานของส่วนนอกของเซลล์รับแสง ประมาณ 3 พันล้านชิ้นตลอดอายุขัย 6) หลังจากอายุ 70 ปี LF และเมลาโนลิโปฟัสซินจะสะสมจนกินพื้นที่ประมาณ 25% ของปริมาตรไซโทพลาซึมของ RPE 6) .
ในการเรืองแสงเองช่วงใกล้อินฟราเรด (NIR-AF) เมลานินจะถูกกระตุ้นให้เป็นสารเรืองแสงหลักด้วยแสงประมาณ 787 นาโนเมตร 7) 6) ซึ่งช่วยให้ประเมินการกระจายของเมลานินใน RPE และคอรอยด์ ได้
Q
FAF กับ FA (การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน) ต่างกันอย่างไร?
A
FA ต้องฉีดสารทึบรังสีทางหลอดเลือดดำ และประเมินโครงสร้างหลอดเลือดและสถานะของสิ่งกีดขวางเลือด-จอประสาทตา FAF ไม่ต้องใช้สารทึบรังสี ใช้การเรืองแสงภายในของลิโปฟัสซินใน RPE เพื่อประเมินสถานะเมแทบอลิซึมของ RPE ความเข้มสัญญาณของ FAF อ่อน ประมาณ 1/100 ของ FA แต่สะท้อนความเสียหายของ RPE โดยตรง ให้ข้อมูลเสริม 7) .
FAF ใช้ในการวินิจฉัยและติดตามโรคจอประสาทตา และคอรอยด์ ที่หลากหลาย
โรคเสื่อมและฝ่อ
จอประสาทตา เสื่อมตามอายุ (AMD ) และจอประสาทตา ฝ่อแบบภูมิศาสตร์ (GA)
โรคสตาร์การ์ดท์ : มีลักษณะเด่นคือการเรืองแสงสูงแบบจุดและการเรืองแสงต่ำจากการฝ่อของรอยบุ๋มจอประสาทตา qAF แสดงค่าเรืองแสงสูงกว่าปกติประมาณ 3 เท่า
จอประสาทตา อักเสบจากเม็ดสี (RP )จอประสาทตา ที่หดตัวลงตามเวลาเป็นตัวบ่งชี้การดำเนินโรค
โรคหลอดเลือดและเมตาบอลิก
จอประสาทตา จากเบาหวาน (DR)จอประสาทตา บวมน้ำแบบถุงน้ำ (CME ) เรืองแสงสูง มีประโยชน์ในการตรวจหาการเปลี่ยนแปลงระยะแรก
โรคคอริโอเรติโนพาทีชนิดเซรุ่มส่วนกลาง (CSC ) : ในกรณีเรื้อรัง การเรืองแสงจะเปลี่ยนไปทีละขั้นจากจุดเรืองแสงมากเกินไปเป็นการเรืองแสงมากเกินไปทั้งบริเวณ จากนั้นเป็นการเรืองแสงน้อยเกินไปบางส่วน
โรคอักเสบและเนื้องอก
ม่านตาอักเสบ (MEWDS , APMPPE ฯลฯ)
มะเร็งเมลาโนมาคอรอยด์
เพื่อทำนายการดำเนินโรคของ GA ใช้การจำแนก IFAG (International FAF Classification Group) ซึ่งแบ่งเป็น 8 รูปแบบ (ปกติ, เปลี่ยนแปลงน้อยที่สุด, เพิ่มขึ้นเฉพาะจุด, เป็นหย่อม, เป็นเส้น, คล้ายลูกไม้, เป็นร่างแห, เป็นจุดด่าง) 6) .
อัตราการดำเนินโรคของแต่ละรูปแบบแสดงไว้ด้านล่าง 3) 6) :
รูปแบบ ลักษณะ อัตราการดำเนินโรค (มม.²/ปี) ไม่มี/น้อยที่สุด ไม่มีการเปลี่ยนแปลงที่ขอบ ช้าที่สุด การซึมกระจาย การเรืองแสงจุดกว้าง ประมาณ 2.61 เป็นหย่อม/เป็นแถบ เป็นหย่อมและเป็นแถบ ปานกลาง
การเรืองแสงต่ำในบริเวณ GA บ่งชี้ถึงการสูญเสีย RPE ในขณะที่การเรืองแสงสูงรอบข้างสะท้อนถึงการโตเกินของ RPE การเคลื่อนที่ของ RPE ที่หลุดลอก และการสะสมของมาโครฟาจ 3) .
Reticular pseudodrusen ตรวจพบได้ใน FAF เป็นจุดเรืองแสงต่ำขนาด 50–400 ไมโครเมตร และมีความไวมากกว่าการถ่ายภาพสีของจอตา 6) .
Q
โรคใดบ้างที่ FAF มีประโยชน์เป็นพิเศษ?
A
การติดตามการดำเนินของฝ่อทางภูมิศาสตร์ (GA) การวัดปริมาณการเรืองแสง (qAF) ในโรค Stargardt และการประเมินการหดตัวของวงแหวนเรืองแสงสูงในจอประสาทตา เสื่อมชนิด RP มีประโยชน์เป็นพิเศษ ทั้งหมดสามารถตรวจพบการเปลี่ยนแปลงโครงสร้างได้เร็วกว่า OCT และการถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน (FA ) ดูรายละเอียดใน “4. การอ่านผลปกติและผิดปกติ”
อุปกรณ์หลักสามประเภทใช้สำหรับการถ่ายภาพ FAF
ชนิด cSLO
กล้องตรวจตาเลเซอร์สแกนแบบคอนโฟคอล : รูเข็มคอนโฟคอลจะปิดกั้นแสงนอกโฟกัส ลดผลกระทบจากการเรืองแสงของเลนส์ตา7) 6) .
Spectralis (Heidelberg) : เลเซอร์สีน้ำเงิน 488 นาโนเมตร ฟิลเตอร์กั้น >500 นาโนเมตร 15-55 องศา ถ่ายภาพ OCT พร้อมกันและรองรับ NIR-AF7) .
Nidek Mirante : การกระตุ้น 490 นาโนเมตร 40-60 องศา7) .
ชนิดกล้องถ่ายภาพจอตา
แฟลชสีขาว + ฟิลเตอร์แบนด์พาส : ช่วยให้ถ่ายภาพมุมกว้างได้
Topcon TRC-50DX : การกระตุ้น 500–610 นาโนเมตร / 535–585 นาโนเมตร (ฟิลเตอร์ Spaide)7)
Zeiss Clarus : FAF แสงสีน้ำเงิน (BLFI), การกระตุ้น 435–585 นาโนเมตร, ครอบคลุม 133–200 องศา7)
มุมกว้างพิเศษ
Optos (Natus) : เลเซอร์สีเขียว 532 นาโนเมตร, ถ่ายภาพมุมกว้างพิเศษ 200 องศา สามารถใช้ได้โดยไม่ต้องขยายม่านตา (เส้นผ่านศูนย์กลางรูม่านตา ขั้นต่ำ 2 มม.)7) 6)
การตรวจหารอยโรคส่วนปลาย : มีประโยชน์ในการประเมินรอยโรคจอประสาทตา ส่วนปลายที่กล้องถ่ายภาพจอประสาทตา ทั่วไปไม่สามารถจับภาพได้
ข้อมูลจำเพาะของอุปกรณ์แต่ละเครื่องแสดงไว้ด้านล่าง7) :
อุปกรณ์ ความยาวคลื่นกระตุ้น มุมมองภาพ Spectralis 488 นาโนเมตร 15–55 องศา ออปโตส 532 นาโนเมตร 200 องศา ไซส์ คลารัส 435-585 นาโนเมตร 133-200 องศา
ในการถ่ายภาพ B-FAF (FAF แสงสีน้ำเงิน) มาตรฐาน ผู้ป่วยจะถูกจัดวางในเครื่องหลังจากขยายรูม่านตา (หรือไม่ขยาย) และถ่ายภาพที่โฟกัสดีที่สุดขณะตรวจสอบภาพสด ในประเภท cSLO อัตราส่วนสัญญาณต่อสัญญาณรบกวนจะดีขึ้นโดยการเฉลี่ยหลายเฟรม
การฟอกสีด้วยแสง (photobleaching) : สัญญาณ FAF สามารถเพิ่มขึ้นได้ประมาณ 30% โดยการให้แสงจ้าเป็นเวลาประมาณ 20 วินาทีก่อนถ่ายภาพ ซึ่งจะฟอกสีสารรับแสง2) 1) วิธีนี้ใช้ในการประเมินรอยโรคเฉียบพลัน เช่น MEWDS
FAF แสงสีเขียว (G-FAF )จอประสาทตา ส่วนกลางมีน้อย ทำให้ประเมินรอยบุ๋มจอตา ได้ดีเยี่ยม4) 6) ความสบายของผู้ป่วยก็สูงขึ้นด้วย
Q
เครื่องมือใดที่ใช้บ่อยที่สุด?
A
สำหรับการตรวจผู้ป่วยนอกมาตรฐาน ประเภท cSLO (เช่น Spectralis) แพร่หลายอย่างกว้างขวาง สำหรับการถ่ายภาพมุมกว้างพิเศษ เลือกใช้ Optos และสำหรับการประเมินรอยบุ๋มจอตา เลือกใช้อุปกรณ์ G-FAF ประเภท cSLO ที่สามารถถ่ายภาพพร้อมกันกับ OCT มีความแม่นยำในการจัดตำแหน่งสูงในการติดตามผล และเหมาะสำหรับการประเมินเชิงปริมาณ เช่น การวัดพื้นที่ GA4) 7) .
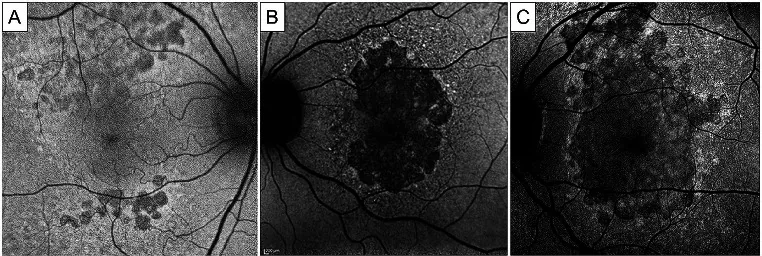
ภาพออโตฟลูออเรสเซนซ์ของจอประสาทตา Matteo Mario Carlà; Federico Giannuzzi; Francesco Boselli; Emanuele Crincoli; Stanislao Rizzo. Extensive macular atrophy with pseudodrusen-like appearance: comprehensive review of the literature. Graefes Arch Clin Exp Ophthalmol. 2024 Aug 12; 262(10):3085-3097. Figure 2. PM
CI D: PMC11458735. License: CC BY.
ภาพถ่ายออโตฟลูออเรสเซนซ์สีน้ำเงินของจอประสาทตา ในภาวะจอประสาทตา ฝ่อลุกลามร่วมกับซูโดดรูเซน (EMAP) แสดงรูปแบบการดำเนินโรคแบบคลาสสิก รอยโรคแบบพูกลดการเรืองแสงอัตโนมัติเห็นได้ในบริเวณรอบรอยบุ๋มจอตา โดยเฉพาะบริเวณรอบรอยบุ๋มจอตา ส่วนบน (A) รอยโรคหลายจุดเหล่านี้มีแนวโน้มรวมตัวกันเป็นแผ่นฝ่อสีเข้มขอบเขตชัดเจน ในระยะแรกไม่กระทบต่อรอยบุ๋มจอตา (B) ในระยะลุกลาม พื้นที่ฝ่อในแนวตั้งจะเกี่ยวข้องกับบริเวณจอประสาทตา และกระทบต่อรอยบุ๋มจอตา (C) สังเกตขอบที่เรืองแสงอัตโนมัติมากขึ้นซึ่งมองเห็นได้ที่ขอบของรอยโรคฝ่อ ได้รับความอนุเคราะห์จาก Antropoli และคณะ [41], Romano และคณะ [4] และ Vilela และคณะ [9]
ผลการตรวจปกติใน SW-AF (FAF ความยาวคลื่นสั้น / B-FAF ):
การเรืองแสงลดลงที่รอยบุ๋มจอตา : เนื่องจากรงควัตถุแซนโทฟิลล์ (รงควัตถุจอประสาทตา ) ดูดซับแสงสีน้ำเงิน รอยบุ๋มจอตา จึงแสดงการเรืองแสงลดลง6) 7) .การเรืองแสงต่ำของจานประสาทตา : เนื่องจากไม่มี RPE จึงทำให้เกิดการเรืองแสงต่ำ 7) .การเรืองแสงต่ำของหลอดเลือดจอตา : เลือดดูดซับแสง จึงแสดงการเรืองแสงต่ำ 7) .บริเวณที่มีการเรืองแสงมากที่สุด : บริเวณพาราฟอเวีย (5-15 องศาจากฟอเวีย) แสดงการเรืองแสงที่แรงที่สุด 6) .
ผลปกติในการตรวจ NIR-AF (การเรืองแสงอัตโนมัติย่านใกล้อินฟราเรด):
เนื่องจากฟอเวียมีความหนาแน่นของเมลานินสูง ในการตรวจ NIR-AF จึงแสดงเป็นบริเวณที่มีการเรืองแสงมากเกินไป 6) 7) . นี่คือความแตกต่างที่สำคัญจาก SW-AF.
สาเหตุของการเรืองแสงมากเกินไปและการเรืองแสงน้อยเกินไปและโรคที่เป็นตัวแทนแสดงไว้ด้านล่าง7) 1) 2) :
รูปแบบ สาเหตุหลัก โรคที่เป็นตัวแทน การเรืองแสงมากเกินไป การสะสมของ LF, การสูญเสียเม็ดสีจอประสาทตา , สารเรืองแสงใต้จอตา โรคสตาร์การ์ดท์, MEWDS , รอบ GA การเรืองแสงต่ำ ฝ่อของ RPE , การบดบังจากเลือดออก, พังผืด GA, เลือดออก, แผลเป็น
การจำแนกกลไกการเรืองแสงมากเกินไป:
กลไกการเกิดการเรืองแสงมากเกินไปแบ่งออกเป็นการเพิ่มขึ้นปฐมภูมิและการเพิ่มขึ้นทุติยภูมิ2) .
การเพิ่มขึ้นปฐมภูมิ : การผลิตบิสเรตินอยด์มากเกินไปเนื่องจากความผิดปกติของ ABCA4 และ RDH12 สอดคล้องกับโรค Stargardt และจอประสาทตา เสื่อมที่เกี่ยวข้องกับ RDH12.การเพิ่มขึ้นทุติยภูมิ : การสะสมของบิสเรตินอยด์ในทางเดินปลายน้ำอันเป็นผลจากความเสียหายของเซลล์รับแสง เกิดขึ้นทุติยภูมิหลังการตายของเซลล์รับแสง ใน RP หรือสาเหตุอื่นๆ
การแยกความแตกต่างจากการฟอกสีด้วยแสง : หากการเรืองแสงมากเกินไปหายไปหลังจากการฟอกสีด้วยแสง อาจเป็นการเรืองแสงมากเกินไปเทียมเนื่องจากการเรืองแสงของเม็ดสีที่รับแสง (โรดอปซิน)1) .
Q
การเรืองแสงมากเกินไปเป็นสิ่งที่ผิดปกติเสมอหรือไม่?
A
การเรืองแสงมากเกินไปอาจเกิดขึ้นได้จากการลดลงของเม็ดสีจอตา (อายุที่มากขึ้น การสัมผัสแสงแดด) หรือการฟอกสีด้วยแสง ควรตรวจสอบการเปลี่ยนแปลงโครงสร้างร่วมกับ OCT เพื่อแยกความแตกต่างจากการเรืองแสงมากเกินไปทางพยาธิวิทยาที่แท้จริง เนื่องจากลักษณะที่ปรากฏอาจแตกต่างกันระหว่างเครื่องมือ การใช้เครื่องมือเดียวกันในการเปรียบเทียบตามช่วงเวลาจึงมีความสำคัญ4) 7) .
การเรืองแสงเป็นปรากฏการณ์ที่โมเลกุลซึ่งดูดซับโฟตอนแล้วปล่อยโฟตอนพลังงานต่ำกว่าเมื่อกลับจากสถานะกระตุ้นสู่สถานะพื้น7) แสงที่ปล่อยออกมาจะมีความยาวคลื่นยาวกว่า (พลังงานต่ำกว่า) กว่าแสงที่ถูกดูดซับเสมอ (สโตกส์ชิฟต์)
เส้นทางการสร้างส่วนประกอบหลักของ LF คือ A2E มีดังนี้7) 2) :
การเปลี่ยนโครงสร้างด้วยแสงของ 11-cis-เรตินัล : all-trans-เรตินัลถูกสร้างขึ้นเมื่อรับแสงปฏิกิริยากับฟอสฟาทิดิลเอทานอลามีน (PE) : all-trans-เรตินัลควบแน่นกับ PE เกิดเป็น N-เรตินิลิดีน-PE (NRPE )NRPE → A2-GP E : ภายในเยื่อดิสก์ NRPE ทำปฏิกิริยากับโมเลกุล all-trans-เรตินัลตัวที่สอง เกิดเป็น A2-GP E (สารตั้งต้นของ A2E)การไฮโดรไลซิสของ A2-GP E → A2E : หลังจากการฟาโกไซโทซิสเยื่อดิสก์โดย RPE A2-GP E จะถูกไฮโดรไลซ์ในไลโซโซมเกิดเป็น A2E
บทบาทของ ABCA4 : ตัวขนส่ง ABCA4 ขนส่ง NRPE ไปยังด้านไซโทพลาสซึมของเยื่อดิสก์ ช่วยให้ถูกรีดิวซ์เป็น all-trans-เรตินอล2) การขาดการทำงานของ ABCA4 (สาเหตุของโรคสตาร์การ์ดท์) ทำให้ NRPE ค้างอยู่ในเยื่อดิสก์และเกิดการสะสมของบิสเรตินอยด์มากเกินไป
เมลานินเป็นสารเรืองแสงหลักสำหรับ NIR-AF (กระตุ้นที่ 787 นาโนเมตร) และกระจายอยู่ใน RPE และคอรอยด์ 7) 6) การลดลงของเมลานินตามอายุสังเกตได้จากการลดทอนสัญญาณ NIR-AF เมลาโนลิโปฟัสซิน (สารประกอบเชิงซ้อนของเมลานินและ LF) ก็มีส่วนทำให้เกิดสัญญาณ NIR-AF เช่นกัน
qAF คือค่าการเรืองแสงเชิงปริมาณที่ได้รับการแก้ไขโดยใช้สารอ้างอิงเรืองแสงภายใน (สารเรืองแสงมาตรฐานในคิวเวตต์) ภายใต้การกระตุ้นที่ 488 นาโนเมตร 2) 7) ค่า qAF แตกต่างกันไปตามอายุ ความเยื้องศูนย์ เพศ และเชื้อชาติ และการทำให้เป็นมาตรฐานยังคงเป็นความท้าทาย
FLIO เป็นเทคนิคที่วัดเส้นโค้งการสลายตัวของการเรืองแสง (อายุ) เฉพาะของสารเรืองแสงแต่ละชนิด และสามารถระบุชนิดของสารเรืองแสงได้นอกเหนือจากความเข้มของการเรืองแสง 6) 7) ปัจจุบัน การใช้งานส่วนใหญ่อยู่ในงานวิจัย
qAF กำลังถูกนำมาใช้เป็นจุดสิ้นสุดในการทดลองทางคลินิกสำหรับโรคจอประสาทตา ทางพันธุกรรม เช่น โรคสตาร์การ์ดท์และจอประสาทตา เสื่อมชนิดรงควัตถุ ซึ่งเป็นตัวบ่งชี้วัตถุประสงค์ของการดำเนินโรค 2) การกำหนดมาตรฐานของอุปกรณ์ที่ผ่านการสอบเทียบและโปรโตคอลการวัดยังคงเป็นความท้าทาย
ในการทดลองทางคลินิกสำหรับการรักษา GA ด้วย pegsetacoplan (APL-2) และ avacincaptad pegol (Zimura) การวัดพื้นที่ GA ด้วยภาพ FAF ถูกนำมาใช้เป็นจุดสิ้นสุดหลัก 4) B-FAF มีแนวโน้มที่จะประเมินพื้นที่ GA สูงเกินไป ในขณะที่ G-FAF รายงานว่าดีกว่าในการประเมินรอยโรคส่วนกลาง 4)
มีการรายงานแบบจำลองการตรวจจับจอประสาทตา เสื่อมตามอายุที่รวมภาพ FAF มุมกว้างพิเศษของ Optos กับอัลกอริทึมการเรียนรู้เชิงลึก ซึ่งช่วยให้ตรวจจับรอยโรคระยะเริ่มต้นได้ด้วยความไวสูง6)
ในการจำแนกประเภทโรคจอประสาทตา ทางพันธุกรรมโดยอัตโนมัติ มีรายงานว่าโครงข่ายประสาทเทียมสามารถแยกโรค Stargardt โรค Best และ RP ได้ด้วยความแม่นยำประมาณ 95%5)
G-FAF มีอิทธิพลจากเม็ดสีจอประสาทตา ส่วนโฟเวียน้อยกว่า และเหนือกว่าในการตรวจจับรอยโรคโฟเวียที่สังเกตได้ยากด้วย SW-AF4) นอกจากนี้ยังทำให้ผู้ป่วยรู้สึกแสบตาน้อยกว่า จึงสบายกว่า คาดว่าจะมีการใช้งานแพร่หลายในอนาคต
การถ่ายภาพอายุฟลูออเรสเซนซ์ (FLIO) แสดงรูปแบบฟลูออเรสเซนซ์เฉพาะโรคในจอประสาทตา เสื่อมตามอายุ โรคสตาร์การ์ดต์ และจอประสาทตาเสื่อมจากเบาหวาน และอาจตรวจจับการเปลี่ยนแปลงเมแทบอลิซึมก่อน FAF ที่ใช้ความเข้ม 7) .
ผ่านการถ่ายภาพหลายรูปแบบที่บูรณาการ FAF , OCT , OCT -A และ FA ระบบการวินิจฉัยที่เสริมข้อจำกัดของแต่ละวิธีการตรวจกำลังถูกสร้างขึ้น 4) .
Q
การพัฒนาในอนาคตของ FAF เป็นอย่างไร?
A
แนวโน้มหลักรวมถึงการติดตามโรคเชิงปริมาณผ่านการมาตรฐานของ qAF การวินิจฉัยอัตโนมัติด้วย AI และการเรียนรู้เชิงลึก (ความแม่นยำประมาณ 95% สำหรับโรคจอประสาทตา ทางพันธุกรรม) การประยุกต์ใช้ทางคลินิกของ FLIO และการแพร่กระจายของ G-FAF 5) 6) FAF ถูกนำมาใช้เป็นจุดสิ้นสุดหลักในการทดลองทางคลินิกของยารักษาจุดรับภาพเสื่อม และคาดว่าความสำคัญในการปฏิบัติทางจอประสาทตา จะเพิ่มขึ้นอีกในอนาคต 4) .
Mantovani A, Corbelli E, Sacconi R, et al. Blue-light fundus autofluorescence in inflammatory photoreceptor diseases. Diagnostics. 2023;13(14):2466.
Parmann R, Bhatt M, Sarraf D, et al. Primary versus secondary autofluorescence elevations in inherited retinal dystrophies. Int J Mol Sci. 2023;24(15):12327.
Curcio CA, Meleth AD, Gelman R, et al. FAF variation in geographic atrophy: clinicopathologic correlation. Invest Ophthalmol Vis Sci. 2025;66(1):49.
Ranetti AE, Ranetti MO, Pop A, et al. Blue-light and green-light fundus autofluorescence in age-related macular degeneration. Diagnostics. 2025;15(13):1688.
Oh J, Lee CS, Kim JM, et al. Fundus autofluorescence in inherited retinal disease. J Clin Med. 2025;14(7):2293.
Sahinoglu Kekek E, Sermet F. Fundus autofluorescence in dry age-related macular degeneration. Turk J Ophthalmol. 2021;51(3):169-176.
Pole C, Ameri H. Fundus autofluorescence and clinical applications. J Ophthalmic Vis Res. 2021;16(3):432-461.