จอประสาทตาเสื่อมจากเบาหวาน (DR) เป็นความผิดปกติของหลอดเลือดเล็กในจอประสาทตา ที่เกิดจากน้ำตาลในเลือดสูง เป็นสาเหตุอันดับสองของการสูญเสียการมองเห็น ที่เกิดขึ้นภายหลัง (ประมาณ 3,000 คนตาบอดต่อปี)
แบ่งเป็น 3 ระยะ: จอประสาทตา เสื่อมระยะง่าย, ระยะก่อนงอกใหม่, และระยะงอกใหม่ (การจำแนกประเภท Davis ที่ปรับปรุงแล้ว)
ภาวะจอประสาทตา บวมจากเบาหวาน (DME) สามารถเกิดขึ้นได้ในทุกระยะและเป็นสาเหตุที่พบบ่อยที่สุดของการมองเห็น ลดลง
เนื่องจากระยะแรกไม่มีอาการ การตรวจอวัยวะภายในตาเป็นประจำจึงสำคัญต่อการตรวจพบแต่เนิ่นๆ
ในทุกระยะ การจัดการระดับน้ำตาลในเลือด ความดันโลหิต และไขมันอย่างเป็นระบบเป็นพื้นฐาน เป้าหมาย HbA1c <7.0%
การรักษาทางเลือกแรกสำหรับ DME คือการรักษาด้วยยาต้าน VEGF (ranibizumab, aflibercept, faricimab ฯลฯ)
หลังจากระยะก่อนงอกใหม่ จะทำการจี้จอประสาทตา ทั่วทั้งจอ (PRP ) และในกรณีรุนแรงจะทำการผ่าตัดน้ำวุ้นตา
จอประสาทตาเสื่อมจากเบาหวาน (DR) เป็นความผิดปกติของหลอดเลือดเล็กในจอประสาทตา ที่เกิดจากความผิดปกติของเมแทบอลิซึมอันเนื่องมาจากน้ำตาลในเลือดสูง ซึ่งกระตุ้นให้เกิดไซโตไคน์และคีโมไคน์ต่างๆ ส่งผลให้เกิดรอยโรคที่อวัยวะภายในตาหลายรูปแบบ และเป็นหนึ่งในสามภาวะแทรกซ้อนหลักร่วมกับโรคเส้นประสาทจากเบาหวานและโรคไตจากเบาหวาน ในช่วงไม่กี่ปีที่ผ่านมา DR ถูกนิยามใหม่เป็น “โรคหลอดเลือดประสาท” แทนที่จะเป็นเพียงโรคหลอดเลือดเล็ก 2) .
เป็นสาเหตุอันดับสองของการสูญเสียการมองเห็น ที่เกิดขึ้นภายหลัง โดยมีผู้ป่วยประมาณ 3,000 คนตาบอดต่อปีจาก DR
ภาวะจอประสาทตา บวมจากเบาหวาน (DME) เป็นชนิดที่พบบ่อยที่สุดของจอประสาทตาเสื่อมจากเบาหวาน จอประสาทตาเสื่อมจากเบาหวานมีสามชนิด: จอประสาทตา บวม, จอประสาทตา ขาดเลือด, และโรคเยื่อบุผิวรงควัตถุจอประสาทตา จอประสาทตา บวมพบได้บ่อยที่สุดและเป็นสาเหตุสำคัญของการมองเห็น ลดลงทางคลินิก DME สามารถเกิดขึ้นได้ในทุกระยะของ DR พยาธิสรีรวิทยาของ DME มีความซับซ้อน เกี่ยวข้องกับหลายปัจจัย เช่น การซึมผ่านของหลอดเลือดเพิ่มขึ้น การไหลเวียนเลือดบกพร่องเนื่องจากการอุดตันของหลอดเลือด ความดันออสโมติกคอลลอยด์ลดลง และแรงดึงของเยื่อไฮยาลอยด์ด้านหลัง
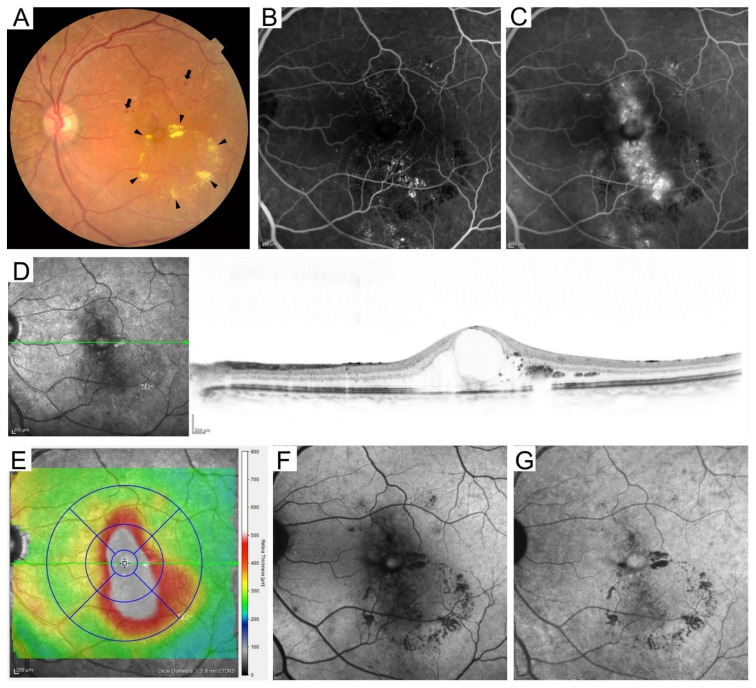
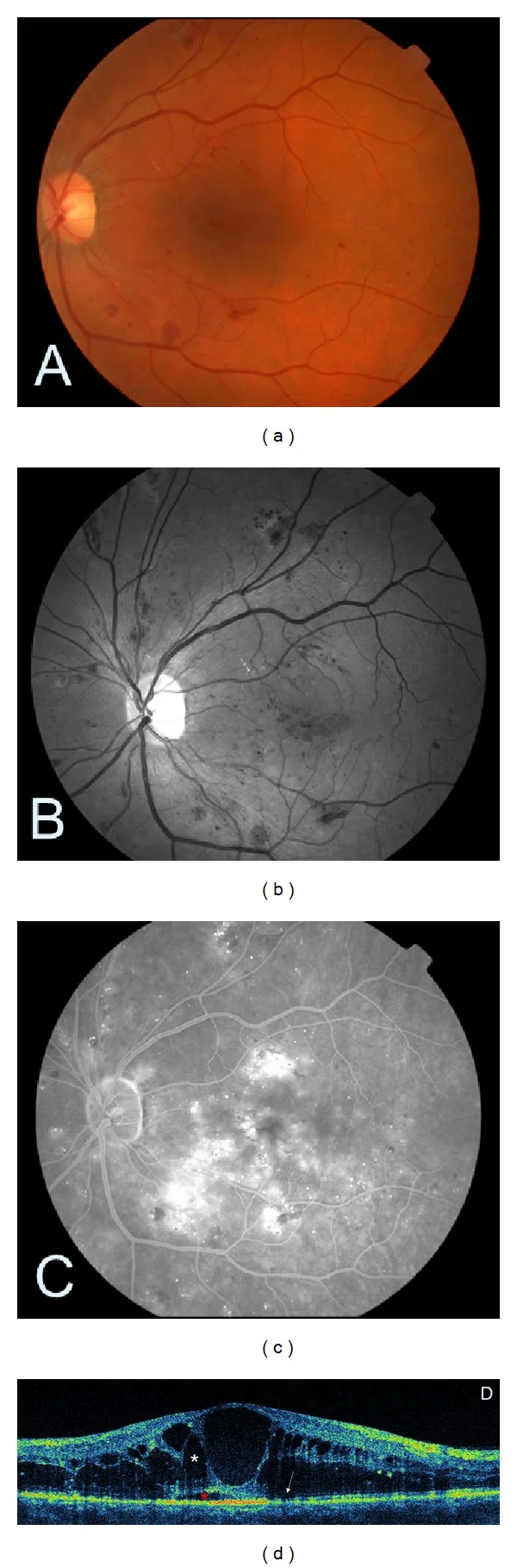
Medicina (Kaunas). 2023;59:896. Figure 1. PM
CI D: PMC10221113. License: CC BY.
ภาพถ่าย
จอประสาทตา แสดงเลือดออกในจอตาและจุดแข็ง (hard exudates) การตรวจ
ฟลูออเรสซีน แองจิโอกราฟี (
FA ) แสดงการรั่วของจุดรับภาพ (macula) และการตรวจออปติคอลโคฮีเรนซ์โทโมกราฟี (
OCT ) แสดงโพรงคล้ายถุงน้ำและจอตาหนาตัว การทำความเข้าใจ DME ควรเริ่มจากการเทียบเคียงภาพถ่าย
จอประสาทตา การตรวจหลอดเลือด และ
OCT ข้อมูลทางระบาดวิทยาที่สำคัญในประเทศญี่ปุ่นแสดงไว้ด้านล่าง1)
ผู้ป่วยเบาหวานชนิดที่ 2 ชาวญี่ปุ่น 976 ราย ติดตามเฉลี่ย 8.3 ปี: อุบัติการณ์ของ DR 3.98% ต่อปี
JDCS (1,221 ราย อายุเฉลี่ย 58.2 ปี HbA1c 8.2%) ติดตาม 8 ปี: อุบัติการณ์ของ DR 3.83% ต่อปี
JDCS 410 ราย: อัตราการดำเนินจาก NPDR เล็กน้อยไปเป็น NPDR รุนแรง/PDR 2.11% ต่อปี
ความชุกของ DR ในภูมิภาคเอเชียรวมถึงญี่ปุ่น 19.9%
ความชุกของ DR ในญี่ปุ่น 23.5% (NPDR เล็กน้อยถึงปานกลาง 18.5%, DME 3.7%)
ประมาณ 30% ของผู้ป่วย DM ชนิดที่ 2 มี DR อยู่แล้วเมื่อได้รับการวินิจฉัย
ในระดับโลก ผู้ป่วยเบาหวาน 34.6% (ประมาณ 93 ล้านคน) มี DR2) การประมาณการในปี 2020 รายงาน DR 103.12 ล้านราย, DR ที่คุกคามการมองเห็น (VTDR) 28.54 ล้านราย, และจอประสาทตา บวมที่มีนัยสำคัญทางคลินิก (CSME) 18.83 ล้านราย และคาดว่าจะเพิ่มขึ้นเป็น 160.5 ล้านรายในปี 20452) ใน DM ชนิดที่ 1 ประมาณ 90% เกิด DR หลังจากเริ่มป่วย 20 ปี11)
Q
จอประสาทตาเสื่อมจากเบาหวานเกิดขึ้นบ่อยแค่ไหน?
A
ในกลุ่มประชากรขนาดใหญ่ของญี่ปุ่น DR เกิดขึ้นด้วยความถี่ 3.8-4.0% ต่อปี และประมาณ 30% ของผู้ป่วย DM ชนิดที่ 2 มี DR อยู่แล้วเมื่อได้รับการวินิจฉัย1) ในระดับโลก ผู้ป่วยเบาหวาน 34.6% (ประมาณ 93 ล้านคน) มี DR2) และหลังจากเริ่มป่วย DM ชนิดที่ 1 20 ปี ประมาณ 90% เกิด DR11)
DR ในระยะเริ่มแรกมักดำเนินไปโดยไม่มีอาการ เมื่อมีอาการปรากฏ มักมีรอยโรคระดับปานกลางขึ้นไปอยู่แล้ว
การมองเห็น ลดลงจอประสาทตา บวมน้ำ (DME) หรือเลือดออกในน้ำวุ้นตา ภาพบิดเบี้ยว จอประสาทตา บวมลามไปถึงรอยบุ๋มจอตา จุดลอย : การปรากฏขึ้นอย่างกะทันหันของจุดลอยจำนวนมากเนื่องจากเลือดออกในน้ำวุ้นตา ข้อบกพร่องของลานสายตา : อาจเกิดจากจอตาลอกแบบดึงรั้ง, บริเวณที่ไม่มีเลือดไปเลี้ยงกว้าง, หรือหลังการจี้จอตาทั้งหมดการแคบลงของลานสายตาอย่างรวดเร็ว : อาจเกิดจากความดันลูกตา สูงมากเนื่องจากต้อหิน ชนิดเส้นเลือดใหม่ (NVG )
Q
อาการเริ่มแรกของจอประสาทตาเสื่อมจากเบาหวานคืออะไร?
A
ในระยะแรกแทบไม่มีอาการที่ผู้ป่วยรู้สึกได้ และโรคดำเนินไปโดยไม่มีอาการ เมื่อมีอาการเช่น การมองเห็น ลดลง จุดลอย หรือภาพบิดเบี้ยว มักมีรอยโรคระดับปานกลางถึงรุนแรง ดังนั้นเมื่อได้รับการวินิจฉัยว่าเป็นเบาหวาน จำเป็นต้องตรวจอวัยวะภายในตาเป็นระยะแม้ไม่มีอาการ
ด้านล่างนี้คือผลการตรวจอวัยวะภายในตาที่สำคัญตามระยะของโรค
จอประสาทตาเสื่อมชนิดไม่รุนแรง
โป่งพองของเส้นเลือดฝอย : อาการแสดงที่เร็วที่สุดของ DR ปรากฏเป็นจุดเรืองแสงมากเกินในการถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน
เลือดออกในจอตา : เลือดออกแบบจุดหรือรอยด่าง เกิดจากเม็ดเลือดแดงรั่วออกจากเส้นเลือดฝอย
ไขมันแข็ง : การรั่วของส่วนประกอบในพลาสมาเนื่องจากความสามารถในการซึมผ่านของหลอดเลือดเพิ่มขึ้น และการสะสมของไขมัน
จอประสาทตาเสื่อมก่อนระยะงอกใหม่
ไขมันอ่อน : จุดขาดเลือดเฉพาะที่เนื่องจากการขนส่งตามแนวแกนของเส้นใยประสาทตาผิดปกติ สะท้อนถึงภาวะจอตาขาดเลือด
การขยายตัวของหลอดเลือดดำแบบลูกปัดและการเกิดห่วง : ปรากฏติดกับบริเวณที่มีการอุดตันของหลอดเลือด
IRMA (ความผิดปกติของหลอดเลือดขนาดเล็กในจอประสาทตา ) : การเชื่อมต่อรอบบริเวณที่ไม่มีการไหลเวียนเลือด จุดที่แตกต่างจากเส้นเลือดใหม่คือไม่มีการรั่วซึมที่ชัดเจนในการตรวจฟลูออเรสซีน แองจิโอกราฟี
จอประสาทตาระยะ proliferative
เส้นเลือดใหม่ : ปรากฏบนจอประสาทตา และหัวประสาทตาเนื่องจากการผลิต VEGF มากเกินไปจากการอุดตันของหลอดเลือดฝอยเป็นบริเวณกว้าง การตรวจฟลูออเรสซีน แองจิโอกราฟีแสดงการรั่วซึมของฟลูออเรสซีน อย่างรุนแรง
เยื่อพังผืดหลอดเลือด proliferative : เกิดจากการเพิ่มจำนวนของเซลล์คล้ายไฟโบรบลาสต์รอบเส้นเลือดใหม่
จอประสาทตาลอก แบบดึงรั้งจอประสาทตา ร่วมกับการดึงรั้งของวุ้นตา หากเกี่ยวข้องกับจุดรับภาพ การพยากรณ์โรคทางสายตาไม่ดี
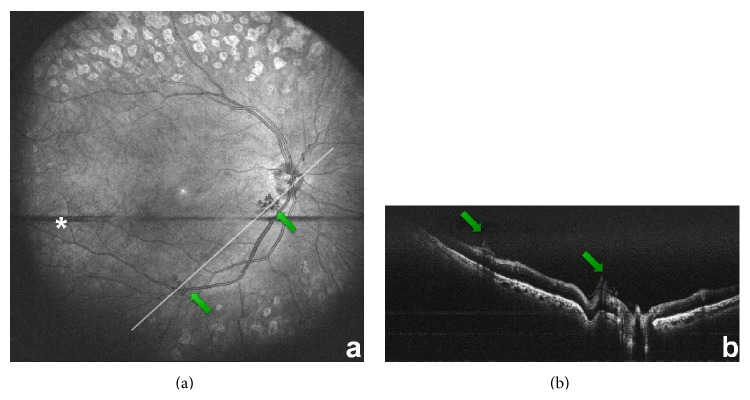
J Diabetes Res. 2015;2015:305084. Figure 5. PM
CI D: PMC4530264. License: CC BY.
ในจอประสาทตา เบาหวานระยะ proliferative เส้นเลือดใหม่ปรากฏรอบหัวประสาทตาและบนพื้นผิวจอประสาทตา เมื่อเปรียบเทียบภาพ en face มุมกว้างกับภาพตัดขวาง จะสามารถระบุได้ง่ายว่าเป็นรอยโรคพังผืดหลอดเลือดที่ยื่นออกมาบนพื้นผิวจอประสาทตา
NPDR ระดับรุนแรงถูกกำหนดโดย “กฎ 4-2-1” 2) กล่าวคือ มีอย่างน้อยหนึ่งข้อต่อไปนี้:
เลือดออกในจอประสาทตา 20 จุดขึ้นไปใน 4 จตุภาค
การขยายตัวของหลอดเลือดดำแบบลูกปัดชัดเจนใน 2 จตุภาคขึ้นไป
IRMA ชัดเจนใน 1 จตุภาคขึ้นไป
การจำแนก Fukuda แบบใหม่ 1) แบ่งเป็นชนิดไม่ร้าย (กลุ่ม A) และชนิดร้าย (กลุ่ม B)
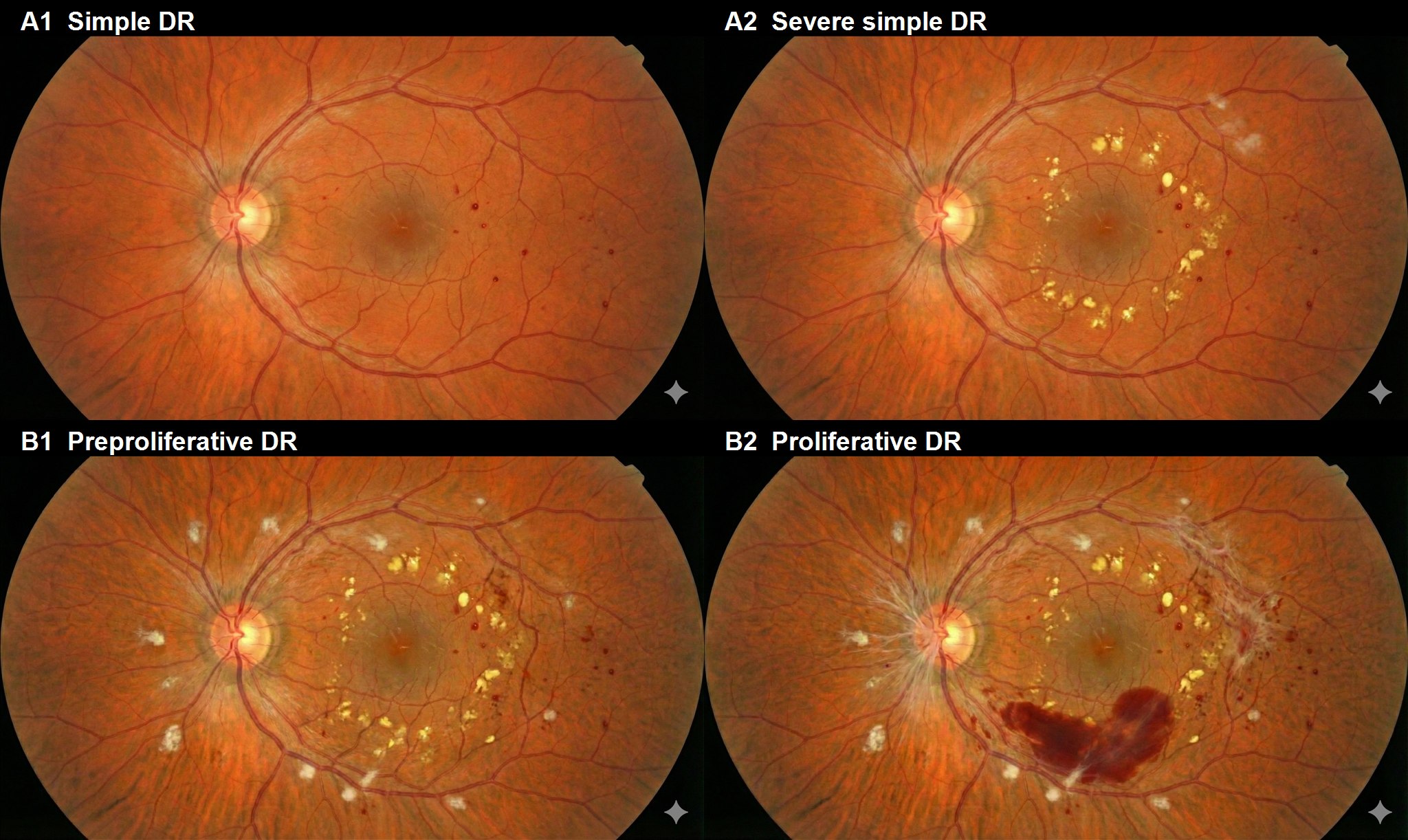
การจำแนก ระยะ ผลการตรวจ A1 ชนิดธรรมดาระดับเล็กน้อย หลอดเลือดฝอยโป่งพองและเลือดออกแบบจุด A2 ชนิดธรรมดาระดับรุนแรง เลือดออกแบบรอยเปื้อน สารคัดหลั่งแข็ง สารคัดหลั่งอ่อนจำนวนน้อย B1 ก่อนงอกใหม่ สารคัดหลั่งอ่อน เส้นเลือดดำขยาย IRMA NPA ในการถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน B2 งอกใหม่ระยะแรก เส้นเลือดใหม่ที่ไม่ติดต่อโดยตรงกับจานประสาทตา B3 งอกใหม่ระยะปานกลาง เส้นเลือดใหม่ที่ติดต่อโดยตรงกับจานประสาทตา B4 ระยะสุดท้ายของการเจริญเติบโตผิดปกติ เลือดออกในวุ้นตา / เลือดออกก่อนจอประสาทตา B5 ระยะสุดท้ายของการเจริญเติบโตผิดปกติ เนื้อเยื่อเจริญผิดปกติชนิดไฟโบรวาสคิวลาร์ A3–A5 การเจริญเติบโตผิดปกติหยุดนิ่ง เส้นเลือดใหม่เก่า / เลือดออกในวุ้นตา / เนื้อเยื่อเจริญผิดปกติ
เมื่อโรคสงบเป็นเวลามากกว่า 6 เดือนหลังการรักษา เรียกว่า จอประสาทตา เสื่อมชนิดเจริญผิดปกติหยุดนิ่ง เพิ่มรหัสภาวะแทรกซ้อน: M (รอยโรคที่จุดรับภาพ), D (จอประสาทตาลอก แบบดึงรั้ง), G (ต้อหิน ชนิดเส้นเลือดใหม่), N (โรคเส้นประสาทตา ขาดเลือด), P (การจี้แข็งด้วยแสง), V (การผ่าตัดวุ้นตา )
Dr.ぐらら(@eye_dr_game). X post. 2025-11-23. Google Nano Banana によるAI生成画像。投稿者許諾済み。
นี่คือภาพจำลอง
จอประสาทตา เพื่อการศึกษาของการจำแนกประเภทฟุกุดะแบบใหม่ A1, A2, B1, B2 ไม่ใช่ภาพผู้ป่วยจริง ดังนั้นการวินิจฉัยทำโดยการรวมภาพถ่าย
จอประสาทตา จริง,
OCT ,
FA /
OCTA และประวัติทางคลินิก
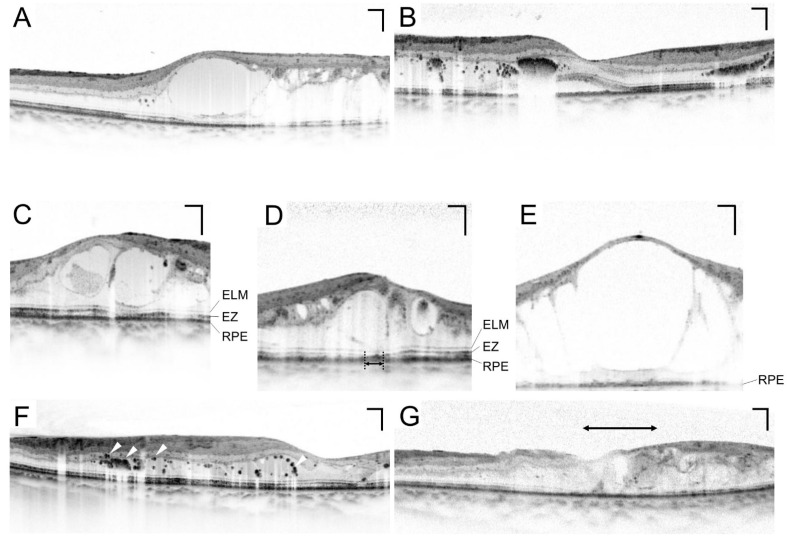
ภาพตัดขวาง OCT ของจอประสาทตา บวมน้ำประเมินโดยการรวมกันของสามรูปแบบพื้นฐาน: จอประสาทตา หนาตัวจอประสาทตา บวมน้ำแบบถุงน้ำจอประสาทตาลอก แบบมีน้ำใต้ชั้นจอประสาทตา
Medicina (Kaunas). 2023;59:896. Figure 5. PM
CI D: PMC10221113. License: CC BY.
ใน
การตรวจ OCT ของ DME จะพบการรวมกันของโพรงคล้ายถุงน้ำ
จอประสาทตา หลุดลอกชนิดมีน้ำขัง ความเสียหายของชั้นนอก และรอยโรคสะท้อนแสงสูง ความหนาของ
จอประสาทตา ไม่เพียงเท่านั้น ความสมบูรณ์ของเยื่อจำกัดชั้นนอกและโซนรูปไข่ยังสัมพันธ์กับการพยากรณ์
การมองเห็น อีกด้วย
ภาวะจอประสาทตา บวมน้ำที่มีนัยสำคัญทางคลินิก (CSME) ตามนิยามของ ETDRS คือข้อใดข้อหนึ่งต่อไปนี้ 2) :
ก. จอประสาทตา หนาขึ้นภายใน 500 ไมครอนจากรอยบุ๋มจอตา
ข. มีไขมันแข็งสีขาวภายใน 500 ไมครอนจากรอยบุ๋มจอตา ร่วมกับจอประสาทตา หนาขึ้นข้างเคียง
ค. จอประสาทตา หนาขึ้นตั้งแต่ 1 เท่าของพื้นที่หัวประสาทตาขึ้นไป และส่วนหนึ่งอยู่ภายใน 1500 ไมครอนจากรอยบุ๋มจอตา
ความหนาจอประสาทตา ส่วนกลาง ≥300 ไมครอนจากการตรวจ SD-OCT ถือเป็นเกณฑ์ของ DME ที่เกี่ยวข้องกับรอยบุ๋มจอตา (ตามเครื่อง: Spectralis 320/305 ไมครอน, Cirrus 305/290 ไมครอน, Stratus 250/250 ไมครอน, ชาย/หญิง) 1) การจำแนกระดับความรุนแรงของ DME ตามสากลมี 3 ระยะ: เล็กน้อย (จอประสาทตา หนาและไขมันแข็งห่างจากศูนย์กลางจอตา), ปานกลาง (ใกล้ศูนย์กลางแต่ไม่เกี่ยวข้องกับรอยบุ๋มจอตา ), และรุนแรง (เกี่ยวข้องกับรอยบุ๋มจอตา ) DME เพิ่มขึ้นตามการดำเนินของ NPDR โดยพบร่วมกับ NPDR เล็กน้อยร้อยละ 1.7–6.3 และ NPDR ปานกลางร้อยละ 20.3–63.2 1)
ปัจจัยเสี่ยงหลักที่เกี่ยวข้องกับการดำเนินของ DR มีดังนี้:
ปัจจัยเสี่ยง หลักฐานสำคัญ ระยะเวลาการเป็นโรค ปัจจัยเสี่ยงสูงสุด ผู้ป่วยเบาหวานชนิดที่ 2 ประมาณร้อยละ 30 มี DR อยู่แล้วเมื่อได้รับการวินิจฉัย 1) การควบคุมระดับน้ำตาล HbA1c <7.0% ป้องกันภาวะแทรกซ้อนทางหลอดเลือดเล็ก (Kumamoto Study) การลด HbA1c 1% → ลดความเสี่ยงภาวะแทรกซ้อนทางหลอดเลือดเล็กลงร้อยละ 37 (UKPDS ) 1) ความดันโลหิตสูง WESDR: ความดันซิสโตลิกเพิ่มขึ้น 10 มม.ปรอท → เพิ่มความเสี่ยง DR ระยะเริ่มต้นร้อยละ 10 และ DR ชนิดเพิ่มจำนวน/DME ร้อยละ 15 UKPDS : ลดลง 10 มม.ปรอท → ลดการดำเนินของ DR ร้อยละ 35 และลดการสูญเสียการมองเห็น ร้อยละ 47 1) ภาวะไขมันในเลือดผิดปกติ Fenofibrate (การศึกษา FIELD): ลดการเริ่มจี้จอตา 31%, ลด DR ชนิด增殖 30% และ DME 31% การศึกษา ACCORD Eye: ลดอัตราเสี่ยงต่อการลุกลามของ DR 40% 1) ความผิดปกติของไต โปรตีนในปัสสาวะและการลดลงของ GFR สัมพันธ์กับความชุกของ DR การมีโรคไต → เพิ่มความเสี่ยงต่อการลุกลามของ PDR 29% 1) การตั้งครรภ์ ไม่มี DR มาก่อน → การเกิด DR ระหว่างตั้งครรภ์ 8-33% มี NPDR มาก่อน → การแย่ลงระหว่างตั้งครรภ์ 10-67% 1) ภาวะน้ำตาลในเลือดต่ำรุนแรง อุบัติการณ์ของ DR เพิ่มขึ้นประมาณ 4 เท่า (JDCS) 1)
การควบคุมระดับน้ำตาลในเลือดอย่างเข้มงวดมีประสิทธิภาพในการป้องกันและยับยั้งการลุกลามของ DR จากการทดลองขนาดใหญ่หลายการศึกษา 1)
การศึกษา Kumamoto : HbA1c <7.0% (เทียบเท่า NGSP) ป้องกันภาวะแทรกซ้อนทางหลอดเลือดขนาดเล็กUKPDS : การลด HbA1c 1% ลดความเสี่ยงของภาวะแทรกซ้อนทางหลอดเลือดขนาดเล็ก 37%DCCT/EDIC : กลุ่มที่ได้รับการรักษาด้วยอินซูลินแบบเข้มข้นตั้งแต่แรกเริ่มยับยั้งการลุกลามของ DR และการเกิด DME อย่างมีนัยสำคัญในการติดตามระยะยาวJ-DOIT3 : กลุ่มที่ได้รับการแทรกแซงหลายปัจจัยลดความเสี่ยงต่อการลุกลามของ DRการศึกษา Steno-2 : การรักษาแบบเข้มข้นหลายปัจจัยลดความเสี่ยงต่อการลุกลามของ DR 58%
ในทางกลับกัน ในผู้ป่วยที่ควบคุมระดับน้ำตาลในเลือดได้ไม่ดีเป็นเวลานาน หากปรับปรุงระดับน้ำตาลอย่างรวดเร็ว อาจเกิดการแย่ลงชั่วคราวของ DR ที่เรียกว่า “early worsening” เนื่องจากการมองเห็น ลดลงยังคงอยู่ประมาณ 50% ของกรณี จึงควรปรับปรุงระดับน้ำตาลอย่างค่อยเป็นค่อยไป และการทำงานร่วมกับอายุรแพทย์เป็นสิ่งสำคัญ 1)
นอกจากนี้ เซลล์จอประสาทตา ที่เคยสัมผัสกับภาวะน้ำตาลในเลือดสูงจะเกิดการเปลี่ยนแปลงทางอีพีเจเนติกส์ (epigenetic changes) และเป็นที่รู้จักกันในชื่อ “ความจำทางเมตาบอลิก” (metabolic memory) ซึ่งรอยโรคยังคงอยู่และดำเนินต่อไปแม้ระดับน้ำตาลจะกลับสู่ปกติแล้ว 11) มีรายงานว่าการลดลงของ SOD2 และการเพิ่มเมทิลเลชันของดีเอ็นเอไมโตคอนเดรียเป็นกลไก
Fenofibrate : การศึกษา FIELD และ ACCORD Eye Study แสดงให้เห็นว่าสามารถยับยั้งความถี่ของการจี้ด้วยแสง และการดำเนินของ DR ได้อย่างมีนัยสำคัญ 1) Statin : ข้อมูลทะเบียนพบว่าความเสี่ยงของ DR ลดลง 40% เมื่อเทียบกับผู้ที่ไม่ได้รับประทาน 1) ยาที่ยับยั้ง RAS : ในการศึกษา DIRECT การให้ candesartan ทำให้ DR หายไป 34% มีรายงานว่ายายับยั้ง ACE มีประสิทธิภาพมากกว่า ARB 1) 9)
การรักษาระดับ HbA1c ต่ำกว่า 7.0% เป็นสิ่งสำคัญที่สุดในการป้องกันและชะลอการดำเนินของจอประสาทตาเสื่อมจากเบาหวาน การควบคุมความดันโลหิต (รับประทานยาลดความดันอย่างต่อเนื่อง) การเลิกบุหรี่ การรับประทานอาหารที่เน้นผัก ผลไม้ และปลา และการออกกำลังกายอย่างสม่ำเสมอก็มีประสิทธิภาพเช่นกัน แม้ไม่มีอาการ ควรตรวจอวัยวะภายในตาอย่างน้อยปีละครั้ง
Q
ควรควบคุม HbA1c ไว้ที่ระดับใดเพื่อยับยั้งการดำเนินโรค?
A
การตั้งเป้าหมาย HbA1c ต่ำกว่า 7.0% ป้องกันภาวะแทรกซ้อนทางหลอดเลือดขนาดเล็ก (การศึกษา Kumamoto) 1) การลด HbA1c ลง 1% ช่วยลดความเสี่ยงของภาวะแทรกซ้อนทางหลอดเลือดขนาดเล็กลง 37% (UKPDS ) 1) เนื่องจากเซลล์ที่เคยสัมผัสกับน้ำตาลในเลือดสูงยังคงมี “ความจำทางเมตาบอลิก” จึงจำเป็นต้องติดตามผลในระยะยาวแม้ระดับน้ำตาลจะกลับสู่ปกติแล้ว 11)
Sikorski et al. Mediators Inflamm. 2013;2013:434560. Figure 4. PM
CI D: PMC3863575. License: CC BY.
แม้ว่าภาพถ่าย
จอประสาทตา สีจะแสดงผลเพียงเล็กน้อย แต่ภาพ red-free และ
FA ทำให้เห็นเลือดออก
หลอดเลือดโป่งพองขนาดเล็ก และการรั่วซึมได้ชัดเจน
OCT ช่วยให้ประเมินอาการบวมน้ำชนิดซีสต์ที่เกี่ยวข้องกับ
รอยบุ๋มจอตา ได้โดยตรง ซึ่งเชื่อมโยงโดยตรงกับการตัดสินใจรักษา
วิธีการตรวจ การใช้หลัก หมายเหตุ การตรวจขยายรูม่านตา ดูจอประสาทตา (กล้องตรวจตาชนิดกลับภาพ/เลนส์วางหน้า) มาตรฐานทองคำในการจำแนกระยะของโรค หากไม่ขยายรูม่านตา จะจำแนกได้ถูกต้องเพียงประมาณ 50% 2) การตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด (Slit lamp)ประเมินความผิดปกติของกระจกตา , รูบิโอซิสของม่านตา , ต้อกระจก , การอักเสบในช่องหน้าลูกตา การสังเกตรายละเอียดของจอประสาทตา ส่วนกลางด้วยเลนส์วางหน้า การถ่ายภาพสีจอประสาทตา บันทึกข้อมูลเชิงวัตถุและเปรียบเทียบตามเวลา การถ่ายภาพ ETDRS 7 ทิศทาง สามารถบันทึกบริเวณรอบนอกด้วย SLO มุมกว้างพิเศษ 3) การตรวจหลอดเลือดด้วยฟลูออเรสซีน (FA ) ระบุบริเวณที่ไม่มีการไหลเวียนเลือด , หลอดเลือดใหม่, และจุดรั่วซึม แยกความแตกต่างระหว่าง DME แบบเฉพาะที่และแบบกระจาย ผลข้างเคียงทั้งหมดของ FA 1.1-11.2%, รุนแรง 0.005-0.48%, เสียชีวิต 0.0005-0.002% 1) การตรวจด้วยเครื่องเอกซเรย์การเชื่อมโยงกันด้วยแสง (OCT ) ประเมินปริมาณจอประสาทตา บวมน้ำและติดตามผล ความละเอียดเชิงลึกของ SD-OCT 5 ไมครอน ความหนาจอประสาทตา ส่วนกลาง ≥300 ไมครอน บ่งชี้ DME ที่รอยบุ๋มจอตา 1) OCTA ประเมินการรั่วของเส้นเลือดฝอย บริเวณที่ไม่มีการไหลเวียนเลือด (NPA) และเส้นเลือดใหม่โดยไม่ใช้สารทึบรังสี ไม่รุกราน สามารถวัดปริมาณ FA Z ได้ด้วย 3) การตรวจอัลตราซาวนด์ ประเมินความสัมพันธ์ระหว่างจอประสาทตา และวุ้นตา ในกรณีที่สื่อนำแสงขุ่น ระบุขอบเขตของจอประสาทตาลอก แบบดึงรั้งและตำแหน่งของเยื่อพังผืด การตรวจคลื่นไฟฟ้าจอประสาทตา (ERG ) การประเมินการทำงานของจอประสาทตา แบบปรนัย การหน่วงเวลาของคลื่น OP ปรากฏตั้งแต่ระยะแรกของ DR. ERG แบบลบ บ่งชี้การพยากรณ์การมองเห็น หลังผ่าตัดไม่ดี 1)
เบาหวานชนิดที่ 1 : ภายใน 5 ปีหลังการวินิจฉัย (การมองเห็น ลดลงก่อนวัยเจริญพันธุ์พบได้น้อย) 1) 2) เบาหวานชนิดที่ 2 : ตรวจตาเมื่อได้รับการวินิจฉัย (ประมาณ 30% เป็น DR แล้วเมื่อวินิจฉัย) 1) เบาหวานร่วมกับการตั้งครรภ์ : ตรวจตั้งแต่ไตรมาสแรก ติดตามทุก 3 เดือนระหว่างตั้งครรภ์ 1) เบาหวานขณะตั้งครรภ์ (GDM) : ไม่จำเป็นต้องตรวจตา 2)
ระยะ (การจำแนก Davis ที่ปรับปรุง) ช่วงเวลาที่แนะนำ เบาหวาน (ไม่มีจอประสาทตา เสื่อม) ปีละ 1 ครั้ง จอประสาทตาเสื่อมจากเบาหวานชนิดธรรมดา (NPDR เล็กน้อยถึงปานกลาง) ทุก 6 เดือน จอประสาทตาเสื่อมจากเบาหวานก่อนงอกใหม่ (NPDR รุนแรง) ทุก 2 เดือน จอประสาทตาเสื่อมจากเบาหวานชนิดงอกใหม่ เดือนละ 1 ครั้ง
AAO PPP แนะนำ NPDR รุนแรงทุก 3-4 เดือน ซึ่งแตกต่างเล็กน้อยจากค่าในตาราง GL3 1) 2)
การวินิจฉัยแยกโรคหลัก ได้แก่ จอประสาทตาเสื่อมจากความดันโลหิตสูง หลอดเลือดแดง/ดำจอประสาทตา อุดตัน โรคอีลส์ โรคโคตส์ โรคเลือด (โลหิตจาง มะเร็งเม็ดเลือดขาว โรคฮอดจ์กิน) จอประสาทตา เสื่อมจากอินเตอร์เฟอรอน จอประสาทตาเสื่อมจากรังสี โรคเพอร์ทเชอร์ โรคทาคายาสุ ม่านตาอักเสบ (โรคเบห์เซ็ต ซาร์คอยโดซิส SLE )
Q
ผู้ป่วยเบาหวานควรตรวจอวัยวะภายในตาครั้งแรกเมื่อใดหลังการวินิจฉัย?
A
ใน DM ชนิดที่ 2 ประมาณ 30% มี DR อยู่แล้วเมื่อวินิจฉัย ดังนั้นจึงแนะนำให้ตรวจอวัยวะภายในตาเมื่อวินิจฉัย 1) ใน DM ชนิดที่ 1 แนะนำให้ตรวจภายใน 5 ปีหลังวินิจฉัย 1) หากมีการตั้งครรภ์ร่วมด้วย ควรตรวจโดยเร็วที่สุดในไตรมาสแรก และจำเป็นต้องติดตามทุก 3 เดือนระหว่างตั้งครรภ์ 1)
การจัดการปัจจัยเสี่ยงทั่วร่างกายเป็นพื้นฐานของการป้องกันและยับยั้งการดำเนินของจอประสาทตาเสื่อมจากเบาหวาน (DR) และดำเนินต่อไปตลอดทุกระยะ
การควบคุมระดับน้ำตาลในเลือด : เป้าหมาย HbA1c น้อยกว่า 7.0% 1) การปรับปรุงอย่างรวดเร็วมีความเสี่ยงต่อการเสื่อมลงในช่วงแรก (early worsening)การควบคุมความดันโลหิต : UKPDS : การลดลง 10 mmHg ช่วยลดการดำเนินของ DR 35% และการสูญเสียการมองเห็น 47% 1) การจัดการไขมัน : Fenofibrate ลดอัตราเสี่ยงของการดำเนินของ DR ลง 40% (ACCORD Eye Study) 1) การรักษาแบบหลายปัจจัย : การศึกษา Steno-2 พบว่าลดความเสี่ยงของการดำเนินของ DR ลง 58% 1)
การรักษาด้วยยาต้าน VEGF
ทางเลือกแรก : การรักษามาตรฐานสำหรับ DME ที่เกี่ยวข้องกับรอยบุ๋มจอตา 1)
Ranibizumab (Lucentis) : 0.5 มก./0.05 มล. ฉีดเข้าแก้วตา ให้เดือนละครั้งจนกว่าการมองเห็น คงที่
Aflibercept 2 มก. (Eylea) : 2 มก./0.05 มล. 5 ครั้งแรกเดือนละครั้ง จากนั้นทุก 2 เดือน
Faricimab (Vabysmo) : 6 มก./0.05 มล. แอนติบอดีแบบคู่จำเพาะต่อต้าน VEGF และต้าน Ang-2 ในการทดลอง YOSEMITE/RHINE ผู้ป่วย 50-70% รักษาช่วงห่าง 12-16 สัปดาห์ 9)
Brolucizumab (Beovu) : 6 มก./0.05 มล. น้ำหนักโมเลกุล 26 kDa ในการทดลอง KESTREL/KITE ผู้ป่วยมากกว่า 50% รักษาช่วงห่าง q12w 5)
สูตรการให้ซ้ำ : สามวิธี: PRN (ให้ตามความจำเป็น), การให้แบบคงที่, TAE (treat and extend) 1)
การรักษาด้วยสเตียรอยด์
Triamcinolone acetonide (MacuAid) : ฉีดเข้าแก้วตา 4 มก./0.1 มล. ใช้ในกรณีดื้อต่อ anti-VEGF หรือฉีดใต้ Tenon capsule 1) .
Dexamethasone implant (Ozurdex ) : ชนิดปลดปล่อยช้า พิจารณาในตาปลอมเลนส์หรือตอบสนองต่อ anti-VEGF ไม่ดี 5) 2) .
ข้อควรระวัง : ความเสี่ยงต่อการลุกลามของต้อกระจก (ในตาที่ยังมีเลนส์ธรรมชาติ) และความดันลูกตา สูง
การจี้จอตาด้วยเลเซอร์ (DME)
ข้อบ่งชี้ : ทางเลือกสำหรับ DME ที่ไม่เกี่ยวข้องกับรอยบุ๋มจอตา 1) .
การจี้โดยตรง : ฉายแสงโดยตรงที่หลอดเลือดโป่งพองขนาดเล็ก ที่เป็นแหล่งรั่ว
การจี้แบบตาราง : ฉายแสงบริเวณที่มีการรั่วแบบกระจายหรือขาดเลือด
วิธี ETDRS ดัดแปลง : หลีกเลี่ยงการฉายแสงภายใน 500 ไมครอนจากศูนย์กลางจอตา ทำด้วยพลังงานต่ำและระยะห่างกว้าง 1) .
คำเตือน : ความเสี่ยงต่อ atrophic creep (การขยายของแผลเป็น) และพังผืดใต้จอตา 1) .
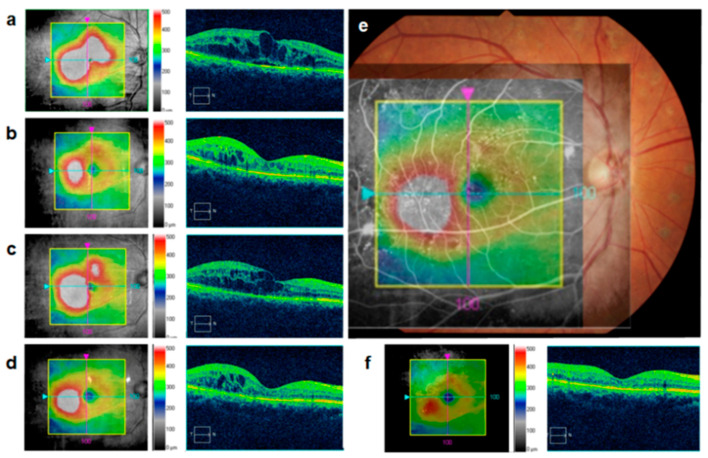
Medicina (Kaunas). 2023;59:435. Figure 4. PM
CI D: PMC10051835. License: CC BY.
อาจมีอาการบวมเฉพาะที่รอบหลอดเลือดโป่งพองขนาดเล็ก หลังการรักษาด้วย anti-VEGF การเปรียบเทียบแผนที่ OCT , ภาพตัดขวาง OCT และภาพถ่ายจอตาช่วยระบุบริเวณที่อาจต้องเลเซอร์เพิ่มเติมหรือปรับช่วงการรักษา
ชื่อยา (ชื่อการค้า) ขนาดยา ลักษณะเฉพาะ รานิบิซูแมบ (ลูเซนติส)0.5 มก./0.05 มล. ชิ้นส่วน Fab. ให้เดือนละครั้ง. ดำเนินต่อไปจนกว่าการมองเห็น จะคงที่ อะฟลิเบอร์เซปต์ 2 มก. (อายลีอา) 2 มก./0.05 มล. โปรตีนฟิวชันที่จับกับ VEGF-A/B และ PlGF. หลังจาก 5 ครั้งแรก ทุก 2 เดือน อะฟลิเบอร์เซปต์ 8 มก. (อายลีอา 8 มก.) 8 มก./0.07 มล. ขนาดสูง. ระยะห่างสูงสุด 16 สัปดาห์ 2) โบรลูซิซูแมบ (บีโอวู)6 มก./0.05 มล. น้ำหนักโมเลกุล 26 kDa. มากกว่า 50% ทุก 12 สัปดาห์. ระวังความเสี่ยงการอักเสบในลูกตา 5) 7) ฟาริซิแมบ (วาบิสโม)6 มก./0.05 มล. ต้าน VEGF + ต้าน Ang-2. ระยะห่างสูงสุด 16 สัปดาห์ 9)
ใน DME ที่เกี่ยวข้องกับโฟเวียซึ่งมีสายตาดี (20/25 หรือดีกว่า) การเลื่อนการรักษาออกไปจนกว่าสายตาจะลดลงเหลือ 20/30 หรือน้อยกว่าเป็นทางเลือกหนึ่ง 2)
การจี้แสงทั่วจอตา (PRP ) : จี้จอตาที่ขาดเลือดเพื่อลดการผลิต VEGF และทำให้เส้นเลือดงอกใหม่ฝ่อลง ทำใน PDR ความเสี่ยงสูงทุกราย 1) แนะนำเมื่อ NPA ≥3 ควอดแรนท์ 1) มาตรฐาน ETDRS : ระยะเวลา 0.2 วินาที, จุด 200 μm, กำลัง 200 mW 1) การจี้แสงจอตาแบบเลือกเฉพาะ : ระบุบริเวณ NPA ด้วย FA และจี้เฉพาะบริเวณนั้น มักทำใน DR ระยะก่อนงอกงาม 1) Anti-VEGF (PDR) : DRCR Protocol S แสดงให้เห็นว่าการฉีด ranibizumab เข้าแก้วตาไม่ด้อยกว่า PRP (ติดตาม 2 ปี) 2) อย่างไรก็ตาม การหยุดรักษามีความเสี่ยงที่เส้นเลือดงอกใหม่จะกลับมาเติบโตอีก จึงต้องมีการจัดการแบบผู้ป่วยนอกอย่างต่อเนื่องDRCR Protocol W : การให้ anti-VEGF เชิงป้องกันใน NPDR ป้องกันการเกิด PDR/DME แต่ผลลัพธ์ทางสายตาในระยะยาวเทียบเท่ากับการสังเกตเบื้องต้น 2) ข้อบ่งชี้การผ่าตัดวุ้นตา : จอตาลอกแบบดึงรั้งที่คุกคามจุดรับภาพ, แบบผสมที่มีรอยฉีกขาด, เลือดออกในวุ้นตา ที่ไม่หายหรือเป็นซ้ำ, ต้อหิน เส้นเลือดงอกใหม่ 1) การแพร่หลายของการผ่าตัดวุ้นตา แบบแผลเล็ก (MIVS) ช่วยลดการรุกราน การมองเห็น วุ้นตา ด้วย triamcinolone และการย้อม ILM ด้วย brilliant blue G (BBG) ช่วยเพิ่มความแม่นยำในการผ่าตัด
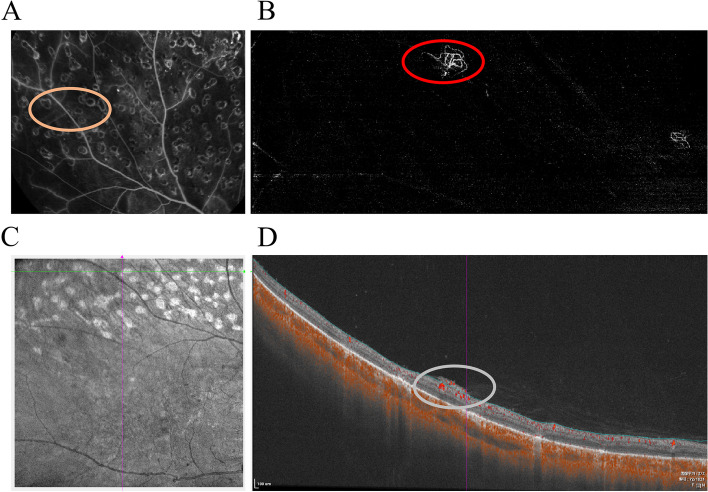
Yang et al. BMC Ophthalmol. 2023;23:315. Figure 3. PM
CI D: PMC10337091. License: CC BY.
ใน PDR หลัง
PRP ,
FA และ
OCTA มีประโยชน์ในการประเมินกิจกรรมของเส้นเลือดงอกใหม่ หลังให้ anti-VEGF การรั่วซึมและสัญญาณการไหลเวียนเลือดอาจลดลง ดังนั้นควรเปรียบเทียบภาพก่อนและหลังการรักษาในบริเวณเดียวกัน
Q
การเลือกใช้ยาต้าน VEGF ในการรักษา DME คืออะไร?
A
สำหรับ DME ที่เกี่ยวข้องกับรอยบุ๋มจอตา การรักษาด้วยยาต้าน VEGF เป็นทางเลือกแรก 1) ยา ranibizumab, aflibercept, faricimab และ brolucizumab ล้วนมีประสิทธิภาพ และ faricimab (สูงสุด q16w) และ brolucizumab (>50% q12w) ได้รับความสนใจเนื่องจากสามารถยืดระยะเวลาการให้ยาได้ 5) 9) หากผลของยาต้าน VEGF ไม่เพียงพอ ให้พิจารณาการรักษาด้วยสเตียรอยด์ โดยใช้ triamcinolone หรือการปลูกถ่าย dexamethasone 2)
ภาวะพยาธิสภาพพื้นฐานของ DR แบ่งออกเป็นสามประเภท: การเพิ่มการซึมผ่านของหลอดเลือด การอุดตันของหลอดเลือด และการสร้างหลอดเลือดใหม่ และระยะของจอประสาทตา เสื่อมแบบง่าย ก่อนงอกงาม และงอกงาม สอดคล้องกับภาวะพยาธิสภาพพื้นฐานเหล่านี้โดยประมาณ
ในภาวะน้ำตาลในเลือดสูง วิถีเมแทบอลิซึมหลักสี่ประการจะถูกกระตุ้น ทำให้เกิดความเสียหายต่อจอประสาทตา ผ่านความเครียดออกซิเดชันและการอักเสบ 11)
วิถี ผลิตภัณฑ์/การเปลี่ยนแปลงหลัก ความผิดปกติปลายน้ำหลัก วิถีโพลิออล การสะสมซอร์บิทอล การพร่อง NADPH → การลดลงของกลูตาไธโอน → การขยายความเครียดออกซิเดชัน การสร้าง AGEs การกระตุ้น RAGE ↑ NF -κB → ↑ VEGF, การตายของเซลล์เพอริไซต์แบบโปรแกรม การกระตุ้น PKC การกระตุ้น PKC-β การเพิ่มขึ้นของ VEGF และ Nox วิถีเฮกโซซามีน UDP-GlcNAc มากเกินไป การเพิ่มขึ้นของ TGF-β และ PAI-1
ทั้ง BRB ด้านใน (tight junction ของ endothelial เส้นเลือดฝอยจอตา) และ BRB ด้านนอก (tight junction ระหว่างเซลล์เยื่อบุผิวรงควัตถุจอตา) ถูกทำลาย 8) .
TNF -α → PKCζ → การลดลงของ claudin-5/ZO-1 → การสลาย BRB ด้านใน
IL-1β → การระดมเม็ดเลือดขาว → การสลาย BRB ด้านใน
CCL2 → การแทรกซึมของโมโนไซต์ → การหลั่ง VEGF และ TNF -α (feed-forward)
การสูญเสียเพอริไซต์: การเปลี่ยนแปลงที่เร็วที่สุดใน DR สาเหตุหลักคือการเหนี่ยวนำ apoptosis โดย AngII 9)
จอตาแสดง RAAS เฉพาะที่ซึ่งเป็นอิสระจากระบบไหลเวียนโลหิต 9) วิถีคลาสสิก (แกน ACE/AngII/AT1R) ส่งเสริมการตายของเพอริไซต์ การหยุดนิ่งของเม็ดเลือดขาว และการสลาย BRB ในขณะที่วิถีป้องกัน (แกน ACE2/Ang-(1-7)/Mas) ต้านฤทธิ์นี้ ความเข้มข้นของ AngII ในจอตาสูงกว่าในระบบไหลเวียน ในการทดลอง DIRECT การให้ candesartan ทำให้ DR หดตัวลง 34% 9) .
เซลล์จอประสาทตา ที่เคยสัมผัสกับภาวะน้ำตาลในเลือดสูงจะยังคงมีการเปลี่ยนแปลงทางอีพีเจเนติกส์แม้หลังจากระดับน้ำตาลในเลือดกลับสู่ปกติ (การยับยั้ง SOD2, การเพิ่มเมทิลเลชันของ DNA ไมโตคอนเดรีย) 11) กลไกที่รายงาน ได้แก่ การเพิ่มการผลิต ROS จากคอมเพล็กซ์ I/III ของสายโซ่ขนส่งอิเล็กตรอนในไมโตคอนเดรีย การแตกตัวของไมโตคอนเดรียมากเกินไปเนื่องจากความไม่สมดุลของ Drp1/OPA1 และการบกพร่องของการตอบสนองต่อสารต้านอนุมูลอิสระผ่าน Nrf2/KEAP1 และ SIRT1
DR ถูกนิยามใหม่ว่าเป็น “โรคทางระบบประสาทและหลอดเลือด” 2) และสามารถตรวจพบการบางลงของ GCI PL ด้วย OCT ก่อนที่รอยโรคหลอดเลือดจะปรากฏ 13) NF L จุดรับภาพจะบางลง 0.25 ไมโครเมตรต่อปี และ GCI PL จะบางลง 0.29 ไมโครเมตรต่อปี นอกจากนี้ยังยืนยันการเกิด gliosis ของเซลล์ Müller (GFA P เพิ่มขึ้น) และการกระตุ้นไมโครเกลีย Fractalkine (CX3CL1) ผลิตโดยเซลล์ปมประสาทจอประสาทตา และออกฤทธิ์ต่อตัวรับ CX3CR1 เพื่อให้เกิดฤทธิ์ต้านการอักเสบและปกป้องระบบประสาท 10)
ในผู้ป่วยเบาหวาน ความเข้มข้นของกลูโคสในวุ้นตา เพิ่มขึ้น และปฏิกิริยาไกลเคชันของเส้นใยคอลลาเจนดำเนินไป ระดับของไกลเคชันสัมพันธ์กับความรุนแรงของ DR และการเปลี่ยนแปลงโครงสร้างคอลลาเจนนำไปสู่การเหลว การหดตัวของคอร์เทกซ์วุ้นตา และการเกิดภาวะวุ้นตา หลุดลอกหลัง (PVD ) ได้ง่าย หากเกิด PVD สมบูรณ์โดยไม่มีแรงดึง การดำเนินไปสู่ DR ชนิด proliferative แทบจะไม่เกิดขึ้น ในทางกลับกัน PVD ไม่สมบูรณ์ (การยึดติดแน่นระหว่างวุ้นตา และเนื้อเยื่อ proliferative) ทำให้เกิดแรงดึงของวุ้นตา อย่างต่อเนื่อง ซึ่งง่ายต่อการเกิดจอประสาทตาลอก แบบ tractional และเลือดออกในวุ้นตา
Q
สามารถป้องกันเบาหวานขึ้นจอประสาทตาได้หรือไม่โดยการทำให้น้ำตาลในเลือดเป็นปกติ?
A
การควบคุมระดับน้ำตาลในเลือดมีความสำคัญที่สุดในการป้องกันและชะลอการดำเนินของ DR โดยมีเป้าหมาย HbA1c ต่ำกว่า 7.0% 1) อย่างไรก็ตาม ตามแนวคิด “ความจำทางเมตาบอลิก” เซลล์ที่เคยสัมผัสกับภาวะน้ำตาลในเลือดสูงยังคงมีการเปลี่ยนแปลงทางอีพีเจเนติกส์ และรอยโรคอาจคงอยู่หรือดำเนินต่อไปแม้หลังจากระดับน้ำตาลในเลือดกลับสู่ปกติ 11) การศึกษาติดตามผล DCCT/EDIC แสดงให้เห็นว่ากลุ่มที่ได้รับการรักษาแบบเข้มข้นตั้งแต่เนิ่นๆ สามารถยับยั้งการดำเนินของ DR ในระยะยาวได้
Aflibercept 8 มก. ได้รับการอนุมัติในปี 2023 สำหรับข้อบ่งชี้ DME และคาดว่าจะช่วยให้ระยะห่างในการให้ยานานถึง 16 สัปดาห์ 2) ในการศึกษา DRCR Protocol W การให้ยาต้าน VEGF เชิงป้องกันสำหรับ NPDR ชนิดรุนแรงช่วยป้องกันการเกิด PDR/DME แต่ผลลัพธ์ทางการมองเห็น ในระยะยาวเทียบเท่ากับการสังเกตในช่วงแรก 2)
LumineticsCore (เดิมชื่อ IDx-DR) เป็นระบบวินิจฉัยจอประสาทตา ด้วย AI แบบอัตโนมัติระบบแรกที่ได้รับการอนุมัติจาก FDA ในปี 2018 โดยไม่ต้องให้แพทย์ตีความ 3) โมเดลการเรียนรู้เชิงลึกรายงานความไว 96.8% และความจำเพาะ 87% 3) และระบบใหม่เช่น EyeArt และ AEYE-DS ก็กำลังได้รับการพัฒนา 2)
การให้เวกเตอร์ AAV ที่แสดง fractalkine ที่ละลายน้ำได้ (rAAV-sFKN) แสดงให้เห็นถึงการมองเห็น ที่ดีขึ้น การรั่วของไฟบรินลดลง และการทำให้ไมโครเกลียเป็นปกติ 10) มีกลไกป้องกันระบบประสาทและต้านการอักเสบที่แตกต่างจากการรักษาด้วย anti-VEGF
การทดลอง EUROCONDOR ระยะ II-III (NCT 01726075) ตรวจสอบยาหยอดตา somatostatin และ brimonidine แต่การวิเคราะห์โดยรวมไม่แสดงประสิทธิผล ในกลุ่มย่อยที่มีความผิดปกติของ mfERG พื้นฐาน พบว่าการดำเนินของความผิดปกติของระบบประสาทหยุดลง 13) ในการทดลองแบบสุ่มปกปิดสองทางเป็นเวลา 36 เดือนของยาหยอดตา citicoline + vitamin B12 มีรายงานการยับยั้งการดำเนินของโรคทั้งในด้านการทำงาน โครงสร้าง และหลอดเลือดใน DR ระดับเล็กน้อย 13)
miRNA ถือเป็น “ตัวควบคุมหลัก” ที่บูรณาการหลายแกนของพยาธิสภาพ DR (ความเครียดออกซิเดชัน การอักเสบ ระบบประสาทเสื่อม ความผิดปกติของหลอดเลือด) 14) มีการเสนอการยับยั้ง miR-195 เพื่อทำให้ SIRT1 คงที่ และการยับยั้งการแปลรหัส VEGF-A โดย miR-497a-5p; มี miRNA ประมาณ 350 ชนิดที่แสดงออกในจอประสาทตา และมากกว่า 86 ชนิดแสดงออกผิดปกติในแบบจำลอง DR
Metformin มีฤทธิ์หลายด้านผ่านการกระตุ้น AMPK: ต้านอนุมูลอิสระ ต้านการอักเสบ ต้านการสร้างหลอดเลือดใหม่ และป้องกันระบบประสาท การศึกษาเชิงสังเกตพบว่า aHR=0.29 สำหรับ STDR (DR ที่คุกคามการมองเห็น ) ในผู้ใช้ 12) อย่างไรก็ตาม ข้อมูล RCT สำหรับข้อบ่งชี้ทางจักษุวิทยายังไม่เพียงพอในปัจจุบัน
ยาต้าน MR ที่ไม่ใช่สเตียรอยด์ finerenone แสดงให้เห็นถึงการลดการแตกของ BRB การสร้างหลอดเลือดใหม่ และการอักเสบในแบบจำลองก่อนทางคลินิก; ความสำคัญของ MR ในฐานะเป้าหมายการรักษาอิสระสำหรับ DR กำลังอยู่ระหว่างการศึกษา 9)
日本糖尿病眼学会診療ガイドライン委員会. 糖尿病網膜症診療ガイドライン(第1版). 日眼会誌. 2020;124(12):955-981.
Flaxel CJ, Adelman RA, Bailey ST, et al. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024;131(1):P49-P130.
Huang Y, et al. Advances in diabetic retinopathy: epidemiology, pathogenesis, diagnosis, and treatment. Front Endocrinol. 2025;16:1664604.
Beuran DI, et al. Sterile endophthalmitis after intravitreal injection of triamcinolone acetonide. Rom J Ophthalmol. 2024;68(1):2-7.
Chakraborty D, et al. Off-label intravitreal brolucizumab for recalcitrant diabetic macular edema: a case series. Am J Ophthalmol Case Rep. 2021;24:101197.
Kikuchi Y, et al. Renal thrombotic microangiopathy induced by intravitreal aflibercept for diabetic macular edema. BMC Nephrology. 2022;23(1):348.
Hirano T, et al. Retinal arterial occlusive vasculitis after brolucizumab injection for diabetic macular edema. Am J Ophthalmol Case Rep. 2023;29:101788.
O’Leary F, Campbell M. The blood-retina barrier in health and disease. FEB S J. 2023;290(4):878-891.
Li X, et al. The role of the renin-angiotensin-aldosterone system in diabetic retinopathy: mechanisms and therapies. Arch Endocrinol Metab. 2024;68:e230292.
Lee CY, Yang CH. The role of fractalkine and its receptor CX3CR1 in diabetic retinopathy. Int J Mol Sci. 2025;26(1):378.
He W, et al. Oxidative stress and diabetic retinopathy: molecular mechanisms, pathological roles, and therapeutic implications. Front Immunol. 2025;16:1571576.
Alasbily H, et al. Metformin and diabetic retinopathy: a comprehensive review. Cureus. 2025;17(7):e87455.
Bianco L, Arrigo A, Aragona E, et al. Neuroinflammation and neurodegeneration in diabetic retinopathy. Front Aging Neurosci. 2022;14:937999.
Chen J, Zhang J, Li C, et al. Targeting microRNAs in diabetic retinopathy: from pathogenic mechanisms to therapeutic potentials. Front Endocrinol. 2025;16:1664604.