변성 및 위축성 질환

안저 자가형광(FAF)
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 안저 자가형광
섹션 제목: “1. 안저 자가형광”안저 자가형광(FAF)은 안저에 존재하는 천연 형광 물질을 빛으로 여기시켜 그 발광을 매핑하는 비침습적 영상 진단법입니다7). 형광안저혈관조영술(FA)과 달리 조영제 정맥 주사가 필요하지 않습니다7).
1995년, 인간 망막의 고유 형광 특성이 처음 보고되었습니다7). 이후 공초점 주사 레이저 검안경(cSLO)의 보급으로 임상 적용이 급속히 확대되었습니다.
주요 형광 물질
섹션 제목: “주요 형광 물질”FAF의 주요 형광단은 RPE 세포 내에 축적되는 리포푸신(LF)입니다7)6). LF는 광수용체 외절 원반막의 불완전한 리소좀 분해로 생성된 부산물이며, 최소 20종의 비스레티노이드 화합물을 포함합니다7).
주요 성분인 A2E(N-레티닐리덴-N-레티닐에탄올아민)는 청색광(최대 흡수 파장 약 470 nm)을 흡수하고 황록색광(600–610 nm)을 방출합니다6)7). A2E는 광산화를 통해 활성산소종(ROS)을 생성하여 막 불안정화와 세포자멸사를 유도합니다7).
각 비스레티노이드의 최대 흡수 파장은 다음과 같습니다7):
| 형광 물질 | 최대 흡수 파장 |
|---|---|
| A2E | 439 nm |
| A2PE | 449nm |
| isoA2E | 426nm |
| A2-DHP-PE | 490nm |
RPE 세포는 일생 동안 약 30억 개의 광수용체 외절 디스크를 탐식합니다6). 70세 이후에는 LF와 멜라노리포푸신이 RPE 세포질 부피의 약 25%를 차지할 때까지 축적됩니다6).
근적외선 자가형광(NIR-AF)은 약 787 nm의 빛으로 멜라닌을 주요 형광물질로 여기시킵니다7)6). 이를 통해 RPE 및 맥락막의 멜라닌 분포를 평가할 수 있습니다.
2. 적응증과 임상적 의의
섹션 제목: “2. 적응증과 임상적 의의”FAF는 다양한 망막 및 맥락막 질환의 진단과 경과 관찰에 사용됩니다.
혈관 및 대사 질환
염증성 및 종양성 질환
GA 주변 FAF 패턴과 진행 속도
섹션 제목: “GA 주변 FAF 패턴과 진행 속도”GA 진행 예측에는 IFAG(International FAF Classification Group) 분류가 사용되며, 8가지 패턴(정상, 미세 변화, 국소 증가, 반점형, 선형, 레이스형, 망상형, 점상형)으로 분류됩니다6).
각 패턴의 진행 속도는 다음과 같습니다3)6):
| 패턴 | 특징 | 진행 속도 (mm²/년) |
|---|---|---|
| 없음/최소 | 경계 변화 없음 | 가장 느림 |
| 미만성 점적 | 광범위한 점상 고형광 | 약 2.61 |
| 반점/띠 모양 | 반점/띠 모양 | 중등도 |
GA 부위의 저형광은 RPE 소실을 나타내며, 주변의 고형광은 RPE 비대, 탈락 RPE의 이동, 대식세포 축적을 반영합니다3).
망상 가성 드루젠은 FAF에서 50–400 μm의 저형광 반점으로 검출되며, 컬러 안저 사진보다 민감도가 높습니다6).
지도상 위축(GA)의 진행 모니터링, 스타가르트병의 형광 정량(qAF), 망막색소변성(RP)의 고형광 링 수축 평가가 특히 유용합니다. 이들은 OCT나 FA보다 구조 변화를 더 일찍 감지할 수 있습니다. 자세한 내용은 “4. 정상 소견과 이상 소견의 판독”을 참조하십시오.
3. 검사 절차와 촬영 방법
섹션 제목: “3. 검사 절차와 촬영 방법”장비 종류
섹션 제목: “장비 종류”FAF 촬영에는 크게 세 가지 장치가 사용됩니다.
cSLO형
안저 카메라형
백색 플래시 + 밴드패스 필터: 광시야 촬영 가능.
Topcon TRC-50DX: 500610 nm / 535585 nm (Spaide 필터) 여기 7).
Zeiss Clarus: 청색광 FAF (BLFI), 435585 nm 여기, 133200도 지원 7).
초광각형
Optos (Natus): 532 nm 녹색 레이저, 200도 초광각 촬영. 무산동 (최소 동공 직경 2 mm)으로 사용 가능 7)6).
말초 병변 검출: 일반 안저 카메라로 포착할 수 없는 주변 망막 병변 평가에 유용.
주요 장비 사양 비교
섹션 제목: “주요 장비 사양 비교”각 장비의 사양은 다음과 같습니다7):
| 장비 | 여기 파장 | 화각 |
|---|---|---|
| Spectralis | 488 nm | 15~55도 |
| Optos | 532 nm | 200도 |
| Zeiss Clarus | 435~585 nm | 133~200도 |
실제 촬영 방법
섹션 제목: “실제 촬영 방법”표준 B-FAF(청색광 FAF) 촬영에서는 환자의 동공을 산동한 후(또는 산동 없이) 장치에 고정하고, 라이브 영상을 확인하면서 최적 초점으로 촬영합니다. cSLO형에서는 여러 프레임의 평균 가산 처리를 통해 신호 대 잡음비를 향상시킵니다.
광표백(photobleaching) 처리: 촬영 전 약 20초간 강한 빛에 노출하여 시색소를 표백하면 FAF 신호를 약 30% 증가시킬 수 있습니다2)1). MEWDS 등의 급성기 병변 평가에 활용됩니다.
녹색광 FAF(G-FAF): 504/532 nm 여기로 촬영하는 방식으로, 황반 색소에 의한 흡수가 적어 중심와 평가에 우수합니다4)6). 환자의 편안함도 높습니다.
외래 표준 검사에는 cSLO형(Spectralis 등)이 널리 보급되어 있습니다. 초광각 촬영에는 Optos, 중심와 평가에는 G-FAF 지원 장치가 선택됩니다. OCT와 동시 촬영이 가능한 cSLO형은 경과 관찰 시 위치 정렬 정확도가 높아 GA 면적 측정 등의 정량 평가에 적합합니다4)7).
4. 정상 소견과 비정상 소견의 판독 방법
섹션 제목: “4. 정상 소견과 비정상 소견의 판독 방법”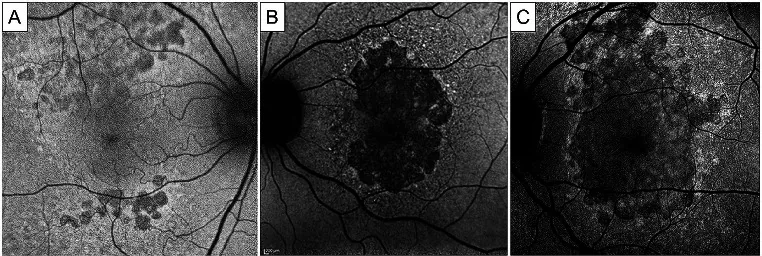
정상 소견
섹션 제목: “정상 소견”SW-AF(단파장 FAF, B-FAF)의 정상 소견:
- 중심와 저형광: 크산토필 색소(황반 색소)가 청색광을 흡수하기 때문에 중심와는 저형광을 나타냅니다6)7).
- 시신경 유두 저형광: RPE가 없어 저형광으로 나타납니다7).
- 망막 혈관 저형광: 혈액이 빛을 흡수하여 저형광을 보입니다7).
- 최대 형광 영역: 중심와에서 5~15도 떨어진 부중심와에서 가장 강한 형광을 보입니다6).
NIR-AF(근적외선 자가형광)의 정상 소견:
중심와는 멜라닌 밀도가 높아 NIR-AF에서는 오히려 과형광으로 나타납니다6)7). 이는 SW-AF와의 중요한 차이점입니다.
비정상 소견의 판독
섹션 제목: “비정상 소견의 판독”과형광 및 저형광의 원인과 대표 질환은 다음과 같습니다7)1)2):
| 패턴 | 주요 원인 | 대표 질환 |
|---|---|---|
| 과형광 | 리포푸신 축적, 황반 색소 소실, 망막하 형광 물질 | 스타가르트병, MEWDS, GA 주변 |
| 저형광 | RPE 위축, 출혈 차폐, 섬유화 | GA, 출혈, 반흔 |
과형광의 메커니즘 분류:
과형광의 발생 기전은 일차적 상승과 이차적 상승으로 분류됩니다2).
- 일차적 상승: ABCA4, RDH12 기능 이상으로 비스레티노이드가 과도하게 생성됩니다. 스타가르트병, RDH12 관련 망막 이영양증에 해당합니다.
- 이차적 상승: 광수용체 손상으로 인해 하류에서 비스레티노이드가 축적됩니다. RP 또는 다른 원인에 의한 광수용체 사멸에 이차적으로 발생합니다.
광표백과의 감별: 광표백 처리 후 과형광이 사라지면 시색소(로돕신)의 형광에 의한 가성 과형광일 가능성이 있습니다1).
황반 색소 감소(노화, 햇빛 노출)나 광표백에 의해서도 과형광이 나타날 수 있습니다. OCT와 병용하여 구조적 변화 유무를 확인하고 진정한 병적 과형광과 감별합니다. 또한 장비 간에 보이는 양상이 다를 수 있으므로 경시적 비교에는 동일한 장비를 사용하는 것이 중요합니다4)7).
5. 주의사항과 한계
섹션 제목: “5. 주의사항과 한계”6. 기술적 원리(리포푸신, 멜라닌, 형광단)
섹션 제목: “6. 기술적 원리(리포푸신, 멜라닌, 형광단)”형광의 물리학적 기초
섹션 제목: “형광의 물리학적 기초”형광은 광자를 흡수한 분자가 들뜬 상태에서 바닥 상태로 돌아갈 때 더 낮은 에너지의 광자를 방출하는 현상입니다7). 방출광은 항상 흡수광보다 긴 파장(낮은 에너지)을 가집니다(스토크스 이동).
리포푸신의 생화학적 형성 과정
섹션 제목: “리포푸신의 생화학적 형성 과정”LF의 주요 성분인 A2E의 형성 경로는 다음과 같습니다7)2):
- 11-시스-레티날의 광이성질화: 광수용으로 올-트랜스-레티날이 생성됩니다.
- 포스파티딜에탄올아민(PE)과의 반응: 올-트랜스-레티날이 PE와 축합하여 N-레티닐리덴-PE(NRPE)를 형성합니다.
- NRPE→A2-GPE: 디스크 막 내에서 NRPE가 두 번째 올-트랜스-레티날 분자와 반응하여 A2-GPE(A2E 전구체)를 형성합니다.
- A2-GPE의 가수분해→A2E: RPE에 의한 디스크 막 식균작용 후, 리소좀에서 A2-GPE가 가수분해되어 A2E가 생성됩니다.
ABCA4의 역할: ABC 수송체 ABCA4는 NRPE를 디스크 막의 세포질 쪽으로 수송하고, 올-트랜스-레티놀로의 환원을 촉진합니다2). ABCA4 기능 결핍(스타가르트병의 원인) 시 NRPE가 디스크 막 내에 머물러 비스레티노이드의 과잉 축적을 초래합니다.
멜라닌과 NIR-AF
섹션 제목: “멜라닌과 NIR-AF”멜라닌은 NIR-AF(787 nm 여기)의 주요 형광 물질이며, RPE 및 맥락막에 분포합니다7)6). 노화에 따른 멜라닌 감소는 NIR-AF 신호의 약화로 관찰됩니다. 멜라노리포푸신(멜라닌과 LF의 복합체)도 NIR-AF 신호에 기여합니다.
형광 정량(qAF)
섹션 제목: “형광 정량(qAF)”qAF는 488 nm 여기 하에서 내부 형광 기준(큐벳 내 표준 형광 물질)을 사용하여 보정된 정량적 형광 값입니다2)7). qAF 값은 연령, 편심도, 성별, 인종에 따라 변동하며, 표준화가 과제로 남아 있습니다.
형광 수명 이미징(FLIO)
섹션 제목: “형광 수명 이미징(FLIO)”FLIO는 각 형광 물질 고유의 형광 감쇠 곡선(수명)을 측정하는 기술로, 형광 강도뿐만 아니라 형광 물질의 종류를 식별할 수 있습니다6)7). 현재는 주로 연구 용도로 사용됩니다.
7. 최신 연구 및 향후 전망
섹션 제목: “7. 최신 연구 및 향후 전망”qAF의 임상 시험 평가변수로의 응용
섹션 제목: “qAF의 임상 시험 평가변수로의 응용”qAF는 Stargardt병, 망막색소변성증 등의 유전성 망막 질환에서 질병 진행의 객관적 지표로서 임상 시험의 평가변수에 채택되고 있습니다2). 보정된 장비와 측정 프로토콜의 표준화가 과제입니다.
GA 치료제 임상시험에서 FAF의 역할
섹션 제목: “GA 치료제 임상시험에서 FAF의 역할”pegcetacoplan(APL-2) 및 avacincaptad pegol(Zimura)을 사용한 GA 치료의 임상 시험에서는 FAF 영상을 통한 GA 면적 측정이 주요 평가변수로 채택되었습니다4). B-FAF는 GA 면적을 과대평가하는 경향이 있으며, G-FAF가 중심 병변 평가에 더 우수하다는 보고도 있습니다4).
AI 및 딥러닝을 통한 자동 분석
섹션 제목: “AI 및 딥러닝을 통한 자동 분석”Optos 초광각 FAF 이미지와 딥러닝 알고리즘을 결합한 연령 관련 황반변성 검출 모델이 보고되었으며, 높은 민감도로 조기 병변 검출이 가능하다고 알려져 있습니다6).
유전성 망막 질환의 자동 분류에서 신경망이 Stargardt병, Best병, RP를 약 95%의 정확도로 식별했다고 보고되었습니다5).
G-FAF의 임상 적용 확대
섹션 제목: “G-FAF의 임상 적용 확대”G-FAF는 중심와 황반 색소의 영향을 덜 받아 SW-AF로 관찰하기 어려운 중심와 병변 검출에 우수합니다4). 환자의 눈부심도 적어 편안함 측면에서 유리합니다. 향후 보급이 기대됩니다.
FLIO의 임상 적용
섹션 제목: “FLIO의 임상 적용”형광 수명 이미징(FLIO)은 연령 관련 황반변성, 스타가르트병, 당뇨 황반병증에서 질환 특이적 형광 수명 패턴을 보이며, 강도 기반 FAF보다 먼저 대사 변화를 감지할 가능성이 있습니다7).
다중 모달 이미징 통합
섹션 제목: “다중 모달 이미징 통합”FAF, OCT, OCT-A, FA를 통합한 다중 모달 이미징을 통해 각 검사 방법의 한계를 보완하는 진단 체계가 구축되고 있습니다4).
주요 전망으로는 qAF 표준화를 통한 정량적 질환 모니터링, AI 및 딥러닝을 이용한 자동 진단(유전성 망막 질환에서 약 95% 정확도), FLIO의 임상 적용, G-FAF의 보급이 있습니다5)6). 지리적 위축 치료제 임상시험에서 FAF가 주요 평가변수로 채택되었으며, 향후 망막 진료에서의 중요성은 더욱 높아질 것으로 예상됩니다4).
8. 참고문헌
섹션 제목: “8. 참고문헌”- Mantovani A, Corbelli E, Sacconi R, et al. Blue-light fundus autofluorescence in inflammatory photoreceptor diseases. Diagnostics. 2023;13(14):2466.
- Parmann R, Bhatt M, Sarraf D, et al. Primary versus secondary autofluorescence elevations in inherited retinal dystrophies. Int J Mol Sci. 2023;24(15):12327.
- Curcio CA, Meleth AD, Gelman R, et al. FAF variation in geographic atrophy: clinicopathologic correlation. Invest Ophthalmol Vis Sci. 2025;66(1):49.
- Ranetti AE, Ranetti MO, Pop A, et al. Blue-light and green-light fundus autofluorescence in age-related macular degeneration. Diagnostics. 2025;15(13):1688.
- Oh J, Lee CS, Kim JM, et al. Fundus autofluorescence in inherited retinal disease. J Clin Med. 2025;14(7):2293.
- Sahinoglu Kekek E, Sermet F. Fundus autofluorescence in dry age-related macular degeneration. Turk J Ophthalmol. 2021;51(3):169-176.
- Pole C, Ameri H. Fundus autofluorescence and clinical applications. J Ophthalmic Vis Res. 2021;16(3):432-461.
