変性・萎縮性疾患

眼底自発蛍光(FAF)
ひとめでわかるポイント
Sezione intitolata “ひとめでわかるポイント”1. 眼底自発蛍光とは
Sezione intitolata “1. 眼底自発蛍光とは”眼底自発蛍光(Fundus Autofluorescence; FAF)は、眼底に存在する天然蛍光物質(fluorophores)を光で励起し、その発光をマッピングする非侵襲的画像診断法である7)。フルオレセイン蛍光造影(FA)と異なり、造影剤の静脈注射を必要としない7)。
1995年、ヒト網膜の固有蛍光特性が初めて報告された7)。その後、共焦点走査型レーザー検眼鏡(cSLO)の普及により臨床応用が急速に広まった。
FAFの主要な蛍光団(fluorophore)はRPE細胞内に蓄積するリポフスチン(lipofuscin; LF)である7)6)。LFは視細胞外節ディスク膜の不完全なライソゾーム分解により生成される副産物であり、少なくとも20種のビスレチノイド化合物を含む7)。
主要成分であるA2E(N-レチニリデン-N-レチニルエタノールアミン)は青色光(ピーク約470 nm)を吸収し、黄緑色光(600〜610 nm)を放出する6)7)。A2Eは光酸化により活性酸素種(ROS)を生成し、膜の不安定化やアポトーシスを誘発する7)。
各ビスレチノイドの吸収極大は以下の通りである7):
| 蛍光物質 | 吸収極大 |
|---|---|
| A2E | 439 nm |
| A2PE | 449 nm |
| isoA2E | 426 nm |
| A2-DHP-PE | 490 nm |
RPE細胞は生涯で約30億個の視細胞外節ディスクを貪食する6)。70歳以降にはLFとメラノリポフスチンがRPE細胞質容積の約25%を占めるまで蓄積する6)。
近赤外自発蛍光(NIR-AF)では787 nm前後の光でメラニンを主蛍光物質として励起する7)6)。これによりRPEおよび脈絡膜のメラニン分布を評価できる。
2. 適応と臨床的意義
Sezione intitolata “2. 適応と臨床的意義”FAFは多岐にわたる網膜・脈絡膜疾患の診断・経過観察に用いられる。
Malattie vascolari e metaboliche
Retinopatia diabetica (DR): gli essudati duri appaiono iperfluorescenti, le emorragie ipofluorescenti, l’edema maculare cistoide (CME) iperfluorescente, utile per rilevare cambiamenti precoci.
Corioretinopatia sierosa centrale (CSC): nei casi persistenti, si evolve gradualmente da iperfluorescenza puntiforme a iperfluorescenza diffusa, fino a parziale ipofluorescenza.
Malattie infiammatorie e neoplastiche
GA周囲FAFパターンと進行速度
Sezione intitolata “GA周囲FAFパターンと進行速度”GAの進行予測にはIFAG(International FAF Classification Group)分類が用いられ、8パターンに分類される(normal, minimal change, focal increase, patchy, linear, lace-like, reticular, speckled)6)。
Di seguito sono riportate le velocità di progressione per ciascun pattern3)6):
| Pattern | Caratteristiche | Velocità di progressione (mm²/anno) |
|---|---|---|
| None/minimal | Nessun cambiamento al bordo | Più lento |
| Diffuse trickling | Iperfluorescenza puntiforme diffusa | Circa 2.61 |
| Patchy/banded | A chiazze/a bande | Moderato |
L’ipofluorescenza nelle aree di GA indica la perdita di RPE, mentre l’iperfluorescenza circostante riflette l’ipertrofia dell’RPE, la migrazione dell’RPE distaccato e l’accumulo di macrofagi3).
I reticoli pseudodrusen (pseudodrusen reticolari) vengono rilevati come macchie ipoflourescenti di 50-400 μm alla FAF, con una sensibilità maggiore rispetto alla fotografia a colori del fondo oculare 6).
Il monitoraggio della progressione dell’atrofia geografica (GA), la quantificazione della fluorescenza (qAF) nella malattia di Stargardt e la valutazione della contrazione dell’anello iperfluorescente nella retinite pigmentosa (RP) sono particolarmente utili. In tutti questi casi, la FAF può rilevare i cambiamenti strutturali prima dell’OCT e dell’FA. Per i dettagli, vedere «4. Lettura dei reperti normali e anomali».
3. Procedura dell’esame e metodo di acquisizione
Sezione intitolata “3. Procedura dell’esame e metodo di acquisizione”Tipi di apparecchiature
Sezione intitolata “Tipi di apparecchiature”Per l’acquisizione di FAF vengono utilizzati principalmente tre tipi di apparecchiature.
Tipo cSLO
Oftalmoscopio laser a scansione confocale: il foro stenopeico confocale blocca la luce fuori fuoco, riducendo l’influenza della fluorescenza del cristallino7)6).
Spectralis (Heidelberg): laser blu a 488 nm, filtro barriera >500 nm, 15-55 gradi. Supporta OCT simultaneo e NIR-AF7).
Nidek Mirante: eccitazione a 490 nm, 40-60 gradi7).
Tipo di camera fundus
Flash bianco + filtro passa-banda: consente l’acquisizione ad ampio campo.
Topcon TRC-50DX: eccitazione 500-610 nm / 535-585 nm (filtro Spaide) 7).
Zeiss Clarus: FAF a luce blu (BLFI), eccitazione 435-585 nm, copertura 133-200 gradi 7).
Ultra-grandangolo
Optos (Natus): laser verde 532 nm, ultra-grandangolo a 200 gradi. Utilizzabile senza dilatazione (diametro pupillare minimo 2 mm) 7)6).
Rilevamento di lesioni periferiche: utile per la valutazione di patologie retiniche periferiche non rilevabili con una normale fotocamera del fondo oculare.
Confronto delle specifiche dei principali dispositivi
Sezione intitolata “Confronto delle specifiche dei principali dispositivi”Le specifiche di ciascun dispositivo sono mostrate di seguito7):
| Dispositivo | Lunghezza d’onda di eccitazione | Angolo di campo |
|---|---|---|
| Spectralis | 488 nm | 15-55 gradi |
| Optos | 532 nm | 200 gradi |
| Zeiss Clarus | 435-585 nm | 133-200 gradi |
Esecuzione pratica della fotografia
Sezione intitolata “Esecuzione pratica della fotografia”Nell’acquisizione standard della B-FAF (FAF a luce blu), dopo aver dilatato la pupilla del paziente (o senza dilatazione), si fissa l’occhio allo strumento e si acquisisce l’immagine a fuoco ottimale controllando l’immagine in tempo reale. Nei sistemi cSLO, il rapporto segnale-rumore viene migliorato mediante la media di più fotogrammi.
Trattamento di fotosbiancamento (photobleaching): esponendo l’occhio a luce intensa per circa 20 secondi prima dell’acquisizione, si sbianca il fotopigmento, aumentando il segnale FAF di circa il 30%2)1). Viene utilizzato per la valutazione di lesioni acute come la MEWDS.
FAF a luce verde (G-FAF): modalità di acquisizione con eccitazione a 504/532 nm, che presenta minore assorbimento da parte del pigmento maculare e risulta superiore per la valutazione della fovea4)6). Offre anche maggiore comfort per il paziente.
Per gli esami standard ambulatoriali, i dispositivi cSLO (come Spectralis) sono ampiamente diffusi. Per la fotografia ultra-widefield si utilizza Optos, mentre per la valutazione della fovea si sceglie un apparecchio compatibile con G-FAF. I dispositivi cSLO, che consentono l’acquisizione simultanea di OCT, offrono un’elevata precisione di allineamento nei follow-up e sono adatti per valutazioni quantitative come la misurazione dell’area di GA4)7).
4. Lettura dei reperti normali e anomali
Sezione intitolata “4. Lettura dei reperti normali e anomali”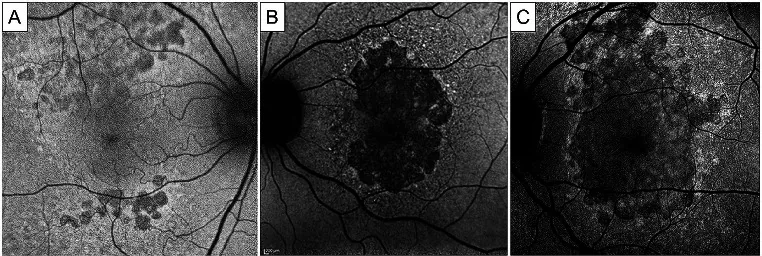
Reperti normali
Sezione intitolata “Reperti normali”Reperti normali in SW-AF (FAF a lunghezza d’onda corta, B-FAF):
- Ipofluorescenza foveale: la fovea mostra ipofluorescenza perché i pigmenti xantofillici (pigmento maculare) assorbono la luce blu6)7).
- Ipofluorescenza del disco ottico: il disco ottico appare ipofluorescente a causa dell’assenza di RPE7).
- Ipofluorescenza dei vasi retinici: il sangue assorbe la luce, quindi mostra ipofluorescenza7).
- Area di massima fluorescenza: l’area parafoveale a 5-15 gradi dalla fovea mostra la fluorescenza più intensa6).
Reperti normali nella NIR-AF (autofluorescenza nel vicino infrarosso):
A causa dell’elevata densità di melanina nella fovea, nella NIR-AF viene invece rappresentata come iperfluorescenza6)7). Questa è una differenza importante rispetto alla SW-AF.
Come interpretare i reperti anomali
Sezione intitolata “Come interpretare i reperti anomali”Le cause di iperfluorescenza e ipofluorescenza e le malattie rappresentative sono mostrate di seguito7)1)2):
| Pattern | Cause principali | Malattie rappresentative |
|---|---|---|
| Iperfluorescenza | Accumulo di LF, perdita di pigmento maculare, sostanza fluorescente sottoretinica | Malattia di Stargardt, MEWDS, intorno a GA |
| Ipofluorescenza | Atrofia dell’RPE, mascheramento da emorragia, fibrosi | GA, emorragia, cicatrice |
Classificazione dei meccanismi di iperfluorescenza:
Il meccanismo di insorgenza dell’iperfluorescenza è classificato in aumento primario e secondario2).
- Aumento primario: produzione eccessiva di bisretinoidi a causa di disfunzione di ABCA4 e RDH12. Corrisponde alla malattia di Stargardt e alla distrofia retinica associata a RDH12.
- Aumento secondario: accumulo di bisretinoidi a valle in seguito a danno dei fotorecettori. Secondario alla morte dei fotorecettori nella RP o per altre cause.
Differenziazione dal photobleaching: se l’iperfluorescenza scompare dopo il trattamento di photobleaching, potrebbe trattarsi di pseudo-iperfluorescenza dovuta alla fluorescenza del fotopigmento (rodopsina)1).
L’iperfluorescenza può manifestarsi anche in caso di riduzione del pigmento maculare (invecchiamento, esposizione solare) o photobleaching. È necessario verificare la presenza di alterazioni strutturali mediante OCT per differenziarla dalla vera iperfluorescenza patologica. Inoltre, poiché l’aspetto può variare tra diversi dispositivi, è importante utilizzare lo stesso apparecchio per i confronti nel tempo4)7).
5. Avvertenze e limiti
Sezione intitolata “5. Avvertenze e limiti”6. Principio tecnico (lipofuscina, melanina, fluorofori)
Sezione intitolata “6. Principio tecnico (lipofuscina, melanina, fluorofori)”Basi fisiche della fluorescenza
Sezione intitolata “Basi fisiche della fluorescenza”La fluorescenza è il fenomeno per cui una molecola che ha assorbito un fotone emette un fotone a energia inferiore quando torna dallo stato eccitato allo stato fondamentale7). La luce emessa ha sempre una lunghezza d’onda maggiore (energia inferiore) rispetto alla luce assorbita (spostamento di Stokes).
Processo biochimico di formazione della lipofuscina
Sezione intitolata “Processo biochimico di formazione della lipofuscina”La via di formazione del principale componente della LF, A2E, è la seguente7)2):
- Fotoisomerizzazione dell’11-cis-retinale: la fotorecezione produce all-trans-retinale.
- Reazione con la fosfatidiletanolammina (PE): l’all-trans-retinale si condensa con la PE formando N-retinilidene-PE (NRPE).
- NRPE→A2-GPE: all’interno della membrana del disco, l’NRPE reagisce con una seconda molecola di all-trans-retinale formando A2-GPE (precursore di A2E).
- Idrolisi di A2-GPE → A2E: dopo la fagocitosi delle membrane dei dischi da parte dell’RPE, l’A2-GPE viene idrolizzato nei lisosomi per formare A2E.
Ruolo di ABCA4: il trasportatore ABC ABCA4 trasporta NRPE sul lato citoplasmatico della membrana del disco, promuovendo la riduzione a tutto-trans-retinolo2). La carenza di ABCA4 (causa della malattia di Stargardt) porta all’accumulo eccessivo di bisretinoidi poiché NRPE rimane all’interno della membrana del disco.
Melanina e NIR-AF
Sezione intitolata “Melanina e NIR-AF”La melanina è il principale fluoroforo della NIR-AF (eccitazione a 787 nm) ed è distribuita nell’RPE e nella coroide7)6). La diminuzione della melanina con l’età si osserva come attenuazione del segnale NIR-AF. Anche la melanolipofuscina (complesso di melanina e LF) contribuisce al segnale NIR-AF.
Quantificazione della fluorescenza (qAF)
Sezione intitolata “Quantificazione della fluorescenza (qAF)”La qAF è un valore di fluorescenza quantitativo corretto utilizzando un riferimento di fluorescenza interna (sostanza fluorescente standard in una cuvetta) sotto eccitazione a 488 nm 2)7). Il valore qAF varia in base a età, eccentricità, sesso ed etnia, e la standardizzazione rimane una sfida.
Imaging della durata di fluorescenza (FLIO)
Sezione intitolata “Imaging della durata di fluorescenza (FLIO)”La FLIO è una tecnica che misura la curva di decadimento della fluorescenza (durata) specifica di ciascun fluoroforo, consentendo di identificare il tipo di fluoroforo oltre all’intensità di fluorescenza 6)7). Attualmente è utilizzata principalmente per la ricerca.
7. Ricerche recenti e prospettive future
Sezione intitolata “7. Ricerche recenti e prospettive future”Applicazione del qAF come endpoint negli studi clinici
Sezione intitolata “Applicazione del qAF come endpoint negli studi clinici”La qAF sta venendo adottata come endpoint in studi clinici per malattie retiniche ereditarie come la malattia di Stargardt e la retinite pigmentosa, in quanto indicatore oggettivo della progressione della malattia 2). La calibrazione degli strumenti e la standardizzazione dei protocolli di misurazione rimangono sfide.
Ruolo della FAF negli studi sui farmaci per il trattamento della GA
Sezione intitolata “Ruolo della FAF negli studi sui farmaci per il trattamento della GA”Negli studi clinici per il trattamento della GA con pegcetacoplan (APL-2) e avacincaptad pegol (Zimura), la misurazione dell’area di GA tramite immagini FAF è stata adottata come endpoint primario 4). È stato riportato che la B-FAF tende a sovrastimare l’area di GA, mentre la G-FAF è superiore nella valutazione delle lesioni centrali 4).
Analisi automatica tramite AI e deep learning
Sezione intitolata “Analisi automatica tramite AI e deep learning”È stato riportato un modello di rilevamento della degenerazione maculare legata all’età che combina immagini FAF ultra-widefield Optos con algoritmi di deep learning, consentendo il rilevamento precoce delle lesioni con elevata sensibilità 6).
Nella classificazione automatica delle malattie retiniche ereditarie, è stato riportato che una rete neurale ha identificato la malattia di Stargardt, la malattia di Best e la RP con una precisione di circa il 95% 5).
Espansione dell’applicazione clinica della G-FAF
Sezione intitolata “Espansione dell’applicazione clinica della G-FAF”La G-FAF è meno influenzata dal pigmento maculare foveale e risulta superiore nel rilevamento delle lesioni foveali difficili da osservare con SW-AF 4). Provoca anche meno abbagliamento per il paziente, risultando vantaggiosa in termini di comfort. Ci si aspetta una sua diffusione in futuro.
Applicazioni cliniche della FLIO
Sezione intitolata “Applicazioni cliniche della FLIO”L’imaging a fluorescenza lifetime (FLIO) mostra pattern di fluorescenza lifetime specifici della malattia nella degenerazione maculare legata all’età, nella malattia di Stargardt e nella maculopatia diabetica, e potrebbe rilevare cambiamenti metabolici prima della FAF basata sull’intensità 7).
Integrazione dell’imaging multimodale
Sezione intitolata “Integrazione dell’imaging multimodale”L’imaging multimodale che integra FAF, OCT, OCT-A e FA sta costruendo un sistema diagnostico in cui i limiti di ciascun esame vengono compensati reciprocamente 4).
Le principali prospettive sono: il monitoraggio quantitativo delle malattie tramite la standardizzazione della qAF, la diagnosi automatica con AI e deep learning (circa 95% di accuratezza per le malattie retiniche ereditarie), l’applicazione clinica della FLIO e la diffusione della G-FAF5)6). La FAF è stata adottata come endpoint primario negli studi clinici per i farmaci contro l’atrofia geografica (GA), e si prevede che la sua importanza nella pratica retinica aumenterà ulteriormente4).
8. Riferimenti
Sezione intitolata “8. Riferimenti”- Mantovani A, Corbelli E, Sacconi R, et al. Blue-light fundus autofluorescence in inflammatory photoreceptor diseases. Diagnostics. 2023;13(14):2466.
- Parmann R, Bhatt M, Sarraf D, et al. Primary versus secondary autofluorescence elevations in inherited retinal dystrophies. Int J Mol Sci. 2023;24(15):12327.
- Curcio CA, Meleth AD, Gelman R, et al. FAF variation in geographic atrophy: clinicopathologic correlation. Invest Ophthalmol Vis Sci. 2025;66(1):49.
- Ranetti AE, Ranetti MO, Pop A, et al. Blue-light and green-light fundus autofluorescence in age-related macular degeneration. Diagnostics. 2025;15(13):1688.
- Oh J, Lee CS, Kim JM, et al. Fundus autofluorescence in inherited retinal disease. J Clin Med. 2025;14(7):2293.
- Sahinoglu Kekek E, Sermet F. Fundus autofluorescence in dry age-related macular degeneration. Turk J Ophthalmol. 2021;51(3):169-176.
- Pole C, Ameri H. Fundus autofluorescence and clinical applications. J Ophthalmic Vis Res. 2021;16(3):432-461.
