变性和萎缩性疾病

眼底自发荧光(FAF)
一目了然的要点
Section titled “一目了然的要点”1. 眼底自发荧光
Section titled “1. 眼底自发荧光”眼底自发荧光(Fundus Autofluorescence; FAF)是一种非侵入性成像诊断方法,通过光激发眼底存在的天然荧光物质并绘制其发光图7)。与荧光素眼底血管造影(FA)不同,它不需要静脉注射造影剂7)。
1995年,人类视网膜的固有荧光特性首次被报道7)。随后,随着共焦扫描激光检眼镜(cSLO)的普及,临床应用迅速扩大。
主要荧光物质
Section titled “主要荧光物质”FAF的主要荧光团是积聚在RPE细胞内的脂褐素(LF)7)6)。LF是感光细胞外节盘膜不完全溶酶体降解的副产物,包含至少20种双视黄醛化合物7)。
主要成分A2E(N-视黄基亚基-N-视黄基乙醇胺)吸收蓝光(峰值约470 nm),发射黄绿光(600–610 nm)6)7)。A2E通过光氧化产生活性氧(ROS),导致膜不稳定和细胞凋亡7)。
各双视黄醛化合物的吸收峰值如下7):
| 荧光物质 | 吸收峰值 |
|---|---|
| A2E | 439 nm |
| A2PE | 449纳米 |
| isoA2E | 426纳米 |
| A2-DHP-PE | 490纳米 |
RPE细胞在一生中吞噬约30亿个感光细胞外节盘膜6)。70岁以后,LF和黑色素脂褐素积累至约占RPE细胞质体积的25%6)。
近红外自发荧光(NIR-AF)使用约787 nm的光激发黑色素作为主要荧光物质7)6)。这可以评估RPE和脉络膜中的黑色素分布。
2. 适应症与临床意义
Section titled “2. 适应症与临床意义”FAF用于多种视网膜和脉络膜疾病的诊断和随访。
血管和代谢性疾病
糖尿病视网膜病变(DR):硬性渗出呈高荧光,出血呈低荧光,囊样黄斑水肿(CME)呈高荧光,有助于检测早期变化。
中心性浆液性脉络膜视网膜病变(CSC):在迁延病例中,从点状高荧光逐渐变为弥漫性高荧光,再变为部分低荧光。
炎症性和肿瘤性疾病
GA周围FAF模式与进展速度
Section titled “GA周围FAF模式与进展速度”GA进展预测采用IFAG(国际FAF分类组)分类,分为8种模式(正常、微小变化、局灶性增强、斑片状、线状、花边状、网状、斑点状)6)。
各模式的进展速度如下所示3)6):
| 模式 | 特征 | 进展速度(mm²/年) |
|---|---|---|
| 无/轻微 | 边界无变化 | 最慢 |
| 弥漫性滴流 | 广泛点状高荧光 | 约2.61 |
| 斑片状/带状 | 斑片状/带状 | 中等 |
GA区域的低荧光表示RPE丧失,周围的高荧光反映RPE肥大、脱落RPE的迁移和巨噬细胞聚集3)。
网状假性玻璃膜疣在FAF上表现为50–400 μm的低荧光斑点,比彩色眼底照片更敏感6)。
地图状萎缩(GA)的进展监测、Stargardt病的荧光定量(qAF)、视网膜色素变性(RP)的高荧光环收缩评估特别有用。这些可能比OCT或FA更早检测到结构变化。详见“4. 正常所见与异常所见的解读”。
3. 检查步骤与拍摄方法
Section titled “3. 检查步骤与拍摄方法”FAF成像主要使用三种设备。
cSLO型
共焦扫描激光检眼镜:通过共焦针孔阻挡离焦光线,减少晶状体荧光的影响7)6)。
Spectralis(Heidelberg):488 nm蓝色激光,>500 nm屏障滤光片,15–55度。支持OCT同步成像和NIR-AF7)。
Nidek Mirante:490 nm激发,40–60度7)。
眼底相机型
白色闪光+带通滤光片:可进行广角拍摄。
Topcon TRC-50DX:500610 nm / 535585 nm(Spaide滤光片)激发7)。
Zeiss Clarus:蓝光FAF(BLFI),435585 nm激发,支持133200度7)。
超广角型
Optos(Natus):532 nm绿色激光,200度超广角拍摄。可在无散瞳(最小瞳孔直径2 mm)下使用7)6)。
周边病变检测:有助于评估常规眼底相机无法捕捉的周边视网膜病变。
主要设备规格比较
Section titled “主要设备规格比较”各设备的规格如下所示7):
| 设备 | 激发波长 | 视角 |
|---|---|---|
| Spectralis | 488 nm | 15~55度 |
| Optos | 532 nm | 200度 |
| Zeiss Clarus | 435~585 nm | 133~200度 |
实际拍摄操作
Section titled “实际拍摄操作”标准B-FAF(蓝光FAF)拍摄时,在散大患者瞳孔后(或无需散瞳),将患者固定在设备上,在观察实时图像的同时以最佳焦点进行拍摄。cSLO型通过多帧平均叠加处理提高信噪比。
光漂白处理:拍摄前进行约20秒的强光照射,使视色素漂白,可将FAF信号增强约30%2)1)。用于评估MEWDS等急性期病变。
绿光FAF(G-FAF):采用504/532 nm激发光拍摄,黄斑色素吸收较少,对中心凹评估效果优异4)6)。患者舒适度也较高。
门诊标准检查广泛使用cSLO型(如Spectralis)。超广角拍摄选择Optos,中心凹评估选择G-FAF兼容设备。可同时拍摄OCT的cSLO型在随访中定位精度高,适用于GA面积测量等定量评估4)7)。
4. 正常所见与异常所见的解读
Section titled “4. 正常所见与异常所见的解读”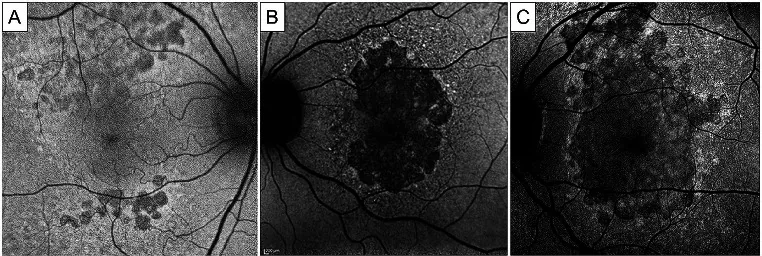
SW-AF(短波长FAF、B-FAF)的正常所见:
- 中心凹低荧光: 由于叶黄素色素(黄斑色素)吸收蓝光,中心凹呈现低荧光6)7)。
- 视盘低荧光:由于缺乏RPE,表现为低荧光7)。
- 视网膜血管低荧光:血液吸收光线,表现为低荧光7)。
- 最强荧光区域:距中心凹5–15度的旁中心凹区域显示最强荧光6)。
NIR-AF(近红外自发荧光)的正常表现:
由于中心凹黑色素密度高,在NIR-AF上反而表现为高荧光6)7)。这是与SW-AF的重要区别。
异常表现的解读
Section titled “异常表现的解读”强荧光和弱荧光的原因及代表性疾病如下所示7)1)2):
| 模式 | 主要原因 | 代表性疾病 |
|---|---|---|
| 强荧光 | 脂褐素沉积、黄斑色素消失、视网膜下荧光物质 | Stargardt病、MEWDS、GA周围 |
| 低荧光 | RPE萎缩、出血遮蔽、纤维化 | GA、出血、瘢痕 |
高荧光机制分类:
高荧光的产生机制分为原发性升高和继发性升高2)。
- 原发性升高:ABCA4、RDH12功能异常导致双视黄醛过度生成。对应Stargardt病、RDH12相关视网膜营养不良。
- 继发性升高:光感受器细胞损伤后,下游双视黄醛积累。继发于RP或其他原因导致的光感受器细胞死亡。
与光漂白的鉴别:如果光漂白处理后高荧光消失,则可能是由于视色素(视紫红质)荧光引起的假性高荧光1)。
黄斑色素减少(老化、阳光暴露)或光漂白也可能出现高荧光。结合OCT检查结构变化,与真正的病理性高荧光进行鉴别。由于不同设备之间表现可能不同,纵向比较时应使用同一设备4)7)。
5. 注意事项与局限性
Section titled “5. 注意事项与局限性”6. 技术原理(脂褐素、黑色素、荧光团)
Section titled “6. 技术原理(脂褐素、黑色素、荧光团)”荧光的物理学基础
Section titled “荧光的物理学基础”荧光是指吸收光子的分子从激发态回到基态时发射出较低能量光子的现象7)。发射光波长总是长于吸收光波长(斯托克斯位移)。
脂褐素的生化形成过程
Section titled “脂褐素的生化形成过程”LF的主要成分A2E的形成途径如下7)2):
- 11-顺式视黄醛的光异构化:光感受产生全反式视黄醛。
- 与磷脂酰乙醇胺(PE)的反应:全反式视黄醛与PE缩合形成N-亚视黄基-PE(NRPE)。
- NRPE→A2-GPE:在盘膜内,NRPE与第二个全反式视黄醛分子反应,形成A2-GPE(A2E前体)。
- A2-GPE水解→A2E:RPE吞噬盘膜后,A2-GPE在溶酶体中水解生成A2E。
ABCA4的作用:ABC转运蛋白ABCA4将NRPE转运至盘膜的胞质侧,并促进其还原为全反式视黄醇2)。ABCA4功能缺陷(Stargardt病的原因)导致NRPE滞留在盘膜内,引起双视黄醛类化合物的过度积累。
黑色素与近红外自发荧光
Section titled “黑色素与近红外自发荧光”黑色素是NIR-AF(787 nm激发)的主要荧光物质,分布于RPE和脉络膜7)6)。与年龄相关的黑色素减少表现为NIR-AF信号减弱。黑色素脂褐素(黑色素与LF的复合物)也对NIR-AF信号有贡献。
荧光定量(qAF)
Section titled “荧光定量(qAF)”qAF是在488 nm激发下,使用内部荧光参考(比色皿中的标准荧光物质)校正后的定量荧光值2)7)。qAF值随年龄、偏心度、性别和种族而变化,标准化仍是一个挑战。
荧光寿命成像(FLIO)
Section titled “荧光寿命成像(FLIO)”FLIO是一种测量每种荧光物质特有荧光衰减曲线(寿命)的技术,除了荧光强度外,还能识别荧光物质的类型6)7)。目前主要用于研究目的。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”qAF在临床试验终点中的应用
Section titled “qAF在临床试验终点中的应用”qAF正逐渐被用作Stargardt病、视网膜色素变性等遗传性视网膜疾病进展的客观指标,并被纳入临床试验终点2)。校准设备和标准化测量方案是当前的挑战。
FAF在地图样萎缩治疗药物试验中的作用
Section titled “FAF在地图样萎缩治疗药物试验中的作用”在使用pegcetacoplan(APL-2)和avacincaptad pegol(Zimura)治疗地图样萎缩的临床试验中,基于FAF图像的GA面积测量已被采用为主要终点4)。有报道称,B-FAF倾向于高估GA面积,而G-FAF在评估中心病变方面更优4)。
AI与深度学习自动分析
Section titled “AI与深度学习自动分析”已有研究报道将Optos超广角FAF图像与深度学习算法相结合用于检测年龄相关性黄斑变性,可实现高灵敏度的早期病变检测6)。
在遗传性视网膜疾病的自动分类中,据报道神经网络识别Stargardt病、Best病和RP的准确率约为95%5)。
G-FAF临床应用的扩展
Section titled “G-FAF临床应用的扩展”G-FAF受中心凹黄斑色素影响较小,在检测SW-AF难以观察的中心凹病变方面具有优势4)。患者眩光感也较轻,在舒适性方面更有利。未来有望得到更广泛的应用。
FLIO的临床应用
Section titled “FLIO的临床应用”荧光寿命成像(FLIO)在年龄相关性黄斑变性、Stargardt病和糖尿病黄斑病变中显示出疾病特异性荧光寿命模式,并可能在基于强度的FAF之前检测到代谢变化7)。
多模态成像整合
Section titled “多模态成像整合”通过整合FAF、OCT、OCT-A和FA的多模态成像,正在建立一种弥补各检查方法局限性的诊断体系4)。
主要前景包括通过qAF标准化进行定量疾病监测、利用AI和深度学习进行自动诊断(遗传性视网膜疾病准确率约95%)、FLIO的临床应用以及G-FAF的普及5)6)。FAF已被用作地理萎缩治疗药物临床试验的主要终点,预计其在未来视网膜诊疗中的重要性将进一步增加4)。
8. 参考文献
Section titled “8. 参考文献”- Mantovani A, Corbelli E, Sacconi R, et al. Blue-light fundus autofluorescence in inflammatory photoreceptor diseases. Diagnostics. 2023;13(14):2466.
- Parmann R, Bhatt M, Sarraf D, et al. Primary versus secondary autofluorescence elevations in inherited retinal dystrophies. Int J Mol Sci. 2023;24(15):12327.
- Curcio CA, Meleth AD, Gelman R, et al. FAF variation in geographic atrophy: clinicopathologic correlation. Invest Ophthalmol Vis Sci. 2025;66(1):49.
- Ranetti AE, Ranetti MO, Pop A, et al. Blue-light and green-light fundus autofluorescence in age-related macular degeneration. Diagnostics. 2025;15(13):1688.
- Oh J, Lee CS, Kim JM, et al. Fundus autofluorescence in inherited retinal disease. J Clin Med. 2025;14(7):2293.
- Sahinoglu Kekek E, Sermet F. Fundus autofluorescence in dry age-related macular degeneration. Turk J Ophthalmol. 2021;51(3):169-176.
- Pole C, Ameri H. Fundus autofluorescence and clinical applications. J Ophthalmic Vis Res. 2021;16(3):432-461.
