眼球内源性风险

视网膜脱离
该疾病群的要点
Section titled “该疾病群的要点”1. 什么是视网膜脱离?
Section titled “1. 什么是视网膜脱离?”视网膜脱离(retinal detachment; RD)是指神经视网膜(感觉视网膜)从视细胞层内侧的部分与视网膜色素上皮(RPE)层分离,两者之间积聚视网膜下液的状态。从胚胎学上讲,神经视网膜由神经外胚层的内层分化而来,RPE由神经外胚层的外层分化而来,因此两者的结合原本较弱,容易因各种原因发生脱离。10,20)
当发生视网膜脱离时,感光细胞与来自RPE和脉络膜的氧气及营养供应分离。发病早期即开始出现感光细胞外节的变性和脱落,若长期持续,则会进展为不可逆的感光细胞损伤。这种时间依赖性构成了视网膜脱离“紧急性”的依据。特别是当黄斑部(中心凹)脱离时,中心视力会迅速且严重下降,术后视力恢复也往往不完全。
视网膜脱离的基本分类
Section titled “视网膜脱离的基本分类”根据发病机制,大致分为以下三种类型(也有将外伤性单独列为第四种类型的观点)。
| 病型 | 英文名称 | 主要缩写 | 裂孔 | 牵拉性 | 渗出性 |
|---|---|---|---|---|---|
| 孔源性 | 孔源性视网膜脱离 | RRD | ◎ | △(继发性) | — |
| 牵拉性 | 牵拉性视网膜脱离 | TRD | — | ◎ | — |
| 渗出性 | 渗出性视网膜脱离 | ERD | — | — | ◎ |
| 外伤性 | 外伤性视网膜脱离 | — | △/◎ | △ | △ |
2. 按病型分类与流行病学
Section titled “2. 按病型分类与流行病学”2-1. 孔源性视网膜脱离(RRD)
Section titled “2-1. 孔源性视网膜脱离(RRD)”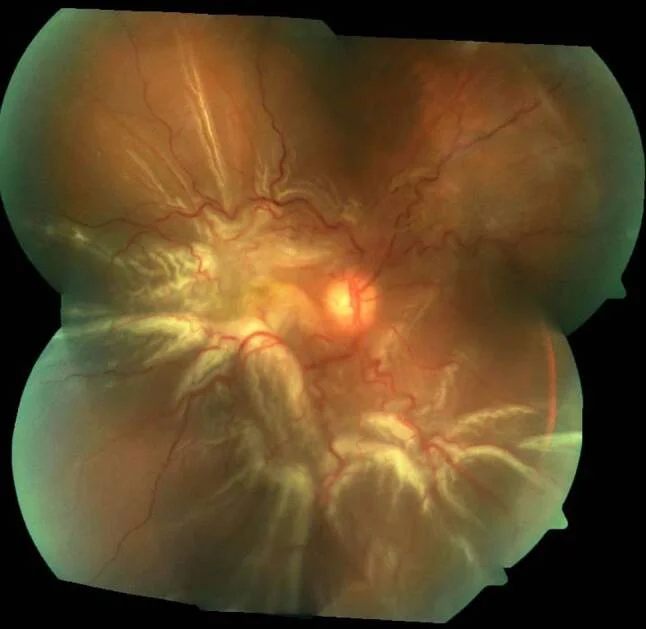
定义与流行病学
孔源性视网膜脱离(rhegmatogenous retinal detachment; RRD)的名称源自希腊语“rhegma”,意为“裂孔”。年发病率因地区而异,但通常为每10万人约10~15例。对侧眼视网膜脱离病史或家族史是发病的危险因素。7)
发病年龄呈双峰分布:
- 年轻高峰(20多岁):格子状变性内萎缩性圆孔引起的扁平脱离
- 中老年高峰(50多岁):后玻璃体脱离(PVD)伴瓣状裂孔引起的高耸脱离
年龄、性别与种族差异
PVD随年龄增长发生,近视或白内障手术后更易早期出现。孔源性视网膜脱离的风险随高龄、男性、近视、白内障术后、外伤、对侧眼孔源性视网膜脱离病史、格子状变性等增加,发病率和地区、种族有关。7)
眼轴长度与近视的关系
随着眼轴延长,视网膜和玻璃体变性进展,孔源性视网膜脱离的风险逐步升高。与眼轴长度小于24mm的正视眼相比,眼轴长度26mm以上(相当于高度近视)的周边视网膜格子状变性和萎缩性圆孔的出现率高出2-3倍。在日本,高度近视(超过-6屈光度)眼中黄斑圆孔型孔源性视网膜脱离占所有孔源性视网膜脱离的约5%,高于欧美的0.5-2.0%。
发病的必要条件
孔源性视网膜脱离的发生必须具备以下两个条件:
- 视网膜的“孔”状缺损(裂孔或圆孔)
- 玻璃体液化(液化玻璃体流入视网膜下的路径)
近视是孔源性视网膜脱离的重要危险因素,据报道,超过-3屈光度的近视可使发病风险增加约10倍。高度近视眼易早期发生玻璃体后脱离(PVD),玻璃体液化和视网膜牵引进展较快。格子状变性也是参与孔源性视网膜脱离发生的代表性周边视网膜变性。7, 9)
主要危险因素
医源性和外部风险
2-2. 牵拉性视网膜脱离
Section titled “2-2. 牵拉性视网膜脱离”牵拉性视网膜脱离是由于后玻璃体不完全脱离,导致玻璃体对视网膜产生强烈牵拉而发病。大致可分为眼内增殖细胞引起的含新生血管的纤维血管膜型和玻璃体视网膜牵拉型两种。
| 类型 | 代表性疾病 | 牵拉特征 |
|---|---|---|
| 纤维血管膜型 | 增殖性糖尿病视网膜病变(PDR)、视网膜静脉阻塞、早产儿视网膜病变(ROP) | 新生血管和成纤维细胞形成的视网膜前膜 |
| 单纯玻璃体牵引型 | 玻璃体黄斑牵引综合征、穿孔性眼外伤 | 无新生血管的单纯牵引 |
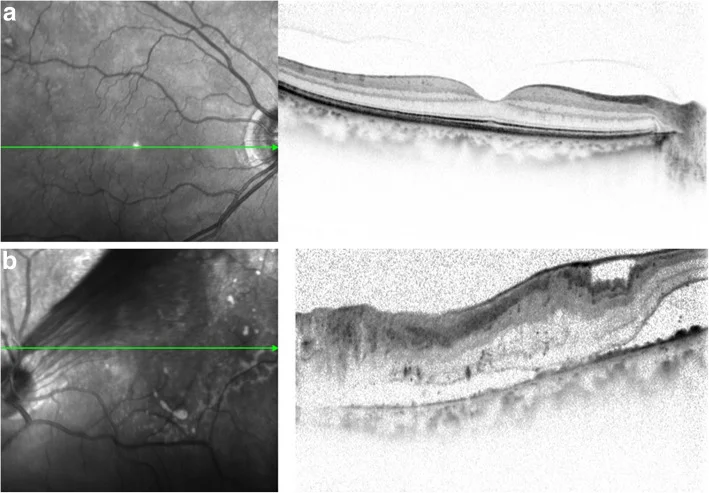
形态特征
牵引性视网膜脱离无活动性,形态呈反向拱形(concave shape)。在新生血管根部(epicenter)或沿视网膜血管出现帐篷状脱离,若粘连广泛则呈“桌面型(富士山型)”。若脱离呈穹顶状且有活动性,需怀疑合并孔源性视网膜脱离(combined tractional-rhegmatogenous retinal detachment)。
2-3. 渗出性视网膜脱离
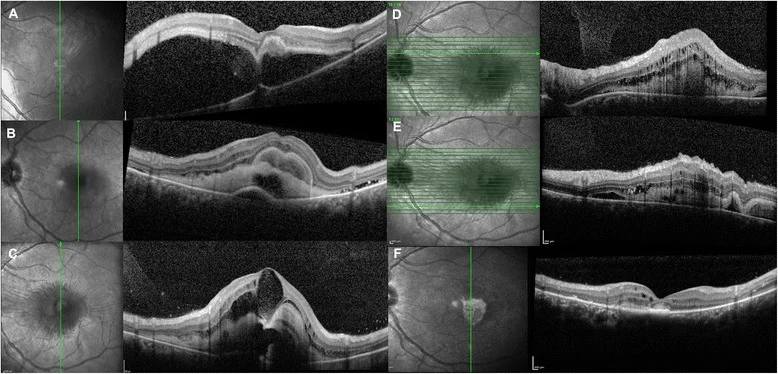
Section titled “2-3. 渗出性视网膜脱离”渗出性视网膜脱离是由于视网膜血管、RPE、脉络膜等功能障碍导致视网膜下渗出液积聚而形成的非孔源性视网膜脱离。血-视网膜屏障(BRB)破坏是最终共同病理状态,原因多种多样。
典型临床特征
- 视网膜脱离面呈穹顶状突出,表面光滑
- 体位改变时液体移动(shifting fluid):与孔源性视网膜脱离的重要鉴别要点
- 可能自然消退(因体位改变使液体排出)
主要病因
| 病因分类 | 代表性疾病 |
|---|---|
| 炎症性/免疫性 | Vogt-小柳-原田病(VKH)、后巩膜炎、交感性眼炎、葡萄膜炎 |
| 血管性 | 中心性浆液性脉络膜视网膜病变(CSC)、Coats病、渗出型AMD、糖尿病性黄斑水肿 |
| 肿瘤性 | 脉络膜恶性黑色素瘤、转移性脉络膜肿瘤、视网膜母细胞瘤 |
| 药物性 | MEK抑制剂(如比美替尼)4)、免疫检查点抑制剂(包括抗PD-1/PD-L1抗体引起的VKH样综合征)12) |
| 全身性疾病 | 妊娠高血压综合征/子痫前期(可能引起双侧渗出性视网膜脱离)6)/恶性高血压 |
| 其他 | 特发性脉络膜脱离/葡萄膜渗漏 |
2-4. 外伤性视网膜脱离
Section titled “2-4. 外伤性视网膜脱离”外伤性视网膜脱离由钝性或穿孔性眼外伤引起。据报道,钝性外伤后立即发生视网膜脱离的比例为12%,1个月内为30%,8个月内为50%,24个月内达80%,因此需要长期随访。一种特殊类型是外伤引起的锯齿缘断裂(retinal dialysis)。
3. 症状与紧急程度
Section titled “3. 症状与紧急程度”主要自觉症状
Section titled “主要自觉症状”前驱症状(尤其是孔源性视网膜脱离)
| 症状 | 机制 | 注意事项 |
|---|---|---|
| 飞蚊症(突然增多或加重) | 玻璃体出血或色素细胞漂浮(Shafer征) | 飞蚊突然增多提示视网膜裂孔形成 |
| 闪光感 | 玻璃体牵拉视网膜 | 在暗处、闭眼或眼球运动时加重 |
| 幕状视野缺损 | 对应脱离区域的敏感度下降 | 易被误认为青光眼或上睑下垂 |
| 视力下降和视物变形 | 黄斑部脱离和水肿 | 黄斑脱离的指标 |
症状与疾病类型的对应
孔源性视网膜脱离
- 飞蚊症和闪光感常为前驱症状
- 青少年型萎缩孔通常无症状
- 窗帘状视野缺损出现在脱离对侧
- 玻璃体内烟草尘(Shafer征)提示裂孔形成
牵拉性视网膜脱离
渗出性视网膜脱离
- 主要表现为视力下降和视物变形
- VKH伴有头痛、耳鸣和感冒样全身症状
- 视野缺损部位可能随体位改变而变化
- 多为双眼(尤其VKH和恶性高血压)
眼压变化
4. 检查方法
Section titled “4. 检查方法”| 确认事项 | 目的 |
|---|---|
| 症状的发作形式与经过 | 鉴别急性(裂孔性)与慢性(牵拉性/渗出性) |
| 闪光感和飞蚊症的有无及变化 | 估计PVD和裂孔形成的时间 |
| 近视的有无及度数 | 孔源性视网膜脱离风险评估 |
| 眼手术或外伤史 | 医源性或外伤性风险 |
| 全身性疾病(糖尿病、高血压、自身免疫性疾病) | 牵拉性或渗出性视网膜脱离的病因查找 |
| 对侧眼或家族视网膜脱离史 | 识别遗传性疾病或高风险人群 |
| 妊娠及用药史 | 寻找渗出性视网膜脱离的原因 |
裂隙灯显微镜检查
Section titled “裂隙灯显微镜检查”散瞳眼底检查
Section titled “散瞳眼底检查”使用间接检眼镜(双目间接检眼镜)和巩膜压迫进行周边部检查是诊断的核心。
- 检查脱离视网膜的范围、形态和颜色(混浊、透明度下降)
- 确定病因性裂孔的位置、大小和形状(瓣状、圆形、巨大裂孔)
- 评估增殖性玻璃体视网膜病变(PVR)的有无及程度
5. 检查(OCT、超声、眼底检查的选择)
Section titled “5. 检查(OCT、超声、眼底检查的选择)”光学相干断层扫描(OCT)
Section titled “光学相干断层扫描(OCT)”OCT是确诊视网膜脱离、鉴别类型、术前规划及术后随访不可或缺的检查。
| 检查目的 | 获得的信息 |
|---|---|
| 确认黄斑部脱离的有无及程度 | 预测视力预后及判断手术适应症 |
| 鉴别病型 | 孔源性 vs 渗出性(SRF的性质和形态) |
| 牵拉性视网膜脱离的评估 | 增殖膜的位置和视网膜牵拉模式 |
| 术后监测 | 视网膜复位和黄斑恢复的随访 |
OCT应观察的结构及其意义
在视网膜脱离的术前和术后评估中阅读OCT时,应关注以下结构。术后椭圆体带(EZ)的恢复取决于脱离的持续时间和范围,EZ长度的恢复可作为术后视力的指标。3,15)
| 结构 | 所见的意义 |
|---|---|
| 椭圆体带(ellipsoid zone; EZ) | 光感受器内节/外节交界处的高反射带。脱离时间越长,越模糊/缺损→术后视力预后的指标 |
| 外界膜(external limiting membrane; ELM) | 位于EZ内层的高反射带。比EZ更受保护,ELM的恢复先于EZ |
| 视网膜下高反射物质(SHRM) | 脱离视网膜下的PRE细胞和炎性残留物。术后残留会阻碍EZ恢复。 |
| 视网膜下液(SRF)的性质 | 孔源性视网膜脱离表现为低反射、均匀;渗出性视网膜脱离可呈穹窿状伴点状高反射。 |
OCT鉴别诊断要点
- 孔源性视网膜脱离:视网膜下液呈淡低反射,脱离边缘陡峭,外节伸展,SHRM较少。
- 渗出性视网膜脱离:视网膜下液呈圆顶状且光滑,可能伴有SHRM,反映移动性液体
- 牵拉性视网膜脱离:增殖膜从内侧牵拉,呈凹形,活动性降低
超声B型检查
Section titled “超声B型检查”当眼底无法透见(玻璃体出血、白内障、角膜混浊)时,这是必需的检查。将探头置于角膜或巩膜上,系统性地拍摄纵切面、横切面和轴切面。
基本成像技术
- 使用10MHz或更高频率(眼科高频)的探头,观察眼球壁的动态。
- 让患者进行眼球运动时:视网膜作为高亮度的硬膜移动(确认后壁附着),玻璃体柔软地晃动(aftermovement阳性),增殖膜显示中间运动。
- 通过在视神经乳头处确认后壁附着,识别完全性视网膜全脱离(V形或T形)。
| 所见 | 意义 |
|---|---|
| 确认视网膜全脱离 | 视神经乳头处后壁附着→判断ERG和手术适应症 |
| 牵拉性视网膜脱离的评估 | 增殖膜的位置、密度和范围 |
| 漏斗型闭合性视网膜脱离(PVR D-3)的确认 | 预后不良的把握 |
| 脉络膜脱离的检测 | 孔源性视网膜脱离的合并及低眼压的原因 |
| 排除眼内肿瘤 | 渗出性视网膜脱离的肿瘤性病因鉴别 |
超广角眼底成像(UWF)的应用
Section titled “超广角眼底成像(UWF)的应用”超广角激光眼底相机(OptosSS、Clarijs等)单次拍摄可捕捉视网膜周边部(近锯齿缘)80–200°的范围。
- 检测传统眼底摄影(45°)容易遗漏的周边裂孔和格子状变性
- 有助于术前客观记录裂孔位置和范围(提高手术计划精度)
- 术后随访中可监测周边新出现的裂孔和脱离
- 但确认小裂孔(<0.5 DD)必须联合巩膜压迫眼底检查;UWF图像上未见裂孔不能作为排除依据
荧光眼底血管造影(FA·ICGA)
Section titled “荧光眼底血管造影(FA·ICGA)”用于查找渗出性视网膜脱离的原因。
超广角眼底照相和眼底相机
Section titled “超广角眼底照相和眼底相机”- 用于术前记录、随访和裂孔位置的记录
- 超广角激光眼底相机(如Optos)可提高周边裂孔的检出率
- 但小裂孔可能无法通过眼底相机发现,因此必须联合使用巩膜压迫眼底检查
6. 治疗方针的考虑
Section titled “6. 治疗方针的考虑”按病型的治疗原则
Section titled “按病型的治疗原则”| 病型 | 治疗原则 | 紧急性 |
|---|---|---|
| 孔源性视网膜脱离 | 手术封闭裂孔、复位视网膜 | 高(黄斑脱离前手术) |
| 牵拉性视网膜脱离 | 玻璃体手术解除牵拉 | 中至高(进展或合并裂孔时紧急) |
| 渗出性视网膜脱离 | 治疗原发病(内科/肿瘤科协作) | 取决于疾病 |
| 外伤性视网膜脱离 | 根据损伤类型进行手术 | 开放性损伤需紧急处理 |
孔源性视网膜脱离的手术选择
Section titled “孔源性视网膜脱离的手术选择”孔源性视网膜脱离的治疗有三种手术方法。
巩膜扣带术(SB)
从眼外通过冷冻凝固和巩膜扣带(硅胶材料)在裂孔处形成压痕,使视网膜复位。
适应症:年轻患者、玻璃体未脱离、周边单纯裂孔 优点:保留晶状体、维持接近自然状态的眼球形态 缺点:不适用于复杂病例或增殖性改变
玻璃体切除术(PPV)
气性视网膜复位术(PR)
向眼内注入膨胀气体,封闭裂孔,使视网膜复位。可作为门诊手术进行。
适应症:局限于上半部分的单个裂孔 优点:无需住院、创伤小 缺点:适应症病例有限、成功率略低于其他术式
术式选择指南
- 年轻患者、玻璃体未脱离、单纯裂孔 → 巩膜扣带术为首选
- 中老年患者、合并PVD、深部裂孔、多发裂孔、合并PVR → 玻璃体手术为适应症
- 初次手术的解剖学成功率在许多报告中高达80-90%以上,但术式间的优劣取决于病例背景(裂孔部位、PVR、有无人工晶状体等)10, 14)
- 多次手术后最终复位的情况很多,但黄斑脱离时间和PVR的有无对视力功能预后影响很大7, 18)
术后管理与气体填充注意事项
玻璃体内气体填充后,需要保持气体压迫裂孔位置的体位限制(通常俯卧或头部倾斜)数天至2周。气体吸收后眼内再次充满液体。
| 气体种类 | 眼内滞留时间 | 膨胀倍数 | 体位限制时间参考 |
|---|---|---|---|
| 空气 | 5~7天 | 无膨胀 | 3~5天 |
| 20% SF₆ | 10~14天 | 约2倍 | 5~10天 |
| 14% C₃F₈ | 6~8周 | 约4倍 | 10~14天 |
气体残留期间的禁忌
- 乘坐飞机/高海拔登山:外界气压降低导致气体膨胀,眼压急剧升高,引起眼循环障碍(失明风险)。在气体消失前禁止乘坐飞机,登机前必须经眼科确认。
- MRI检查:过去使用的气体是铁磁性的,但目前使用的眼内气体(SF₆、C₃F₈)是非磁性的,直接风险较低。但体位限制期间的磁场环境仍令人担忧,术后管理中需向主治医生确认。
- 氧化亚氮(笑气)麻醉:笑气溶解于眼内气体,导致气体急剧膨胀,引起眼压升高。在气体残留期间进行全身麻醉时,务必告知麻醉医生不要使用笑气。
术后再脱离风险较高的时期
再脱离常在术后早期至数月内被发现,PVR和新发现或遗漏的裂孔是主要原因。指导患者若出现症状(飞蚊症增加、视野缺损再次出现)应立即就诊,并坚持术后定期复查。19, 22)
增殖性玻璃体视网膜病变(PVR)的管理
Section titled “增殖性玻璃体视网膜病变(PVR)的管理”PVR是孔源性视网膜脱离的严重并发症,是阻碍视网膜复位的主要原因。脱离视网膜的伤口愈合过程过度,导致由RPE细胞、胶质细胞、成纤维样细胞和巨噬细胞组成的增殖膜在视网膜上、下及玻璃体内形成,膜收缩使脱离的视网膜固定。
- 术后5–10%发生19)
- 发病时间:术后2–3周开始,6–8周完成
- 1983年视网膜学会分类(旧分类):A–D级
视网膜学会分类(旧分类,1983年)
| 分级 | 表现 |
|---|---|
| A | 玻璃体混浊(色素块、玻璃体中的色素颗粒、视网膜上的色素块) |
| B | 视网膜表面皱褶形成、视网膜血管迂曲、裂孔边缘翘起、玻璃体活动性降低 |
| C-1至C-3 | 视网膜全层皱褶(1至3个象限) |
| D-1至D-3 | 涉及四个象限的固定皱襞(宽漏斗/窄漏斗/闭合漏斗) |
1991年,Machemer等人提出了新分类。新分类考虑了前部PVR和视网膜下病变,并用钟点方位描述病变范围。11) 伴有PVR的孔源性视网膜脱离通常需要玻璃体切除术,联合增殖膜剥离、长效气体或硅油填充,可能需要多次手术。7, 19)
近年来,越来越多的机构首次选择PPV,导致前部PVR病例增加。玻璃体术后发生的PVR进展迅速,需要早期再次手术。
牵引性视网膜脱离的治疗
Section titled “牵引性视网膜脱离的治疗”牵引性视网膜脱离的治疗原则是通过玻璃体手术解除牵引。增殖膜的处理需运用膜剥离和玻璃体剪,彻底进行眼内光凝和周边玻璃体切除。若合并裂孔,则参照孔源性视网膜脱离追加气液交换。
术前抗VEGF药物给药可用于增殖性糖尿病视网膜病变伴牵拉性视网膜脱离手术,以促使新生血管消退并减少术中出血。但由于纤维血管膜收缩可能加重牵拉,需谨慎判断手术时机和适应证。5)
渗出性视网膜脱离的治疗
Section titled “渗出性视网膜脱离的治疗”渗出性视网膜脱离的治疗以原发病治疗为基础,很少直接进行视网膜手术复位。应确定炎症性、血管性、肿瘤性等原因,并根据各自情况选择相应的内科和眼科治疗。21)
| 原因 | 主要治疗 |
|---|---|
| VKH病 | 以全身类固醇为主,复发或迁延病例可考虑免疫抑制剂(VKH是渗出性视网膜脱离的典型炎症性原因)。2, 21) |
| CSC | 观察、激光光凝、光动力疗法(PDT)、抗VEGF |
| 恶性高血压、子痫前期 | 降压治疗、产科管理(分娩) |
| Coats病 | 激光光凝、冷冻凝固、抗VEGF、玻璃体手术 |
| 脉络膜肿瘤 | 按肿瘤类型的肿瘤科治疗(放射、摘除等) |
| 药物性 | 停用致病药物(MEK抑制剂停药后数日消退) |
| 葡萄膜渗漏 | 巩膜减压术(涡静脉减压) |
7. 各类型的特征与鉴别流程
Section titled “7. 各类型的特征与鉴别流程”7-0. 基于眼底表现的病型鉴别实践
Section titled “7-0. 基于眼底表现的病型鉴别实践”根据眼底表现鉴别视网膜脱离的类型时,从以下三个视角进行评估。
① 裂孔或圆孔的有无及形状
| 裂孔类型 | 特征 | 提示的病型 |
|---|---|---|
| 瓣状裂孔(马蹄形) | 玻璃体牵拉导致盖膜残留;裂孔边缘隆起 | 孔源性视网膜脱离(PVD后);快速进展 |
| 萎缩性圆孔 | 格子状变性内的圆形全层缺损;边缘平坦 | 孔源性视网膜脱离(青少年型);缓慢进展 |
| 巨大裂孔 | ≥1个象限(90°);边缘可翻转 | 孔源性视网膜脱离(高度近视);难治性 |
| 锯齿缘离断 | 沿锯齿缘;多见于颞下侧 | 外伤性视网膜脱离;年轻男性 |
| 无裂孔 | — | 牵拉性视网膜脱离/渗出性视网膜脱离 |
② 增殖膜的有无与形态
- 无:多见于原发性孔源性视网膜脱离和渗出性视网膜脱离
- 帐篷状膜(凸型、不可动):牵拉性视网膜脱离(增殖性糖尿病视网膜病变、ROP等)
- 固定皱襞(star fold):PVR合并裂孔源性视网膜脱离;处理困难
③ 视网膜下液的性状与移动性
| 性状 | 提示的疾病类型 |
|---|---|
| 透明、可移动(shifting fluid) | 渗出性视网膜脱离 |
| 透明,无移动性 | 孔源性视网膜脱离 |
| 混浊,黄白色 | 肿瘤性/炎症性渗出性视网膜脱离;陈旧性视网膜脱离 |
| 体位改变时液体移动 | 渗出性视网膜脱离(如VKH、CSC) |
7-1. 孔源性视网膜脱离
Section titled “7-1. 孔源性视网膜脱离”孔源性视网膜脱离是最常见的视网膜脱离类型,是眼科急症的代表性疾病之一。主要亚型包括:
瓣状裂孔(马蹄形裂孔)型:因PVD导致视网膜撕裂。在有晶状体眼的孔源性视网膜脱离中约占30%,表现为快速进展、高度泡状脱离。
萎缩圆孔型:格子样变性区内萎缩形成的圆孔。多见于年轻人和近视眼,表现为低平局限性脱离,进展缓慢。
巨大裂孔型:90度(1个象限)以上的裂孔。好发于伴有格子样变性的高度近视眼。裂孔边缘卷曲,使用比水重的液体全氟碳(PFC)进行玻璃体手术复位。
黄斑裂孔型:多见于高度近视女性,在日本约占孔源性视网膜脱离的5%(高于欧美的0.5%~2.0%)。包括内界膜(ILM)剥离的玻璃体手术为标准术式。
详细信息 → 孔源性视网膜脱离文章
7-2. 牵拉性视网膜脱离
Section titled “7-2. 牵拉性视网膜脱离”增殖性糖尿病视网膜病变是最常见的原因。含有新生血管的纤维血管膜收缩,形成帐篷状脱离。最初局限于周边部,当累及黄斑部时会导致急剧的视力下降。
- 增殖性糖尿病视网膜病变(PDR):从反复玻璃体出血的阶段,进展为膜收缩引起的牵拉性视网膜脱离。
- 早产儿视网膜病变(4/5期):周边视网膜的纤维血管增生膜引起的牵拉延伸至晶状体后表面
- 镰状细胞病、Eales病、视网膜静脉阻塞等缺血性视网膜疾病:来自缺血性增殖膜的牵引7, 8)
详情请见 → 牵拉性视网膜脱离的文章
7-3. 渗出性视网膜脱离
Section titled “7-3. 渗出性视网膜脱离”非裂孔性、非牵拉性的视网膜下液积聚。体位改变时液体移动(shifting fluid)是其特点。VKH急性期可出现多发性双侧穹隆状脱离,适当的免疫抑制治疗有望自然消退。肿瘤性原因则优先进行肿瘤的检查和治疗。
详情请见 → 渗出性视网膜脱离的文章
7-4. 外伤性视网膜脱离及相关病变
Section titled “7-4. 外伤性视网膜脱离及相关病变”钝性外伤(眼球挫伤)后数周至数月内可能发生视网膜脱离,因此必须长期随访观察。
锯齿缘断裂(Retinal Dialysis):沿锯齿缘(ora serrata)的全层断裂,多见于年轻男性外伤后。好发于下颞侧,因缓慢进展常无症状。
脉络膜破裂和视网膜震荡(Berlin水肿):钝挫伤后立即出现的后极部水肿和出血。光感受器损伤可能永久存在。
相关文章 → 视网膜裂孔、圆孔和格子样变性
7-5. 儿童视网膜脱离的特殊性
Section titled “7-5. 儿童视网膜脱离的特殊性”儿童视网膜脱离较成人少见,但由于基础疾病不同,需要特殊考虑。
基础疾病类型
| 疾病 | 特征 | 脱离类型 |
|---|---|---|
| 早产儿视网膜病变(ROP)4/5期 | 增殖膜牵拉;可能延伸至晶状体后表面 | 主要为牵拉性视网膜脱离 |
| 家族性渗出性玻璃体视网膜病变(FEVR) | 遗传性(FZD4、LRP5等);周边无血管区→裂孔/牵引 | 孔源性视网膜脱离合并牵拉性视网膜脱离 |
| Stickler综合征 | II型胶原基因突变;玻璃体变性/格子样变性;血管旁变性 | 孔源性视网膜脱离;多发裂孔 |
| Norrie病 | X连锁隐性遗传;仅见于男性;玻璃体出血、眼球萎缩 | 牵拉性视网膜脱离 |
| Bloch-Sulzberger综合征(色素失禁症) | 仅见于女性(男性致死);无血管区→新生血管→牵拉 | 牵拉性视网膜脱离 |
| 先天性视网膜劈裂症 | X连锁隐性遗传;黄斑劈裂及周边劈裂;1%~2%进展为视网膜脱离 | 孔源性视网膜脱离,劈裂型 |
治疗的特殊性
- 儿童巩膜固定容易且眼球顺应性高,因此巩膜扣带术比成人更受青睐。特别是ROP 4A期,为减轻对增殖膜的牵引,环扎术为首选。
- 用于扣带的硅胶条会因眼球生长而加重缩窄,因此建议在6个月内取出。
- ROP引起的牵拉性视网膜脱离,在4A期应在专业机构考虑手术适应症。4B/5期解剖和视功能预后较差,需个体化判断是否保留晶状体。13)
- Stickler综合征确诊后,建议进行360°激光预防性凝固。
7-6. 与特殊病理状态的关系
Section titled “7-6. 与特殊病理状态的关系”增殖性玻璃体视网膜病变(PVR):孔源性视网膜脱离术后最严重的并发症。形成固定皱襞,视网膜变硬固定。术后5-10%发生,常需再次手术。
视网膜劈裂症:视网膜在内丛状层或外丛状层分离。与视网膜脱离不同,无RPE分离。通过OCT、荧光血管造影和ERG鉴别。
详情见 → 视网膜劈裂症文章
与青光眼的关系:孔源性视网膜脱离可出现Schwartz综合征(外节碎片堵塞引起的继发性开角型青光眼),合并脉络膜脱离的视网膜脱离可出现低眼压。渗出性视网膜脱离可合并原发疾病引起的继发性青光眼。
孔源性视网膜脱离的预后
Section titled “孔源性视网膜脱离的预后”解剖学预后:通过适当的手术,95%以上可实现视网膜解剖复位。首次手术成功率约90%以上,包括多次手术在内的最终复位率约达98%。
功能性预后(视力)
| 黄斑部脱离的有无 | 视力预后 |
|---|---|
| 黄斑未脱离(macula-on) | 可望维持接近术前视力的视力 |
| 黄斑脱离(macula-off) | 术后视力约半数在0.5以下,常残留视野缺损和视物变形 |
术后并发症的发生率
| 并发症 | 发生率/时间 | 处理 |
|---|---|---|
| PVR(增生性玻璃体视网膜病变) | 术后5%–10%;2–8周内形成19) | 玻璃体再手术、硅油 |
| 视网膜前膜(ERM) | PPV后可能发生(根据报告,频率大致为10%至百分之十几)16) | 如果视力或视物变形恶化,则行脱离手术 |
| 囊样黄斑水肿(CME) | 黄斑脱离型10–20%;术后数月 | 抗VEGF、类固醇滴眼液、NSAIDs |
| 白内障进展 | PPV后2-3年核性白内障进展 | 白内障手术(多在PPV后1-2年) |
| 再脱离(孔源性) | 初次手术后5-10%;多数在术后6个月内 | 再次手术(追加巩膜扣带或再次PPV) |
复发与长期管理
- PVR导致的再脱离:术后5%~10%。发病时间多在术后2~8周
- 对侧眼视网膜脱离:长期风险持续约10%
- 术后随访中发现新裂孔:5%~14%(尤其最初几个月内)1)
- 需指导患者出现症状时立即就诊
牵拉性视网膜脱离的预后
Section titled “牵拉性视网膜脱离的预后”原发疾病的控制直接影响视力预后。在糖尿病性牵拉性视网膜脱离中,血糖管理和全视网膜光凝是基础。手术成功率低于孔源性视网膜脱离,进展为PVR和再次手术的风险较高。
渗出性视网膜脱离的预后
Section titled “渗出性视网膜脱离的预后”通过治疗原发疾病有望改善,但如果发生RPE萎缩或光感受器的器质性损伤,视力恢复将不完全。在VKH中,首次发作的早期治疗可获得良好预后,但复发病例可能出现日落现象、Dalen-Fuchs结节等慢性期改变。在肿瘤性渗出性视网膜脱离中,肿瘤的控制决定预后。
取决于手术方式和有无并发症。巩膜扣带术住院时间约1-2周,几乎不需要体位限制。玻璃体切除术由于术后气体填充,需要保持体位(俯卧或侧卧)数天至2周。气体残留期间禁止航空旅行、登山等低气压环境。视力恢复在视网膜复位后可能需要数月,尤其是黄斑脱离的病例,需要随访半年至1年。
強度近視(−6ジオプトリ超・眼軸長26mm以上)は網膜剥離の主要リスク因子であり、年1回以上の散瞳眼底検査が推奨される。特に新たな飛蚊症・光視症の出現後は1〜2週間以内に精査する。格子状変性が検出された場合はリスクに応じて予防的レーザー光凝固を検討する。白内障手術後や僚眼の網膜剥離既往がある場合はさらに頻繁な受診が必要で、症状出現時は当日受診が理想。
網膜復位(解剖学的成功)と視機能回復(機能的成功)は必ずしも一致しない。特に黄斑部が剥離していた症例では、OCTで確認される楕円体帯(EZ)の回復に数か月〜1年以上かかり、完全に回復しないこともある。剥離期間が長いほどEZの欠損が広くなり、術後視力は低くとどまる傾向がある。また術後に黄斑上膜や嚢胞様黄斑浮腫が生じた場合も視力回復を妨げることがあるため、術後のOCT定期検査が重要である。
PVRとは、網膜剥離の術後に眼内の創傷治癒反応が過剰になり、網膜色素上皮やグリア細胞・線維芽細胞が増殖して網膜の表面や下面に膜を形成した状態である。膜が収縮すると固定皺襞(star fold)が形成され、網膜の可動性が著しく低下して再剥離をきたす。術後5〜10%に発症し、初期の硬化したGrade A〜Bなら強膜バックリング術が奏効することもあるが、重症例(Grade C〜D)では硝子体再手術による増殖膜除去と長期タンポナーデが必要で、複数回の手術を要することも多い。
9. 相关文章
Section titled “9. 相关文章”- Flaxel CJ, Adelman RA, Bailey ST, et al. Posterior Vitreous Detachment, Retinal Breaks, and Lattice Degeneration Preferred Practice Pattern. Ophthalmology. 2020;127(1):P146-P181. 1)
- Goto H, Mochizuki M, Yamaki K, et al. Epidemiological survey of intraocular inflammation in Japan. Jpn J Ophthalmol. 2007;51(1):41-44. 2)
- Obata R, Yanagi Y, Tamaki Y, et al. Quantitative analysis of optical coherence tomography after vitreous surgery for rhegmatogenous retinal detachment. Am J Ophthalmol. 2005;139(6):1003-1008. 3)
- Urner-Bloch U, Urner M, Stieger P, et al. Transient MEK inhibitor-associated retinopathy in metastatic melanoma. Ann Oncol. 2014;25(7):1473-1476. 4)
- Zhao LQ, Zhu H, Zhao PQ, Hu YQ. A systematic review and meta-analysis of clinical outcomes of vitrectomy with or without intravitreal bevacizumab pretreatment for severe diabetic retinopathy. Br J Ophthalmol. 2011;95(9):1216-1222. doi:10.1136/bjo.2010.189514. PMID: 21216799. 5)
- Mackeen LD. Bilateral retinal detachment in preeclampsia. Am J Obstet Gynecol. 1997;177(4):948-949. 6)
- Xiong J, Mehta N, Sandhu S, et al. A review of rhegmatogenous retinal detachment: past, present and future. Wien Med Wochenschr. 2025;175:146-160. PMCID: PMC12031774. 7)
- Hayreh SS. Ocular vascular occlusive disorders: natural history of visual outcome. Prog Retin Eye Res. 2014;41:1-25. doi:10.1016/j.preteyeres.2014.04.001. PMID: 24769221. 8)
- Akiba J. Prevalence of posterior vitreous detachment in high myopia. Ophthalmology. 1993;100(9):1384-1388. 9)
- Yan X, Xu M, Su F. Surgical managements for rhegmatogenous retinal detachment: a network meta-analysis of randomized controlled trial. PLoS One. 2024;19(11):e0310859. 10)
- Machemer R, Aaberg TM, Freeman HM, et al. An updated classification of retinal detachment with proliferative vitreoretinopathy. Am J Ophthalmol. 1991;112(2):159-165. 11)
- Denu RA, Nair S, Patel S, et al. Vogt-Koyanagi-Harada-Like Uveitis Secondary to Pembrolizumab in Metastatic Gastric Cancer: A Case Report and Review of the Literature. Case Rep Oncol. 2024;17(1):1071-1086. doi:10.1159/000541133. PMID: 39474530. 12)
- Sahin A, Yonekawa Y, et al. Surgical Management and Outcomes for Retinopathy of Prematurity-Associated Retinal Detachment: Lens-Sparing Vitrectomy vs Lensectomy. Retina. 2020;40(4):610-617. doi:10.1097/IAE.0000000000002608. PMID: 31403588. 13)
- Tam AL, Yan P, Gan NY, Lam WC. The current surgical management of rhegmatogenous retinal detachments: a review. Clin Exp Ophthalmol. 2021;49(8):905-917. doi:10.1111/ceo.13976. PMID: 34272822. 14)
- Fawzi AA, Lee NG, Cheng L, et al. Recovery of photoreceptor outer segment length and the ellipsoid zone following surgery for rhegmatogenous retinal detachment. Br J Ophthalmol. 2011;95(4):570-573. 15)
- Wickham L, Bunce C, Wong D, et al. Epiretinal membrane formation and visual outcome after pars plana vitrectomy for primary retinal detachment. Retina. 2016;36(7):1213-1221. doi:10.1097/IAE.0000000000001178. PMID: 27308274. 16)
- Kim J, Ryu SY, Hong JH, Chung EJ. Incidence and risk factors for retinal detachment after cataract surgery in Korea: a nationwide population-based study from 2011 to 2015. Graefes Arch Clin Exp Ophthalmol. 2019;257(10):2193-2202. doi:10.1007/s00417-019-04423-x. PMID: 31388742. 17)
- Schwartz SG, Flynn HW Jr, Lee WH, et al. Primary retinal detachment: scleral buckle or pars plana vitrectomy? Curr Opin Ophthalmol. 2015;26(3):245-250. doi:10.1097/ICU.0000000000000157. PMID: 25789772. 18)
- Pastor JC, de la Rúa ER, Martín F. Proliferative vitreoretinopathy: risk factors and pathobiology. Prog Retin Eye Res. 2002;21(1):127-144. 19)
- Wolfensberger TJ. The historical discovery of the retinal detachment. Doc Ophthalmol. 2003;107(1):1-5. 20)
- Amer R, Nalcı H, Yalçındağ N. Exudative retinal detachment: a systematic approach to diagnosis and management. Curr Opin Ophthalmol. 2020;31(6):455-461. doi:10.1097/ICU.0000000000000731. PMID: 32776566. 21)
- Kunikata H, Nishida K. Long-term follow-up of vitrectomy for recurrent retinal detachment and established proliferative vitreoretinopathy. Jpn J Ophthalmol. 2001;45(6):626-631. PMID: 11792656. 22)
