IOL偏位和脱位
Zinn小带断裂导致IOL坠落的诊断和手术适应证。巩膜内固定术(法兰法、镊子法)的选择。

眼内透镜(intraocular lens; IOL)是在白内障手术中摘除混浊的晶状体后永久植入眼内的人工晶状体。植入IOL的眼睛称为假晶状体眼(pseudophakia)。与眼镜或隐形眼镜矫正不同,IOL直接整合到眼球光学系统中,因此不会产生图像放大或缩小,可获得最自然、最生理的视觉功能。
目前最普及的IOL是可折叠的折叠式IOL,由光学部(optic)和支撑部(haptic)构成。标准光学直径为6.0 mm,可通过超声乳化白内障吸除术(PEA)的2.4–2.8 mm小切口使用注射器植入。在某些复杂病例中,使用7.0 mm大光学直径IOL,有助于改善眼底检查时的观察性和囊外固定时的中心固定性。
按材料分类如下。
| 材料 | 特点 | 主要适应症 |
|---|---|---|
| 疏水性丙烯酸酯 | 后发性白内障较少。注意闪辉(glistenings) | 当前标准选择 |
| 亲水性丙烯酸酯 | 生物相容性高。长期使用有钙沉积(IOL混浊)风险 | 特殊设计IOL |
| 硅胶 | 折叠性好。不适用于硅油眼内填充术后的眼睛。 | 部分PIOL |
| PMMA | 硬性材料。需将切口扩大至5-7毫米。 | 特殊固定IOL、二次植入 |
在结构方面,有光学部和支撑部采用相同材料的一片式人工晶状体和采用不同材料的三片式人工晶状体。一片式通常用于囊袋内固定,三片式适用于囊袋外固定、巩膜固定和缝线固定。需注意,如果将一片式错误地固定在囊袋外(睫状沟),支撑部可能摩擦虹膜,导致虹膜色素播散和炎症迁延。
球面人工晶状体会产生球差,即通过光轴附近的近轴光线和周边光线的焦点位置不一致。相比之下,非球面人工晶状体通过改变各折射面的曲率,使周边光线和近轴光线汇聚到同一焦点,从而减少球差。目前几乎所有人工晶状体都采用非球面设计,可提高对比敏感度。但非球面设计在偏心或倾斜时会导致彗差增加,因此在Zinn小带脆弱、人工晶状体固定不稳定的病例中,也可选择球面人工晶状体。
着色(黄色滤光)人工晶状体降低短波长光(蓝光)的透射率,使其接近成人晶状体的光谱透射率,有望降低视网膜光损伤风险。
1981年,Sanders等人提出了SRK公式(Sanders-Retzlaff-Kraff公式),使人工晶状体屈光度计算系统化1)。1984年,Mazzocco开发了可折叠硅胶人工晶状体,为小切口手术开辟了道路。日本是全球首个批准可折叠人工晶状体的国家,随后在推注器开发方面也发挥了国际领先作用。1953年,Strampelli进行了前房型人工晶状体植入,但数年后70%~80%的病例出现大疱性角膜病变,导致失败;然而,这成为后来人工晶状体设计改进的动力。
最普及的IOL,设计为仅聚焦于一个点。它是保险适用(选定医疗)的标准选择。如果以术后正视眼为目标,远视力无需眼镜即可良好,但近视力需要阅读眼镜。其优势在于对比敏感度最高,夜间眩光和光晕最小。
术后老视管理有以下选择:
→ 详情请参阅单焦点人工晶体。
多焦点人工晶体可在多个焦距提供良好视力,是一种旨在减少对眼镜依赖(脱镜)的增值型人工晶体。由于光能利用率分散,容易导致对比敏感度下降和眩光、光晕,术前需充分说明。作为选择性治疗,患者需自费。
聚焦于远和近两个点。对中间距离(如50–80厘米的电脑工作)不太适合。有衍射型(AcrySof IQ ReSTOR、TECNIS Multifocal)和折射型。
衍射型中,0级衍射光聚焦于远,1级衍射光聚焦于近,而更高阶衍射光(约18%)会导致高频对比敏感度下降。渐变型通过降低瞳孔周边阶梯高度,改善黄昏时的远视力。
一项包含8个RCT的荟萃分析显示,与单焦点IOL相比,多焦点IOL在裸眼近视力(UCNVA,6/6或更好的比例:RR 0.20,95% CI 0.07–0.58,782眼)和眼镜脱镜率(RR 0.63,95% CI 0.55–0.73,1000眼)方面更优。然而,多焦点IOL的光晕频率(RR 3.58,95% CI 1.99–6.46,662眼)显著更高。3)
三焦点人工晶体聚焦于远、中、近三个点,是目前多焦点人工晶体的主流。首个三焦点人工晶体于2010年临床引入4),当前代表产品包括AcrySof IQ PanOptix(爱尔康)、AT LISA tri(蔡司)、FineVision(PhysIOL)、TECNIS Synergy(强生视力)等。
一项包含22项试验、2200只眼的荟萃分析显示,三焦点人工晶体在近视力(UCNVA: MD = 0.12 logMAR, p < 0.00001)和脱镜率(OR = 0.26, p = 0.02)方面优于EDOF人工晶体。同时,两组在远视力(UDVA)和中视力(UIVA)方面无显著差异,三焦点人工晶体的视觉质量评分显著更高(MD = 1.24, p = 0.03)。5)
三焦点人工晶体的系统评价显示,与双焦点人工晶体相比,三焦点人工晶体的中视力显著更好(DCIVA: MD −0.16 logMAR, 95% CI −0.22至−0.10),但在CDVA、远视力、近视力、对比敏感度和患者满意度方面无显著差异。4)
景深扩展型(EDOF)人工晶体将光线分散到连续焦点范围而非单一焦点,提供从远到中的宽景深。首个获得CE标志的产品于2014年问世4)。代表产品包括TECNIS Symfony(强生视力)、TECNIS Eyhance和AcrySof IQ Vivity(爱尔康)等。
在上述荟萃分析(22项试验)中,EDOF IOL在远距离矫正视力(CDVA: MD = −0.01 logMAR, p = 0.01)方面略优于三焦点IOL,两组间眩光和光晕的发生频率无显著差异。5) ESCRS指南推荐EDOF IOL作为“重视中距离视力并希望最小化光学副作用的患者的选择”。4) 评估EDOF IOL(AcrySof IQ Vivity)的美国注册试验显示,最佳矫正远视力(BCVA)与单焦点对照组相当(单眼CDVA 0.00 logMAR),暗视对比敏感度的下降为中度。17)
→ 详情请参见多焦点人工晶状体。
散光矫正型IOL旨在矫正角膜规则散光,其光学部沿弱主径线有标记,植入时需将此标记与角膜强主径线对齐并固定于囊袋内。轴位每偏移1°,矫正效果约降低3.3%;偏移30°时不仅矫正效果消失,还可能比非散光矫正型IOL更差,导致视功能下降。
ESCRS 指南(2024)建议在角膜散光 ≥1.0 D 的眼考虑使用 Toric IOL,≥2.0 D 时有强证据(GRADE ++)。4) 13 项试验的荟萃分析显示,与非 Toric IOL(有或无松解切口)相比,Toric IOL 在术后 UDVA(MD −0.07 logMAR,95% CI −0.10 至 −0.04)和未达到 20/25 的比例(RR 0.59,95% CI 0.50 至 0.70)方面更优。14)
悬韧带脆弱、后囊破裂或瞳孔散大不充分的病例通常不适合,因为难以精确对轴。计算时使用各制造商提供的在线计算器或设备内置的 Barrett Toric 公式或 Haigis-T 公式。
→ 详情请参阅 Toric 人工晶状体。
这是一种在保留自身晶状体的同时固定于虹膜后面或睫状沟的 IOL,是屈光手术的一种形式。代表性的是 ICL(Implantable Collamer Lens;EVO+ ICL),一种由 Collamer 材料制成的后房型 PIOL,具有高生物相容性。它不切削角膜,可逆,适用于中到高度近视的广泛范围。
日本眼科学会的屈光矫正手术指南(第8版)规定,有晶状体眼内镜手术的适应年龄原则上为21至45岁,适应屈光度为6 D以上的近视。对于3至6 D以下的中度近视和超过15 D的高度近视,需要谨慎处理。除了与准分子激光手术相同的禁忌症(活动性外眼炎症、白内障、葡萄膜炎等)外,浅前房、角膜内皮损伤和进行性圆锥角膜为额外禁忌症。6)
术前评估必须包括角膜内皮细胞密度检查、眼前段图像分析(包括前房深度)和角膜直径测量(水平直径)。6)
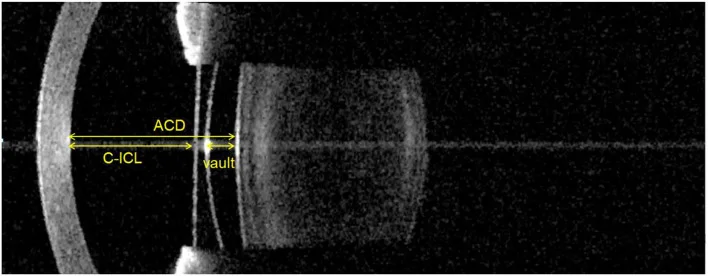
→ 详情请参见有晶状体眼后房型人工晶状体(ICL)。
这是一种辅助人工晶体,通过睫状沟固定,附加在现有的单焦点人工晶体之上。即使之前植入过单焦点人工晶体的眼睛,也可以后期进行老视矫正、散光矫正和近视矫正。它与囊袋内固定人工晶体的距离相对恒定,长期稳定性良好。
→ 详情请参阅附加型人工晶体。
| 类型 | 焦点范围 | 对比敏感度 | 眩光/光晕 | 散光矫正 | 保险适用 | 额外费用估算(双眼) |
|---|---|---|---|---|---|---|
| 单焦点 | 1点(远或近) | ◎ | 无 | △(散光型另计) | ○(选定医疗) | 0~数万日元 |
| 双焦点(衍射型) | 远+近 | ○ | ++(中等) | △〜○ | × | 30~50万日元 |
| 三焦点 | 远+中+近 | ○ | ++(中等度) | △〜○ | × | 40〜60万日元 |
| EDOF | 远至中(连续) | ◎〜○ | +(轻度) | △〜○ | × | 35万~55万日元 |
| 散光型(单焦点) | 1点(远距离优先) | ◎ | 无 | ◎ | ×(选定疗养) | 10~15万日元 |
| 有晶状体眼(PIOL/ICL) | 远距离(无需角膜矫正) | ◎ | 无 | EVO+ 为△~○ | × | 50~70万日元 |
| 附加型 | 现有IOL+老视矫正 | ○ | + | ○ | × | 30~45万日元 |
费用为双眼自费治疗的粗略估算。因机构和所选镜片不同而有很大差异。
IOL选择直接影响术后视力,因此术前仔细确认患者意愿至关重要。ESCRS白内障指南明确指出:“评估患者期望并进行详细的知情同意是恰当选择IOL的最重要前提。”4) 需要掌握的信息:
适合多焦点IOL(三焦点/EDOF)的条件:
荟萃分析显示,如果多焦点IOL植入后眼镜依赖未消除或光学副作用未改善,一年内的IOL置换率会升高。3)
散光矫正型IOL对矫正角膜规则散光有效,但需满足若干前提条件。
为考虑后角膜散光的影响,建议使用Barrett Toric公式或光学眼轴长测量仪内置的Haigis-T公式。7) 此外,坐位和仰卧位时的眼球旋转(ocular cyclotorsion)平均为4–5°,因此使用照片标记或图像引导系统(CALLISTO eye, VERION)进行自动轴对齐有助于提高精度。一项比较图像引导系统与手动标记的前瞻性研究显示,图像引导组的术后残余散光显著更少(0.33 D vs. 0.51 D,p = 0.003)。19)
精确的IOL度数计算通常采用光学眼轴长度测量仪同时测量多个参数。与超声A型法相比,光学测量误差更小。在日本,2010年“光学眼轴长度测量”被纳入医保后迅速普及。采用FD(傅里叶域)技术后,测量成功率从约90%提高到约98%,测量值的标准差也控制在0.02 mm以内。7)
| 设备 | 测量方式 | 主要功能 |
|---|---|---|
| IOLMaster 700(卡尔蔡司) | SS-OCT(扫频源) | 眼轴长度、角膜屈光力、前房深度、晶状体厚度、角膜直径,金标准 |
| ARGOS(参天/Santek) | FD-OCT(分段方式) | 单独测量各组织的折射率。倾向于比IOLMaster 700测得的眼轴长度更短 |
| OA-2000(Tomey) | FD-OCT | 并排显示B扫描图像和A扫描波形 |
| 超声A模式法 | 超声波(1,550 m/s) | 适用于所有病例但误差较大(被认为是术后屈光误差的主要原因)7) |
光学式比超声波法显示的眼轴长度长0.2~0.3 mm,因此必须使用测量装置专用的IOL常数(如A常数)。由于ARGOS采用分段方式,必须避免与IOLMaster 700互换使用IOL常数。7)
| 计算公式 | 世代 | 特点 | 主要用途 |
|---|---|---|---|
| SRK/T公式 | 第三代 | 日本国内90%以上使用。临床经验丰富,A常数 | 标准眼轴(22~25 mm)的首选 |
| Haigis公式 | 第三代 | 使用前房深度作为独立变量。a0、a1、a2三个常数(需在200眼以上优化) | 前房浅/深的眼 |
| Barrett Universal II 公式 | 第四代 | 基于厚透镜理论。低度数 IOL 精度良好。可在 APACRS 网站免费计算。 | 长眼轴、短眼轴、低度数 IOL |
| Hill-RBF | AI(机器学习) | 从大数据中进行模式识别。不依赖公式。 | 长眼轴、高度近视 |
| Kane 公式 | AI(机器学习 + 理论公式) | 性别也作为变量使用 | 极度高度近视(眼轴长 ≥ 30 mm) |
在日本,第三代 SRK/T 公式被广泛使用,但建议根据眼轴长度和眼前节解剖(眼球生物测量)比较多个计算结果。约 15% 的白内障手术患者存在眼轴长度和角膜屈光力不匹配的眼球,因此选择计算公式时需注意。7)
一项涉及 13,301 只眼的多中心研究表明,Barrett Universal II、Olsen 和 Haigis 公式的准确性显著高于 SRK/T、Holladay 1 和 Hoffer Q(Holladay 2 的准确性几乎相当),且第四代及以后的公式在长眼轴和短眼轴方面均更优。15) 另一项针对短眼轴(AL < 22 mm)的荟萃分析也发现,Barrett Universal II 的 MAE 显著小于 Haigis 和 SRK/T(p < 0.05)。18)
在一项针对80只高度近视眼(眼轴长度≥30 mm)的研究中,AI公式(Kane、Hill-RBF)的平均绝对误差(MAE)显著小于SRK/T(Kane: 0.51 D, Hill-RBF: 0.52 D, Barrett Universal II: 0.66 D, SRK/T: 有显著差异,p < 0.05)。Kane和Hill-RBF的屈光误差超过1.0 D的比例控制在7.5%,而SRK/T则达到42.5%。8) 在眼轴长度≥32 mm的眼中,Kane公式实现了最低的MAE(0.44 D)和MedAE(0.40 D)。8) Rong 2019的另一项针对眼轴长度≥28 mm的研究中,Barrett Universal II的MedAE为0.37 D,显著小于Haigis的0.46 D(p = 0.038)。在眼轴长度≥30 mm的眼中,Barrett Universal II比Haigis表现出更好的精度。16)
| 病例 | 推荐公式 | 注意事项 |
|---|---|---|
| 标准眼(AL 22~25 mm) | SRK/T、Haigis、Barrett Universal II | 多种公式比较 |
| 长眼轴(AL > 26 mm) | Barrett Universal II、Hill-RBF、Kane | 注意低度数IOL时的精度差异15,16) |
| 短眼轴(AL < 22 mm) | Barrett Universal II、Haigis、Holladay 2 | 存在高度屈光误差风险。ELP预测误差较大18) |
| 角膜屈光手术后(LASIK术后) | Haigis-L、Shammas No-history、Barrett True-K、OKULIX | 使用ASCRS在线计算器比较多种公式9,20) |
| 睫状沟(囊外)固定 | 用SRK/T等计算后调整−1.0 D | 长眼轴低度数时调整较少,短眼轴高度数时调整−2.0 D |
| 巩膜内固定(镊子法) | 与囊外固定相同的矫正 | 因术式而异 |
| 圆锥角膜/角膜移植术后 | 专用公式(Seitz-Langenbucher等)或专家判断 | 标准公式误差较大 |
LASIK术后角膜局部变平,自动角膜曲率计容易高估中央屈光力,导致术后远视漂移。即使没有LASIK术前数据,各光学眼轴长测量装置也配备了可用的计算公式(如Haigis-L、Shammas No-history、Barrett True-K等),此外,使用ASCRS(美国白内障与屈光手术学会)的免费在线计算器进行多种公式比较也是一种对策。7,9) 一项针对110只LASIK术后眼的研究显示,单独使用Barrett True-K生物测量仪的精度与多种公式平均值方法相当(MAE 0.41 D vs. 0.42 D,p = 0.81),表明单独使用也具有可靠性。20)
术前根据患者的生活环境、工作、爱好设定目标屈光值(以等效球镜度预测)。
| 生活方式 | 推荐目标屈光值 |
|---|---|
| 远视力优先(驾驶、运动) | 正视(0.00 D)〜−0.25 D |
| 平衡型 | −0.25〜−0.50 D(轻度近视倾向) |
| 近视力优先(阅读、精细工作) | −1.50〜−2.00 D(单眼视候选) |
| 单眼视(非优势眼) | −1.50〜−2.00 D |
| 多焦点人工晶状体(大多数产品) | 正视(必须在±0.25 D以内) |
对于散光矫正型IOL的计算,使用光学眼轴长测量仪内置的公式(如Haigis-T公式或Barrett Toric公式)可以省去测量值输入的麻烦,也无需担心输入错误。基本原则是始终一致地使用光学眼轴长、角膜屈光力和IOL常数。7)
植入IOL后,原有的晶状体调节(睫状肌收缩引起的厚度变化)消失。然而,临床上可能出现称为“伪调节”的现象,从而获得轻微的近视力。伪调节由角膜的多焦点性、散光、瞳孔的针孔效应以及IOL的球差等引起,即使是单焦点IOL也可能观察到约0.5至1.0D的伪调节。
单焦点IOL可获得与年轻正常晶状体相当或更好的对比敏感度。另一方面,多焦点IOL由于光散射导致高频区域的对比敏感度下降。在轻度白内障或IOL植入眼中,即使视力没有变化,对比敏感度也可能下降。三焦点IOL与EDOF IOL的荟萃分析(22项研究)显示,两组间的对比敏感度无显著差异。5) 多焦点IOL总体(包括8项RCT的Cochrane荟萃分析)与单焦点相比,对比敏感度略有下降,但其临床意义尚不明确。3)
术后5年内发生后发性白内障(PCO)时,对比敏感度可能显著下降。疏水性丙烯酸IOL与亲水性丙烯酸相比,PCO发生率较低,方边光学部设计也有助于预防。10)
光晕(halo)是指光源周围可见的光环,眩光(glare)是指光源引起的刺眼或视野白浊。多焦点IOL与单焦点IOL相比,光晕(RR 3.58,95% CI 1.99~6.46)和眩光显著增加。3) EDOF IOL比传统的双焦点或三焦点IOL光学副作用更少,但并未完全消失。5)
应对措施:
植入无色人工晶体后,由于其对短波长光的透射率高于人眼晶状体,患者可能会感觉视物偏蓝(蓝视症)。有色(黄色滤光)人工晶体可减轻此现象。数天至数周内神经适应,大多数患者不再察觉。
疏水性丙烯酸酯人工晶体光学部出现的点状反光称为闪烁现象(glistenings)。深层发生的称为glistenings,表层发生的称为亚表面纳米闪烁(SSNG)。两者均为房水进入光学材料内部微小间隙所致,并非材料退化。通常不影响视功能,但在视网膜功能减退的患者中也有视功能下降的报道。目前市售的人工晶体已改进工艺,这些现象较前减轻。亲水性丙烯酸酯人工晶体长期使用后,表面可能沉积磷酸钙,导致严重混浊(钙沉积)。10)
| 并发症 | 发生率(参考) | 概述 | 处理 |
|---|---|---|---|
| 后发性白内障(后囊混浊) | 术后5年发生率为20~40% | 晶状体上皮细胞在IOL后方的后囊上增殖,导致视功能下降 | Nd:YAG激光后囊切开术 |
| IOL偏位或脱位 | 悬韧带薄弱的眼睛每年发生率为百分之几 | 因老化、外伤或假性剥脱综合征导致悬韧带断裂,IOL落入玻璃体腔 | 巩膜内固定术、缝合术或IOL置换11) |
| 瞳孔夹持(虹膜夹持) | 巩膜内固定等术后约百分之几 | IOL光学部脱位至瞳孔前方的状态。 | 散瞳、体位改变、更换为光学部直径更大的IOL12) |
| IOL混浊 | 疏水性闪辉:百分之几;亲水性钙沉积:数年后 | 因材质变质导致视功能下降 | IOL更换10) |
| PIOL术后青光眼 | ICL术后眼压升高1~5% | 房角关闭和瞳孔阻滞引起的眼压升高 | 术前前房深度评估及术后定期管理13) |
IOL偏位和脱位
Zinn小带断裂导致IOL坠落的诊断和手术适应证。巩膜内固定术(法兰法、镊子法)的选择。
IOL 混浊
生物测量(IOL 度数计算)
使用光学眼轴长测量装置同时精确测量眼轴长、角膜屈光力和前房深度。 IOL 度数计算的生物测量
巩膜内固定术
Sanders DR, Retzlaff J, Kraff MC. Comparison of the SRK II formula and other second generation formulas. J Cataract Refract Surg. 1988;14(2):136-141.1)
European Society of Cataract and Refractive Surgeons. ESCRS recommendations for cataract surgery. Draft version September 2024. Chapter 4.6: patient selection for correcting presbyopia. https://www.escrs.org/escrs-guideline-for-cataract-surgery/2)
de Silva SR, Evans JR, Kirthi V, Ziaei M, Leyland M. Multifocal versus monofocal intraocular lenses after cataract extraction. Cochrane Database Syst Rev. 2016;12(12):CD003169. doi:10.1002/14651858.CD003169.pub4. PMID:27943250; PMCID:PMC6463930.3)
European Society of Cataract and Refractive Surgeons. ESCRS recommendations for cataract surgery. Draft version September 2024. Chapters 4.6-4.7 and 6.1-6.3. https://www.escrs.org/escrs-guideline-for-cataract-surgery/4)
Karam M, Alkhowaiter N, et al. Extended Depth of Focus Versus Trifocal for Intraocular Lens Implantation: An Updated Systematic Review and Meta-Analysis. J Refract Surg. 2022. 22 studies, 2200 eyes.5)
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第 8 版). 日眼会誌. 2024;128(2):135-142.6)
Werner L. Intraocular lenses: overview of designs, materials, and pathophysiologic features. Ophthalmology. 2021;128(11):e74-e93.7)
Suzuki Y, Kamoi K, Uramoto K, Ohno-Matsui K. Artificial intelligence driven intraocular lens power calculation in extreme axial myopia. Sci Rep. 2025. 80 eyes, axial length ≥30.0 mm, Institute of Science Tokyo.8)
American Academy of Ophthalmology. Cataract in the Adult Eye Preferred Practice Pattern®. AAO; 2021.9)
Grzybowski A, Markeviciute A, Zemaitiene R. A narrative review of intraocular lens opacifications: update 2020. Ann Transl Med. 2020;8(22):1547. doi:10.21037/atm-20-4207. PMID:33313292; PMCID:PMC7729367.10)
Tripathi M, Rao S, Sinha R. Scleral-fixated IOLs - A comprehensive review of current practices and emerging trends. Indian J Ophthalmol. 2025;73(7):933-945. doi:10.4103/IJO.IJO_2812_24. PMID:40586185; PMCID:PMC12356440.11)
Choi SR, Jeon JH, Kang JW, Heo JW. Risk factors for and management of pupillary intraocular lens capture after intraocular lens transscleral fixation. J Cataract Refract Surg. 2017;43(12):1557-1562. PMID: 29335100. doi:10.1016/j.jcrs.2017.08.021.12)
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第 8 版). 有水晶体眼内レンズ手術の禁忌・慎重事項. 日眼会誌. 2024;128(2):135-142.13)
Kessel L, Andresen J, Tendal B, Erngaard D, Flesner P, Hjortdal J. Toric intraocular lenses in the correction of astigmatism during cataract surgery: a systematic review and meta-analysis. Ophthalmology. 2016;123(2):275-286. doi:10.1016/j.ophtha.2015.10.002. PMID:26601819.14)
Melles RB, Holladay JT, Chang WJ. Accuracy of intraocular lens calculation formulas. Ophthalmology. 2018;125(2):169-178. doi:10.1016/j.ophtha.2017.08.027. PMID:28951074.15)
Rong X, He W, Zhu Q, et al. Intraocular lens power calculation in eyes with extreme myopia: comparison of Barrett Universal II, Haigis, and Olsen formulas. J Cataract Refract Surg. 2019;45(6):732-737.16)
McCabe C, Berdahl J, Reiser H, et al. Clinical outcomes in a U.S. registration study of a new EDOF intraocular lens with a nondiffractive design. J Cataract Refract Surg. 2022;48(11):1297-1304. PMID: 35616507. PMCID: PMC9622364. doi:10.1097/j.jcrs.0000000000000978.17)
Wang Q, Jiang W, Lin T, Wu X, Lin H, Chen W. Meta-analysis of accuracy of intraocular lens power calculation formulas in short eyes. Clin Exp Ophthalmol. 2018;46(4):356-363. doi:10.1111/ceo.13058. PMID:28887901.18)
Webers VSC, Bauer NJC, Visser N, et al. Image-guided system versus manual marking for toric intraocular lens alignment in cataract surgery. J Cataract Refract Surg. 2017;43(6):781-788. doi:10.1016/j.jcrs.2017.03.041. PMID:28732612.19)
Ferguson TJ, Downes RA, Randleman JB. IOL power calculations after LASIK or PRK: Barrett True-K biometer-only calculation strategy yields equivalent outcomes as a multiple formula approach. J Cataract Refract Surg. 2022;48(7):784-789. doi:10.1097/j.jcrs.0000000000000883. PMID:35067661.20)